Биологические свойства пленок из регенерированного фиброина шелка
Цель исследования — изучение биологических и механических свойств пленок, изготовленных из фиброина шелка, и композитных пленок на его основе, содержащих 30% коллагена по массе.
Материалы и методы. Пленки изготовлены методом кастинга с применением двух различных растворителей — воды и муравьиной кислоты. Использованы методы сканирующей электронной микроскопии, атомно-силовой микроскопии. Проверку биосовместимости пленок осуществляли с помощью культуры клеток гепатокарциномы человека Hep-G2.
Результаты. Определена степень шероховатости поверхности полученных пленок. Для пленок, изготовленных из водных растворов, установлено свойство проницаемости для низкомолекулярных веществ. Измерены показатели эластичности и прочности на разрыв исследуемых пленок. Выявлено, что добавление коллагена в состав пленки существенно не влияет на показатель прочности на разрыв, но при этом повышает показатель эластичности пленки. Проведено исследование деградации пленок. Показано, что присутствие коллагена существенно не влияет на скорость деградации пленок как в нейтральной, так и в окисляющей средах. На примере культуры клеток Hep-G2 показано, что в наибольшей степени пролиферативную активность клеток поддерживают пленки, изготовленные из водных растворов фиброина шелка и коллагена.
Заключение. Для создания пленок с оптимальными свойствами, которые можно использовать в регенеративной медицине, наиболее подходящим является водный раствор фиброина шелка.
Одной из актуальных проблем современной трансплантологии является нехватка донорских органов для пересадки. Решением этой проблемы может стать создание искусственных органов, представляющих собой конструкции, содержащие матриксный и клеточный компоненты.
Функциональная активность полученного изделия зависит от пролиферативной активности клеток, входящих в его состав. Однако выбор материала, который будет использоваться как каркас будущего искусственного органа, является не менее важной задачей. Этот материал должен максимально имитировать свойства нативного внеклеточного матрикса и выполнять его функции: определять физические свойства тканей, обеспечивать адгезию, пролиферацию, дифференцировку и миграцию клеток. В настоящее время в качестве таких материалов рассматривают как синтетические, так и материалы природного происхождения [1–3].
Одним из универсальных материалов, используемых в качестве каркасного компонента, является фиброин шелка из коконов тутового шелкопряда Bombyx mori. Фиброин относится к классу фибриллярных белков и характеризуется присутствием большого количества повторов в его первичной структуре. Такое строение обусловливает однородность вторичной структуры фиброина, представляющей собой антипараллельные β-слои, связанные водородными связями. Аморфные участки белка образуют α-спирали, и их доля возрастает при гидратации белка. В третичной структуре фиброина выделяют две цепи: тяжелую цепь с молекулярной массой 390 кДа и легкую цепь — 26 кДа, присутствующие в отношении 1:1 и соединенные дисульфидными связями [4]. Изменяя долю β-слоев в структуре, можно контролировать механические свойства изделия и скорость биодеградации [5]. Медленная биодеградация фиброина шелка может быть преимуществом для его использования в тканевой инженерии в тех случаях, когда требуется длительное время для пролиферации и дифференцировки клеток в имплантируемом изделии [6].
В структуре фиброина присутствует большое количество свободных химических групп, которые могут быть модифицированы или использованы для создания конъюгатов с другими соединениями [7], а также композитных материалов с улучшенными свойствами [8, 9].
Таким образом, фиброин обладает свойствами, которые позволяют формировать из него различные изделия: покрытия, пленки, трубки, пористые матриксы, микро- и наночастицы, гели, а также широко использовать его в тканевой инженерии — как самостоятельный материал и в составе композитов.
Цель исследования — изучение механических и биологических свойств пленок из фиброина шелка тутового шелкопряда B. mori, а также композитных пленок на его основе, содержащих 30% коллагена, изготовленных с использованием различных растворителей.
Материалы и методы
Получение фиброина шелка. Фиброин шелка получали из коконов тутового шелкопряда B. mori. На первом этапе коконы подвергали очистке от серицина. Навеску шелка из коконов массой 1 г кипятили на водяной бане в 500 мл бидистиллированной воды с добавлением 1260 мг соды в течение 40 мин, затем промывали 3,6 л дистиллированной воды. Далее кипятили в 500 мл бидистиллированной воды 30 мин и промывали 3,6 л дистиллированной воды. Последнюю процедуру повторяли 3 раза. Очищенный фиброин шелка сушили на воздухе при комнатной температуре.
Получение водного раствора фиброина шелка. Для получения водного раствора фиброина к 130 мг отмытого шелка добавляли раствор, содержащий 389 мг CaCl2, 388 мкл C2H5OH и 544 мкл H2Oна 1 мл раствора. Смесь нагревали в течение 5 ч на водяной бане до полного растворения шелка. Полученный раствор центрифугировали в течение 7 мин при 12 100 g. Супернатант диализовали против 500 мл бидистиллированной воды, всего проводили 5 смен диализа по 30 мин. Раствор фиброина центрифугировали 7 мин при 12 100 g, концентрацию фиброина определяли спектрофотометрически при длине волны 280 нм, молярный коэффициент экстинкции составлял 473 480 М–1см–1, что соответствует теоретически рассчитанному коэффициенту экстинкции по аминокислотной последовательности тяжелой цепи фиброина шелка (номер в базе данных UniProt: P05790).
Получение водного раствора коллагена. Раствор коллагена из крысиных хвостов в уксусной кислоте [10] центрифугировали в течение 20 мин при 5000 g. Супернатант диализовали против 1 л бидистиллированной воды при комнатной температуре, смены диализа проводили 5 раз через каждый час. Концентрация полученного раствора составила 9 мг/мл. Полученный раствор содержит от 60 до 85% коллагена, 60% которого составляет коллаген I типа [11].
Получение раствора фиброина шелка в муравьиной кислоте. Навеску отмытого шелка растворяли в муравьиной кислоте из расчета 20 мг/мл при нагревании до 40°С на водяной бане в течение 30 мин. Полученный раствор центрифугировали 5 мин при 12 100 g.
Изготовление пленок из фиброина шелка и композиции фиброин–коллаген. Пленки получали методом кастинга. Для изготовления пленки диаметром 1 см2 наносили 100 мкл раствора на поверхность полированного тефлона и высушивали в течение двух дней при комнатной температуре. Общая концентрация белка в растворе для изготовления пленки составляла 20 мг/мл, содержание коллагена в композитных пленках — 30% по массе. Пленки снимали с поверхности тефлона с помощью скальпеля, предварительно инкубировав их в спирте в течение 15 мин, и хранили в 96% спирте при температуре 4°С.
Анализ структуры пленок методом сканирующей электронной микроскопии. Образцы пленок фиксировали глутаровым альдегидом, дегидратировали возрастающими концентрациями этанола и помещали в ацетон. После этого образцы высушивали методом «перехода критической точки» с помощью прибора HCP-2 (Hitachi Ltd., Япония). Высушенные образцы покрывали слоем золота толщиной 20 нм в атмосфере аргона при ионном токе 6 мА и давлении 0,1 мм рт. ст. с использованием прибора IB-3 Ion Coater (Eiko Engineering, Япония), затем анализировали с помощью сканирующего электронного микроскопа Camscan S2 (CambridgeInstruments, Великобритания). Разрешение микроскопа — 10 нм, рабочее напряжение — 20 кВ. Изображения получали с использованием программного обеспечения MicroCapture.
Анализ поверхности пленок с помощью атомно-силовой микроскопии. Образцы пленок приклеивали на двусторонний скотч. После высыхания образец на скотче помещали на платформу прибора Solver P47-PRO («Нанотехнология МДТ», Россия). Сканирование осуществляли в полуконтактном режиме с частотой сканирования 0,3–0,4 Гц и амплитудой 20–40 нм с помощью кантилевера NSC15/ALBSс резонансной частотой 265–410 кГц и силовой константой 20–80 Н/м (Micromasch, США). Площадь сканируемой области составляла 11,324×11,324 мкм. Получение изображений, их обработку, построение сечений и трехмерных изображений осуществляли с помощью программы Nova.
Оценку шероховатости поверхности проводили в программе Nova с помощью функции Roughness Analysis, которая позволяет получить среднее значение шероховатости поверхности в нанометрах для одной линии сканирования.
Оценка пористости пленок. Пористость пленок оценивали по их проницаемости для двух красителей: бромфенолового синего (молекулярная масса=691,9 г/моль) и трипанового синего (М=872,88). Для этого на поверхность влажной пленки наносили 5 мкл раствора красителя и визуально оценивали количество красителя, прошедшего через пленку на фильтровальную бумагу за 1 мин.
Изучение механических свойств пленок из фиброина шелка. Исследование механических свойств пленок проводили с помощью разрывной машины Zwick/Roell BZ 2.5/TN1S (ZwickRoell, Германия). Образцы пленок длиной 4 см, шириной 5 мм помещали в зажимы прибора. Предварительная нагрузка составляла 0,05 Н. Далее проводили испытание образцов на растяжение со скоростью 50 мм/мин. Измеряли значения двух величин: прочности на разрывв МПа и эластичности, или удлинения, в процентах от первоначальной длины образца. Полученные кривые зависимости силы от удлинения обрабатывали в программе TestXpert (Zwick Roell, Германия).
Тест на деградацию пленок in vitro. Исследование деградации пленок проводилось согласно ГОСТ 10993-13–2009 «Оценка биологического действия медицинских изделий». В качестве окисляющего реагента использовали реактив Фентона, содержащий 100 мкМ FeSO4 и 1 мМ Н2О2. Смены раствора окисляющего реагента проводили каждые 3 дня. В качестве контроля применяли раствор фосфатно-солевого буфера (PBS) с рН=7. Образцы инкубировали в десятикратных объемах растворов и измеряли массу через каждые 7 дней в течение 1 мес.
Анализ пролиферативной активности клеток гепатокарциномы человека Hep-G2 на пленках различного состава. Для исследования пролиферативной активности пленки прикрепляли к поверхности лунок 96-луночного планшета с помощью 5% раствора желатина. В качестве контроля использовали культуральный пластик. Перед проведением теста планшет подвергали стерилизации: обрабатывали 70% спиртом 30 мин и облучали ультрафиолетом в течение 30 мин. В лунки планшета вносили стерильный раствор PBS на 15 мин, а затем на 30 мин — стерильный 0,9% раствор NaCl. Далее в лунки планшета вносили по 300 мкл среды инкубации DMEM с добавлением 20 ммоль/мл HEPES, 10% эмбриональной телячьей сыворотки и 40 мкг/мл гентамицина и инкубировали 15 мин. Суспензию клеток гепатокарциномы человека Hep-G2 с концентрацией 4,2·106 кл./мл в среде инкубации переносили в 96-луночные планшеты по 200 мкл на лунку. Клетки инкубировали в термостате при 37°С, 5% CO2 в течение 9 дней.
Оценку пролиферативной активности клеток проводили с помощью МТТ-теста на 3-, 6- и 9-й дни эксперимента. Для этого в каждую лунку планшета вносили по 50 мкл раствора 3-[4,5-диметилтиазолил-2-ел]-2,5-дифенилтетразолиум бромида. Инкубировали в термостате при 37°С при содержании 5% CO2 в течение 3–4 ч до выпадения темно-синих кристаллов формазана. Затем планшет центрифугировали в течение 5 мин при 1500 об./мин. Супернатант удаляли, осадок формазана растворяли в DMSO и измеряли оптическую плотность раствора при длине волны 540 нм.
Обработка данных. Статистический анализ результатов проводили методом дисперсионного анализа, уровень статистической значимости р принимали равным 0,05.
Результаты и обсуждение. Сравнение биологических и механических свойств пленок, полученных с применением различных растворителей, было проведено впервые. Были изготовлены 4 вида пленок на основе фиброина шелка тутового шелкопряда B. mori (табл. 1). Полученные изделия были бесцветными и имели толщину 50 мкм.
 Таблица 1. Состав полученных образцов пленок на основе фиброина шелка тутового шелкопряда B. mori Таблица 1. Состав полученных образцов пленок на основе фиброина шелка тутового шелкопряда B. mori
|
Для улучшения биосовместимости пленок в состав изделия введена композитная добавка, в качестве которой выбран коллаген, так как он является самым распространенным белком межклеточного матрикса и имеет в своей структуре RGD-последовательность, к которой аффинны рецепторы на поверхности клеток.
Структура поверхности пленок была исследована с помощью сканирующей электронной микроскопии. Установлено, что поверхность пленок имеет микро- и нанорельеф в виде шероховатостей (рис. 1).
Шероховатость поверхности определяет адгезию клеток, поэтому наличие шероховатостей на поверхности субстрата увеличивает площадь поверхности, доступную для адгезии. По-видимому, существует оптимальный уровень шероховатости субстрата, который индивидуален для различных культур клеток [12]. Анализ шероховатости поверхности проводили с помощью атомно-силовой микроскопии. Шероховатость составила 70–90 нм для пленок, изготовленных из растворов полимеров в муравьиной кислоте, и 30–50 нм — для пленок, изготовленных из водных растворов полимеров (табл. 2). Присутствие коллагена в составе пленки существенно не влияет на величину показателя шероховатости.
 Таблица 2. Данные о средних высотах рельефа пленок различного состава (указаны значения стандартного отклонения для шести независимых измерений) Таблица 2. Данные о средних высотах рельефа пленок различного состава (указаны значения стандартного отклонения для шести независимых измерений)
|
Качественный анализ проницаемости пленок показал, что пленки, изготовленные из водных растворов, имеют бóльшую проницаемость, чем пленки, изготовленные из растворов полимеров в муравьиной кислоте (табл. 3). Проницаемость характеризует возможность изделия пропускать низкомолекулярные биологически активные вещества, необходимые для правильного развития ткани.
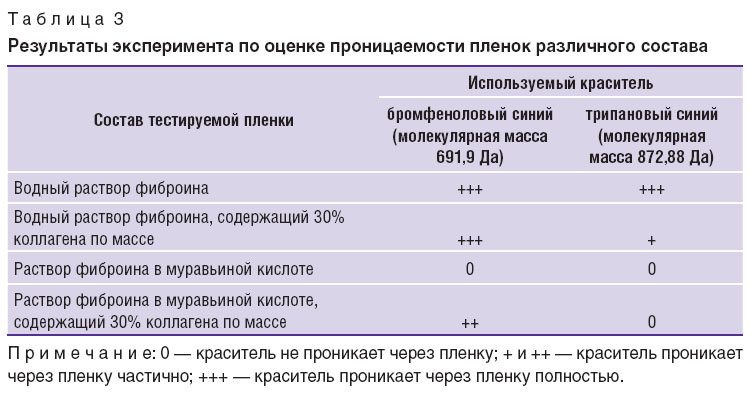 Таблица 3. Результаты эксперимента по оценке проницаемости пленок различного состава Таблица 3. Результаты эксперимента по оценке проницаемости пленок различного состава
|
Изделия, предназначенные для применения в регенеративной хирургии, должны быть механически прочными и эластичными, так как при имплантации непрочных и/или ломких изделий могут возникать сложности. Показатель эластичности применяемого материала должен соответствовать показателю эластичности нативной ткани, которая была повреждена. Пленки, содержащие в составе коллаген, имеют значительно меньшие показатели прочности при растяжении по сравнению с пленками, изготовленными из растворов фиброина шелка (табл. 4). Добавление коллагена в состав пленки практически не влияет на показатель эластичности изделия. Наиболее высокой механической прочностью наряду с высокими показателями эластичности обладают пленки, изготовленные из водного раствора фиброина шелка.
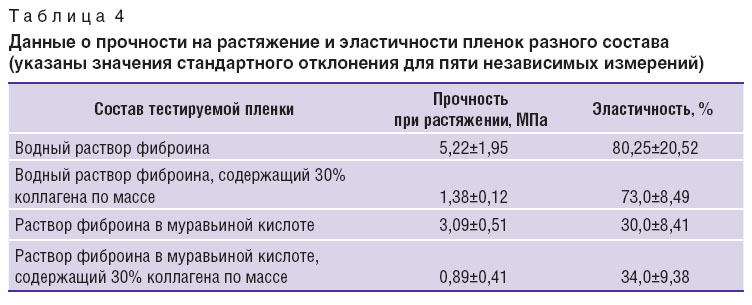 Таблица 4. Данные о прочности на растяжение и эластичности пленок разного состава (указаны значения стандартного отклонения для пяти независимых измерений) Таблица 4. Данные о прочности на растяжение и эластичности пленок разного состава (указаны значения стандартного отклонения для пяти независимых измерений)
|
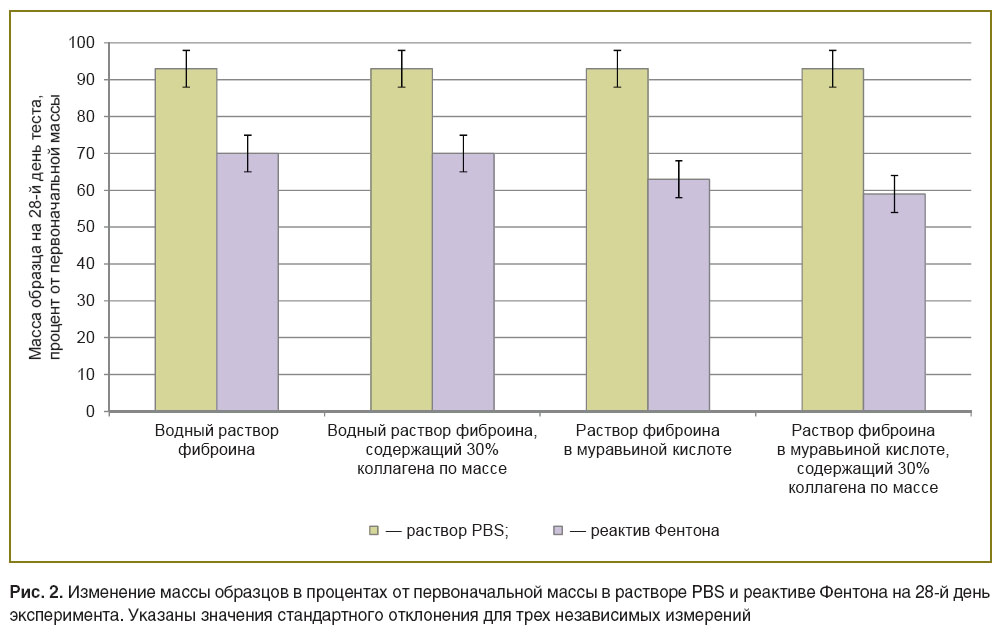
Процесс деградации изделия был изучен в условиях двух сред: нейтральной и окисляющей. В качестве нейтральной среды использовали раствор PBS как систему, близкую по составу к внутренней среде организма. В таких условиях масса образцов за 28 дней изменилась в пределах 7%. В качестве окисляющей среды применяли реактив Фентона, который моделирует реакции клеточного ответа на имплантат за счет гидроксильных радикалов, образующихся в ходе реакции Фентона и взаимодействующих с образцом. В окисляющей среде масса образцов в среднем уменьшилась на 34% (рис. 2).
Деградация пленки из водного раствора фиброина с добавлением коллагена в окисляющих условиях сопровождалась резким ухудшением механических свойств и, как следствие, неспособностью изделия сохранять форму, в то время как остальные изделия к 4-й неделе эксперимента сохраняли форму. Анализ результатов показал, что присутствие коллагена существенно не влияет на скорость деградации пленок как в нейтральной, так и в окисляющей средах.
Тест по оценке пролиферативной активности клеток проводился на культуре клеток гепатокарциномы человека Hep-G2. Клетки этой культуры имеют рецепторы-интегрины [13], которые аффинны к последовательности RGD, присутствующей в структуре коллагена.
Конструкции из фиброина шелка, а также из его композитов с коллагеном, желатином, хитозаном и другими материалами используются в тканевой инженерии в качестве матрикса для выращивания клеток гепатокарциномы человека. Примером такой конструкции является трехмерный пористый матрикс из фиброина шелка с хитозаном [14]. Пролиферативная активность культуры клеток Hep-G2 на таком матриксе была сопоставима с положительным контролем, что позволяет считать его пригодным для тканевой инженерии печени.
Наибольшая пролиферативная активность клеток была зарегистрирована на пленках из водного раствора фиброина шелка (рис. 3). На пленках из водного раствора фиброина с добавлением коллагена она увеличивалась в течение проведения теста и была сопоставима с пролиферативной активностью клеток на пленках из водного раствора фиброина шелка. Это может быть связано с тем, что коллаген в составе композита не обеспечивает увеличения пролиферативной активности вследствие экранирования молекулами фиброина RGD-последовательности коллагена от рецепторов клеток. Однако в литературе все же существуют примеры успешного использования коллагена в качестве композитной добавки для повышения пролиферативной активности клеток культуры Hep-G2 как в составе трехмерных матриксов [15], так и в составе пленок [16].
 Рис. 3. Пролиферативная активность клеток культуры Hep-G2 на пленках различного состава на 3-, 6- и 9-й дни эксперимента. Указаны значения стандартного отклонения для пяти независимых измерений Рис. 3. Пролиферативная активность клеток культуры Hep-G2 на пленках различного состава на 3-, 6- и 9-й дни эксперимента. Указаны значения стандартного отклонения для пяти независимых измерений
|
Наиболее низкая пролиферативная активность была зарегистрирована на пленках из растворов полимеров в муравьиной кислоте.
По полученным данным можно сделать вывод о том, что для создания пленок с оптимальными свойствами для тканевой инженерии лучше всего подходит водный раствор фиброина шелка.
Заключение. Изучение свойств пленок из регенерированного фиброина шелка, которые потенциально могут влиять на пролиферативную активность клеток и возможность применения изделия в тканевой инженерии (в качестве таких свойств были выбраны проницаемость, шероховатость поверхности, механические свойства, скорость деградации, а также способность обеспечивать адгезию и пролиферацию эукариотических клеток), показало, что изделия из водных растворов полимеров характеризуются проницаемостью для низкомолекулярных веществ, высокой механической прочностью и эластичностью. Шероховатость поверхности зарегистрирована на всех видах изготовленных пленок и зависит от применяемого растворителя. Все изделия поддерживают пролиферативную активность клеток. Добавление коллагена в состав изделия не влияет на пролиферативную активность клеток, но изменяет механические свойства изделия.
Благодарности. Авторы благодарят руководителя Лаборатории химии и технологии материалов для сердечно-сосудистой хирургии Научного центра сердечно-сосудистой хирургии имени А.Н. Бакулева РАМН Светлану Петровну Новикову и научного сотрудника Регину Рушановну Салохединову за помощь в проведении эксперимента по измерению механических свойств.
Финансирование исследования. Работа осуществлялась при поддержке Министерства образования и науки Российской федерации в рамках Федеральной целевой программы «Исследования и разработки по приоритетным направлениям развития научно-технологического комплекса России на 2014–2020 годы» по Соглашению о предоставлении субсидии от 17 июня 2014 г. №14.604.21.0017 «Новые средства для лечения травматических и ишемических повреждений тканей на основе биодеградируемых материалов с иммобилизованными пептидами-агонистами рецепторов, активируемых протеиназами», уникальный идентификатор соглашения RFMEFI60414X0017.
Конфликт интересов. У авторов нет конфликта интересов.
Литература
- Moisenovich M.M., Pustovalova O., Shackelford J., Vasiljeva T.V., Druzhinina T.V., Kamenchuk Y.A., Guzeev V.V., Sokolova O.S., Bogush V.G., Debabov V.G., Kirpichnikov M.P., Agapov I.I. Tissue regeneration in vivo within recombinant spidroin 1 scaffolds. Biomaterials 2012; 33(15): 3887–3898, http://dx.doi.org/10.1016/j.biomaterials.2012.02.013.
- Bonartsev A., Yakovlev S., Boskhomdzhiev A., Zharkova I., Bagrov D., Myshkina V., Mahina T., Kharitonova E., Samsonova O., Zernov A., Zhuikov V., Efremov Y., Voinova V., Bonartseva G., Shaitan K. The terpolymer produced by Azotobacter chroococcum 7B: effect of surface properties on cell attachment. PLoS One 2013; 8(2): e57200, http://dx.doi.org/10.1371/journal.pone.0057200.
- Moisenovich M.M., Pustovalova O.L., Arhipova A.Y., Vasiljeva T.V., Sokolova O.S., Bogush V.G., Debabov V.G., Sevastianov V.I., Kirpichnikov M.P., Agapov I.I. In vitro and in vivo biocompatibility studies of a recombinant analogue of spidroin 1 scaffolds. J Biomed Mater Res A 2011; 96(1): 125–131, http://dx.doi.org/10.1002/jbm.a.32968.
- He Y.-H., Zhang N.-N., Li W.-F., Jia N., Chen B.-Y., Zhou K., Zhang J., Chen Y., Zhou C.-Z. N-terminal domain of Bombyx mori fibroin mediates the assembly of silk in response to pH decrease. J Mol Biol 2012; 418(3–4): 197–207, http://dx.doi.org/10.1016/j.jmb.2012.02.040.
- Kasoju N., Bora U. Silk fibroin based biomimetic artificial extracellular matrix for hepatic tissue engineering applications. Biomed Mater 2012; 7(4): 045004, http://dx.doi.org/10.1088/1748-6041/7/4/045004.
- Hu Y., Zhang Q., You R., Wang L., Li M. The relationship between secondary structure and biodegradation behavior of silk fibroin scaffolds. Advances in Materials Science and Engineering 2012; 2012: 185905, http://dx.doi.org/10.1155/2012/185905.
- Baran E.T., Tuzlakoğlu K., Mano J.F., Reis R.L. Enzymatic degradation behavior and cytocompatibility of silk fibroin–starch–chitosan conjugate membranes. Materials Science and Engineering 2012; 32(6): 1314–1322, http://dx.doi.org/10.1016/j.msec.2012.02.015.
- Moisenovich M.M., Arkhipova A.Y., Orlova A.A., Drutskaya M.S., Volkova S.V., Zacharov S.E., Agapov I.I., Kirpichnikov M.P. Composite scaffolds containing silk fibroin, gelatin, and hydroxyapatite for bone tissue regeneration and 3D cellc. Acta Naturae 2014; 6(1): 96–101.
- Agapov I.I., Moisenovich M.M., Druzhinina T.V., Kamenchuk Y.A., Trofimov K.V., Vasilyeva T.V., Konkov A.S., Arhipova A.Y., Sokolova O.S., Guzeev V.V., Kirpichnikov M.P. Biocomposite scaffolds containing regenerated silk fibroin and nanohydroxyapatite for bone tissue regeneration. Dokl Biochem Biophys 2011; 440: 228–230, http://dx.doi.org/10.1134/S1607672911050103.
- Chandrakasan G., Torchia D.A., Piez K.A. Preparation of intact monomeric collagen from rat tail tendon and skin and the structure of the nonhelical ends in solution. J Biol Chem 1976; 251(19): 6062–6067.
- Kjaer M. Role of extracellular matrix in adaptation of tendon and skeletal muscle to mechanical loading. Physiol Rev 2004; 84(2): 649–698, http://dx.doi.org/10.1152/physrev.00031.2003.
- Zhang Q., Zhao Y., Yan S., Yang Y., Zhao H., Li M., Lu S., Kaplan D.L. Preparation of uniaxial multichannel silk fibroin scaffolds for guiding primary neurons. Acta Biomaterialia 2012; 8(7): 2628–2638, http://dx.doi.org/10.1016/j.actbio.2012.03.033.
- Rosenow F., Ossig R., Thormeyer D., Gasmann P., Schlüter K., Brunner G., Haier J., Eble J.A. Integrins as antimetastatic targets of RGD-independent snake venom components in liver metastasis. Neoplasia 2008; 10(2): 168–176.
- She Z., Jin C., Huang Z., Zhang B., Feng Q., Xu Y. Silk fibroin/chitosan scaffold: preparation, characterization, and culture with HepG2 cell. J Mater Sci Mater Med 2008; 19(12): 3545–3553, http://dx.doi.org/10.1007/s10856-008-3526-y.
- Lv Q., Feng Q., Hu K., Cui F. Three-dimensional fibroin/collagen scaffolds derived from aqueous solution and the use for HepG2 culture. Polymer 2005; 46(26): 12662–12669, http://dx.doi.org/10.1016/j.polymer.2005.10.137.
- Hu K., Lv Q., Cui F.Z., Feng Q.L., Kong X.D., Wang H.L., Huang L.Y., Li T. Biocompatible fibroin blended films with recombinant human-like collagen for hepatic tissue engineering. Journal Bioactive and Compatible Polymers 2006; 21(1): 23–37, http://dx.doi.org/10.1177/0883911506060455.