Распределение S100-позитивных клеток в островках Лангерганса поджелудочной железы человека в разные возрастные периоды
Цель исследования — изучить распределение S100-позитивных клеток в островках Лангерганса поджелудочной железы человека во время внутриутробного и раннего постнатального развития, а также у взрослых людей.
Материалы и методы. При помощи антител к белку S100, к основным гормонам, вырабатываемым в клетках островков Лангерганса поджелудочной железы человека (инсулин, глюкагон и соматостатин), и к нейронспецифической енолазе (NSE) проведено иммуногистохимическое исследование образцов поджелудочных желез человека. Образцы были получены от взрослых людей, не страдавших заболеваниями поджелудочной железы, и от больных сахарным диабетом 2-го типа, а также от плодов и новорожденных.
Результаты. В островках Лангерганса человека начиная с 15–16-й недели гестационного развития выявляются два типа S100-позитивных клеток: клетки, расположенные по периферии островка, и клетки, расположенные внутри него. Тела клеток, расположенных на периферии, отличаются уплощенной формой и небольшим количеством цитоплазмы. Эти клетки имеют длинные отростки, проходящие в основном по периферии островков. Клетки, расположенные внутри островка, — округлой или овальной формы и, как правило, не имеют отростков.
Заключение. Начиная с раннефетального периода развития в островках Лангерганса поджелудочной железы человека выявляются два типа S100-позитивных клеток, которые различаются по своему строению. Клетки, расположенные на периферии островков, сходны по своей морфологии с клетками глии. Клетки, расположенные внутри островков, не отличаются по своему строению от остальных эндокринных клеток. Можно предположить, что эти два типа S100-позитивных клеток играют роль как в морфогенезе островков, так и в регуляции выброса гормонов эндокринными клетками.
Сахарный диабет — одна из наиболее распространенных в мире болезней. Несмотря на успехи в лечении, продолжается рост числа заболевших и увеличение количества осложнений [1]. При этом бóльшая часть людей больна сахарным диабетом 2-го типа, который долгое время может оставаться недиагностированным. В настоящее время разрабатываются новые методы лечения сахарного диабета, которые предполагают достижение компенсации углеводного и липидного обмена при отсутствии гипогликемии, чего можно добиться только применением технологий, предусматривающих наличие нормальной обратной связи регуляции углеводного обмена. Идеальной для достижения такого состояния является разработка конструкций, функционирующих на принципах гормональной регуляции углеводного обмена [2]. Однако для достижения этой цели требуется детальная информация о строении и функциях клеток эндокринной части поджелудочной железы (ПЖ) человека.
В последнее время развитие сахарного диабета обоих типов связывают с нарушением функции или избирательной гибелью β-клеток островков Лангерганса ПЖ, синтезирующих инсулин [3]. Кроме этих клеток в эндокринной части ПЖ человека описано еще несколько их типов, основные из которых: α-клетки, синтезирующие глюкагон, δ-клетки — соматостатин, РР-клетки — панкреатический полипептид и ε-клетки, синтезирующие грелин. В ПЖ некоторых видов млекопитающих обнаружены еще некоторые типы клеток, например EC-клетки, синтезирующие серотонин, и G-клетки — гастрин. Однако они малочисленны и встречаются только на некоторых стадиях внутриутробного развития [4, 5].
Кроме указанных типов клеток в ПЖ человека еще в 1989 г. обнаружили S100-содержащие клетки [6]. Они были выявлены во всех островках и, по мнению авторов, образовывали отдельную клеточную популяцию. Клетки, позитивные к антителам к белку S100, были иммунонегативны к антителам к инсулину, глюкагону и панкреатическому полипептиду. Как правило, S100-позитивные (S100+клетки) и δ-клетки представляли собой две различные популяции, но иногда удавалось выявить колокализацию S100 и соматостатина.
У целого ряда животных тоже были обнаружены S100+клетки [7–10]. Данные об их расположении и форме, а также о колокализации с гормонами эндокринной части ПЖ во многом противоречивы. Так, например, у крыс S100+клетки выявлены на периферии островков и, как считается, образуют подобие оболочки из глиальных клеток. У морской свинки и яванского макака обнаружено два различных типа клеток: один тип располагается на периферии островков, имеет отростки и может представлять собой глиальные клетки; клетки второго типа выявлены внутри островков и сходны по своей морфологии с эндокринными клетками. При этом у морской свинки S100+клетки второго типа коэкспрессируют инсулин, а у макака — образуют отдельную популяцию. Кроме того, у некоторых видов животных [11] и у человека [12] S100+клетки обнаружены в составе нейроинсулярных комплексов.
Цель исследования — изучить распределение S100-позитивных клеток в островках Лангерганса поджелудочной железы человека во время внутриутробного и раннего постнатального развития, а также у взрослых людей.
Материалы и методы. Работа выполнена на аутопсийном материале ПЖ человека (эмбрионы, плоды, новорожденные, взрослые) из коллекции лаборатории развития нервной системы НИИ морфологии человека, а также собранном в 2007–2012 гг. в больницах Москвы. Всего были исследованы образцы ПЖ 27 плодов человека на разных сроках развития (гестационный возраст 10–35 нед), четырех недоношенных новорожденных, проживших от нескольких часов до 13 сут, двух доношенных новорожденных, одного ребенка (3 мес 17 дней), 15 взрослых людей (в возрасте от 30 до 90 лет), не страдавших заболеваниями ПЖ и нарушениями углеводного обмена, и 10 взрослых людей (42–82 года), страдавших сахарным диабетом 2-го типа. Работа была одобрена локальным этическим комитетом.
Материал фиксировали в 10% кислом формалине, нейтральном формалине (4% параформальдегид на 0,1 М фосфатном буфере, рН=7,5) или в жидкости Буэна, обезвоживали в спиртах восходящей крепости и диоксане и заливали в гистомикс (Histomix, «БиоВитрум», Россия). Затем были сделаны серийные срезы толщиной 10 мкм, а для некоторых образцов — также срезы толщиной 5 и 3 мкм. В ходе проведения иммуногистохимических реакций депарафинированные гидратированные срезы обрабатывали 3% раствором Н2О2 в течение 10 мин для блокировки эндогенной пероксидазы. В целях блокировки неспецифического связывания срезы обрабатывали раствором Ultra V Block (Lab Vision Corp., США) в течение 5 мин и ополаскивали в фосфатном буфере (PВS), pH=7,3–7,5. Использованные в работе антитела и условия проведения иммуногистохимических реакций приведены в таблице.
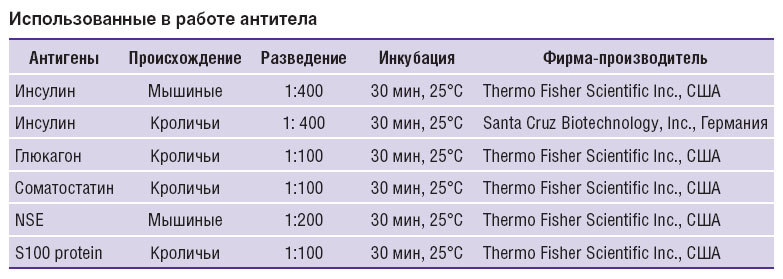 Использованные в работе антитела Использованные в работе антитела
|
Далее пользовались системой визуализации UltraVision Detection System Anti-polyvalent, HRP/DAB (Lab Vision Corp., США) согласно спецификации фирмы. На заключительном этапе срезы обрабатывали свежим раствором хромогена (DAB, Lab Vision Corp., США).
Для более детального изучения распределения в ПЖ человека основных гормонов и пан-нейрональных маркеров были проведены реакции двойного иммуногистохимического окрашивания. На всех образцах ПЖ на последовательных срезах были поставлены реакции выявления следующих антигенов:
а) NSE (мышиные моноклональные антитела) + глюкагон (кроличьи поликлональные антитела);
б) NSE (мышиные моноклональные антитела) + инсулин (кроличьи поликлональные антитела);
в) инсулин (мышиные моноклональные антитела) + соматостатин (кроличьи поликлональные антитела);
г) инсулин (мышиные моноклональные антитела) + S100 (кроличьи поликлональные антитела);
д) NSE (мышиные моноклональные антитела) + S100 (кроличьи поликлональные антитела).
Для этих целей была использована система детекции MultiVision Polymer Detection System: MultiVision anti-rabbit/HRP + anti-mouse/AP polymers (Thermo Fisher Scientific Inc., США).
Все полученные препараты оценивали визуально с помощью микроскопов Leica DMLS (Leica, Германия) и Микмед-6 («Ломо», Россия). Видеозахват осуществлялся с помощью камер Sony SSc-Dc50P (Sony, Япония) и Lomo TCA-5.0C («Ломо», Россия) соответственно.
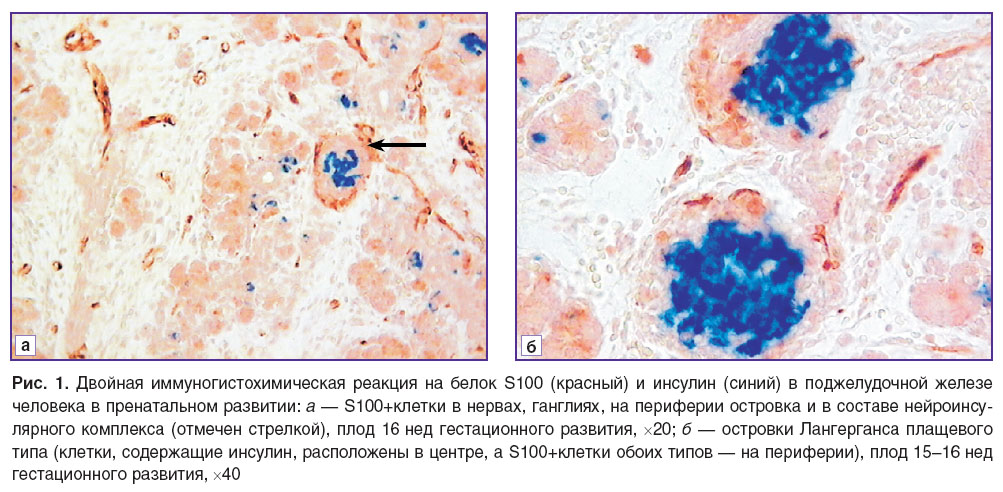
Результаты. Начиная с префетального периода иммунопозитивная реакция на белок S100 была выявлена в ПЖ человека в элементах нервной системы (ганглии, нервы). Кроме того, с 14-й недели гестационного развития на периферии некоторых островков ПЖ также начинают обнаруживаться S100+клетки. Положительная реакция к этому белку выявляется как в ядре, так и в цитоплазме этих клеток. S100+клетки обладают длинными отростками, также проходящими по периферии островков, не образуя полностью замкнутой оболочки. Достаточно часто наблюдается, что такие островки образуют нейроинсулярный комплекс с ганглиями автономной нервной системы (рис. 1, a).
Уже на 15–16-й неделе гестационного развития в ряде островков появляются S100+клетки не только на периферии, но и внутри островков. Такие клетки имеют преимущественно овальную форму, у них нет длинных отростков, они крупнее по размеру, чем тела клеток, расположенных на периферии. S100+клетки выявлены преимущественно в достаточно зрелых островках (диаметр не менее 40 мкм), часто расположенных вблизи крупных протоков. При помощи двойного иммуногистохимического окрашивания на серийных срезах установлено, что во время внутриутробного развития S100+клетки располагаются преимущественно в зоне локализации глюкагона и соматостатина (рис. 1, б).
Необходимо отметить, что величина реакции на антитела к белку S100 существенно варьирует в разных структурах нервной системы и эндокринной части ПЖ: сильнее всего она проявляется в элементах нервной системы (крупные нервы и ганглии); в клетках, расположенных на периферии островков, она более интенсивная, чем в клетках, расположенных внутри них.
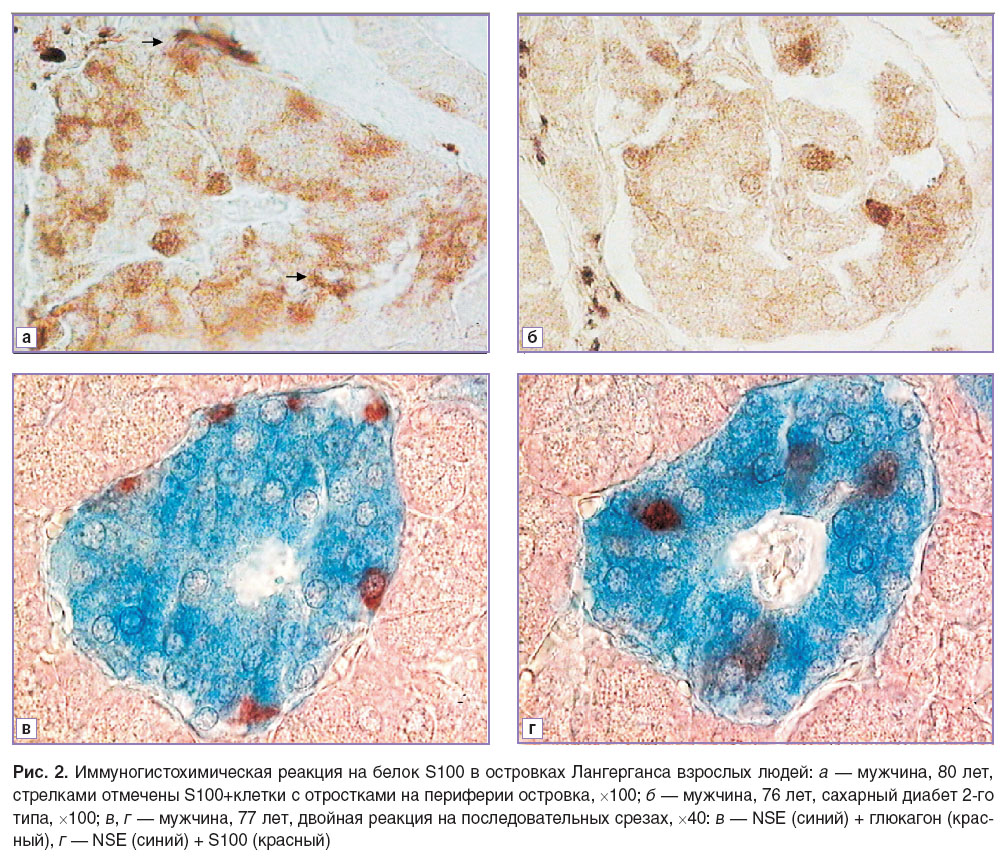
В дальнейшем внутриутробном, раннем постнатальном развитии и у взрослых людей мы также обнаружили оба типа S100+клеток в островках (рис. 2, а, б).
Клетки, расположенные внутри островков, всегда обнаруживали колокализацию S100 и NSE. Сходная картина наблюдалась и при исследовании образцов ПЖ больных сахарным диабетом 2-го типа. В данном исследовании мы не проводили морфометрический анализ, так как количество выявляемых клеток сильно зависит от сохранности материала и качества фиксации, однако иммуногистохимические данные позволяют утверждать, что с увеличением размера островка число выявляемых клеток внутри него становится больше. При этом число таких клеток заметно меньше, чем инсулин- или глюкагонсодержащих клеток, и сопоставимо с количеством соматостатинсодержащих клеток. Однако их расположение в островках взрослых людей отличается от расположения глюкагон- и соматостатинсодержащих клеток: α- и δ-клетки встречаются обычно на периферии островков или (в крупных островках) по ходу кровеносных капилляров, а S100+клетки выявляются в области β-содержащих клеток (рис. 2, в, г). При этом S100+клетки могли быть как инсулинпозитивными, так и инсулиннегативными.
Обсуждение. Белок S100 — кальцийсвязывающий протеин, впервые описанный Б.В. Муром в 1965 г., долгое время считался специфичным для нервной ткани. В настоящее время обнаружено, что это целая группа белков (известно уже 24), функционально распределенных в три основные подгруппы: 1) белки, которые оказывают только внутриклеточные регуляторные эффекты; 2) белки, которые в основном осуществляют функцию внеклеточного сигнала; 3) белки, осуществляющие обе эти функции [13]. Внутри клеток S100-белки участвуют в процессах регуляции пролиферации, дифференцировки и апоптоза, Ca2+-гомеостаза и клеточного метаболизма через взаимодействие с различными белками-мишенями, в том числе ферментами и рецепторами факторов транскрипции. Внеклеточно S100-белки оказывают регулирующее действие на большое количество различных типов клеток (нейроны, астроциты, шванновские клетки, микроглия, тучные клетки, суставные хондроциты, эндотелиальные и гладкомышечные клетки сосудистой системы, клетки эпителия миобластов и кардиомиоцитов, моноциты, макрофаги, нейтрофилы, лимфоциты), тем самым участвуя в формировании врожденного и приобретенного иммунного ответа и регулируя миграцию клеток и хемотаксис, развитие и регенерацию тканей, а также воспалительные процессы и рост опухолей [13, 14].
В островках Лангерганса ПЖ человека во всех исследованных возрастных периодах, начиная с раннефетального, нами было обнаружено два типа S100+клеток: клетки, расположенные по периферии островка, и клетки, расположенные внутри него. Эти два типа клеток имеют отличия.
Клетки, расположенные на периферии, по своей морфологии напоминают клетки, обнаруженные ранее в панкреатических островках грызунов [8, 9, 15]. На настоящий момент большинство авторов считают эти клетки глиальными. Однако их функциональная роль не ясна. Кроме того, в ряде работ [8, 10, 12] выявлена связь S100+клеток с нейроинсулярными комплексами. Нейроэндокринные комплексы наиболее многочисленны у плодов во II и начале III триместра беременности, когда в зачатке ПЖ наблюдается активный морфогенез панкреатических островков [12]. Поэтому мы предполагаем, что в данном случае S100+клетки играют вспомогательную роль при формировании внутренней архитектуры зрелых островков.
Клетки, расположенные внутри островка, по своей морфологии не отличаются от остальных эндокринных клеток островка и схожи по описанию с клетками, обнаруженными ранее у взрослых людей, в том числе страдавших сахарным диабетом и панкреатитом [6], а также у различных видов животных [7, 8, 10].
Некоторые авторы, в том числе и изучавшие S100+клетки у человека [6], считают, что это отдельный тип клеток, в то время как другая часть авторов [7, 8] обнаруживает колокализацию S100 с инсулином.
Анализ серийных срезов в нашем исследовании показал различия в количестве и расположении S100+клеток, α- и δ-клеток у взрослых. Необходимо отметить, что на взаимное расположение этих клеток внутри островков влияют размеры и форма островков [16]. В ПЖ взрослого человека выявляются разные формы организации эндокринной части: единичные клетки, содержащие гормоны, их небольшие скопления, островки плащевого (мышиного) типа и мозаичные островки. В островках плащевого типа инсулинсодержащие клетки расположены в центре, а глюкагонсодержащие — на периферии, в то время как в мозаичных островках глюкагонсодержащие клетки расположены как на периферии, так и вдоль капилляров, разделяя островок на отдельные кластеры. В плодном периоде в ПЖ выявлен так называемый биполярный тип островков, при котором клетки, содержащие инсулин и глюкагон, формируют два «полюса» островка [17]. У взрослых людей такие островки не выявлены. В пренатальном развитии разные типы распределения эндокринных клеток появляются по мере формирования поджелудочной железы [18–20].
У плодов на разных сроках развития мы выявляли S100+клетки в плащевых и биполярных островках преимущественно в зоне локализации глюкагон- и соматостатинсодержащих клеток. В зрелых мозаичных островках человека обнаружено гораздо меньше S100+клеток, чем клеток, содержащих глюкагон. Их количество было сопоставимо с числом соматостатинсодержащих клеток. Однако S100-содержащие клетки располагаются в таких островках не на периферии и не вдоль капилляров (в отличие от α- и δ-клеток), а совместно с β-клетками. При этом S100-клеток меньше, чем инсулинсодержащих, и только в небольшой части клеток островков обнаруживается колокализация S100 и инсулина. (стр.65): При использовании двойного окрашивания была выявлена четкая колокализация S100 и NSE в клетках островков, при этом общее количество S100+клеток было гораздо меньше, чем NSE+клеток. Таким образом, наличие или отсутствие в клетках белка S100 может быть связано с различным функциональным состоянием гормонпродуцирующих клеток. Однако, чтобы подтвердить эту гипотезу, требуются физиологические эксперименты.
Островки ПЖ — это функциональные единицы секреции, где активность между β-клетками координирует одновременный выброс инсулина. Секреторный ответ целого островка больше, чем сумма ответов отдельных β--клеток. Исследования последнего времени выявили экспрессию внеклеточного кальцийчувствительного рецептора (CaSR) β-клеток у грызунов и человека [21]. Рецептор выявляет небольшие локальные изменения свободного кальция, которые происходят сразу после введения питательных веществ и/или непищевой стимуляции. Данные подтверждают возможность того, что CaSR обеспечивает альтернативный механизм аутокринной и паракринной регуляции между β-клетками. Некоторые из S100-белков как раз регулируют функции клеток благодаря активации поверхностных рецепторов.
Поэтому, учитывая функции кальцийсвязывающего белка S100 в ЦНС [13, 14], мы можем предположить, что S100+клетки островков Лангерганса 2-го типа играют роль и в синхронизации выделения эндокринных гормонов, так как этот процесс носит кальцийзависимый характер [21].
Заключение. Установлено существование в поджелудочной железе человека двух типов S100-позитивных клеток. Эти клетки были обнаружены у людей разного возраста начиная с раннефетального периода развития. Мы предполагаем, что клетки 1-го типа, расположенные на периферии островков, являются глиальными и необходимы при формировании клеточной архитектуры островков. Клетки 2-го типа, расположенные внутри островков, возможно, играют роль пейсмекеров, регулируя согласованный выброс гормонов эндокринными клетками. Требуется дальнейшее изучение функций этих клеток в эндокринной части поджелудочной железы с целью установления возможности использования полученных данных в терапии сахарного диабета.
Финансирование исследования. Исследование поддержано специализированным фондом управления целевым капиталом для поддержки научно-исследовательских работ в области биологии и медицины «Фундаментальный» и частично поддержано грантом РФФИ №15-04-03155.
Конфликт интересов. Авторы подтверждают отсутствие конфликта интересов.
Литература
- IDF Diabetes Atlas. 6-th ed. Brussels: International Diabetes Federation; 2013; 159 p.
- Дедов И.И., Балаболкин М.И., Клебанова Е.М. Современные аспекты трансплантации островков поджелудочной железы при сахарном диабете. Сахарный диабет 2004; 2: 34–41.
- Scheen A.J. Diabetes mellitus in the elderly: insulin resistance and/or impaired insulin secretion? Diabetes & Metabolism 2005; 31(1): 5S27–5S34, http://dx.doi.org/10.1016/s1262-3636(05)73649-1.
- Wierup N., Svensson H., Mulder H., Sundler F. The ghrelin cell: a novel developmentally regulated islet cell in the human pancreas. Regul Pept 2002; 107(1–3): 63–69, http://dx.doi.org/10.1016/S0167-0115(02)00067-8.
- Wierup N., Sundler F., Heller R.S. The islet ghrelin cell. J Mol Endocrinol 2013; 52(1): R35–R49, http://dx.doi.org/10.1530/jme-13-0122.
- Lászik Z., Krenács T., Dobó E. S-100 protein immunoreactivity in human islets of Langerhans. Acta Morphol Hung 1989; 37(1–2): 117–124.
- Takayanagi M., Watanabe T. Immunocytochemical colocalizations of insulin, aromatic L-amino acid decarboxylase, dopamine beta-hydroxylase, S-100 protein and chromogranin A in B-cells of the chicken endocrine pancreas. Tissue Cell 1996; 28(1): 17–24, http://dx.doi.org/10.1016/S0040-8166(96)80040-1.
- Uchida T., Endo T. Identification of cell types containing S-100b protein-like immunoreactivity in the islets of Langerhans of the guinea pig pancreas with light and electron microscopy. Cell Tissue Res 1989; 255(2): 379–384, http://dx.doi.org/10.1007/bf00224121.
- Sunami E., Kanazawa H., Hashizume H., Takeda M., Hatakeyama K., Ushiki T. Morphological characteristics of Schwann cells in the islets of Langerhans of the murine pancreas. Arch Histol Cytol 2001; 64(2): 191–201, http://doi.org/10.1679/aohc.64.191.
- Girod C., Durand N., Raccurt M. Immunostaining of a cell type in the islets of Langerhans of the monkey Macaca irus by antibodies against S-100 protein. Cell Tissue Res 1987; 247(1): 11–16, http://dx.doi.org/10.1007/bf00216541.
- Fujita T. Histological studies on the neuro-insular complex in the pancreas of some mammals. Z Zellforsch Mikrosk Anat 1959; 50: 94–109, http://dx.doi.org/10.1007/bf00342656.
- Proshchina A.E., Krivova Y.S., Barabanov V.M., Saveliev S.V. Ontogeny of neuro-insular complexes and islets innervation in the human pancreas. Front Endocrinol 2014; 5: 57, http://dx.doi.org/10.3389/fendo.2014.00057.
- Donato R., Cannon B.R., Sorci G., Riuzzi F., Hsu K., Weber D.Y., Geczy C.L. Functions of S100 proteins. Curr Mol Med 2013; 13(1): 24–57, http://dx.doi.org/10.2174/1566524011307010024.
- Donato R., Sorci G., Riuzzi F., Arcuri C., Bianchi R., Brozzi F., Tubaro C., Giambanco I. S100B’s double life: intracellular regulator and extracellular signal. Biochim Biophys Acta 2009; 1793(6): 1008–1022, http://dx.doi.org/10.1016/j.bbamcr.2008.11.009.
- Fujita T., Iwanaga T., Nakajima T. Immunohistochemical detection of nervous system-specific proteins in normal and neoplastic paraneurons in the gut and pancreas. In: Gut peptides and ulcer. Miyoshi A. (editor). Tokyo: Biomedical Research Foundation; 1983; p. 81–88.
- Proshchina A.E., Savel’yev S.V. Immunohistochemical study of α- and β-cell distribution in human pancreatic Langerhans islets of various types. Bull Exp Biol Med 2013; 155(6): 798–801, http://dx.doi.org/10.1007/s10517-013-2255-5.
- Jeon J., Correa-Medina M., Ricordi C., Edlund H., Diez J.A. Endocrine cell clustering during human pancreas development. J Histochem Cytochem 2009; 57(9): 811–824, http://dx.doi.org/10.1369/jhc.2009.953307.
- De Krijger R.R., Aanstoot H.J., Kranenburg G., Reinhard M., Visser W.J., Bruining G.J. The midgestational human fetal pancreas contains cells coexpressing islet hormones. Dev Biol 1992; 153(2): 368–375, http://dx.doi.org/10.1016/0012-1606(92)90121-V.
- Piper K., Brickwood S., Turnpenny L.W., Cameron I.T., Ball S.G., Wilson D.I., Hanley N.A. Beta cell differentiation during early human pancreas development. J Endocrinol 2004; 181(1): 11–23, http://dx.doi.org/10.1677/joe.0.1810011.
- Meier J.J., Köhler C.U., Alkhatib B., Sergi C., Junker T., Klein H.H., Schmidt W.E., Fritsch H. Beta-cell development and turnover during prenatal life in humans. Eur J Endocrinol 2010; 162(3): 559–568, http://dx.doi.org/10.1530/EJE-09-1053.
- Squires P.E., Jones P.M., Younis M.Y., Hills C.E. The calcium-sensing receptor and β-cell function. Vitam Horm 2014; 95: 249–267, http://dx.doi.org/10.1016/B978-0-12-800174-5.00010-7.