Кросс-поляризационная ОКТ в оценке динамики состояния патологических и нормальных тканей при проведении лучевой и фотодинамической терапии
Цель исследования — оценить возможности применения кросс-поляризационной оптической когерентной томографии (КП ОКТ) для мониторинга эффективности лечения рака полости рта, кожи и шейки матки после фотодинамической (ФДТ) и лучевой терапии (ЛТ).
Материалы и методы. КП ОКТ-исследование выполняли с использованием установки «ОКТ-1300У» (ИПФ РАН, ООО «Биомедтех», Россия). Мониторинг двух видов лечения проводили на разных сроках воздействия: при ЛТ рака полости рта — один раз в 2–3 дня на протяжении всего курса лечения, начиная с первого дня облучения; при ФДТ рака кожи и шейки матки — до воздействия, непосредственно после воздействия, через 1 сут, 7 сут и 1 мес после воздействия. Всего обследовано 14 пациентов.
Результаты. Данные изучения лечебного патоморфоза разного вида опухолей, проведенного у 14 пациентов, показали, что визуальная оценка КП ОКТ-изображений опухоли не выявляет видимых изменений в ответ на ЛТ, однако обнаруживает реакцию нормальной слизистой оболочки, попавшей в зону облучения. В ходе ФДТ опухолей кожи и слизистой оболочки шейки матки (отек, некроз, восстановление структуры) КП ОКТ способна детектировать ключевые морфологические изменения. Наиболее эффективно она может быть использована на поздних сроках наблюдения (через 30–35 дней после ФДТ) для оценки полноценности восстановления стромального компонента тканей.
Заключение. Применение КП ОКТ способствует реализации неинвазивного мониторинга ответа опухоли и прилежащих нормальных тканей на проведение ФДТ и ЛТ, что может быть полезным для оценки эффективности терапии с целью выбора оптимальной тактики лечения.
Основной тенденцией современной клинической онкологии является персонифицированный подход к больному, т.е. назначение и коррекция лечения в соответствии с индивидуальными биологическими свойствами опухоли и ее чувствительностью к конкретным терапевтическим воздействиям. Известно, что в опухоли на фоне лечения возникает последовательный комплекс изменений, получивший название «ответ опухоли» (tumor response) — терапевтический патоморфоз [1], при этом изменениям размера и структуры опухоли предшествуют более слабые и более ранние изменения ткани на молекулярно-метаболическом уровне [2]. Изучение подобных изменений может дать ценную информацию о чувствительности опухоли к лечебному воздействию и существенно расширить возможности индивидуализации терапии. Разработка способов ранней оценки ответа новообразования на лечение является одним из приоритетных направлений современной онкологии.
В связи с этим все более широкое применение находят методы метаболической и функциональной визуализации, которые позволяют оценить динамику биологической активности опухолей еще до появления в них структурных изменений. К таким методам относятся позитронно-эмиссионная томография (ПЭТ) [3, 4] и магнитно-резонансная томография (МРТ) [5–9]. В настоящее время начаты работы по изучению состояния сосудистой системы и метаболизма опухолей в процессе лучевой терапии (ЛТ) с использованием микро-КТ и микро-ПЭТ, а также высокочастотного ультразвука [10–14].
В последние годы для оценки динамики метаболической активности опухолевого процесса на фоне лечения активно применяются методы биофотоники [15–24].
Метод оптической когерентной томографии (ОКТ), основанный на приеме и анализе обратно рассеянного тканями низкокогерентного излучения ближнего ИК-диапазона, позволяет изучить внутреннюю структуру поверхностных слоев биотканей [25, 26] и используется в клинической практике для диагностики широкого спектра патологических процессов [27]. Одним из перспективных клинических приложений ОКТ является мониторинг состояния злокачественных новообразований в процессе лечения и после его окончания [27–30]. Изучение состояния нормальных тканей, подвергающихся воздействию ионизирующего излучения в процессе лечения злокачественных новообразований, является не менее важной задачей, чем поиск минимальных изменений опухолевой ткани [28, 29].
В настоящем исследовании в качестве инструмента, позволяющего изучать ранние изменения в опухолевых и нормальных прилежащих тканях, подвергающихся противоопухолевому лечению, используется метод кросс-поляризационной оптической когерентной томографии (КП ОКТ). Этот метод дает возможность не только оценить структуру тканей, но и косвенным образом судить о состоянии соединительнотканной стромы, что расширяет его возможности в диагностике и мониторинге [31, 32].
Цель исследования — оценить возможности применения кросс-поляризационной оптической когерентной томографии для мониторинга эффективности лечения рака полости рта, кожи и шейки матки после фотодинамической и лучевой терапии.
Материалы и методы
Общие сведения о пациентах. КП ОКТ-мониторинг опухолевой ткани и нормальной слизистой оболочки полости рта был проведен 3 пациентам с гистологически подтвержденным плоскоклеточным раком полости рта. Критериями включения в исследование служили отсутствие отдаленных метастазов и общее состояние больных, соответствующее 0–1 баллам по шкале ECOG [33].
Облучение осуществлялось на линейном ускорителе Clinac-600, 6 МэВ (Varian Medical Systems, США) в режиме стандартного фракционирования до суммарно-очаговой дозы (СОД) 66–70 Гр. Степень тяжести побочных эффектов облучения определяли в соответствии со шкалой CTCAE [34]. В качестве контроля использовали КП ОКТ-изображения слизистой оболочки щеки трех здоровых добровольцев.
КП ОКТ-мониторинг при проведении ФДТ применяли у 4 пациентов с гистологически подтвержденным первичным базально-клеточным раком кожи и у 7 пациенток с предопухолевыми заболеваниями (цервикальные интраэпителиальные неоплазии — cervical intraepithelial neoplasia, CIN) и ранним (внутриэпителиальным — cancer in situ, CIS) раком шейки матки без предшествующего лечения (CIN II–III — у 4 человек, рак in situ — у 3, средний возраст — 32 года).
ФДТ проводили по стандартной методике [35]. Лазерное воздействие выполняли с использованием полупроводникового источника лазерного излучения «Лахта-Милон», 662 нм («Милон», Россия). Параметры воздействия для шейки матки: плотность мощности — 0,28 Вт/см2, плотность дозы — 150 Дж/см2; для кожи: плотность мощности — 0,30 Вт/см2, плотность дозы для базально-клеточного рака — 200 Дж/см2.
Исследование проведено в соответствии с Хельсинкской декларацией (принятой в июне 1964 г. (Хельсинки, Финляндия) и пересмотренной в октябре 2000 г. (Эдинбург, Шотландия)) и одобрено Этическим комитетом НижГМА. От каждого пациента получено информированное согласие.
Технические характеристики прибора КП ОКТ. Работа выполнена на кросс-поляризационном оптическом когерентном томографе «ОКТ-1300У», разработанном и сконструированном в Институте прикладной физики РАН (Н. Новгород, Россия) со следующими основными техническими параметрами: длина волны зондирования — 1,3 мкм, пространственное разрешение — 15–25 мкм, глубина зондирования ~1,7 мм; скорость получения изображения — 1 кадр/с. Прибор оснащен гибким эндоскопическим торцевым зондом с размером поперечного сканирования около 2 мм.
Методика КП ОКТ-исследования пациентов. В случае применения ЛТ КП ОКТ-мониторинг проводили один раз в 2–3 дня на протяжении всего курса лечения, начиная с первого дня облучения. Отдельно оценивалась динамика КП ОКТ-изображений опухолей полости рта и нормальной слизистой оболочки полости рта, попадающей в зону воздействия ионизирующего излучения. В качестве стандартных зон сканирования нормальной слизистой оболочки были выбраны реперные точки слизистой оболочки средней зоны щеки, так как они легкодоступны для проведения КП ОКТ-исследования и изображения отличаются отчетливой слоистой структурой.
Исследование опухолей полости рта начинали с визуального осмотра, фотографирования очага и определения точек сканирования (условные 3, 6, 9, 12 ч, центр опухоли и неизмененная слизистая оболочка на границе с опухолью). Для получения КП ОКТ-изображений стерильный торцевой зонд подводили непосредственно к интересующему участку.
КП ОКТ-мониторинг в случае применения ФДТ проводили до начала лечения, непосредственно после осуществления процедуры, на ранних этапах динамического наблюдения (через 1 и 7 сут после ФДТ) и на поздних этапах динамического наблюдения (через 1 мес после ФДТ). Затем из области КП ОКТ-исследования выполняли биопсию для проведения морфологического анализа.
Оценка КП ОКТ-изображений заключалась в описании визуальных признаков КП ОКТ-изображений в исходной и ортогональной поляризации. Оценивали следующие параметры: интенсивность ОКТ-сигнала, его однородность, глубину проникновения ОКТ-сигнала, слоистость изображения.
Результаты
Исследование возможностей КП ОКТ для оценки раннего ответа опухолей и прилежащих тканей полости рта на проводимую ЛТ. Визуально плоскоклеточный рак слизистой оболочки полости рта до облучения чаще выглядит как экзофитное образование с бугристой поверхностью, цвет может быть различным — от бледно- до темно-розового. Граница между опухолью и окружающими здоровыми тканями, как правило, определяется нечетко (рис. 1, а).
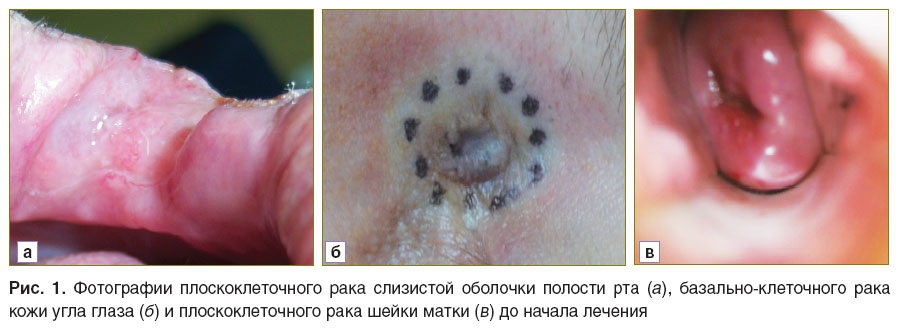 |
Рис. 1. Фотографии плоскоклеточного рака слизистой оболочки полости рта (а), базально-клеточного рака кожи угла глаза (б) и плоскоклеточного рака шейки матки (в) до начала лечения |
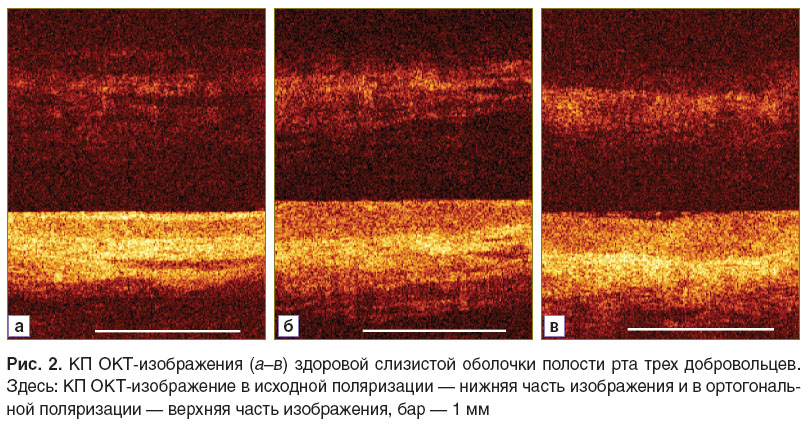
Для КП ОКТ-изображений здоровой слизистой оболочки полости рта (рис. 2) в исходной поляризации характерна слоистая структура, где хорошо визуализируются три контрастных горизонтально ориентированных слоя, соответствующих многослойному плоскому неороговевающему эпителию, соединительнотканной строме, в которой могут визуализироваться области с низким уровнем сигнала различной формы, резкими или слегка размытыми границами, и подслизистому слою с умеренно интенсивным сигналом.
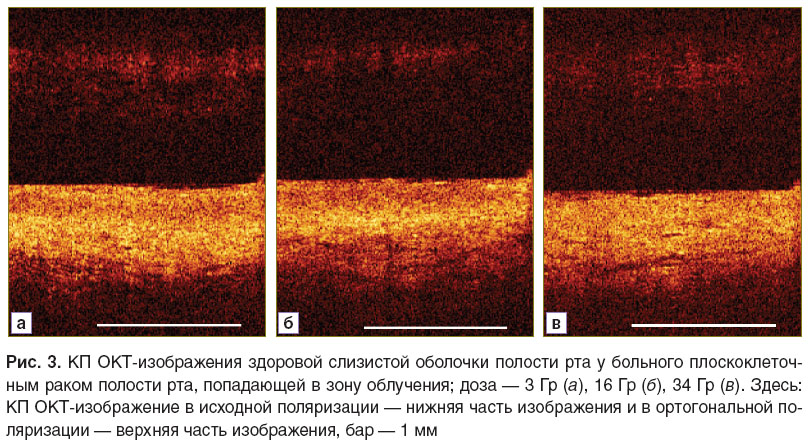
При изучении динамики КП ОКТ-изображений нормальной слизистой оболочки у пациентов в процессе ЛТ новообразований полости рта обнаружено, что изменения на изображениях появлялись уже после первого сеанса облучения при отсутствии клинических проявлений лучевой реакции. В исходной поляризации наблюдалось снижение четкости границы между эпителием и подлежащей соединительной тканью и уменьшение контраста этих слоев на КП ОКТ-изображениях, а также уменьшение толщины эпителиального слоя (рис. 3). В процессе ЛТ структурность КП ОКТ-изображений в исходной поляризации продолжала снижаться, при этом на максимуме интенсивности лучевой реакции (после подведения к опухоли СОД 24–36 Гр) изображения характеризовались полной потерей слоистой структуры в исходной поляризации и существенным снижением интенсивности сигнала — в ортогональной.
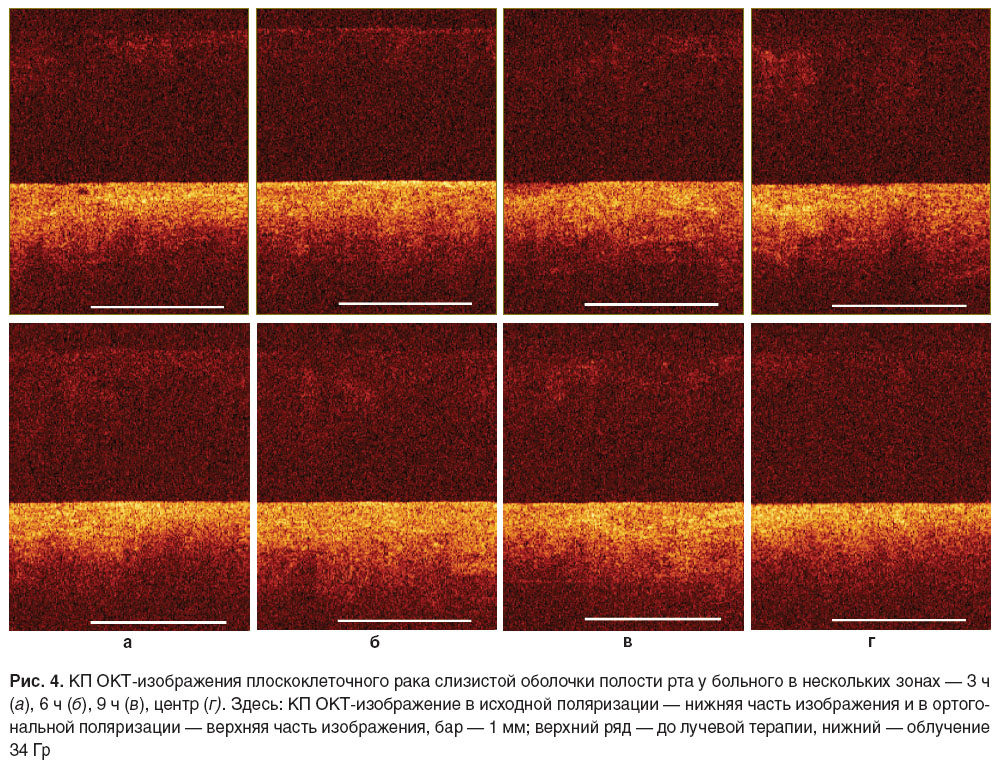
Для опухолевой ткани в исходной поляризации характерно отсутствие структурных КП ОКТ-изображений, на них не удается визуализировать соответствующие слои (рис. 4). В ортогональной поляризации сигнал на изображениях практически полностью отсутствует. Визуальная оценка КП ОКТ-изображений опухолевой ткани в динамике не позволила выявить изменений даже при подведении более половины запланированной дозы.
Исследование возможностей КП ОКТ для оценки раннего ответа опухоли и нормальной кожи на ФДТ. Визуально до начала терапии базально-клеточный рак кожи выглядит как экзофитное образование, часто — с валикообразной эрозией, подрытыми краями светло-коричневого или розового цвета. Граница между опухолью и окружающими здоровыми тканями, как правило, хорошо определяется (см. рис. 1, б).
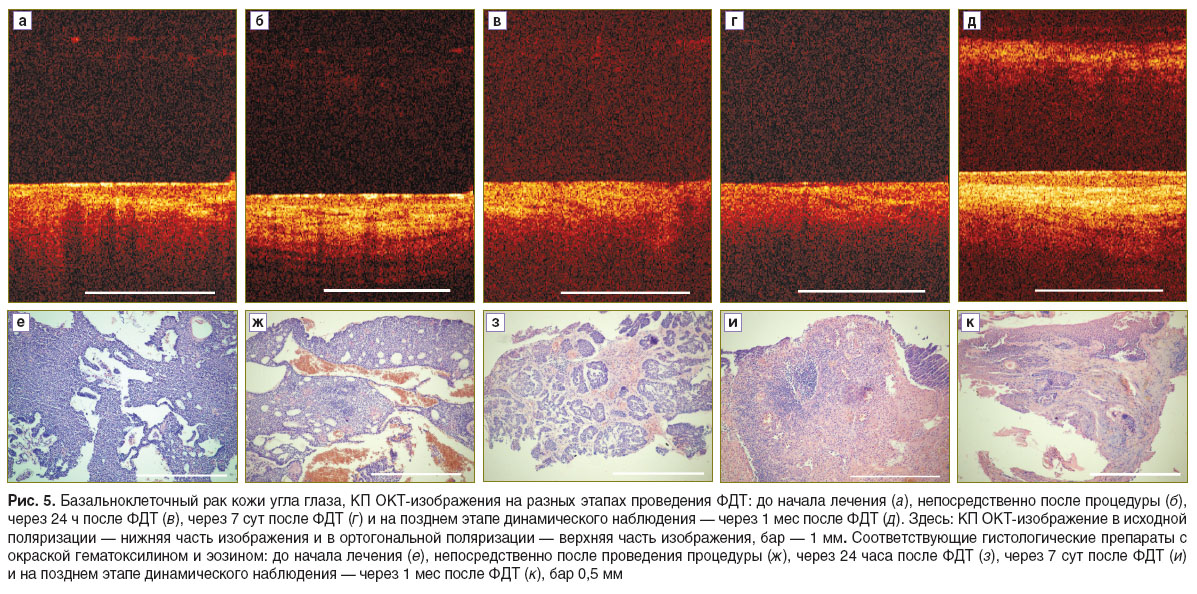
До проведения ФДТ получены типичные КП ОКТ-изображения опухоли кожи (рис. 5, а). В исходной поляризации визуализируется нарушенная слоистая структура, что соответствует наличию групп базалоидных клеток на гистологическом препарате (рис. 5, е). В ортогональной поляризации — сигнал отсутствует, что в свою очередь указывает на отсутствие или незрелость деполяризующих структур соединительной ткани (коллагеновых волокон) (см. рис. 5, е).
Непосредственно после завершения процедуры лазерного воздействия (рис. 5, б) в исходной поляризации КП ОКТ-изображения отмечается увеличение глубины проникновения сигнала, визуализируются участки чередования более сильного и слабого сигнала неправильных очертаний с нечеткими границами, подтверждая наличие отека на гистологическом препарате (рис. 5, ж); в ортогональной поляризации — сигнал на изображении отсутствует.
Через 24 ч на КП ОКТ-изображении (рис. 5, в) в исходной поляризации отмечаются нарушенная слоистая структура ткани и признаки отека, что подтверждается на гистологическом препарате (рис. 5, з); в ортогональной поляризации сохраняется отсутствие сигнала.
Через 7 сут (морфологически соответствует некрозу (рис. 5, и)) на КП ОКТ-изображении (рис. 5, г) в исходной поляризации отмечается отсутствие структур с умеренным или высоким уровнем сигнала, особенно на поверхности изображения. Наблюдается равномерное, быстрое затухание сигнала на глубину кадра. В ортогональной поляризации сигнал отсутствует.
Через 1 мес на КП ОКТ-изображении (рис. 5, д) в исходной поляризации — восстановление слоистой структуры ткани с интенсивным уровнем сигнала, в ортогональной поляризации обнаруживается интенсивный сигнал, что указывает на появление или созревание деполяризующих структур (коллагеновых волокон) и соответствует формированию соединительнотканного рубца на гистологическом препарате (рис. 5, к).
Исследование возможностей КП ОКТ для оценки раннего ответа опухоли и нормальной прилежащей ткани шейки матки на ФДТ. Наиболее частыми визуальными характеристиками плоскоклеточного рака шейки матки являются ее деформация и локальная гиперемия экзоцервикса, а кольпоскопические проявления ранних форм неоплазии известны как атипические кольпоскопические признаки (рис. 1, в).
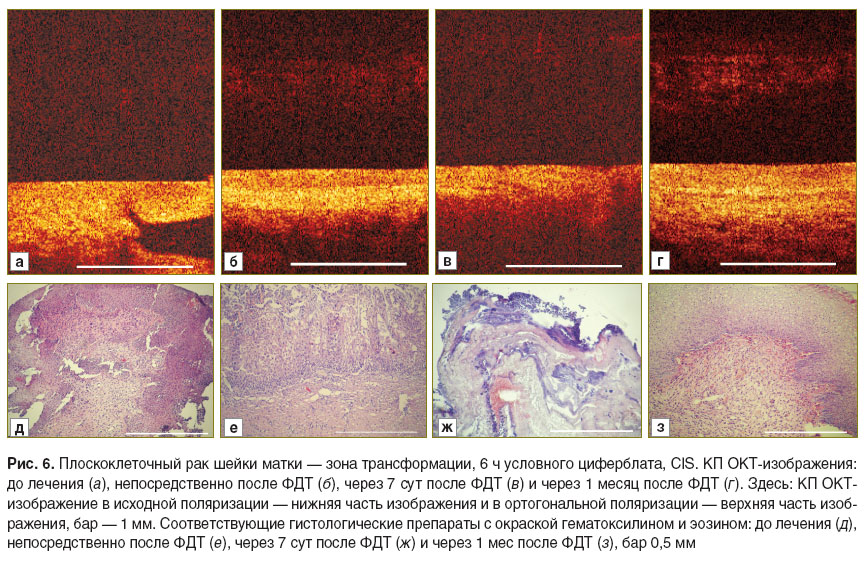
Для КП ОКТ-изображений зоны опухоли до ФДТ (рис. 6, а) характерен интенсивный сигнал без визуализации слоев в исходной поляризации и отсутствие сигнала — в ортогональной поляризации. Низкоинтенсивная контрастная зона, по всей вероятности, соответствует железе с открытым протоком. На гистологическом препарате плоскоклеточный рак шейки матки характеризуется наличием атипичных, полиморфных клеток многослойного плоского эпителия, формирующих группы и поля, разделенные узкими прослойками фиброзной ткани. Видно небольшое количество мелких кровеносных сосудов (рис. 6, д).
Находкой стало появление слоистости в зоне опухоли непосредственно после ФДТ (рис. 6, б), что может быть объяснено контрастирующим эффектом характерного для данного срока наблюдения отека ткани (рис. 6, е). Также на гистологическом препарате местами видны едва заметные мелкие полнокровные кровеносные сосуды.
Через 7 сут, когда морфологически отмечается тотальный некроз опухоли (рис. 6, ж), на КП ОКТ-изображении наблюдаются типичное повышение интенсивности сигнала в исходной поляризации и полная потеря сигнала в ортогональной поляризации (рис. 6, в).
Через 1 мес после ФДТ визуализируется практически полное восстановление структуры шейки матки, однако эпителий остается незрелым (рис. 6, з), что обусловливает отсутствие четкой слоистости КП ОКТ-изображения (рис. 6, г). Достаточно интенсивный сигнал в ортогональной поляризации говорит о восстановлении способности коллагена к деполяризации.
Обсуждение. Полученные результаты позволяют нам сделать предварительные выводы о целесообразности применения КП ОКТ для прижизненного мониторинга различных видов лечения поверхностных опухолей наружной локализации. В то же время проведенная ограниченная серия исследований выдвигает ряд новых вопросов, требующих дальнейшего изучения.
Так, нами обнаружено, что при контроле результатов ЛТ КП ОКТ информативна только относительно окружающих тканей, в то время как при мониторинге результатов ФДТ метод способен визуализировать изменения и в фокусе опухоли, и в перифокальной зоне. Причем полученные КП ОКТ-изображения неизмененной кожи, находящейся на границе с опухолью и попадающей в зону ФДТ, до лечения демонстрируют наличие структурности в прямой поляризации и сигнала — в ортогональной поляризации (что отражает свойства здоровой ткани) и сохранение этих признаков на 7-е сутки после ФДТ (что может свидетельствовать о сохранности коллатеральной зоны). При мониторинге ФДТ неоплазии шейки матки мы наблюдали, что на КП ОКТ-изображениях неизмененной слизистой оболочки шейки матки, попадающей в зону ФДТ, аналогично изображениям кожи, до лечения в прямой поляризации визуализируются характерная для здоровой ткани слоистость и наличие сигнала в ортогональной поляризации. Но в отличие от кожи эти признаки не сохраняются на 7-е сутки после ФДТ, что свидетельствует о вероятном повреждении коллатеральной зоны.
Отсутствие очевидных изменений на КП ОКТ-изображениях опухолей слизистой оболочки полости рта в процессе ЛТ может быть связано с несколькими факторами. Во-первых, жизнеспособная опухолевая ткань и опухолевая ткань в состоянии дистрофии и некроза могут иметь общие визуальные ОКТ-признаки, что не позволяет дифференцировать начавшиеся процессы регресса новообразования. Во-вторых, в ранние сроки от момента начала ЛТ еще не происходит формирования упорядоченной структуры соединительнотканного матрикса на месте опухоли, что является причиной существенного снижения сигнала на ортогональных КП ОКТ-изображениях. По нашему мнению, продолжение мониторинга в более поздние сроки позволит зафиксировать характерные изменения КП ОКТ-изображений и в зоне опухоли. Для большей информативности и объективизации данных целесообразно провести дополнительную обработку полученных результатов с расчетом численных параметров КП ОКТ-изображений.
Относительно различной динамики оптических характеристик пограничных зон кожи и слизистой оболочки шейки матки после ФДТ разумно предположить, что существуют различия для этих органов в контрасте накопления фотосенсибилизатора, что приводит к демонстрации поражения коллатеральной зоны при ФДТ опухоли шейки матки. Но КП ОКТ-контроль отдаленных результатов (через 1 мес после ФДТ) свидетельствует о восстановлении свойств здоровых тканей как в зоне опухоли, так и в прилежащих областях в обеих локализациях. Для подтверждения данного наблюдения требуется продолжение исследований с применением комбинированного мониторинга — сочетание КП ОКТ- и флюоресцентной визуализации. Однако уже на данном этапе не вызывает сомнений целесообразность КП ОКТ-мониторинга окружающих нормальных тканей с позиций прогнозирования реальной зоны повреждения, оценки качества рубца, функциональных и косметических результатов лечения. Анализ поляризационной составляющей ОКТ, несомненно, может быть полезным для ранней диагностики рецидива опухоли в рубце и выбора оптимальных зон биопсии для морфологического контроля.
Заключение. Использование КП ОКТ в клинических условиях для изучения лечебного патоморфоза в опухолях и оценки реакции окружающих нормальных тканей в ответ на лучевую и фотодинамическую терапию имеет большие перспективы. При дальнейшем развитии метод может стать неинвазивной альтернативой морфологическому исследованию серийных биоптатов в целях контроля непосредственных и отдаленных результатов лечения. Привлекательно использование неинвазивного КП ОКТ-исследования как на этапах планирования терапии, так и на фоне лечения для оценки эффективности первичных реакций с целью персонификации режимов воздействия. Для реализации этих подходов исследования будут продолжены.
Финансирование исследования. Исследования финансировались по программе Правительства РФ, договор №14.В25.31.0015.
Конфликт интересов. У авторов нет конфликта интересов.
Литература
- Грабовой А.Н., Тарасова Т.О., Кошубарова М.В. Гистологическая оценка ответа опухоли на химио-/лучевую терапию. Клиническая онкология 2012; 6(2): 138–143.
- Tannock I.F., Lee C. Evidence against apoptosis as a major mechanism for reproductive cell death following treatment of cell lines with anti-cancer drugs. Br J Cancer 2001; 84(1): 100–105, http://dx.doi.org/10.1054/bjoc.2000.1538.
- Postema E.J., McEwan A.J.B., Riauka T.A., Kumar P., Richmond D.A., Abrams D.N., Wiebe L.I. Initial results of hypoxia imaging using 1-α-D-(5-deoxy-5-[18F]-fluoroarabinofuranosyl)-2-nitroimidazole (18F-FAZA). Eur J Nucl Med Mol Imaging 2009; 36(10): 1565–1573, http://dx.doi.org/10.1007/s00259-009-1154-5.
- Grosu A.L., Souvatzoglou M., Röper B., Dobritz M., Wiedenmann N., Jacob V., Wester H.J., Reischl G., Machulla H.J., Schwaiger M., Molls M., Piert M. Hypoxia imaging with FAZA-PET and theoretical considerations with regard to dose painting for individualization of radiotherapy in patients with head and neck cancer. Int J Radiat Oncol Biol Phys 2007; 69(2): 541–551, http://dx.doi.org/10.1016/j.ijrobp.2007.05.079.
- Gilad A.A., Israely T., Dafni H., Meir G., Cohen B., Neeman M. Functional and molecular mapping of uncoupling between vascular permeability and loss of vascular maturation in ovarian carcinoma xenografts: the role of stroma cells in tumor angiogenesis. Int J Cancer 2005; 117(2): 202–211, http://dx.doi.org/10.1002/ijc.21179.
- Kiessling F., Huppert J., Zhang C., Jayapaul J., Zwick S., Woenne E.C., Mueller M.M., Zentgraf H., Eisenhut M., Addadi Y., Neeman M., Semmler W. RGD-labeled USPIO inhibits adhesion and endocytotic activity of alpha v beta3-integrin-expressing glioma cells and only accumulates in the vascular tumor compartment. Radiology 2009; 253(2): 462–469, http://dx.doi.org/10.1148/radiol.2532081815.
- Frascione D., Diwoky C., Almer G., Opriessnig P., Vonach C., Gradauer K., Leitinger G., Mangge H., Stollberger R., Prassl R. Ultrasmall superparamagnetic iron oxide (USPIO)-based liposomes as magnetic resonance imaging probes. Int J Nanomedicine 2012; 7: 2349–2359, http://dx.doi.org/10.2147/IJN.S30617.
- Tripathy D., Jiang L., Rao N., McColl R., Xie X., Weatherall P., Story M., Ding L., Mason R. Blood oxygen level dependent (BOLD) contrast MRI and breast cancer chemotherapy response. J Clin Oncol (Meeting Abstracts) 2006; 24(18 Suppl): 10514.
- Warren R., Hayes C., Pointon L., Hoff R., Gilbert F.J., Padhani A.R., Rubin C., Kaplan G., Raza K., Wilkinson L., Hall-Craggs M., Kessar P., Rankin S., Dixon A.K., Walsh J., Turnbull L., Britton P., Sinnatamby R., Easton D., Thompson D., Lakhani S.R., Leach M.O.; UK MRC study of MRI screening for breast cancer in women at high risk (MARIBS). A test of performance of breast MRI interpretation in a multicentre screening study. Magn Reson Imaging 2006; 24(7): 917–929, http://dx.doi.org/10.1016/j.mri.2006.03.004.
- Pantaleo M.A., Nannini M., Maleddu A., Fanti S., Nanni C., Boschi S., Lodi F., Nicoletti G., Landuzzi L., Lollini P.L., Biasco G. Experimental results and related clinical implications of PET detection of epidermal growth factor receptor (EGFr) in cancer. Ann Oncol 2009; 20(2): 213–226, http://dx.doi.org/10.1093/annonc/mdn625.
- Weber B., Winterdahl M., Memon A., Sorensen B.S., Keiding S., Sorensen L., Nexo E., Meldgaard P. Erlotinib accumulation in brain metastases from non-small cell lung cancer: visualization by positron emission tomography in a patient harboring a mutation in the epidermal growth factor receptor. J Thorac Oncol 2011; 6(7): 1287–1289, http://dx.doi.org/10.1097/JTO.0b013e318219ab87.
- Gupta S., Siddiqui S., Haldar P., Raj J.V., Entwisle J.J., Wardlaw A.J., Bradding P., Pavord I.D., Green R.H., Brightling C.E. Qualitative analysis of high-resolution CT scans in severe asthma. Chest 2009; 136(6): 1521–1528, http://dx.doi.org/10.1378/chest.09-0174.
- Bussink J., Kaanders J.H., van der Graaf W.T., Oyen W.J. PET-CT for radiotherapy treatment planning and response monitoring in solid tumors. Nat Rev Clin Oncol 2011; 8(4): 233–242, http://dx.doi.org/10.1038/nrclinonc.2010.218.
- Kolios M.C., Czarnota G.J., Lee M., Hunt J.W., Sherar M.D. Ultrasonic spectral parameter characterization of apoptosis. Ultrasound Med Biol 2002; 28(5): 589–597, http://dx.doi.org/10.1016/S0301-5629(02)00492-1.
- Tromberg B.J., Pogue B.W., Paulsen K.D., Yodh A.G., Boas D.A., Cerussi A.E. Assessing the future of diffuse optical imaging technologies for breast cancer management. Med Phys 2008; 35(6): 2443–2451, http://dx.doi.org/10.1118/1.2919078.
- Maslennikova A., Orlova A., Golubjatnikov G., Kamensky V., Plekhanov V., Shakhova N., Snopova L., Babaev A., Prjanikova T. Noninvasive detection of tumour’s oxygen status using diffuse optical tomography. EJC Supplements 2009; 7(2): 160, http://dx.doi.org/10.1016/S1359-6349(09)70545-2.
- Zhu Q., DeFusco P.A., Ricci A. Jr., Cronin E.B., Hegde P.U., Kane M., Tavakoli B., Xu Y., Hart J., Tannenbaum S.H. Breast cancer: assessing response to neoadjuvant chemotherapy by using US-guided near-infrared tomography. Radiology 2013; 266(2): 433–442, http://dx.doi.org/10.1148/radiol.12112415.
- Cerussi A.E., Tanamai V.W., Hsiang D., Butler J., Mehta R.S., Tromberg B.J. Diffuse optical spectroscopic imaging correlates with final pathological response in breast cancer neoadjuvant chemotherapy. Philos Trans A Math Phys Eng Sci 2011; 369(1955): 4512–4530, http://dx.doi.org/10.1098/rsta.2011.0279.
- Chung S.H., Yu H., Su M.-Y., Cerussi A. E., Tromberg B.J. Molecular imaging of water binding state and diffusion in breast cancer using diffuse optical spectroscopy and diffusion weighted MRI. J Biomed Opt 2012; 17(7): 071304, http://dx.doi.org/10.1117/1.JBO.17.7.071304.
- O’Sullivan T., Leproux A., Chen J., Bahri S., Matlock A., Roblyer Darren, McLaren C.E., Chen W., Cerussi A., Su M., Tromberg B.J. Optical imaging correlates with magnetic resonance imaging breast density and reveals composition changes during neoadjuvant chemotherapy. Breast Cancer Rese 2013; 15(1): R14, http://dx.doi.org/10.1186/bcr3389.
- Ueda S., Saeki T. Near-infrared optical imaging of cancer vascular remodeling after antiangiogenic therapy. Breast Cancer 2014; 21(6): 776–769, http://dx.doi.org/10.1007/s12282-014-0534-2.
- Xiang L., Xing D., Gu H., Yang D., Yang S., Zeng L., Chen W.R. Real-time optoacoustic monitoring of vascular damage during photodynamic therapy treatment of tumor. J Biomed Opt 2007; 12(1): 014001, http://dx.doi.org/10.1117/1.2437752.
- Chen B., Crane C., He C., Gondek D., Agharkar P., Savellano M.D., Hoopes P.J., Pogue B.W. Disparity between prostate tumor interior versus peripheral vasculature in response to verteporfin-mediated vascular-targeting therapy. Int J Cancer 2008; 123(3): 695–701, http://dx.doi.org/10.1002/ijc.23538.
- Ueda S., Roblyer D., Cerussi A., Durkin A., Leproux A., Santoro Y., Xu S., O'Sullivan T.D., Hsiang D., Mehta R., Butler J., Tromberg B.J. Baseline tumor oxygen saturation correlates with a pathologic complete response in breast cancer patients undergoing neoadjuvant chemotherapy. Cancer Res 2012; 72(17): 4318–4328, http://dx.doi.org/10.1158/0008-5472.CAN-12-0056.
- Huang D., Swanson E.A., Lin C.P., Schuman J.S., Stinson W.G., Chang W., Hee M.R., Flotte T., Gregory K., Puliafito C.A., et al. Optical coherence tomography. Science 1991; 254(5035): 1178–1181, http://dx.doi.org/10.1126/science.1957169.
- Fercher A.F., Drexler W., Hitzenberger C.K., Lasser T. Optical coherence tomography — principles and applications. Rep Prog Phys 2003; 66(22): 239–303, http://dx.doi.org/10.1088/0034-4885/66/2/204.
- Фомина Ю.В., Гладкова Н.Д., Масленникова А.В., Урутина М.Н., Раденска-Лоповок С.Г., Островский А.Д., Рабинович И.М., Фельдштейн Ф.И. Оптическая когерентная томография в стоматологии. В кн.: Руководство по оптической когерентной томографии. Под ред. Гладковой Н.Д., Шаховой Н.М., Сергеева A.M. М: Физматлит, Медицинская книга; 2007; с. 203–246.
- Масленникова А.В., Балалаева И.В., Гладкова Н.Д., Карабут М.М., Киселева Е.Б., Иксанов Р.Р., Ильин Н.И. Прогнозирование степени тяжести мукозита слизистой оболочки полости рта методом оптической когерентной томографии. Вопросы онкологии 2009; 55(5): 572–579.
- Davoudi B., Lindenmaier A., Standish B.A., Allo G., Bizheva K., Vitkin A. Noninvasive in vivo structural and vascular imaging of human oral tissues with spectral domain optical coherence tomography. Biomed Opt Express 2012; 3(5): 826–839, http://dx.doi.org/10.1364/BOE.3.000826.
- Standish B.A., Lee K.K., Jin X., Mariampillai A., Munce N.R., Wood M.F., Wilson B.C., Vitkin I.A., Yang V.X. Interstitial Doppler optical coherence tomography as a local tumor necrosis predictor in photodynamic therapy of prostatic carcinoma: an in vivo study. Cancer Res 2008; 68(23): 9987–9995, http://dx.doi.org/10.1158/0008-5472.CAN-08-1128.
- Gelikonov V.M., Gelikonov G.V. New approach to cross-polarized optical coherence tomography based on orthogonal arbitrarily polarized modes. Laser Physics Letters 2006; 3(9): 445-451, http://dx.doi.org/10.1002/lapl.200610030.
- Feldchtein F.I., Gelikonov V.M., Gelikonov G.V. Polarization-sensitive common path optical coherence reflectometry/tomography device. Patent US 7,728,985 B2. 2010.
- The Eastern Cooperative Oncology Group. URL: http://ecog-acrin.org/resources/ecog-performance-status.
- Cancer Therapy Evaluation Program. Common terminology criteria for adverse events. Version 4.0. 2009. URL: http://www.nih.gov/.
- Цыб А.Ф., Каплан М.А., Романенко Ю.С. и др. Клинические аспекты фотодинамической терапии. Калуга: Издательство научной литературы Н.Ф. Бочкаревой; 2009.