Новая версия метода ДНК-комет
Цель исследования — оценить возможность использования озона для создания индуцированных повреждений ДНК в индивидуальных клетках при их анализе с помощью метода ДНК-комет.
Материалы и методы. Экспериментальные исследования выполнены на образцах цельной крови белых нелинейных интактных крыс-самцов (n=16) массой 250±25 г. Проведены две серии экспериментов по индукции повреждений ДНК в лейкоцитах на слайдах. В первой серии образцы подвергали воздействию гамма-излучения, во второй — слайды обрабатывали озонированным фосфатно-солевым буфером. Далее проводили лизис клеток, денатурацию ДНК, электрофорез, промывку, окрашивание ДНК SYBR GREEN I, флюоресцентную микроскопию и обработку изображений.
Результаты. Разработана новая версия метода ДНК-комет. Установлено, что концентрация озона в озоно-кислородной смеси 900 мкг/л и время воздействия 10 мин на клетки в слайдах оптимальны для детекции повреждений ДНК и их анализа, при этом применение озона позволяет минимизировать недостатки и ограничения использования с этой целью источника гамма-излучения.
Метод ДНК-комет, позволяющий определять уровень повреждений и репарации ДНК в отдельных неделящихся ядросодержащих клетках, впервые был разработан шведскими исследователями Остлингом и Йохансоном в 1984 г. [1, 2]. В базе данных PubMed тысячи работ посвящены применению метода в фундаментальных исследованиях и лишь десятки — в клинической медицине [1, 3–26] (рис. 1).
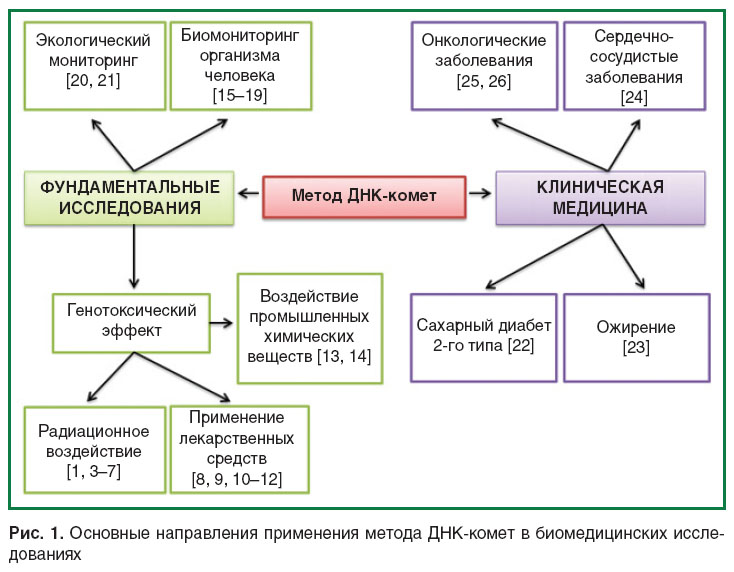 Рис. 1. Основные направления применения метода ДНК-комет в биомедицинских исследованиях Рис. 1. Основные направления применения метода ДНК-комет в биомедицинских исследованиях
|
В ряде сообщений приводятся сведения о том, что при таких заболеваниях, как ишемическая болезнь сердца, сахарный диабет 2-го типа, ожирение и злокачественные новообразования, наблюдается повышенный уровень повреждений в ДНК лейкоцитов периферической крови [22–26].
Опубликованы данные по определению базального уровня повреждений ДНК в лимфоцитах периферической крови при раке молочной железы и орофарингеальной зоны и при различных солидных опухолях на фоне лучевой, химиотерапии и химиолучевой терапии, после хирургического удаления опухоли мастэктомией и квадрантэктомией [27–30]. В исследованиях показан высокий уровень повреждений ДНК, который авторы считают серьезным фактором риска рецидива злокачественных новообразований.
В литературном обзоре, посвященном критериям использования нового метода в клинике для диагностики рака, S.E. Taube с соавт. [31] утверждает, что каждый новый диагностический способ должен пройти три основных теста, прежде чем он будет принят для рутинного клинического использования. Во-первых, он должен быть хорошо отлаженным и воспроизводимым, во-вторых, клиническое назначение способа должно быть доказано (т.е. с его помощью должен заключаться правильный диагноз, приводящий к улучшению состояния здоровья пациента), в-третьих, медицинское сообщество должно быть убеждено в необходимости использования этого способа и в преимуществах, которыми он обладает.
По мнению европейских исследователей [32, 33], метод ДНК-комет в силу своего удобства пригоден именно для использования в клинической практике — для анализа повреждений и репарации ДНК достаточно 50–100 отдельных ядросодержащих клеток. К тому же, что немаловажно, данный метод фактически является экспресс-диагностикой: результаты анализа могут быть получены в течение нескольких часов. Однако несмотря на эти преимущества, метод ДНК-комет в настоящее время все еще не используют в качестве стандартного аналитического способа в клинических лабораториях. И одной из причин этого является наличие некоторых методических трудностей, которые препятствуют хорошей воспроизводимости и отлаженности данного метода [32, 33].
В настоящее время исследователи создают индуцированные повреждения ДНК в индивидуальных клетках на слайдах рентгеновским и гамма-излучением [1, 4, 34–37]. Для обеспечения такого подхода необходимо соблюдение ряда технических требований, существенно ограничивающих широкое применение метода ДНК-комет в практической медицине [38].
В специальном выпуске Оксфордского журнала Mutagenesis профессор Норвежского университета фундаментальной медицины Andrew R. Collins призывает ученых публиковать больше материалов, посвященных развитию и модернизации метода и использованию его в относительно новых или неизученных областях исследований [39].
Все сказанное обусловливает актуальность поиска новой модификации способа создания индуцированных повреждений ДНК в индивидуальных клетках при использовании метода ДНК-комет.
Цель исследования — оценить возможность использования озона для создания индуцированных повреждений ДНК в индивидуальных клетках при их анализе с помощью метода ДНК-комет.
Материалы и методы. Эксперименты выполнены на лейкоцитах цельной крови 16 белых нелинейных интактных крыс-самцов массой 250±25 г. Взятие крови (20 мкл) производили из подъязычной вены и смешивали с 500 мкл 0,5% легкоплавкой агарозы.
Работа проведена в полном соответствии с этическими принципами, установленными Европейской конвенцией по защите позвоночных животных, используемых для экспериментальных и других научных целей (принятой в Страсбурге 18.03.1986 г. и подтвержденной в Страсбурге 15.06.2006 г.) и одобрена Этическим комитетом НижГМА.
Конечная концентрация лейкоцитов в растворе составляла 500 000 кл./мл. Такое разбавление клеток является оптимальным для того, чтобы наблюдаемые кометы равномерно располагались в поле зрения на предметном стекле. Далее готовили слайды с индивидуальными клетками в агарозном геле. Для этого на предметное стекло наносили слой 1% тугоплавкой агарозы и сушили его при комнатной температуре для лучшей адгезии следующих наносимых слоев [9, 40]. Суспензию клеток, смешанных с 500 мкл 0,5% легкоплавкой агарозы, наносили на застывший слой 1% тугоплавкой агарозы по 2 капли на стекло и накрывали покровными стеклами размером 24×24 мм. Таким образом, на каждом стекле было по 2 слайда с иммобилизованными клетками в агарозном слое. Далее после застывания слайдов в течение 4–5 мин при комнатной температуре покровные стекла снимали для дальнейших манипуляций с клетками в агарозном слое.
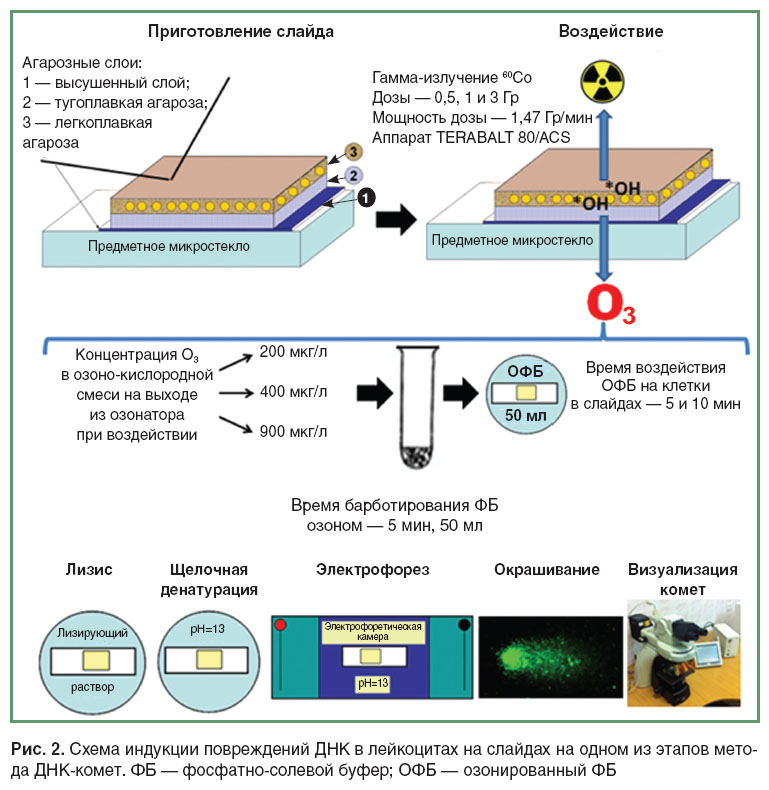
Для индукции повреждений ДНК в лейкоцитах на слайдах проводили две серии экспериментов по оригинальной схеме, представленной на рис. 2.
|
|
Основные процедуры обработки слайдов: лизис клеток в составе агарозного геля (1 ч), денатурацию ДНК, электрофорез при pH>13, промывку, окрашивание ДНК SYBR GREEN I — проводили, как указано в работе [4]. После окрашивания изображения комет фотографировали, главным образом в центральной части слайдов, где кометы располагались в одной плоскости.
Фотографирование проводили цифровой камерой серии DS, модель DS-Fi2 (Nikon Corporation, Япония), соединенной с прямым микроскопом Nikon EclipseNi-U (Nikon Corporation, Япония). Полученные изображения обрабатывали с помощью специализированного программного обеспечения Comet.exe, разработанного для регистрации и анализа отображений В.Н. Степановым [41]. Всего в эксперименте было приготовлено 68 слайдов на 34 стеклах. Анализировали по 100 комет на стекло и из полученных данных рассчитывали среднее значение для каждой экспериментальной точки. Для оценки уровня повреждений ДНК использовали параметр %TDNA — процент ДНК в хвосте кометы [1]. Контролем служили клетки без каких-либо воздействий. Полученные данные были обработаны с помощью пакетов прикладных программ Microsoft Excel 2010 и AtteStat.
Результаты и обсуждение. Известно, что воздействие ионизирующего излучения на клетки подразделяют на прямое и косвенное. В первом случае радиация напрямую взаимодействует с компонентами клетки, в частности с ДНК, повреждение которой нарушает нормальное функционирование клетки или вызывает ее гибель. В случае косвенного воздействия излучение взаимодействует с молекулами воды, которые составляют около 80% вещества клетки, что приводит к ее радиационному разложению — радиолизу воды. В результате этого процесса образуются свободные радикалы, в частности высокореакционный гидроксильный радикал ОН•, который обладает сильным цитотоксическим действием [42, 43].
Озон, реагируя с двойными связями азотистых оснований нуклеиновых кислот, образует озониды, что в конечном итоге приводит к образованию однонитевых или двойных разрывов в спиралях [44, 45]. В водных же растворах происходит спонтанное разложение озона и его реакция с ионом гидроксила ОН–, который образуется в воде за счет диссоциации части ее молекул. Ион гидроксила легко и быстро реагирует с озоном по достаточно сложному многостадийному механизму с образованием свободных радикалов ОН• и ОН2• [46]. Радикалы ОН• в свою очередь взаимодействуют с дезоксирибозой, входящей в состав нуклеиновых кислот, и это взаимодействие лежит в основе мутагенного действия гидроксильных радикалов. Кроме этого, гидроксил-радикалы взаимодействуют с пуриновыми и пиримидиновыми основаниями нуклеиновых кислот, что может привести к нарушению комплементарности оснований в цепи ДНК и в конечном итоге вызвать мутацию или гибель клетки [44].
Таким образом, механизм действия ионизирующего излучения и озона на ДНК клетки одинаков: в обоих случаях возникает окислительный стресс, при котором происходит чрезмерная выработка гидроксильного радикала ОН•.
При воздействии, вызывающем повреждение ДНК, выявляются особенности в морфологии ДНК-комет.
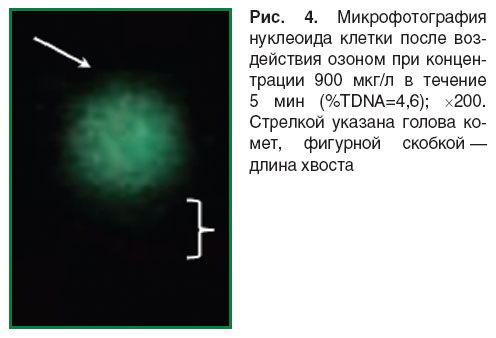
Нуклеоиды клеток, не подвергавшихся воздействию, имеют вид сферы со светящимся «гало» вокруг кόровой части. «Гало» представляет собой петли ДНК, прикрепленные к белкам ядерного матрикса [47] (рис. 3). Кометы, полученные после воздействия на клетки в слайдах озоном в озоно-кислородной смеси при концентрации 900 мкг/л в течение 5 мин, имели небольшой короткий хвост, состоящий из различных фрагментов ДНК (рис. 4). У нуклеоидов клеток после воздействия озоном в той же концентрации — 900 мкг/л, но в течение 10 мин наблюдался уже хорошо выраженный, протяженный хвост (рис. 5). Рис. 3–4 выполнены с использованием функции «Авто», встроенной в микроскоп, которая позволяет регулировать яркость изображения для обеспечения наилучшего цветовоспроизведения объекта.
 Рис. 3. Микрофотография нуклеоида клетки, не подвергавшейся воздействию (%TDNA=0,9); ×200 Рис. 3. Микрофотография нуклеоида клетки, не подвергавшейся воздействию (%TDNA=0,9); ×200
|
|
Рис. 4. Микрофотография нуклеоида клетки после воздействия озоном при концентрации 900 мкг/л в течение 5 мин (%TDNA=4,6); ×200. Стрелкой указана голова комет, фигурной скобкой — длина хвоста |
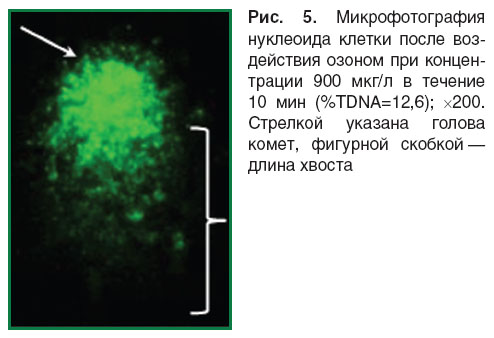 |
Рис. 5. Микрофотография нуклеоида клетки после воздействия озоном при концентрации 900 мкг/л в течение 10 мин (%TDNA=12,6); ×200. Стрелкой указана голова комет, фигурной скобкой — длина хвоста |
При сравнении микрофотографий нуклеоидов клеток, полученных после воздействия озоном (см. рис. 5) и гамма-излучением в дозе 3 Гр (рис. 6), оказалось, что ДНК-кометы имели одинаково протяженные и хорошо выраженные хвосты в обоих способах индуцированного повреждения ДНК.
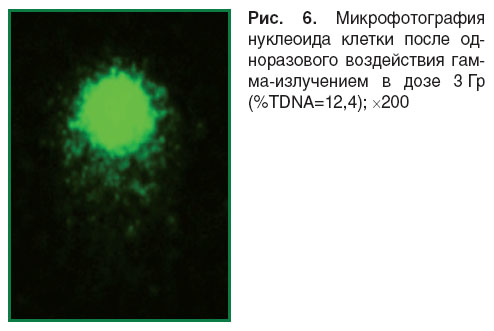 Рис. 6. Микрофотография нуклеоида клетки после одноразового воздействия гамма-излучением в дозе 3 Гр (%TDNA=12,4); ×200 Рис. 6. Микрофотография нуклеоида клетки после одноразового воздействия гамма-излучением в дозе 3 Гр (%TDNA=12,4); ×200
|
Анализ распределения выборочных данных по критерию Колмогорова–Смирнова показал отсутствие отличий от нормального распределения, поэтому в дальнейшем был использован параметрический критерий Стьюдента с поправкой Бонферрони при множественных сравнениях. Анализ результатов исследований не выявил статистически значимых различий средних значений уровня индуцированных повреждений ДНК в лейкоцитах цельной крови крыс после воздействия озоном при разных концентрациях в озоно-кислородной смеси — 200, 400 и 900 мкг/л — в течение 5 мин (рис. 7). Однако уровень индуцированных повреждений ДНК в лейкоцитах крови после воздействия на клетки озоном при концентрации 900 мкг/л в течение 10 мин был статистически значимо выше, чем уровень таковых повреждений после воздействия озоном при всех трех концентрациях в течение 5 мин и при концентрациях 200 и 400 мкг/л в течение 10 мин.
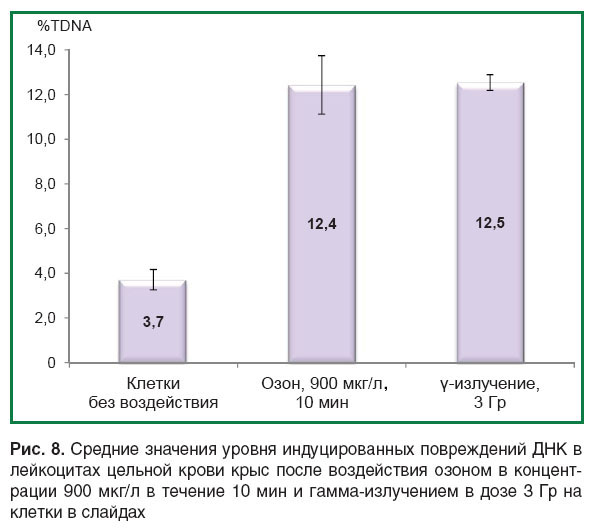
Сравнение средних значений уровня индуцированных повреждений ДНК в лейкоцитах цельной крови крыс после воздействия озоном в озоно-кислородной смеси при концентрации 900 мкг/л в течение 10 мин (%TDNA=12,4±1,3) и после воздействия гамма-излучением 60Co в дозе 3 Гр (%TDNA 12,5±0,4) статистически значимых различий не выявило (рис. 8).
Таким образом, замена гамма-излучения на озонирование при анализе повреждений и репарации ДНК помогает устранить методические трудности, ограничивающие широкое применение метода ДНК-комет в практической медицине.
Заключение. Разработанная версия метода ДНК-комет — воздействие на клетки в слайдах озоном при концентрации озона в озоно-кислородной смеси 900 мкг/л и времени воздействия 10 мин — является оптимальным решением для применения ее в целях детекции повреждений ДНК и их анализа и позволяет избежать недостатков традиционного использования гамма-излучения.
Благодарности. Авторы выражают искреннюю благодарность сотрудникам Института теоретической и экспериментальной биофизики РАН (Пущино Московской области): старшему научному сотруднику Николаю Петровичу Сироте и к.б.н. Елене Ананьевне Кузнецовой за помощь в освоении метода ДНК-комет, ценные указания и теплое отношение. Кроме того, благодарят сотрудника ННГУ им. Н.И. Лобачевского к.б.н. Алексея Анатольевича Радаева за консультационную помощь при проведении статистической обработки полученных результатов исследований.
Финансирование исследования и конфликт интересов. Исследование не финансировалось какими-либо источниками, и конфликты интересов, связанные с данным исследованием, отсутствуют.
Литература
- Сирота Н.П., Кузнецова Е.А. Применение метода «комета тест» в радиобиологических исследованиях. Радиационная биология. Радиоэкология 2010; 50(3): 329–339.
- Liao W., McNutt M.A., Zhu W.G. The comet assay: a sensitive method for detecting DNA damage in individual cells. Methods 2009; 48(1): 46–53, http://dx.doi.org/10.1016/j.ymeth.2009.02.016.
- Пелевина И.И., Антощина М.М., Бондаренко В.А., Воробьева Н.Ю., Воронков Ю.И., Готлиб В.Я., Кудряшова О.В., Осипов А.Н., Рябченко Н.И., Серебряный А.М., Цетлин В.В. Индивидуальные цитогенетические и молекулярно-биологические особенности лимфоцитов крови летчиков и космонавтов. Радиационная биология. Радиоэкология 2007; 47(2): 141–150.
- Хаймович Т.И., Нагиба В.И., Никанорова Е.А., Калиновская О.В., Иванов К.Ю., Паточка Г.Л. Репаративный статус и конформационное состояние хроматина клеток крови профессионалов-атомщиков, работавших с тритием и его окисью. Экологический вестник 2010; 12(2): 84–94.
- Газиев А.И. Низкая эффективность репарации критических повреждений ДНК, вызываемых малыми дозами радиации. Радиационная биология. Радиоэкология 2011; 51(5): 512–529.
- Osipov A.N., Smetanina N.M., Pustovalova M.V., Arkhangelskaya E., Klokov D. The formation of DNA single-strand breaks and alkali-labile sites in human blood lymphocytes exposed to 365-nm UVA radiation. Free Radic Biol Med 2014; 73: 34–40, http://dx.doi.org/10.1016/j.freeradbiomed.2014.04.027.
- Hornhardt S., Rößler U., Sauter W., Rosenberger A., Illig T., Bickeböller H., Wichmann H.E., Gomolka M. Genetic factors in individual radiation sensitivity. DNA Repair (Amst) 2014; 16: 54–65, http://dx.doi.org/10.1016/j.dnarep.2014.02.001.
- Котова Е.В., Сергиенко Т.Ф., Иванова М.А., Смольникова В.В., Глушен С.В., Меркулова И.П., Свирновский А.И. Влияние цисплатина на репарацию разрывов ДНК в лимфоцитах периферической крови человека. Медицинский журнал 2006; 2(16): 1–5.
- Дурнев А.Д., Жанатаев А.К., Анисина Е.А. и др. Применение метода щелочного гель-электрофореза изолированных клеток для оценки генотоксических свойств природных и синтетических соединений. М: Полиграфсервис; 2006.
- Ordzhonikidze K.G., Zanadvorova A.M., Abilev S.K. Organ specificity of the genotoxic effects of cyclophosphane and dioxidine: an alkaline comet assay study. Russian Journal of Genetics 2011; 47(6): 754–756, http://dx.doi.org/10.1134/s1022795411050127.
- Recio L., Hobbs C., Caspary W., Witt K.L. Witt doze-response assessment of four genetoxic chemecals in a combined mouse and rat micronucleus and comet assay. Toxicol Sci 2010; 35(2): 149–162.
- Braz M.G., Mazoti M.Á., Giacobino J., Braz L.G., Golim Mde A., Ferrasi A.C., de Carvalho L.R., Braz J.R., Salvadori D.M. Genotoxicity, cytotoxicity and gene expression in patients undergoing elective surgery under isoflurane anaesthesia. Mutagenesis 2011; 26(3): 415–420, http://dx.doi.org/10.1093/mutage/geq109.
- Сорочинская У.Б., Михайленко В.М. Применение метода ДНК-комет для оценки повреждений ДНК, вызванных различными агентами окружающей среды. Онкология 2008; 10(3): 303–309.
- García-Lestón J., Roma-Torres J., Vilares M., Pinto R., Prista J., Teixeira J.P., Mayan O., Conde J., Pingarilho M., Gaspar J.F., Pásaro E., Méndez J., Laffon B. Genotoxic effects of occupational exposure to lead and influence of polymorphisms in genes involved in lead toxicokinetics and in DNA repair. Environment International 2012; 43: 29–36, http://dx.doi.org/10.1016/j.envint.2012.03.001.
- Pacini S., Giovannelli L., Gulisano M., Peruzzi B., Polli G., Boddi V., Ruggiero M., Bozzo C., Stomeo F., Fenu G., Pezzatini S., Pitozzi V., Dolara P. Association between atmospheric ozone levels and damage to human nasal mucosa in Florence, Italy. Environ Mol Mutagen 2003; 42(3): 127–135, http://dx.doi.org/10.1002/em.10188.
- Faust F., Kassie F., Knasmüller S., Boedecker R.H., Mann M., Mersch-Sundermann V. The use of the alkaline comet assay with lymphocytes in human biomonitoring studies. Mutat Res 2004; 566(3): 209–229, http://dx.doi.org/10.1016/j.mrrev.2003.09.007.
- Szeto Y.T., Benzie I.F., Collins A.R., Choi S.W., Cheng C.Y., Yow C.M., Tse M.M. A buccal cell model comet assay: development and avaluation for human biomonitoring and nutritional studies. Mut Res 2005; 578(1–2): 371–381, http://dx.doi.org/10.1016/j.mrfmmm.2005.06.014.
- Dusinska M., Collins A.R. The comet assay in human biomonitoring: gene-environment interactionset. Mutagenesis 2008; 23(3): 191–205, http://dx.doi.org/10.1093/mutage/gen007.
- Stcherbatyuk Т.G., Davydenko D.V., Novikova V.А. Oxidative stress level and anthropogenic load index as prognostic criteria of disease outcome in patients with oropharyngeal cancer. Sovremennye tehnologii v medicine 2013; 5(4): 25–32.
- Скальский С.В., Ступакова Л.В., Роскошная Д.В., Турчанинов Д.В., Полещук Е.И., Охлопков В.А., Говоруха Ю.С. Перспективы метода ДНК-комет в технологиях биомониторинга и оценки влияния окружающей среды на здоровье населения. Современные проблемы науки и образования 2015; 3: 1–6.
- Lee R.F., Steinert S. Use of single cell gel electrophoresis/comet assay for detecting DNA damage in aquatic (marine and freshwater) animals. Mutat Res 2003; 544(1): 43–64, http://dx.doi.org/10.1016/S1383-5742(03)00017-6.
- Blasiak J., Arabski M., Krupa R., Wozniak K., Zadrozny M., Kasznicki J., Zurawska M., Drzewoski J. DNA damage and repair in type 2 diabetes mellitus. Mutat Res 2004; 554(1–2): 297–304, http://dx.doi.org/10.1016/j.mrfmmm.2004.05.011.
- Harangi M., Remenyik E.E., Seres I., Varga Z., Katona E., Paragh G. Determination of DNA damage induced by oxidative stress in hyperlipidemic patients. Mutat Res 2002; 513(1–2): 17–25, http://dx.doi.org/10.1016/S1383-5718(01)00285-6.
- Demirbag R., Yilmaz R., Kocyigit A. Relationship between DNA damage, total antioxidant capacity and coronary artery disease. Mut Res 2005; 570(2): 197–203, http://dx.doi.org/10.1016/j.mrfmmm.2004.11.003.
- Sánchez P., Peñarroja R., Gallegos F., Bravo J.L., Rojas E., Benítez-Bribiesca L. DNA damage in peripheral lymphocytes of untreated breast cancer patients. Arch Med Res 2004; 35(6): 480–483, http://dx.doi.org/10.1016/j.arcmed.2004.11.008.
- Sigurdson A.J., Hauptmann M., Alexander B.H., Doody M.M., Thomas C.B., Struewing J.P., Jones I.M. DNA damage among thyroid cancer and multiple cancer cases, controls, and long-lived individuals. Mutat Res 2005; 586(2): 173–188, http://dx.doi.org/10.1016/j.mrgentox.2005.07.001.
- Gamulin M., Garaj-Vrhovac V., Kopjar N. Evaluation of DNA damage in radiotherapy-treated cancer patients using the alkaline comet assay. Coll Antropol 2007; 31(3): 837–845.
- Gamulin M., Kopjar N., Grgić M., Ramić S., Bisof V., Garaj-Vrhovac V. Genome damage in oropharyngeal cancer patients treated by radiotherapy. Croat Med J 2008; 49(4): 515–527, http://dx.doi.org/10.3325/cmj.2008.4.515.
- Gamulin M., Garaj-Vrhovac V., Kopjar N., Ramić S., Viculin T., Juretić A., Grgić M. DNA and cytogenetic damage in white blood cells of postmenopausal breast cancer patients treated with radiotherapy. J Environ Sci Health A Tox Hazard Subst Environ Eng 2010; 45(3): 292–304, http://dx.doi.org/10.1080/10934520903467881.
- Sánchez-Suárez P., Ostrosky-Wegman P., Gallegos-Hernández F., Peñarroja-Flores R., Toledo-García J., Bravo J.L., Del Castillo E.R., Benítez-Bribiesca L. DNA damage in peripheral blood lymphocytes in patients during combined chemotherapy for breast cancer. Mutat Res 2008; 640(1–2): 8–15, http://dx.doi.org/10.1016/j.mrfmmm.2007.11.008.
- Taube S.E., Jacobson J.W., Lively T.G. Cancer diagnostics: decision criteria for marker utilization in the clinic. Am J Pharmacogenomics 2005; 5(6): 357–364, http://dx.doi.org/10.2165/00129785-200505060-00003.
- McKenna D.J., McKeown S.R., McKelvey-Martin V.J. Potential use of the comet assay in the clinical management of cancer. Mutagenesis 2008; 23(3): 183–190, http://dx.doi.org/10.1093/mutage/gem054.
- Fikrová P., Štětina R., Hronek M., Hyšpler R., Tichá A., Zadák Z. Application of the comet assay method in clinical studies. Wien Klin Wochenschr 2011; 123(23–24): 693–699, http://dx.doi.org/10.1007/s00508-011-0066-0.
- Тронов В.А., Гринько Е.В., Бериташвили Д.Р., Филиппович И.В. Микроэлектрофорез ДНК индивидуальных интактных и гамма-облученных тимоцитов. Цитология 1991; 33(2): 94–102.
- Chaubey R.C., Bhilwade H.N., Rajagopalan R., Bannur S.V. Gamma ray induced DNA damage in human and mouse leucocytes measured by SCGE-Pro: a software developed for automated image analysis and data processing for Comet assay. Mutat Res 2001; 490(2): 187–197, http://dx.doi.org/10.1016/S1383-5718(00)00166-2.
- Lankoff A., Bialczyk J., Dziga D., Carmichael W.W., Gradzka I., Lisowska H., Kuszewski T., Gozdz S., Piorun I., Wojcik A. The repair of gamma-radiation — induced DNA damage is inhibited by microcystin — LR, the PP1 and PP2A phosphatase inhibitor. Mutagenesis 2006; 21(1): 83–90, http://dx.doi.org/10.1093/mutage/gel002.
- Vorob’eva Nlu., Antonenko A.V., Osipov A.N. Particularities of blood lymphocyte response to irradiation in vitro in breast cancer patients. Radiats Biol Radioecol 2011; 51(4): 451–456.
- Требования радиационной безопасности при производстве, эксплуатации и выводе из эксплуатации (утилизации) медицинской техники, содержащей источники ионизирующего излучения. Постановление Главного государственного санитарного врача РФ №91 от 07.07.2011.
- Collins A.R. The comet assay: a heavenly method! Mutagenesis 2015; 30(1): 1–4, http://dx.doi.org/10.1093/mutage/geu079.
- Speit G., Hartmann A. The comet assay: a sensitive genotoxicity test for the detection of DNA damage and repair. Methods Mol Biol 2006; 314: 275–286, http://dx.doi.org/10.1385/1-59259-973-7:275.
- Степанов B.H. Методы и программные средства автоматизации анализа изображений медико-биологических микрообъектов. Автореф. дис. … канд. техн. наук. М; 2005.
- Киселева Е.С., Голдобенко Г.В., Канаев С.В. и др. Лучевая терапия злокачественных опухолей. Под ред. Киселевой Е.С. М: Медицина; 1996; 464 с.
- Ильин Л.А., Кириллов В.Ф., Коренков И.П. Радиационная безопасность и защита. М: Медицина; 1996; 336 с.
- Меньщикова Е.Б., Ланкин В.З., Зенков Н.К. и др. Окислительный стресс. Прооксиданты и антиоксиданты. М: Слово; 2006; 556 с.
- Viebahn-Hänsler R., León Fernández O.S., Fahmy Z. The low-dose ozone concept — guidelines and treatment strategies. Ozone: Science & Engineering Journal 2012; 34(6): 408–424.
- Разумовский С.Д., Константинова М.Л., Гриневич Т.В., Коровина Г.В., Зайцев В.Я. Брутто — закономерности разложения озона в физиологическом растворе и методика оценки количества озона, введенного больному вместе с дозой раствора. Биомедицинская химия 2010; 56(3): 380–386.
- Тронов В.А., Никольская Т.А., Коноплянников М.А. ДНК-кометы как маркер клеточной гибели. Биофизика 1999; 44(2): 288–295.