Вклад лазероиндуцированной газопарожидкостной динамики в механизм эндовенозной лазерной облитерации
Цель исследования — экспериментальное обоснование механизма эндовенозной лазерной облитерации (ЭВЛО), основанного на лазероиндуцированной конвективной теплоотдаче крови венозным стенкам, обусловленной ее кипением, как доминирующего процесса в сложном механизме теплообмена при эндовазальных лазерных манипуляциях.
Материалы и методы. В эксперименте по моделированию ЭВЛО были использованы фрагменты варикозно-измененных стволов больших подкожных вен, удаленных при комбинированной флебэктомии. Лазерное излучение с длиной волны 970 нм и мощностью 6 и 7 Вт подводили в вену через кварцевый световод с плоским предварительно зачерненным торцом. Скорость тракции составляла 0,5 мм/с. В процессе облучения с помощью тепловизора FLIR A600 (Швеция) измеряли температуру поверхности вены. Денатурацию коллагена венозной стенки в результате лазерного воздействия определяли методом дифференциальной сканирующей калориметрии.
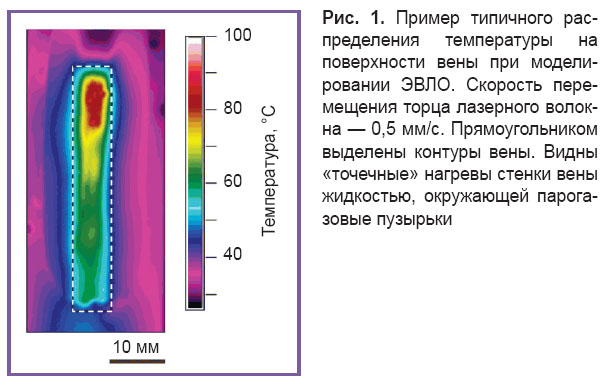
Результаты. Регистрация динамики температуры на поверхности вены с помощью тепловизора позволила визуализировать «точечные» нагревы стенки вены жидкостью, окружающей парогазовые пузырьки. Установлено существование температурного насыщения в динамике прогрева исследуемых сред, что является одним из характерных признаков фазового перехода первого рода. Степень денатурации коллагена в образцах венозной стенки при мощностях излучения 6 и 7 Вт составила 87±5 и 97±3% соответственно.
Заключение. Экспериментально подтверждено пузырьковое кипение крови в венозном сосуде, которое обеспечивает быструю и эффективную теплоотдачу разогретой крови от нагретого торца кварцевого волокна на венозные стенки. Для успешного проведения ЭВЛО перемещение волокна нужно начинать с момента закипания крови; при меньших мощностях лазерного излучения волокно необходимо удерживать большее время. В клинической процедуре ЭВЛО можно использовать менее мощные и более безопасные в смысле возможных осложнений лазерные аппараты.
Эндовенозная лазерная облитерация — ЭВЛО (коагуляция, абляция), в том числе и большой подкожной вены — безопасный, малотравматичный и эффективный хирургический метод лечения варикозной болезни. В последнее время он занимает ведущее положение среди других используемых хирургических методов. С момента первого применения в 1999 г. данной технологии [1] физический механизм ЭВЛО, на основе которого можно было бы выработать единый подход к выбору режима, экспозиции и длины волны лазерного излучения, остается дискуссионным.
Использование эндовенозного лазерного излучения в хирургической практике основано на преобразовании лазерного излучения в тепло, которое посредством теплообмена доставляется к патологически измененным венозным стенкам. Для успешной облитерации сосуда должна произойти необратимая денатурация коллагена, образующего каркас венозной стенки. Таким образом, достигаемая температура венозной стенки должна превышать температуру денатурации основного структурного белка ткани [2].
Как известно, существует три вида теплообмена — теплопроводность (кондукция), конвекция (перемешивание) и излучение (радиация) [3]. В соответствии с ними рассматриваются различные способы доставки преобразованного в тепло лазерного излучения к венозным стенкам. Эти способы во многом определяют физические механизмы ЭВЛО.
Кондуктивный теплообмен требует непосредственного контакта теплоносителя с интимой — внутренним, взаимодействующим с кровью слоем вены. В ранних исследованиях полагали, что венозная стенка нагревается вследствие контакта генерируемых лазерным излучением пузырьков пара с интимой [4]. Затем этот механизм расширили за счет учета конденсации пара с выделением теплоты и предположения, что вена разогревается по принципу работы тепловой трубки [5, 6].
Этот механизм доминировал в представлениях клиницистов достаточно долго, пока не появились сомнения в его физической состоятельности. Пузырьки пара не могут значительно нагреть венозную стенку, поскольку плотность насыщенного пара при атмосферном давлении даже при температуре 100°С составляет только 6·10–4 от плотности воды, а аналогия с тепловой трубкой некорректна из-за того, что в пузырьках присутствуют не только пары воды, но и другие газы [7–9].
В отношении радиационного теплообмена проведено значительное количество исследований по изучению влияния длины волны излучения на эффективность ЭВЛО. Первыми в процедуре были использованы лазеры с длинами волны в диапазоне 0,75–1,06 мкм, попадающими в полосы поглощения окси- и дезоксигемоглобина [10]. Эта группа лазеров получила название гемоглобинпоглощающих [4, 11–13]. Позднее нашли применение лазеры, излучение которых попадало в область максимумов поглощения воды (полоса 1,32–1,56 мкм). По отношению к ЭВЛО эти лазеры стали называть водопоглощающими [14–16]. Считается, что излучение водопоглощающих лазеров может свободно достигать венозной стенки, минуя поглощение клетками крови — эритроцитами, в то время как гемоглобинпоглощающие лазеры изначально действуют только на эритроциты, инициируя образование тромбов. В результате сложного кондуктивно-радиационного теплообмена между разогретыми излучением тромбами и окружением венозная стенка нагревается. Такое представление было подвергнуто критике уже потому, что эритроциты на 65–70% состоят из воды [7]. В итоге оказалось, что различия в клинической эффективности водопоглощающих и гемоглобинпоглощающих лазеров несущественны, значимы лишь методологические особенности проведения процедур различными авторами [7, 8, 17].
В некоторых исследованиях [8, 18, 19] обращено внимание на то, что в процессе лазерного облучения вены контактирующий с кровью торец световода (волокна) покрывается слоем нагара (чернится). Как почти абсолютно черное тело, этот рабочий конец поглощает лазерное излучение любой длины волны и нагревается до температур порядка 1000°С и выше [20–25]. При этом такой горячий торец (hot tip) становится источником мощного теплового излучения (излучения Планка), которое может непосредственно прогревать венозные стенки, что, по мнению авторов [8], и обусловливает физический механизм ЭВЛО. Такому прогреву препятствует поглощающая тепловое излучение вода, которая окружает торец оптического волокна. В связи с этим авторы предлагают использовать лазерное излучение большой мощности (около 20 Вт), которое должно «осушить» окрестное пространство. Однако при больших мощностях наблюдаются серьезные осложнения [26, 27], такие как перфорация стенки вены, перифлебит, гематомы и парестезии.
Искусственное чернение торца волокна — нанесение на его поверхность слоя углерода — с целью создания разогретого до высоких температур точечного источника тепла (диаметр кварцевой жилы световода — 100–600 мкм) широко используется в хирургической практике. По такому принципу, в частности, работает лазерный скальпель для контактного рассечения водонасыщенных биологических тканей [23, 24]. Черненый торец используют в пункционных операциях для лечения грыжевых дисков [28, 29], истинных кист [30] и др. Важно отметить, что сильный разогрев зачерненного участка световода достигается уже при низких мощностях лазерного излучения. На практике горячий торец можно успешно получить уже при мощностях лазерного излучения ~0,5–1,0 Вт [23].
Разогретый до высоких температур торец волокна при введении в вену вступает в контакт с кровью (водная дисперсия), что приводит к ее взрывному кипению и экзотермическому окислению органических компонентов [21, 23]. Эти процессы инициируют потоки горячей крови с последующей конвективной теплоотдачей венозным стенкам. Обеспечить закипание крови в окрестности черненого торца достаточно просто уже при умеренной мощности (1–7 Вт) лазерного излучения, причем с любой длиной волны [23, 31].
Для обоснования механизма ЭВЛО нужна регистрация в динамике действия потоков нагретой жидкости на стенку вены. Проводимые же исследования распределения тепловых потоков в вене с использованием точечных термопар [2, 17] позволяют оценить распределение температуры непосредственно на венозной стенке очень приближенно и без учета динамики нагрева. Эта задача, необходимая для уточнения механизма ЭВЛО, может быть решена с применением современной скоростной высокочувствительной тепловизионной камеры, которая использована в предлагаемой работе.
Цель исследования — экспериментальное обоснование механизма эндовенозной лазерной облитерации, основанного на лазероиндуцированной конвективной теплоотдаче крови венозным стенкам, обусловленной ее кипением, как доминирующего процесса в сложном механизме теплообмена при эндовазальных лазерных манипуляциях.
Материалы и методы. Для моделирования ЭВЛО использовали варикозно-измененные стволы больших подкожных вен, удаленных при комбинированной флебэктомии (4 пациента, средний возраст — 51,6±7,8 года, клинический класс болезни — С2 по классификации СЕАР). Стволы хранили в 0,15 М растворе NaCl при температуре 4–8°С до начала эксперимента не более 8 ч. Каждый ствол разделяли на фрагменты длиной 50±5 мм, средний диаметр фрагментов составлял 5,4±1,6 мм. В эксперименте было использовано 15 фрагментов.
Концы участков вен стягивали в 1–2 мм от края таким образом, чтобы уменьшить внутренний диаметр до ~1 мм, сохраняя при этом форму сечения отверстия, наиболее близкую к кругу. Затем концы закрепляли со слабым натяжением на пластиковой подложке треугольного сечения, при этом одна из сторон оставалась открытой. В вену с обоих концов вводили около 0,5 мл гепаринизированной крови, которую равномерно распределяли по длине. С дистального конца внутрь фрагмента вены вводился кварцевый световод с плоским, предварительно зачерненным торцом диаметром 600 мкм. Всю конструкцию помещали горизонтально в контейнер размером 11×70 мм, заполненный 0,15 М раствором NaCl. Полоска вены шириной ~1 мм выступала над поверхностью раствора, что позволило регистрировать интенсивность теплового излучения от внешней поверхности венозной стенки. Регистрацию динамики температурных полей осуществляли с помощью инфракрасного термографа FLIR A600 (Швеция) с постоянной времени датчика 8 мс и скоростью съемки 50 кадров в секунду.
В эксперименте использовали полупроводниковый лазер ЛС-0,97 («ИРЭ-Полюс», Россия) с длиной волны излучения 0,97 мкм и максимальной мощностью 11 Вт. Мощность излучения контролировали измерителем мощности UP12-H (Gentec Electro-Optics, Канада). Тракцию световода в сосуде осуществляли в автоматическом режиме с аппаратно-заданной скоростью 0,5 мм/с.
После проведения лазерной обработки образцы из средней части фрагмента анализировали методом дифференциальной сканирующей калориметрии. Препараты массой 7–10 мг герметично закрывали в стандартных алюминиевых тиглях (20 мкл) и нагревали в ячейке калориметра DSC204F (Netzch, Германия): от комнатной температуры до 85°C со скоростью 10°K/мин. Образцом сравнения служил пустой тигель. Энтальпию денатурации (ΔНd) пересчитывали на сухой остаток препарата.
Статистическую обработку количественных результатов выполняли, используя t-критерий Стьюдента, среднее арифметическое и стандартное отклонение. Предварительно проводили анализ на соответствие сравниваемых выборок нормальному закону распределения. Различия считали статистически значимыми при p<0,001. Рассчитывали средние величины и стандартную ошибку среднего (M±m).
Результаты. С помощью инфракрасного термографа получено типичное изображение поверхности раствора NaCl c веной в контейнере (рис. 1). Выделяется нагретый участок выступающей полоски венозной стенки. В наиболее горячей области, соответствующей положению торца волокна, отчетливо визуализируются тепловые проекции парогазовых пузырьков. На рис. 2 приведены примеры временнóй эволюции максимальной температуры на внешней поверхности венозной стенки при движении световода для мощностей лазерного излучения 6 и 7 Вт. Зависимость максимальной температуры от времени имеет вид кривой с насыщением. Насыщение начиналось примерно через 7 с после включения лазера, когда температура достигала 70–80°С, и волокно перемещалось на расстояние ~3,5 мм. Неожиданный результат заключается в том, что кривая 1, полученная при мощности лазерного излучения 7 Вт, в период времени 0–9 с лежит ниже кривой 2, полученной при мощности 6 Вт. Например, для времени 5,0±0,2 с значение температуры для 6 Вт — Т6=68,5±0,5°С, а для 7 Вт — Т7=64,7±0,4°С, при этом выборки статистически значимо отличаются, p=0,008, т.е. большей мощности соответствует меньшая скорость роста температуры. При бóльших временах (25±5 с), как видно из рис. 2, большей мощности лазерного излучения соответствует большая температура: Т6=83,0±0,5°С, а Т7=91,1±0,3°С, при статистически значимом отличии выборок, p=0,002.
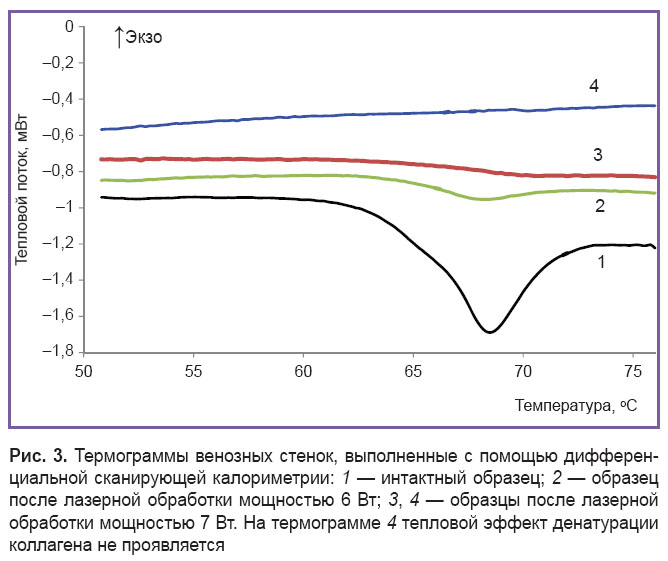
На рис. 3 представлены термограммы образцов венозной стенки, выполненные с помощью дифференциальной сканирующей калориметрии. На термограммах интактных препаратов (кривая 1) наблюдается эндотермический пик с максимумом 68,0±0,7°C, связанный с поглощением теплоты при денатурации (переход спираль–клубок) макромолекул коллагена [32]. Площадь пика соответствует энтальпии денатурации ΔHd, которая составляет 10±3Дж/г сухого остатка. После лазерной обработки площадь пика существенно уменьшается вплоть до полного исчезновения (кривые 2–4). Уменьшение энтальпии перехода ΔH указывает на уменьшение в результате лазерного воздействия доли интактных макромолекул в препаратах. Степень денатурации коллагена α определяли по соотношению α=(1–ΔH/ΔHd)·100%. Для мощностей 6 и 7 Вт величина α составляла 87±5 и 97±3% соответственно; ΔHd=–18,4 мДж/г сухого остатка. Таким образом, происходила практически полная деградация коллагенового каркаса стенки сосуда.Следует отметить сложный профиль кривых на линии насыщения. В частности, наблюдаются локальные максимумы, когда температура превышает 90°С, и минимумы. Это можно объяснить активными гидродинамическими процессами, а также влиянием (экранировкой) пузырьков, возникающих при кипении крови.
|
|
Рис. 3. Термограммы венозных стенок, выполненные с помощью дифференциальной сканирующей калориметрии: 1 — интактный образец; 2 — образец после лазерной обработки мощностью 6 Вт; 3, 4 — образцы после лазерной обработки мощностью 7 Вт. На термограмме 4 тепловой эффект денатурации коллагена не проявляется |
Обсуждение. В работе исследовались температурные характеристики процессов, генерируемых лазерным излучением, в заполненном гепаринизированной кровью венозном сосуде. Установлено, что лазероиндуцированная гидродинамика в такой модели, связанная с кипением крови, обеспечивает конвективную теплоотдачу на стенки сосудов и создает необходимые и достаточные условия для успешного проведения ЭВЛО. Главным условием является прогрев венозной стенки до температур, при которых происходит необратимая денатурация белков, входящих в ее состав, а достаточным — полная деградация каркаса матрикса ткани [2].
Экспериментальные результаты доказали, что при условии предварительного чернения торца волокна температура внешней поверхности стенки сосуда быстро достигает значений ~80–90°С (см. рис. 2), которые значительно превышают температуру денатурации коллагена в тканях [33]. В первые 9 с скорость температурного роста с увеличением мощности лазерного излучения уменьшается. Это можно объяснить тем, что с увеличением мощности излучения растет объем вовлеченной в движение жидкости и на ее прогрев требуется большее время. При бóльших временах (в период 25–40 с) температура на поверхности венозной стенки с увеличением мощности поднимается до бóльших значений.
Следующий важный результат — температурное насыщение в динамике прогрева исследуемых сред (см. рис. 2). Он означает, что при лазерном нагреве наполненной кровью вены срабатывает некий механизм теплоотвода, который слабо зависит от мощности теплового источника; от нее зависит только скорость достижения температуры насыщения. Аналогичный результат — достижение температурного плато в экспериментальной модели ЭВЛО для лазерного излучения с длиной волны 1470 нм — показан в работе [2]. Однако авторы решали другую задачу и не обсуждали полученный результат, который в сопоставлении с нашими данными, в частности, означает, что от длины волны эффект вскипания крови не зависит.
Это заключение очевидно для хорошо зачерненного торца волокна (предварительно либо по ходу проведения процедуры), когда слой углерода на торце световода (как абсолютно черное тело) будет разогреваться при поглощении лазерного излучения практически с любой длиной волны.
Наличие температурного плато при нагреве — один из характерных признаков фазового перехода первого рода [3]; в случае обсуждаемой системы таким переходом является кипение. Кипение — это процесс интенсивного парообразования и интенсивной конвекции, сопровождающихся перемещением в пространстве жидкости и паровых пузырьков. Динамика пузырьков обусловлена температурными градиентами и, собственно, обеспечивает теплоотвод.
Ранее в работах [21, 22] было показано, что раскаленный лазерным излучением предварительно зачерненный торец световода в воде генерирует образование и интенсивное движение пузырьков с размерами от 10 мкм до 0,5 см (пузырьковое кипение). При этом линейные скорости мелких пузырьков достигают 100 мм/с. В движение пузырьков вовлечена присоединенная масса разогретой жидкости, которая для сферического тела равна половине массы жидкости, заключенной в объеме пузырька, и в случае пузырькового кипения обеспечивает быструю и эффективную теплоотдачу на стенки сосуда [3]. Траектории пузырьков в капиллярах имеют сложную форму закрученной спирали, а также линейных трансляций — затопленных микроструй [22, 23]. Мы считаем, что подобная лазероиндуцированная динамика в системе «венозная стенка/кровь» приводит к разогреву стенки посредством конвективной теплоотдачи от кипящей крови на интиму вен. Наш вывод подтверждается клиническими данными, полученными при проведении операций ЭВЛО под УЗ-контролем. Клиницисты отмечают пелену кипящих пузырьков в венозном сосуде под действием лазера при проведении УЗ-ассистированных операций, однако связывают это явление с физически неубедительными механизмами разогрева вен [6, 34].
Таким образом, найдено решение актуальной проблемы современной флебологии — установлен физический механизм эндовенозной лазерной облитерации варикозно-расширенных вен. В предлагаемых ранее механизмах не рассматривали индуцированную лазерным излучением гидродинамику и связанную с ней динамику парогазовых пузырьков, генерируемых в вене при контакте разогретого до высоких температур (~1000°С) торца кварцевого волокна с кровью.
Выполненное моделирование ЭВЛО экспериментально подтвердило пузырьковое кипение крови в венозном сосуде, которое обеспечивает быструю и эффективную теплоотдачу разогретой крови венозным стенкам. Проведенные температурные измерения доказали, что венозная стенка быстро и эффективно разогревается до температур, превышающих температуру необратимой денатурации основного структурного белка матрикса ткани — коллагена. В конечном итоге обеспечивается надежная облитерация венозного сосуда. При этом чернение волокна обеспечивает эффективность ЭВЛО вне зависимости от длины волны лазерного излучения.
Поскольку кипение является пороговым процессом, то оно не возникнет, если мощность подводимого лазерного излучения будет меньше пороговой. Следовательно, для успешного проведения ЭВЛО перемещение волокна нужно начинать с момента закипания крови. При меньших мощностях лазерного излучения волокно необходимо удерживать большее время. Из этого следует, что в клинической процедуре ЭВЛО в принципе можно использовать менее мощные, а значит, более безопасные в смысле возможных осложнений и более дешевые лазерные аппараты.
Заключение. Экспериментально подтверждено пузырьковое кипение крови в венозном сосуде, которое обеспечивает быструю и эффективную теплоотдачу разогретой крови от нагретого торца кварцевого волокна на венозные стенки. Для успешного проведения ЭВЛО перемещение волокна нужно начинать с момента закипания крови; при меньших мощностях лазерного излучения волокно необходимо удерживать большее время. В клинической процедуре ЭВЛО можно использовать менее мощные и более безопасные лазерные аппараты.
Финансирование исследования. Работа выполнена при поддержке Российского научного фонда (грант №14-15-00840).
Конфликт интересов. У авторов нет конфликта интересов.
Литература
- Bone Salat C. Tratamiento endoluminal de las varices con láser de diodo. Estudio preliminar. Revista de Patología Vascular 1999; 5(1): 31–39.
- Шевченко Ю.Л., Стойко Ю.М., Мазайшвили К.В., Максимов С.В., Циплящук А.В., Париков М.А., Игнатьева Н.Ю., Захаркина О.Л. Выбор оптимальных параметров излучения 1470 нм для эндовенозной лазерной облитерации. Флебология 2013; 7(4): 18–24.
- Кутателадзе С.С. Основы теории теплообмена. М: Атомиздат; 1979; 416 с.
- Proebstle T.M., Lehr H.A., Kargl A., Espinola-Klein C., Rother W., Bethge S., Knop J. Endovenous treatment of the greater saphenous vein with a 940-nm diode laser: thrombotic occlusion after endoluminal thermal damage by laser-generated steam bubbles. J Vasc Surg 2002; 35(4): 729–736, http://dx.doi.org/10.1067/mva.2002.121132.
- Proebstle T., Sandhofer M., Kargl A., Gül D., Rother W., Knop J., Lehr H.A. Thermal damage of the inner vein wall during endovenous laser treatment: key role of energy absorption by intravascular blood. Dermatol Surg 2002; 28(7): 596–600, http://dx.doi.org/10.1046/j.1524-4725.2002.01309.x.
- van der Geld C.W., van den Bos R.R., van Ruijven P.W., Nijsten T., Neumann H.A., van Gemert M.J. The heat-pipe resembling action of boiling bubbles in endovenous laser ablation. Lasers Med Sci 2010; 25(6): 907–909, http://dx.doi.org/10.1007/s10103-010-0780-2.
- Malskat W.S., Poluektova A.A., van der Geld C.W., Neumann H.A., Weiss R.A., Bruijninckx C.M., van Gemert M.J. Endovenous laser ablation (EVLA): a review of mechanisms, modeling outcomes, and issues for debate. Lasers Med Sci 2014; 29(2): 393–403, http://dx.doi.org/10.1007/s10103-013-1480-5.
- Шевченко Ю.Л., Стойко Ю.М., Мазайшвили К.В., Хлевтова Т.В. Механизм эндовенозной лазерной облитерации: новый взгляд. Флебология 2011; 5(1): 46–50.
- Жилин К.М. Влияние длины волны лазерного излучения ближнего ИК-диапазона на характер силового воздействия на биологические ткани (кровь, венозная стенка, слизистая оболочка и костная ткань). Автореф. дис. ... канд. физ.-мат. наук. Москва; 2013.
- Roggan A., Friebel M., Dörschel K., Hahn A., Müller G. Optical properties of circulating human blood in the wavelength range 400–2500 nm. J Biomed Opt 1999; 4(1): 36–46, http://dx.doi.org/10.1117/1.429919.
- Proebstle T.M., Gül D., Kargl A., Knop J. Endovenous laser treatment of the lesser saphenous vein with a 940-nm diode laser: early results. Dermatol Surg 2003; 29(4): 357–361, http://dx.doi.org/10.1046/j.1524-4725.2003.29085.x.
- Oh C.K., Jung D.S., Jang H.S., Kwon K.S. Endovenous laser surgery of the incompetent greater saphenous vein with a 980-nm diode laser. Dermatol Surg 2003; 29(11): 1135–1140, http://dx.doi.org/10.1046/j.1524-4725.2003.29353.x.
- Weiss R.A. Comparison of endovenous radiofrequency versus 810 nm diode laser occlusion of large veins in an animal model. Dermatol Surg 2002; 28(1): 56–61, http://dx.doi.org/10.1046/j.1524-4725.2002.01191.x.
- Schwarz T., von Hodenberg E., Furtwängler C., Rastan A., Zeller T., Neumann F.J. Endovenous laser ablation of varicose veins with the 1470-nm diode laser. J Vasc Surg 2010; 51(6): 1474–1478, http://dx.doi.org/10.1016/j.jvs.2010.01.027.
- Rathod J., Taori K., Joshi M., Mundhada R., Rewatkar A., Dhomane S., Gour P. Outcomes using a 1470-nm laser for symptomatic varicose veins. J Vasc Interv Radiol 2010; 21(12): 1835–1840, http://dx.doi.org/10.1016/j.jvir.2010.09.009.
- Соколов А.Л., Лядов К.В., Луценко М.М., Лавренко С.В., Любимова А.А., Вербицкая Г.О., Минаев В.П. Применение лазерного излучения 1,56 мкм для эндовазальной облитерации вен в лечении варикозной болезни. Ангиология и сосудистая хирургия 2009; 15(1): 69–76.
- Шайдаков Е.В., Илюхин Е.А., Петухов А.В., Росуховский Д.А. Сравнение лазеров с длиной волны 970 и 1470 нм при моделировании эндовазальной лазерной облитерации вен in vitro. Флебология 2011; 5(4): 23–30.
- Amzayyb M., van den Bos R.R., Kodach V.M., de Bruin D.M., Nijsten T., Neumann H.A., van Gemert M.J. Carbonized blood deposited on fibres during 810, 940 and 1470 nm endovenous laser ablation: thickness and absorption by optical coherence tomography. Lasers Med Sci 2010; 25: 439–447, http://dx.doi.org/10.1007/s10103-009-0749-1.
- Mordon S., Wassmer B., Servell P., Desmyttère J., Grard C., Stalnikiewicz G. Is a vein filled with blood a good model for studying endovenous laser ablation? Lasers Surg Med 2009; 41(8): 543–544, http://dx.doi.org/10.1002/lsm.20809.
- van den Bos R.R., Kockaert M.A., Martino Neumann H.A., Bremmer R.H., Nijsten T., van Gemert M.J. Heat conduction from the exceedingly hot fiber tip contributes to the endovenous laser ablation of varicose veins. Lasers Med Sci 2009; 24(2): 247–251, http://dx.doi.org/10.1007/s10103-008-0639-y.
- Yusupov V.I., Chudnovskii V.M., Bagratashvili V.N. Laser-induced hydrodynamics in water-saturated biotissues. 1. Generation of bubbles in liquid. Laser Phys 2010; 20(7): 1641–1647, http://dx.doi.org/10.1134/S1054660X1014001X.
- Yusupov V.I., Chudnovskii V.M., Bagratashvili V.N. Laser-induced hydrodynamics in water-saturated biotissues: 2. Effect on delivery fiber. Laser Phys 2011; 21(7): 1230–1234, http://dx.doi.org/10.1134/S1054660X11140015.
- Yusupov V.I., Chudnovskii V.M., Bagratashvili V.N. Laser-induced hydrodynamics in water and biotissues nearby optical fiber tip. In: Hydrodynamics — advanced topics. Schulz H.E. (editor). InTech; 2011; p. 95–118, http://dx.doi.org/10.5772/28517.
- Чудновский В.М., Юсупов В.И. Пункционная световодная игла (варианты) и ограничитель для нее. Патент на полезную модель 58904. 2006.
- Шевченко Ю.Л., Стойко Ю.М., Мазайшвили К.В. Лазерная хирургия варикозной болезни. М: Боргес; 2010.
- Dexter D., Kabnick L., Berland T., Jacobowitz G., Lamparello P., Maldonado T., Mussa F., Rockman C., Sadek M., Giammaria L.E., Adelman M. Complications of endovenous lasers. Phlebology 2012; 27(Suppl 1): 40–45, http://dx.doi.org/10.1258/phleb.2012.012S18.
- Dunst K.M., Huemer G.M., Wayand W., Shamiyeh A. Diffuse phlegmonous phlebitis after endovenous laser treatment of the greater saphenous vein. J Vasc Surg 2006; 43(5): 1056–1058, http://dx.doi.org/10.1016/j.jvs.2006.01.030.
- Чудновский В., Буланов В., Юсупов В. Лазерное индуцирование акустогидродинамических эффектов в хирургии. Фотоника 2010; 1: 30–36.
- Чудновский В.М., Юсупов В.И., Маховская Т.Г. Лазер-индуцированные акустогидродинамические эффекты в хирургии грыжевых дисков. Вестник неврологии, психиатрии и нейрохирургии 2013; 4: 76–82.
- Кухарева Л.И., Невожай В.И., Чудновский В.М. Возможности эхографии в диагностике и склерозирующей терапии кистозных образований молочных желез. Дальневосточный медицинский журнал 2008; 3: 49–51.
- Yusupov V.I., Bulanov V.V., Chudnovskii V.M., Bagratashvili V.N. Laser-induced hydrodynamics in water-saturated tissue: III. Optoacoustic effects. Laser Phys 2014; 24(1), http://dx.doi.org/10.1088/1054-660X/24/1/015601.
- Willett T.L., Labow R.S., Lee J.M. Mechanical overload decreases the thermal stability of collagen in an in vitro tensile overload tendon model. J Orthop Res 2008; 26(12): 1605–1610, http://dx.doi.org/10.1002/jor.20672.
- Игнатьева Н.Ю. Термическая стабильность коллагена в соединительных тканях. Автореф. дис. ... докт. хим. наук. М; 2011.
- van der Geld C.W.M. The dynamics of a boiling bubble before and after detachment. Heat Mass Transf 2009; 45(7): 831–846, http://dx.doi.org/10.1007/s00231-007-0254-7.