Многофотонная микроскопия в изучении морфологических особенностей радиационно-индуцированных повреждений мочевого пузыря
Цель исследования — оценить возможности многофотонной микроскопии (МФМ) для изучения динамики структурных изменений мочевого пузыря после однократного гамма-облучения в разных дозах (2, 10 и 40 Гр) в эксперименте.
Материалы и методы. Объектом исследования служили образцы мочевого пузыря крыс (9 групп по две крысы на каждые дозу и срок и две интактные крысы — всего 20 наблюдений) после однократного локального облучения в дозе 2, 10 или 40 Гр. Исследование проводили через 1 сут, 1 нед и 1 мес после радиационного воздействия. Часть гистологических препаратов мочевого пузыря окрашивали пикрофуксином по Ван-Гизону. Другую часть срезов, полученных с этих же блоков, без дополнительного окрашивания исследовали с помощью МФМ. С этой целью использовали лазерный сканирующий микроскоп LSM Axiovert 510 Meta (Carl Zeiss, Германия). Возбуждение осуществляли фемтосекундным титан-сапфировым лазером (MAI TAI HP, Spectra Physics, США) на длине волны 800 нм, регистрацию — в диапазоне 362–415 нм (сигнал второй гармоники от коллагена) и 512–576 нм (сигнал двухфотонно возбуждаемой автофлюоресценции эластина).
Результаты. Использование метода МФМ позволило выявить, что в ранние сроки (1 сут и 1 нед) после радиационного воздействия при всех выбранных дозах ведущим был процесс альтерации коллагенсодержащих структур стенки мочевого пузыря. Через 1 мес после облучения в дозе 2 и 10 Гр было зафиксировано увеличение содержания коллагеновых структур, что свидетельствовало о начале формирования радиационного фиброза. При дозе 40 Гр в экстрацеллюлярном матриксе стенки мочевого пузыря сохранялось снижение сигнала второй гармоники. Это позволило сделать вывод о длительно сохраняющейся дезорганизации коллагена в случае применения высоких доз облучения.
Заключение. Метод МФМ дает возможность установить, что разрушение структур экстрацеллюлярного матрикса ткани возникает уже после использования малых доз облучения и в ранние сроки после применения радиационного воздействия, что не удается выявить при стандартной микроскопии. Продолжительность процессов дезорганизации коллагенсодержащих структур зависит от дозы облучения: при использовании высоких доз альтерация носит более продолжительный характер. МФМ позволяет также оценить ход восстановительных процессов.
Изменения нормальных тканей, происходящие в различные сроки после проведения лучевой терапии по поводу злокачественных новообразований, представляют собой одну из нерешенных проблем современной радиационной онкологии [1]. Особое значение имеют побочные эффекты облучения для органов малого таза (мочевой пузырь и прямая кишка), когда они возникают у больных с прогнозируемой длительной продолжительностью жизни, для которых сохранение качества жизни является не менее важной задачей, чем излечение от онкологического заболевания [2].
Ключевым моментом в патогенезе радиационно-индуцированных осложнений является формирование фиброзных изменений в зоне облучения вследствие избыточного синтеза коллагена и замещения им поврежденных клеток и фибриллярных структур [3]. В течение последних 10 лет изучены и идентифицированы основные молекулярно-генетические механизмы, ответственные за ранние и поздние радиационные изменения нормальных тканей [3–5]. Исследование радиационно-индуцированных изменений коллагена на модельной среде позволило выявить основные молекулярные и тканевые механизмы процессов деградации и последующего восстановления его в различные сроки после однократного облучения в возрастающих дозах [6]. Однако остался неизученным вопрос о динамике состояния коллагена на различных уровнях его иерархической организации (молекулы, фибриллы, волокна, пучки) во время этих процессов. Следует подчеркнуть, что в структурной организации фибриллярных элементов внутренних органов участвует не только коллаген, но и эластин. Детального исследования дозо-временных зависимостей состояния коллаген- и эластинсодержащих элементов внутренних органов, подвергнутых воздействию ионизирующего излучения, до настоящего времени также не проводилось.
В последние годы в практику морфологических исследований активно внедряется многофотонная лазерная сканирующая микроскопия (МФМ). Метод дает возможность получения структурных изображений биологических тканей с визуализацией таких компонентов, как никотинамидадениндинуклеотид, флавопротеины, кератин, липофусцин, эластин, меланин и порфирины, по их автофлюоресценции за счет феномена двухфотонного возбуждения [7, 8]. Коллаген визуализируется за счет феномена генерации второй гармоники от молекул, не имеющих центра симметрии [9, 10, 11]. В условиях воздействия короткоимпульсного (~100 фс) лазерного излучения с высокой пиковой мощностью коллаген генерирует нелинейный оптический отклик на удвоенной частоте [12, 13]. Сканирование остро сфокусированным лазерным пучком дает возможность получать изображения, детально отражающие особенности укладки коллагена в ткани. В настоящее время использование феноменов двухфотонного возбуждения и генерации второй гармоники позволяет решать большое количество экспериментальных и клинических задач ex vivo [14, 15] и in vivo [15, 16] в офтальмологии [17, 18], дерматологии [19, 20], кардиологии [21], а также в экспериментальной и клинической онкологии [22–24].
Цель исследования — оценить возможности многофотонной микроскопии для изучения динамики структурных изменений мочевого пузыря после однократного гамма-облучения в разных дозах (2, 10 и 40 Гр) в эксперименте.
Материалы и методы. Эксперименты проведены на белых беспородных крысах (n=20), содержащихся в стандартных условиях вивария. Животные были разделены на 9 групп (по две крысы на каждые дозу и срок и две крысы — необлученные). Исследование выполнено в соответствии с этическими принципами, установленными Европейской конвенцией по защите позвоночных животных, используемых для экспериментальных и других научных целей (принятой в Страсбурге 18.03.1986 г. и подтвержденной в Страсбурге 15.06.2006 г.), и одобрено Этическим комитетом НижГМА.
Облучение мочевого пузыря осуществлялось в условиях общей анестезии (Золетил 50 мг/кг) на аппарате для дистанционной лучевой терапии «Терабалт» (энергия пучка — 1,25 МэВ) (UJP, Чешская Республика), однократно, локальным полем, в дозах, эквивалентных 2, 10 и 40 Гр. Через 1 сут, 1 нед и 1 мес после воздействия животных выводили из эксперимента с использованием эфирного наркоза. Мочевой пузырь препарировали, образцы для гистологического исследования и МФМ фиксировали в течение 24 ч в 10% растворе нейтрального формалина. Затем проводили заливку образцов в парафин (использовалась среда Histomix extra, «БиоВитрум», Россия) с последующей монтировкой парафиновых блоков. На ротационном микротоме Leica 450 RM (Leica Microsystems, Германия) с полученных блоков изготавливали срезы толщиной 0,1 и 10 мкм. Срезы толщиной 0,1 мкм окрашивали пикрофуксином по Ван-Гизону. Образцы толщиной 10 мкм, полученные с тех же блоков, депарафинировали и исследовали методом МФМ без дополнительного окрашивания. В качестве контрольных использовали препараты мочевого пузыря необлученных животных.
Исследования проводили на инвертированном лазерном сканирующем микроскопе LSM Axiovert 510 Meta (Carl Zeiss, Германия). В качестве источника возбуждающего излучения использован короткоимпульсный фемтосекундный лазер MAI TAI HP (Spectra Physics, США) с частотой следования импульсов 80 МГц и длительностью порядка 100 фс. Изображения тонкой структуры получали с помощью масляно-иммерсионного объектива EC Plan Neofluar (Carl Zeiss, Германия) с сорокакратным увеличением и числовой апертурой 1,3, что позволило добиться поля зрения 318×318 мкм с разрешением 1024×1024 пикселя.
Использовали следующие спектральные характеристики системы визуализации: возбуждение на длине волны 800 нм, регистрация в двух спектральных диапазонах длин волн: 362–415 нм, который содержит пик нелинейного отклика коллагена на второй гармонике (400 нм) [12], и 512–576 нм, который соответствует диапазону автофлюоресценции эластина при двухфотонном возбуждении [21]. Регистрацию проводили в режиме полностью открытого пинхола.
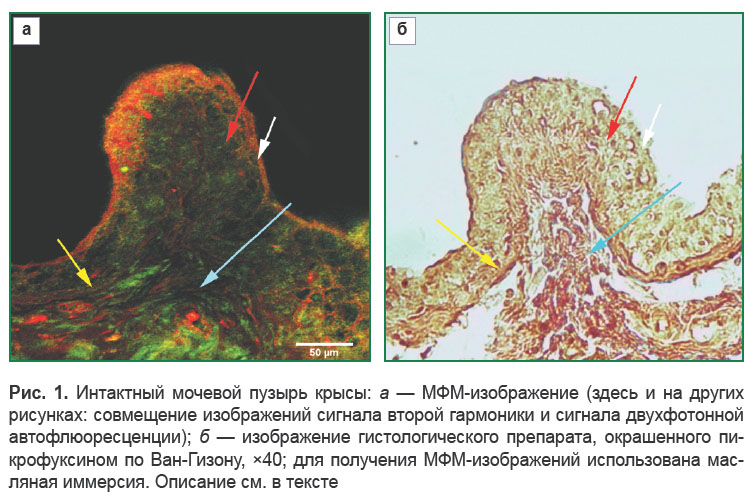
Результаты. Начальным этапом работы было МФМ-исследование топографических характеристик коллаген- и эластинсодержащих структур мочевого пузыря, не подвергнутого лучевому воздействию. На полученных МФМ-изображениях хорошо различимы слизистая оболочка с ее собственной пластинкой, подслизистая основа и элементы мышечного слоя стенки органа (рис. 1, а, белая стрелка). Эпителий слизистой оболочки мочевого пузыря (уротелий) представлен ровным пластом плотно прилегающих друг к другу клеток, при этом соединительнотканных элементов в межклеточных пространствах не зафиксировано (рис. 1, а, красная стрелка). Базальная мембрана представляет собой совокупность коллагеновых и эластических волокон с преобладанием последних и отличается ровным контуром, повторяющим ход эпителиального пласта (рис. 1, а, желтая стрелка). Ее толщина достигает 21 мкм. В собственной пластинке слизистой оболочки и подслизистом слое, представленных сетью коллагеновых волокон с небольшой примесью эластических и некоторым количеством мышечных элементов, определяются артериолы, венулы и капилляры с содержанием в адвентиции сосудов и базальной мембране эндотелия только коллагеновых волокон. Мышечные волокна формируют пучки приблизительно одинаковой толщины, идущие в разных направлениях, детерминированных функциональной нагрузкой. Между мышечными пучками располагается небольшое количество коллагеновых волокон с единичными эластическими волокнами, которые представляют собой каркас мышечного слоя (рис. 1, а, голубая стрелка). В интактном мочевом пузыре крыс основными локализациями коллаген- и эластинсодержащих элементов являются: базальная мембрана уротелия, собственная пластинка слизистой оболочки, подслизистая основа, стенки кровеносных сосудов и стромальный каркас мышечной оболочки. Соотношение коллагеновые волокна/эластические волокна в разных структурах — различное. Базальная мембрана эпителия отличается преобладанием эластических волокон; собственная пластинка слизистой оболочки, подслизистый слой, стенки кровеносных сосудов и стромальный каркас мышечной оболочки демонстрируют преимущественное содержание коллагеновых волокон.
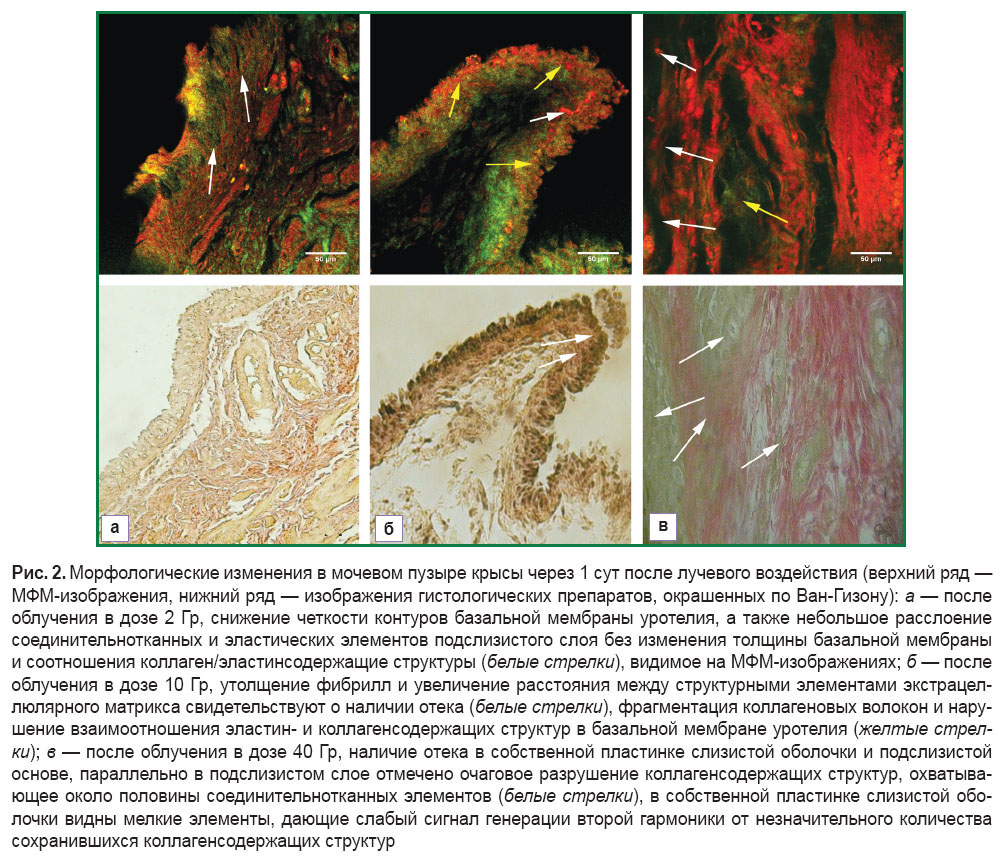
Изменения, обнаруженные в стенке мочевого пузыря через 1 сут после облучения, существенно зависят от величины радиационной нагрузки. После воздействия в дозе 2 Гр на МФМ-изображениях отмечается незначительное снижение четкости контуров базальной мембраны уротелия, а также слабое набухание основного вещества экстрацеллюлярного матрикса, расположенного между коллаген- и эластинсодержащими элементами подслизистого слоя, при этом существенного изменения толщины базальной мембраны и соотношения коллаген/эластинсодержащие структуры не наблюдается (рис. 2, а, верхний ряд). Данные изменения могут служить проявлениями поверхностной дезорганизации экстрацеллюлярного матрикса (мукоидное набухание). Нарушений со стороны соединительнотканных элементов стенок кровеносных сосудов и мышечного слоя не обнаружено. Следует заметить, что вышеописанные изменения мочевого пузыря через 1 сут после облучения в дозе 2 Гр при рутинной световой микроскопии не определяются (рис. 2, а, нижний ряд).
Через 1 сут после облучения в дозе 10 Гр на МФМ-изображениях был выявлен отек подслизистого слоя, проявившийся в виде утолщения фибрилл и увеличения расстояния между структурными элементами экстрацеллюлярного матрикса (рис. 2, б, верхний ряд). В базальной мембране уротелия отмечается фрагментация коллагеновых волокон и нарушение взаимоотношения эластин- и коллагенсодержащих структур, т.е. происходит разрушение соединительнотканных структур, не видимое при обычной микроскопии (рис. 2, б, нижний ряд).
Через 1 сут после воздействия в дозе 40 Гр на МФМ-изображениях в волокнистом каркасе обнаружены ожидаемо более грубые деструктивные процессы. В собственной пластинке слизистой оболочки и подслизистой основе отмечается отек, а в подслизистом слое параллельно — очаговое разрушение коллагенсодержащих структур, охватывающее около половины соединительнотканных элементов. Обращает на себя внимание практически полное отсутствие сигнала в диапазоне 352–416 нм (рис. 2, в, верхний ряд). В собственной пластинке слизистой оболочки определялись мелкие элементы, дающие сигнал генерации второй гармоники, которые являлись, по всей видимости, не до конца разрушенными коллагенсодержащими объектами.
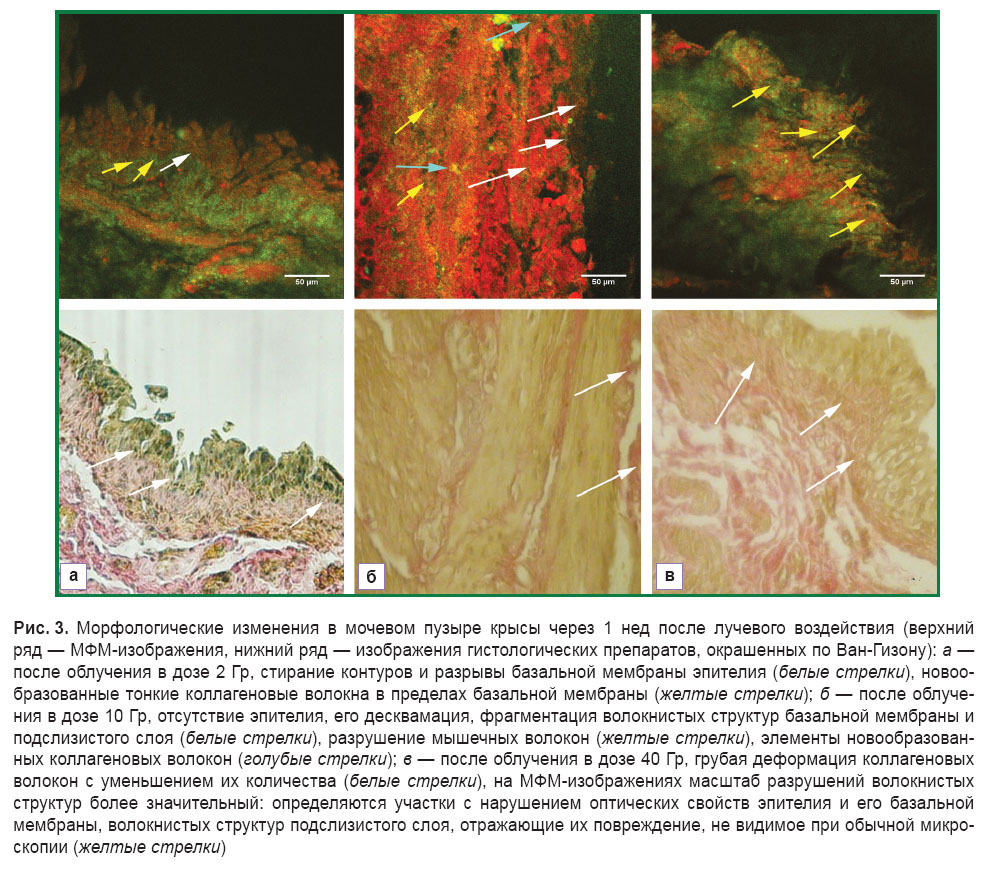
Динамическое наблюдение за состоянием фибриллярных структур было продолжено через 1 нед после лучевого воздействия. После облучения в дозе 2 Гр на МФМ-изображениях определялись неравномерность, прерывистость и ослабление сигнала в диапазоне 362–416 нм, наблюдаемые в зоне уротелия, его базальной мембраны и подслизистом слое (рис. 3, а, верхний ряд). Эти изменения служили отражением альтерации, структурными проявлениями которой являлись стирание контуров базальной мембраны эпителия, появление в ней разрывов, и в целом совпадали с картиной, наблюдаемой обычно в гистологических препаратах (рис. 3, б, нижний ряд). В пределах базальной мембраны уротелия найдены единичные тонкие коллагеновые волокна, отличающиеся от ранее наблюдаемых интенсивностью МФМ-сигнала, что нами было расценено как проявление неоколлагеногенеза (начало репаративных процессов) (см. рис. 3, а, верхний ряд). Изменений в волокнистых элементах кровеносных сосудов и каркаса мышечного слоя не было.
Через 1 нед после облучения в дозе 10 Гр во всех отделах стенки мочевого пузыря выявлены альтеративные процессы в виде крупных участков слущивания уротелия, фрагментации волокнистых структур базальной мембраны и подслизистого слоя. При этом на МФМ-изображениях более яркими по сравнению со стандартным окрашиванием были проявления разрушения коллагеновых волокон в виде их гомогенизации и фрагментации, что отражалось как диффузное снижение сигнала в диапазоне 362–416 нм (рис. 3, б, верхний ряд). Среди элементов разрушенного коллагена визуализировались тонкие коллагенсодержащие фибриллы без признаков дезорганизации, что позволило отнести их к новообразованным волокнам. Параллельно было выявлено разрушение гладкомышечных волокон, которое не обнаруживалось при рутинном гистологическом исследовании (см. рис. 3, б, нижний ряд).
Картина структурных изменений, обнаруженных через 1 нед после лучевого воздействия при дозе 40 Гр при обычной микроскопии, мало чем отличалась от изменений, отмеченных через 1 сут при той же дозе, и характеризовалась грубой деформацией пучков коллагеновых волокон с уменьшением их количества (рис. 3, в, нижний ряд). На МФМ-изображениях масштаб разрушений волокнистых структур был значительным: общая анатомическая структура слизистой оболочки нарушена, эпителий слущен, на некоторых участках отчетливо видно полное разрушение базальной мембраны уротелия (сигнал генерации второй гармоники в диапазоне 362–416 нм практически полностью отсутствовал). В мышечном слое наблюдался отек с хаотичным расположением волокон и их фрагментацией. При этом признаков появления новых коллаген- и эластинсодержащих структур не обнаружено (рис. 3, в, верхний ряд). Мы полагаем, что в данном случае имеет место «запаздывание» репаративных процессов, обусловленное блокированием их запуска вследствие использования высокой дозы облучения.
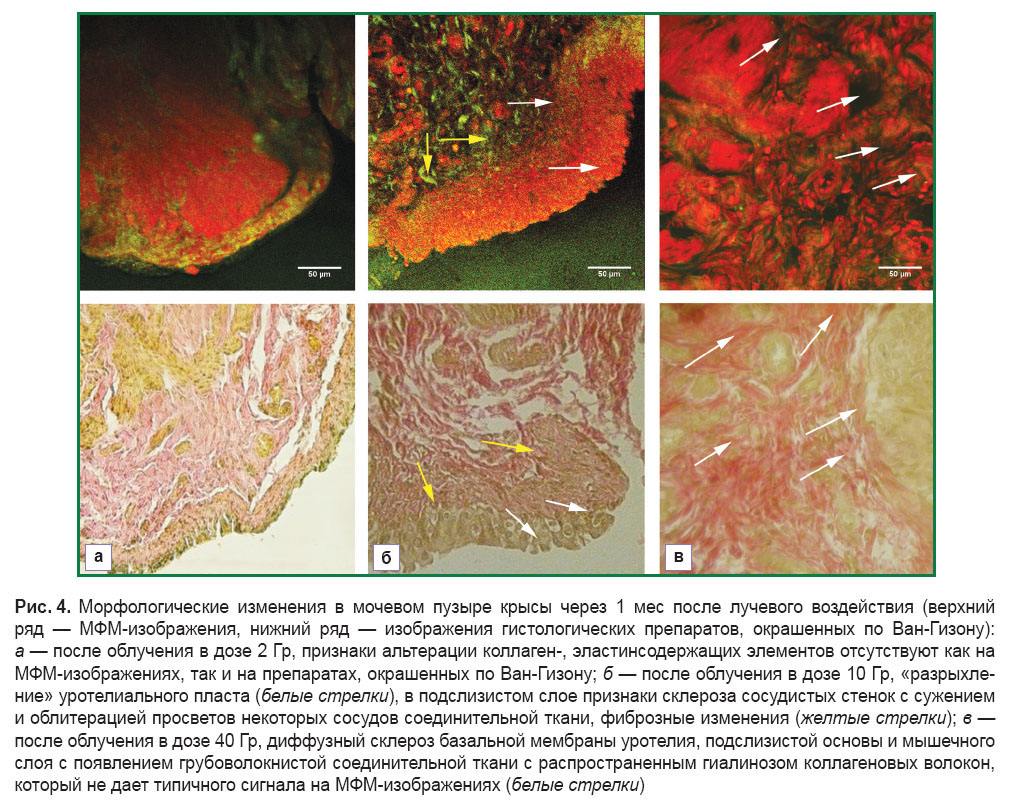
При изучении препаратов мочевого пузыря спустя 1 мес после облучения в дозе 2 Гр признаки альтерации коллаген- и эластинсодержащих элементов отсутствовали как на МФМ-изображениях (рис. 4, а, верхний ряд), так и на препаратах, окрашенных по Ван-Гизону (рис. 4, а, нижний ряд).
Морфологические изменения, обнаруженные через 1 мес после облучения в дозе 10 Гр, характеризовались «разрыхлением» уротелиального пласта, что обусловлено, по всей видимости, ослаблением межклеточных взаимосвязей вследствие высокого содержания разрушенных соединительнотканных элементов в базальной мембране, мышечной пластинке слизистой оболочки и подслизистом слое. В свою очередь в подслизистом слое были обнаружены признаки формирующегося фиброза экстрацеллюлярного матрикса и редукция сосудистого русла (развитие склероза сосудистых стенок с сужением и облитерацией просветов некоторых сосудов соединительной ткани).
При исследовании мочевого пузыря через 1 мес после применения дозы 40 Гр в препаратах, окрашенных по Ван-Гизону, обнаружен диффузный склероз базальной мембраны уротелия, подслизистой основы и мышечного слоя с появлением грубоволокнистой соединительной ткани с распространенным гиалинозом коллагеновых волокон (рис. 4, в, нижний ряд). Данный тип коллагена не давал типичного сигнала генерации второй гармоники на МФМ-изображениях (рис. 4, в, верхний ряд).
Обсуждение. В данном исследовании изучение морфологических изменений стенки мочевого пузыря экспериментальных животных в различные сроки после однократного локального гамма-облучения в дозе 2, 10 и 40 Гр выполнено методом МФМ. Основные биомедицинские приложения метода были до настоящего времени связаны с дифференциальной диагностикой нормальных и патологических тканей [25]. В нашем исследовании этот метод был впервые применен для динамической оценки состояния органа, подвергнутого воздействию ионизирующего излучения.
Как при гистологическом исследовании, так и при использовании метода МФМ в мочевом пузыре были установлены два параллельно идущих процесса: разрушение (дезорганизация) и восстановление поврежденных структур коллагенсодержащих элементов. Дезорганизация волокнистого каркаса структурных элементов стенки мочевого пузыря при гистологическом исследовании по Ван-Гизону проявлялась в виде набухания, фибриноидных изменений и фрагментации коллагеновых элементов вплоть до их полного разрушения при использовании высоких доз облучения (40 Гр). Этим изменениям соответствовало диффузное снижение сигнала в диапазоне 362–416 нм на МФМ-изображениях. Аналогичные изменения (снижение интенсивности сигнала генерации второй гармоники коллагена) были детектированы при in vivo мониторинге состояния кожи после термического ожога [26], а также при системных заболеваниях, характеризующихся дезорганизацией соединительнотканных структур внутренних органов [27]. Наше исследование подтвердило, что данный феномен можно считать универсальным признаком дезорганизации структуры соединительнотканного матрикса. Метод МФМ позволил наблюдать развитие повреждения волокнистых структур в более ранние сроки и при меньших дозах облучения, чем при рутинном гистологическом исследовании (через 1 сут после использования дозы 2 Гр).
Было продемонстрировано, что процессы развития повреждения и последующего ремоделирования экстрацеллюлярного матрикса органа под воздействием ионизирующего излучения носят этапный характер и начинаются с дезорганизации и деградации коллагена на уровне волокон и пучков, что удается обнаружить в ранние сроки уже после облучения в дозе 2 Гр. Следующим этапом ответа ткани на радиационное повреждение является восстановление — процесс неоколлагеногенеза, начало которого было зафиксировано уже через 1 нед после повреждающего воздействия. Кроме того, установлено, что скорость процессов ремоделирования экстрацеллюлярного матрикса зависит от дозы облучения и существенно замедляется при воздействии более высоких доз (40 Гр). Проведенное исследование открывает новые возможности изучения состояния нормальных тканей, подвергнутых воздействию ионизирующего излучения. Дальнейшая работа в этом направлении связана с разработкой методик мониторинга радиационно-индуцированных повреждений in vivo с помощью метода МФМ.
Заключение. Метод многофотонной микроскопии в отличие от традиционного гистологического исследования позволяет обнаружить деградацию коллагена тканей мочевого пузыря и его восстановление в более ранние сроки и при меньшей дозе радиационного воздействия, что дает возможность оценивать и корректировать динамику радиационных изменений в экстрацеллюлярном матриксе.
Финансирование исследования. Финансирование исследования. Работа выполнена при поддержке РНФ (проект №14-25-00055, выполнение исследований радиационно-индуцированных изменений методом лазерной сканирующей микроскопии), РФФИ (проект №16-02-00670, выполнение радиационного воздействия, исследование радиационно-индуцированных изменений методом стандартного гистологического исследования).
Конфликт интересов. У авторов нет конфликта интересов.
Литература
- Dörr W. Radiation effect in normal tissue — principles of damage and protection. Nuklearmedizin 2010; 49(Suppl 1): S53–S58.
- Fiorino C., Valdagni R., Rancati T., Sanguineti G. Dose-volume effects for normal tissues in external radiotherapy: pelvis. Radiother Oncol 2009; 93(2): 153–167, http://dx.doi.org/10.1016/j.radonc.2009.08.004.
- Yarnold J., Brotons M.C.V. Pathogenetic mechanisms in radiation fibrosis. Radiother Oncol 2010; 97(1): 149–161, http://dx.doi.org/10.1016/j.radonc.2010.09.002.
- Stewart F.A., Akleyev A.V., Hauer-Jensen M., Hendry J.H., Kleiman N.J., Macvittie T.J., Aleman B.M., Edgar A.B., Mabuchi K., Muirhead C.R., Shore R.E., Wallace W.H. ICRP publication 118: ICRP statement on tissue reactions and early and late effects of radiation in normal tissues and organs — threshold doses for tissue reactions in a radiation protection context. Ann ICRP 2012; 41(1–2): 1–322, http://dx.doi.org/10.1016/j.icrp.2012.02.001.
- Brush J., Lipnick S.L., Phillips T., Sitko J., McDonald J.T., McBride W.H. Molecular mechanisms of late normal tissue injury. Semin Radiat Oncol 2007; 17(2): 121–130, http://dx.doi.org/10.1016/j.semradonc.2006.11.008.
- Maslennikova A., Kochueva M., Ignatieva N., Vitkin A., Zakharkina O., Kamensky V., Sergeeva E., Kiseleva E., Bagratashvili V. Effects of gamma irradiation on collagen damage and remodeling. Int J Radiat Biol 2015; 91(3): 240–247, http://dx.doi.org/10.3109/09553002.2014.969848.
- Göppert-Mayer M. Über elementarakte mit zwei quantensprüngen. Ann Phys 1931; 401(3): 273–295, http://dx.doi.org/10.1002/andp.19314010303.
- Alex A., Weingast J., Weinigel M., Kellner-Höfer M., Nemecek R., Binder M., Pehamberger H., König K., Drexler W. Three-dimensional multiphoton/optical coherence tomography for diagnostic applications in dermatology. J Biophotonics 2013; 6(4): 352–362, http://dx.doi.org/10.1002/jbio.201200085.
- Denk W., Strickler J.H., Webb W.W. Two-photon laser scanning fluorescence microscopy. Science 1990; 248(4951): 73–76, http://dx.doi.org/10.1126/science.2321027.
- Theodossiou T.A., Thrasivoulou C., Ekwobi C., Becker D.L. Second harmonic generation confocal microscopy of collagen type I from rat tendon cryosections. Biophys J 2006; 91(12): 4665–4677, http://dx.doi.org/10.1529/biophysj.106.093740.
- Seidenari S., Arginelli F., Bassoli S., Cautela J., French P.M., Guanti M., Guardoli D., König K., Talbot C., Dunsby C. Multiphoton laser microscopy and fluorescence lifetime imaging for the evaluation of the skin. Dermatol Res Pract 2012; 2012: 810749, http://dx.doi.org/10.1155/2012/810749.
- Williams R.M., Zipfel W.R., Webb W.W. Interpreting second-harmonic generation images of collagen I fibrils. Biophys J 2005; 88(2): 1377–1386, http://dx.doi.org/10.1529/biophysj.104.047308.
- Raub C.B., Unruh J., Suresh V., Krasieva T., Lindmo T., Gratton E., Tromberg B.J., George S.C. Image correlation spectroscopy of multiphoton images correlates with collagen mechanical properties. Biophys J 2008; 94(6): 2361–2373, http://dx.doi.org/10.1529/biophysj.107.120006.
- Chen J., Wong S., Nathanson M.H., Jain D. Evaluation of Barrett esophagus by multiphoton microscopy. Arch Pathol Lab Med 2014; 138(2): 204–212, http://dx.doi.org/10.5858/arpa.2012-0675-OA.
- Dimitrow E., Ziemer M., Koehler M.J., Norgauer J., König K., Elsner P., Kaatz M. Sensitivity and specificity of multiphoton laser tomography for in vivo and ex vivo diagnosis of malignant melanoma. J Invest Dermatol 2009; 129(7): 1752–1758, http://dx.doi.org/10.1038/jid.2008.439.
- Balu M., Kelly K.M., Zachary C.B., Harris R.M., Krasieva T.B., König K., Durkin A.J., Tromberg B.J. Distinguishing between benign and malignant melanocytic nevi by in vivo multiphoton microscopy. Cancer Res 2014; 74(10): 2688–2697, http://dx.doi.org/10.1158/0008-5472.CAN-13-2582.
- Huang A.S., Gonzalez J.M. Jr., Le P.V., Heur M., Tan J.C. Sources of structural autofluorescence in the human trabecular meshwork.Invest Ophthalmol Vis Sci 2013; 54(7): 4813–4820, http://dx.doi.org/10.1167/iovs.12-11235.
- Morishige N., Yamada N., Zhang X., Morita Y., Yamada N., Kimura K., Takahara A., Sonoda K.H. Abnormalities of stromal structure in the bullous keratopathy cornea identified by second harmonic generation imaging microscopy. Invest Ophthalmol Vis Sci 2012; 53(8): 4998–5003, http://dx.doi.org/10.1167/iovs.12-10214.
- Koehler M.J., König K., Elsner P., Bückle R., Kaatz M. In vivo assessment of human skin aging by multiphoton laser scanning tomography. Opt Lett 2006; 31(19): 2879–2881, http://dx.doi.org/10.1364/ol.31.002879.
- Tsai T.H., Jee S.H., Dong C.Y., Lin S.J. Multiphoton microscopy in dermatological imaging. J Dermatol Sci 2009; 56(1): 1–8, http://dx.doi.org/10.1016/j.jdermsci.2009.06.008.
- Cicchi R., Matthäus C., Meyer T., Lattermann A., Dietzek B., Brehm B.R., Popp J., Pavone F.S. Non-linear imaging and characterization of atherosclerotic arterial tissue using combined two photon fluorescence, second-harmonic generation and CARS microscopy. Proc. SPIE8948, Multiphoton Microscopy in the Biomedical Sciences XIV, 894807 (February 28, 2014), http://dx.doi.org/10.1117/12.203701822.
- Chen W.S., Wang Y., Liu N.R., Zhang J.X., Chen R. Multiphoton microscopic imaging of human normal and cancerous oesophagus tissue. J Microsc 2014; 253(1): 79–82, http://dx.doi.org/10.1111/jmi.12102.
- Paoli J., Smedh M., Ericson M.B. Multiphoton laser scanning microscopy — a novel diagnostic method for superficial skin cancers.Semin Cutan Med Surg 2009; 28(3): 190–195, http://dx.doi.org/10.1016/j.sder.2009.06.007.
- Burke K., Tang P., Brown E. Second harmonic generation reveals matrix alterations during breast tumor progression. J Biomed Opt 2012; 18(3): 031106, http://dx.doi.org/10.1117/1.JBO.18.3.031106.
- Campagnola P. Second harmonic generation imaging microscopy: applications to diseases diagnostics. Anal Chem 2011; 83(9): 3224–3231, http://dx.doi.org/10.1021/ac1032325.
- Yasui T., Tanaka R., Hase E., Fukushima Sh., Araki T. In vivo time-laps imaging of skin-burn wound healing using second-harmonic generation microscopy. Proc. SPIE 8948, Multiphoton Microscopy in the Biomedical Sciences XIV, 89480B (February 28, 2014), http://dx.doi.org/10.1117/12.2038022.
- Kiseleva E., Kirillin M., Feldchtein F., Vitkin A., Sergeeva E., Zagaynova E., Streltzova O., Shakhov B., Gubarkova E., Gladkova N. Differential diagnosis of human bladder mucosa pathologies in vivo with cross-polarization optical coherence tomography. Biomed Opt Express 2015; 6(4): 1464–1476, http://dx.doi.org/10.1364/BOE.6.001464.