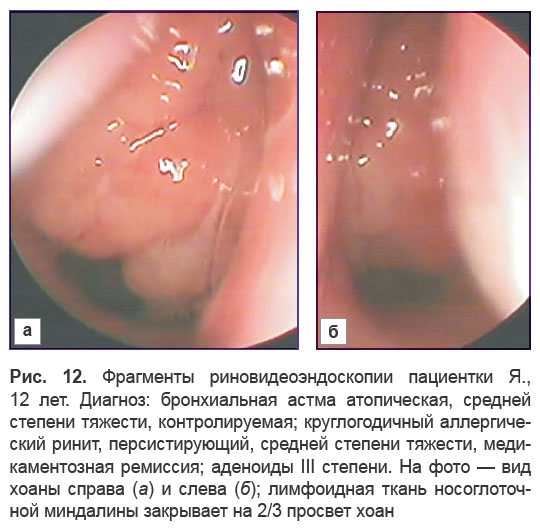
Возможности риновидеоэндоскопии в диагностике состояния глоточной миндалины у детей с бронхиальной астмой
Цель исследования — оценить возможности риновидеоэндоскопии в диагностике состояния глоточной миндалины у детей с атопической бронхиальной астмой (БА).
Материалы и методы. С использованием жестких риноскопов (Кarl Storz, Германия) с углом зрения 0 и 30° диаметром 2,7 и 4,0 мм, ларингоскопа 90° (Atmos, Германия) и гибкого назофарингоскопа 3,2 мм, видеокамеры (Atmos, Германия) проведено изучение состояния глоточной миндалины у 116 пациентов с атопической БА различной степени тяжести, имевших жалобы на нарушение носового дыхания, в возрасте от 3 до 17 лет (средний возраст 9,7±4,3 года). Контрольную группу составили 108 детей с жалобами на нарушения носового дыхания, сопоставимых по возрасту и полу, не имевших БА.
Результаты. Применение метода риновидеоэндоскопии позволило установить, что среди детей с БА частота встречаемости гипертрофии глоточной миндалины II–III степеней во все возрастные периоды статистически значимо превышает таковую у детей группы контроля (без БА). По данным этого исследования, гипертрофия глоточной миндалины вносит существенный вклад в формирование назальной обструкции у 86,1% детей с БА дошкольного возраста, у 74,2% детей младшего школьного возраста, у 45,8% детей старшего школьного возраста и у 20% подростков, что должно быть учтено при ведении данных пациентов.
Заключение. Метод риновидеоэндоскопии позволяет в значительной степени устранить диагностические трудности и позволяет объективно оценить состояние глоточной миндалины у пациентов с бронхиальной астмой различного возраста. Заслуга риновидеоэндоскопии — в получении новых данных о том, что гипертрофия глоточной миндалины в целом более распространена в группе пациентов с астмой, чем среди детей, не имеющих этого заболевания, что необходимо учитывать при ведении данных пациентов.
При изучении взаимосвязи аллергических заболеваний респираторного тракта и патологии лимфоэпителиального кольца глотки вызывает большой интерес состояние глоточной миндалины [1]. В норме максимальное развитие аденоидной ткани наблюдается у детей в возрасте от 3 до 5 лет, оно носит физиологический характер и обусловлено закономерными транзиторными изменениями иммунной системы, свойственными данному возрасту. При отсутствии патологии с 5–7-летнего возраста, как правило, начинается естественная инволюция глоточной миндалины [2]. Гипертрофия глоточной миндалины (ГГМ) может развиваться у пациентов с респираторной инфекцией, локализующейся в верхних дыхательных путях (ВДП), и довольно характерна также, по мнению некоторых авторов [3, 4], для пациентов с аллергическими заболеваниями респираторного тракта, включая бронхиальную астму (БА).
Аллергическое воспаление, являющееся патогенетической основой БА, локализуется не только в структурах бронхиального дерева, но и затрагивает ВДП (единые дыхательные пути — единая болезнь) и асcоциированную со слизистыми оболочками MALT-систему (Mucosa associated lymphoid tissue) [5]. Ретроназальная направленность мукоцилиарного транспорта определяет ведущую роль глоточной миндалины как индуктивного органа мукозального иммунитета ВДП [6]. Основной поток антигенов задерживается и улавливается в первую очередь эпителиальными структурами глоточной миндалины. Взаимодействуя с вирусно-микробным окружением и респираторными аллергенами, глоточная миндалина осуществляет барьерную функцию слизистых оболочек, участвует в формировании мукозального иммунитета и в патогенезе воспалительных процессов в полости носа и околоносовых пазухах [7].
Структурной основой иммунного ответа носоглоточной миндалины является гиперплазия ее лимфоидной ткани [8]. Ранее нами было показано [9], что ГГМ у пациентов с БА может усугублять симптомы назальной обструкции, свойственные данному контингенту больных вследствие частой коморбидности БА и аллергического ринита.
Существует мнение, что у детей с атопией риск формирования ГГМ и степень гипертрофии выше, чем в популяции в целом [3, 10–12]. У детей с аллергическими заболеваниями дыхательных путей патология лимфоэпителиального глоточного кольца может усугубить течение основного заболевания и является дополнительным фактором, отягощающим качество жизни больного [13]. Взаимосвязь алергического ринита и ГГМ подтверждается редукцией лимфоэпителиальных структур носоглоточной миндалины и уменьшением симптомов назальной обструкции на фоне применения топических стероидов и антигистаминных препаратов [14, 15].
Современные исследования свидетельствуют, что воспалительные изменения в носоглотке у пациентов с БА приводят к системным эффектам вследствие системной адсорбции медиаторов воспаления, синтезированных в ВДП [16]. Воспалительная постнатальная секреция влияет на нижележащие дыхательные пути. В литературе обсуждается влияние назобронхиального рефлекса на течение БА у пациентов, имеющих коморбидные заболевания со стороны ВДП. По мнению B. Undem и соавт., раздражение рецепторов слизистой оболочки полости носа может приводить к развитию удушья, возникновению кашля или бронхоспазма у больных БА [17–19]. Это свидетельствует о необходимости тщательной диагностики и лечения патологии ВДП у пациентов для достижения более полного контроля БА.
Истинную распространенность ГГМ и заболеваний, ассоциированных с данным компонентом лимфоэпителиального кольца глотки, у детей с БА в настоящее время нельзя считать установленной. Это связано в том числе и с тем, что диагностика патологии лимфоэпителиального кольца глотки продолжает оставаться сложной задачей. При этом особую сложность вызывает описание состояния глоточной миндалины, так как ее визуализация при стандартном оториноларингологическом осмотре невозможна из-за особенностей топографии. Существуют различные рекомендации по диагностике патологии носоглотки, такие как рентгенография шеи в боковой проекции, пальпаторное исследование носоглотки, задняя непрямая риноскопия и видеоэндоскопическое исследование. Однако информативность каждого из перечисленных диагностических методов очевидно недостаточна [20].
Нами для оценки состояния глоточной миндалины был выбран метод риновидеоэндоскопии как наиболее информативный, экспрессный из имеющихся современных методов и не ассоциированный с лучевой нагрузкой.
Цель исследования — оценить возможности риновидеоэндоскопии в диагностике состояния глоточной миндалины у детей с атопической бронхиальной астмой.
Материалы и методы. Проведен анализ результатов обследования 116 пациентов с атопической БА различной степени тяжести в сочетании с патологией ВДП в возрасте от 3 до 17 лет (средний возраст — 9,7±4,3 года), из них мальчиков — 87, девочек — 29. Выделены следующие возрастные группы: дошкольный возраст (от 3 до 6 лет) — 36 детей, младший школьный возраст (от 7 до 11 лет) — 35, старший школьный возраст (от 12 до 14 лет) — 24, подростковый возраст (от 15 до 17 лет) — 21. Контрольную группу составили 108 детей без БА, имеющих жалобы на нарушение носового дыхания, сопоставимых по возрасту и полу: дошкольный возраст — 34 ребенка, младший школьный возраст — 39 детей, старший школьный возраст — 20 и подростковый возраст — 15.
Верификацию диагноза БА выполняли в соответствии с рекомендациями Национальной программы «Бронхиальная астма у детей. Стратегия лечения и профилактика» и с учетом положений Глобальной стратегии лечения и профилактики бронхиальной астмы пересмотров 2011–2015 гг. [21, 22]. Критериями исключения служили наличие симптомов острой респираторной инфекции и повышение температуры.
Обследование детей проводили на базе Городской детской клинической больницы №1 Нижнего Новгорода и клиники НижГМА «Александрия». Оно включало в себя общеклиническое обследование согласно отраслевым медицинским стандартам, лабораторные и инструментальные методы исследования, определение параметров функции внешнего дыхания, кожные пробы с небактериальными аллергенами, определение общего и аллергенспецифических IgE. При изучении данных анамнеза и клинического обследования оценивали тяжесть БА и уровень контроля заболевания согласно критериям GINA (Global initiative asthma guidelines) и укороченной версии теста Asthma Control Questionnaire-5 (ACQ-5) по истории болезни или по записям в амбулаторной карте. Исследование осуществлено в соответствии с Хельсинкской декларацией (принятой в июне 1964 г. (Хельсинки, Финляндия) и пересмотренной в октябре 2000 г. (Эдинбург, Шотландия)) и одобрено Этическим комитетом Первого МГМУ им. И.М. Сеченова. Информированное согласие получено от всех пациентов в возрасте 15–17 лет и от родителей пациентов, не достигших 15-летнего возраста, согласно Федеральному закону «Основы законодательства Российской Федерации об охране здоровья граждан» от 22 июля 1993 г. №54871.
При оценке патологии ВДП верификацию диагнозов проводили с учетом Международной классификации болезней IХ пересмотра (МКБ-Х) [23], рекомендаций «Аллергический ринит и его влияние на бронхиальную астму ARIA» [24], Международного консенсуса по диагностике и лечению ринита [25], Европейского руководства по риносинуситу и полипам носа [26], классификации патологии лимфоэпителиального кольца глотки [27, 28].
Диагноз аллергического ринита формировали на основании результатов анамнеза, оценки клинических симптомов (назальной обструкции, зуда, чихания, ринореи, данных визуальной оценки — риноскопии). При этом оценивали цвет, тонус, наличие отека, гипертрофические изменения слизистой оболочки носовой полости, наличие и характер выделений в носовых ходах.
Исследование ВДП включало помимо стандартного осмотра ЛОР-органов видеоэндоскопическое обследование полости носа и носоглотки с применением эндоскопической техники и эндоскопического фотографирования. Применяли жесткие риноскопы фирмы Кarl Storz (Германия) с углом зрения 0 и 30°, диаметром 2,7 и 4,0 мм; видеоларингоскопию выполняли ларингоскопом 90° (Atmos, Германия) и гибким назофарингоскопом 3,2 мм; видеофиксацию — видеокамерой (Atmos, Германия). Риновидеоскопическое обследование проводили после инстилляции 2% раствора лидокаина на слизистую оболочку полости носа и аппликационной анестезии с применением 0,1% раствора адреналина гидрохлорида и 10% лидокаина.
При осмотре носоглотки оценивали размеры глоточной миндалины, наличие воспалительной реакции ткани, характер и количество секрета на поверхности миндалины. Также проводили оценку трубных миндалин, зоны устьев слуховых труб. Обработку и архивирование результатов видеоэндоскопического обследования осуществляли на персональном компьютере в графическом редакторе Adobe Photoshop.
Статистический анализ выполнен с применением программ Statgraphics plus и Biostаt. Данные представлены в виде M±m, где М — среднее,m— стандартное отклонение. Статистические различия количественных признаков оценены с применением критерия Стьюдента и ANOVA, качественные — с использованием критерия χ2. Различия считали статистически значимыми при р<0,05.
Результаты и обсуждение. Детальное обследование патологии ВДП у детей с атопической БА различной степени тяжести, имевших жалобы на затруднение носового дыхания, позволило выявить у них различные варианты нарушений, при этом отмечено явное преобладание изменений со стороны носовой полости. У всех обследованных детей диагностирован аллергический ринит различной степени тяжести [29]. Применение риновидеоэндоскопического метода диагностики позволило комплексно и с большой степенью точности оценить состояние структур носа и носоглотки, патологические изменения лимфоидной ткани и сопряженные с ними заболевания ЛОР-органов.
Патология глоточной миндалины была диагностирована у 62,0% (72/116) обследованных пациентов с атопической БА. Корреляции данной патологии с тяжестью течения БА не обнаружено (F=0,91; р=0,34). По данным риновидеоэндоскопического обследования ГГМ II степени (глоточная миндалина закрывала просвет хоан не менее, чем на 1/2 (рис. 1)) была установлена у 29,3% детей (34/116).
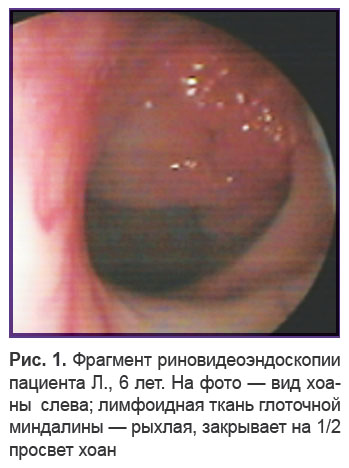 Рис. 1. Фрагмент риновидеоэндоскопии пациента Л., 6 лет. На фото — вид хоаны слева; лимфоидная ткань глоточной миндалины — рыхлая, закрывает на 1/2 просвет хоан Рис. 1. Фрагмент риновидеоэндоскопии пациента Л., 6 лет. На фото — вид хоаны слева; лимфоидная ткань глоточной миндалины — рыхлая, закрывает на 1/2 просвет хоан
|
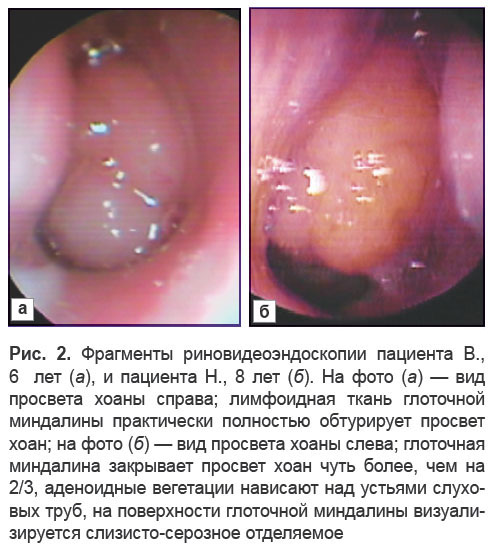
Аденоидные вегетации III степени наблюдались у 32,7% пациентов (38/116). В данной группе ткань ГГМ закрывала просвет хоан на 2/3 и более (рис. 2).
Таким образом, в целом аденоидная гипертрофия, выявляемая методом риновидеоэндоскопии, отмечена более чем у половины обследованных пациентов с БА, и у 32,7% детей с БА увеличение глоточной миндалины было значительным (III степень гипертрофии).
Поскольку аденотонзиллярная гипертрофия имеет возрастные закономерности, с помощью риновидеоэндоскопии проведен анализ частоты встречаемости лимфоэпителиальной гипертрофии с учетом возраста детей с БА. Установлено, что пациенты с увеличением глоточной миндалины встречаются во всех возрастных группах. Средний возраст детей с БА, имеющих нормальные размеры глоточной миндалины, составил 12,50±4,14 года. Дети с ГГМ в целом были статистически значимо младше — средний возраст данных пациентов составил 8,1±3,6 года (F=36,27; р<0,0001). При этом средний возраст пациентов с ГГМ II степени составил 9,2±4,0 года, пациентов с ГГМ III степени — 7,2±2,9 года (F=19,8;p<0,0001).
В связи с обнаруженной зависимостью состояния глоточной миндалины от возраста детей проведен анализ данных риновидеоэндоскопии носоглотки с учетом возраста пациентов с БА.
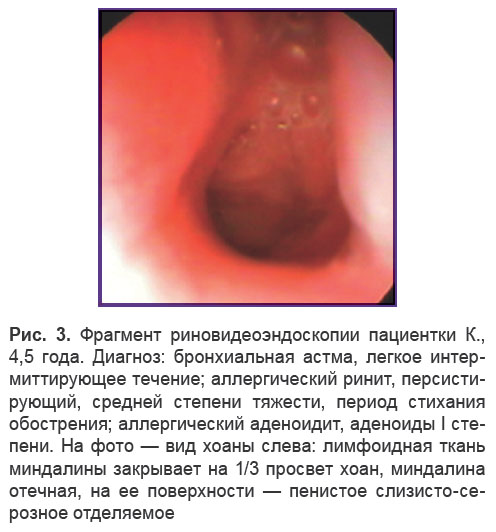
Младшая возрастная группа. У пациентов младшей возрастной группы (n=36) эндоскопическое исследование носа и носоглотки проводилось преимущественно с использованием гибкой оптики. В стадии обострения аллергического процесса наблюдались признаки аллергического аденоидита: бледно-розовый цвет лимфоидной ткани, выраженная отечность, сглаженность борозд, наличие на поверхности глоточной миндалины слизисто-серозного секрета (рис. 3).
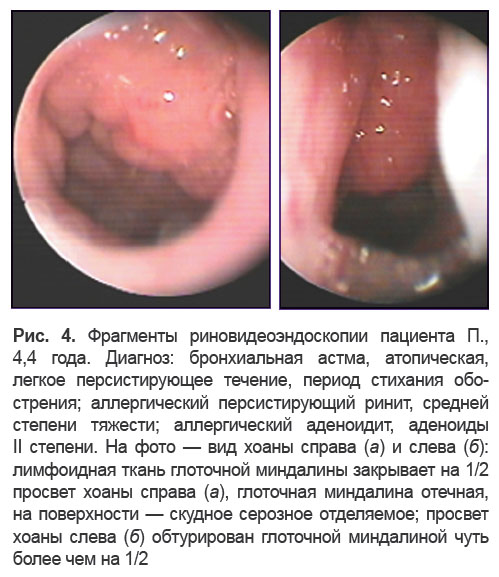
По результатам исследования, доля пациентов с ГГМ на фоне атопической БА в дошкольном возрасте достигает 86,1% (31/36). У 11 детей отмечена гипертрофия аденоидов II степени (рис. 4), у 20 детей — III степени (рис. 5).
Основной жалобой у пациентов с ГГМ как III, так и II степени было затруднение носового дыхания. При III степени нарушение носового дыхания носило стойкий характер, что было обусловлено механической обтурацией просвета хоан гипертрофированной тканью глоточной миндалины. При этом нередко отмечалось нависание лимфоидной ткани миндалины над устьями слуховых труб или полная их обструкция (см. рис. 5). Отоскопически у таких пациентов отмечалась втянутость барабанных перепонок, обусловленная дисфункцией слуховых труб.
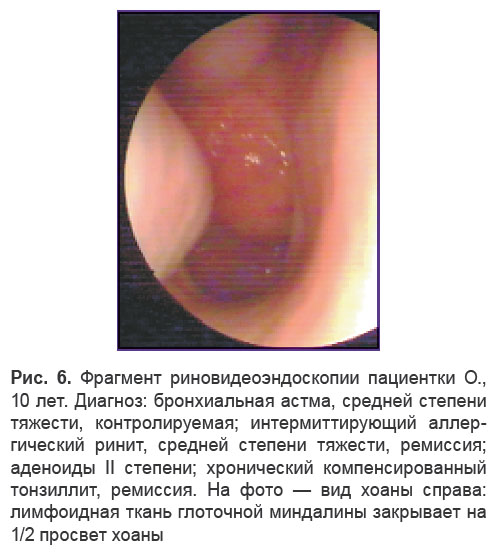
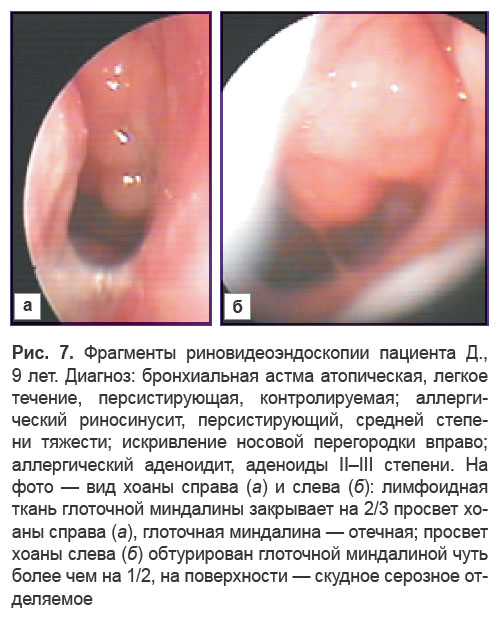
Средняя возрастная группа. У пациентов этой возрастной группы осмотр носа и носоглотки проводили с использованием как гибкой, так и ригидной оптики с углом обозрения 0°. По мере увеличения возраста детей отмечалось снижение частоты встречаемости гипертрофии глоточной миндалины до 74,3% (26/35). При этом у 13 пациентов отмечено увеличение глоточной миндалины до II степени — лимфоидная ткань миндалины закрывала у таких детей просвет хоан на 1/2 (рис. 6, 7).
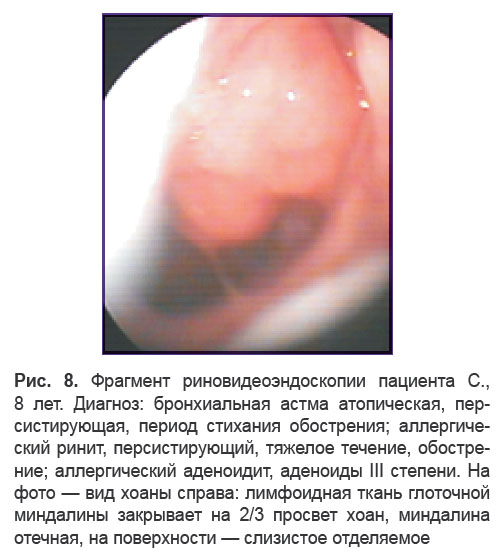
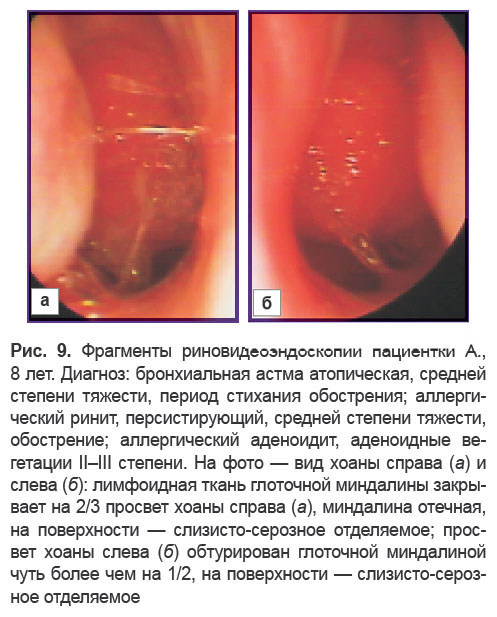
Еще у 13 детей с БА данной возрастной группы диагностированы аденоиды III степени (рис. 8, 9). Кроме нарушения носового дыхания, беспокоившего данных больных, у многих пациентов, особенно в стадии обострения аллергического ринита, отмечались жалобы на кашель, усиливающийся в горизонтальном положении (в том числе в ночные часы), что у детей с БА требует дифференцированного подхода к диагностике и терапии кашля. Эндоскопически для таких пациентов было характерно скопление в задних отделах нижних носовых ходов и на поверхности глоточной миндалины слизистого секрета, что четко визуализировалось в ходе риновидеоэндоскопического обследования.
Старшая возрастная группа. Метод риновидеоэндоскопии позволил выявить ГГМ у довольно значительной доли детей с БА старшей возрастной группы — 45,8% (11/24), что отличалось от данных у детей такого же возраста группы контроля, среди которых ГГМ (II степени) была выявлена лишь у 10% пациентов (2/20). Среди детей с БА в этой возрастной группе ГГМ II степени выявлена у 10 пациентов (рис. 10).
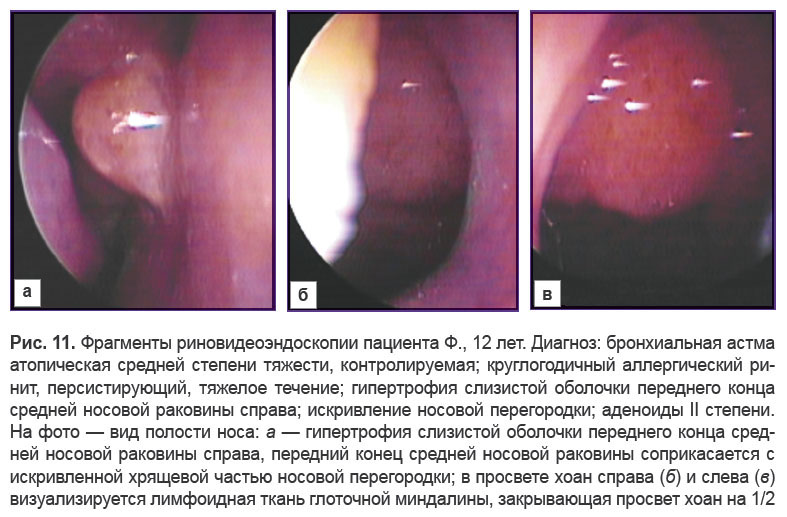
Аденоиды III степени среди детей данной группы выявлены у 20,8% (5/24) пациентов с БА. Видеоэндоскопическая инспекция позволила диагностировать у ряда пациентов наличие гипертрофических процессов не только в назально-ассоциированной лимфоидной ткани, но и в слизистой оболочке носовой полости (рис. 11, а). Так же, как и у детей младших возрастных групп, при значительных размерах глоточной миндалины отмечалась обструкция слуховых труб (рис. 12).
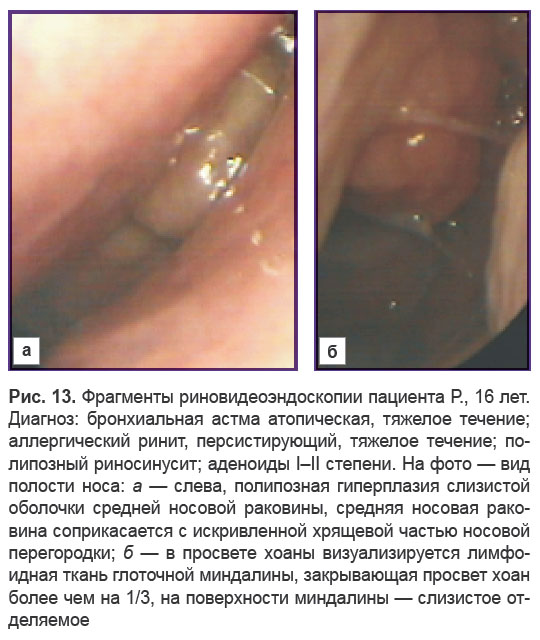
Подростки. Несмотря на то, что для пациентов с БА подростковой возрастной группы (n=21) в целом ГГМ не была характерна, применение метода риновидеоэндоскопии помогло выявить у 19% из них (4/21) ГГМ II степени (рис. 13). При этом видеоэндоскопическая инспекция дала возможность диагностировать у некоторых пациентов наличие гипертрофических процессов не только в назально-ассоциированной лимфоидной ткани, но и в слизистой оболочке носовой полости (рис. 13, а). Нарушения носового дыхания у части подростков усугублялись нарушениями архитектоники полости носа.
Таким образом,по данным риновидеоэндоскопии, ГГМ встречалась ожидаемо чаще у детей с БА дошкольного и младшего школьного возраста, чем среди пациентов старшей возрастной группы (z=5,1; р<0,0001), однако обращает на себя внимание отсутствие редукции глоточной миндалины у значительной доли детей с БА старшей возрастной группы и даже у некоторых подростков.
Сравнительная риновидеоэндоскопическая характеристика глоточной миндалины у пациентов с БА и у детей контрольной группы. Анализ возрастного состава показал, что ГГМ наиболее характерна для детей дошкольного и младшего школьного возраста как при БА, так и в контрольной группе, но при этом во все возрастные периоды величина глоточной миндалины у пациентов с БА в целом выше, чем у детей, не имеющих диагноза БА. Метод риновидеоэндоскопии позволил установить сохранение ГГМ у достаточно большого количества детей (у детей с БА старшей возрастной группы — 45,8% и даже у единичных пациентов в подростковой группе), что продемонстрировано на рис. 14.
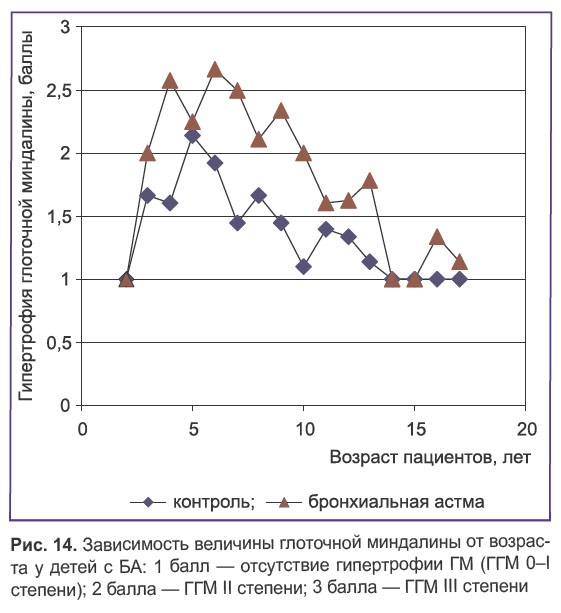 Рис. 14. Зависимость величины глоточной миндалины от возраста у детей с БА: 1 балл — отсутствие гипертрофии ГМ (ГГМ 0–I степени); 2 балла — ГГМ II степени; 3 балла — ГГМ III степени Рис. 14. Зависимость величины глоточной миндалины от возраста у детей с БА: 1 балл — отсутствие гипертрофии ГМ (ГГМ 0–I степени); 2 балла — ГГМ II степени; 3 балла — ГГМ III степени
|
Различия в состоянии глоточной миндалины у детей с БА и у детей без БА установлены во всех возрастных группах: в дошкольном возрасте — χ2=13,3; р=0,0013; в младшем школьном возрасте — χ2=16,2; р<0,0003; в старшем школьном возрасте — χ2=7,5; р<0,02. Среди подростков контрольной группы ГГМ не выявлена, тогда как среди подростков с БА у 4 пациентов отмечена ГГМ II степени.
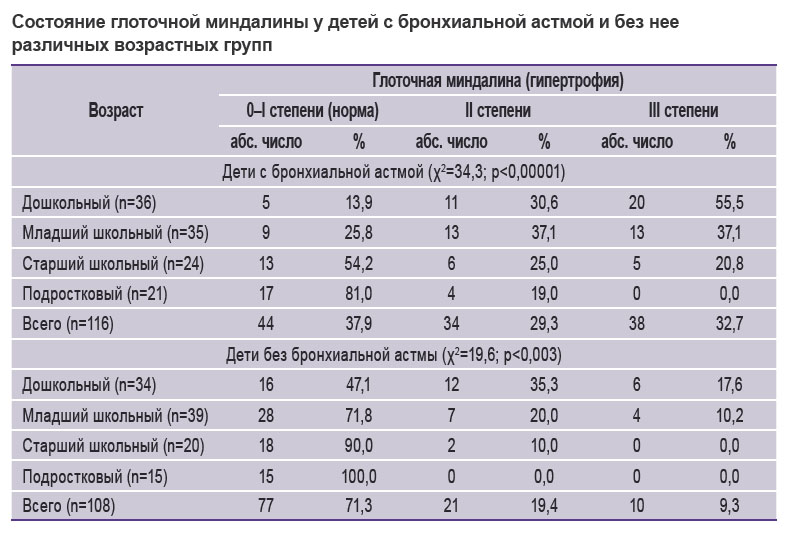
Риновидеоэндоскопические исследования подтвердили взаимосвязь степени ГГМ с возрастом как у детей контрольной группы (не имеющих БА), так и у пациентов с БА (см. таблицу). Однако в целом для детей с БА во всех возрастных группах характерна бóльшая степень ГГМ, чем у пациентов контрольной группы.
|
Состояние глоточной миндалины у детей с бронхиальной астмой и без нее различных возрастных групп |
Заключение. Гипертрофия глоточной миндалины вносит существенный вклад в формирование назальной обструкции у детей с бронхиальной астмой, что требует точных данных о состоянии аденоидной ткани для формирования оптимальных программ терапии. Метод риновидеоэндоскопии позволяет в значительной степени устранить диагностические трудности и позволяет объективно оценить состояние глоточной миндалины у пациентов с бронхиальной астмой различного возраста. Заслуга риновидеоэндоскопии — в получении новых данных о том, что гипертрофия глоточной миндалины в целом более распространена в группе пациентов с астмой, чем среди детей, не имеющих данного заболевания, что необходимо учитывать при ведении данных пациентов.
Финансирование исследования и конфликт интересов. Исследование не финансировалось какими-либо источниками, и конфликты интересов, связанные с данным исследованием, отсутствуют.
Литература
- Борзов Е.В. Аденоиды и аденоидиты у детей. М: ГЭОТАР-Медиа; 2011.
- Evcimik M.F., Dogru M., Cirik A.A., Nepesov M.I. Adenoid hypertrophy in children with allergic disease and influential factors. Int J Pediatr Otorhinolaryngol 2015; 79(5): 694–697, http://dx.doi.org/10.1016/j.ijporl.2015.02.017.
- Nuhoglu C., Nuhoglu Y., Bankaoglu M., Ceran O. A retrospective analysis of adenoidal size in children with allergic rhinitis and nonallergic idiopathic rhinitis. Asian Pac J Allergy Immunol 2010; 28(2–3): 136–140.
- Матвеева А.Ю., Зайцева О.В., Самсыгина Г.А., Богомильский М.Р. Аденоиды и бронхиальная астма у детей: роль местной терапии. Педиатрия. Журнал им. Г.Н. Сперанского 2005; 84(3): 48–53.
- Grossman J. One airway, one disease. Chest 1997; 111(2 Suppl): 11S–16S, http://dx.doi.org/10.1378/chest.111.2_supplement.11s.
- Быкова В.П., Бруевич О.В., Пакина В.Р., Паюшина О.В. Аденоиды как индуктивный орган мукозального иммунитета верхних дыхательных путей. Российская ринология 2005; 2: 175–176.
- Brandtzaeg P. Immune functions of nasopharyngeal lymphoid tissue. Adv Otorhinolaryngol 2011; 72: 20–24, http://dx.doi.org/10.1159/000324588.
- Быкова В.П. Структурные основы мукозального иммунитета верхних дыхательных путей. Российская ринология 1999; 1: 5–9.
- Красильникова С.В., Елисеева Т.И., Шахов А.В., Прахов А.В., Балаболкин И.И. Видеоэндоскопический метод оценки состояния полости носа и носоглотки у детей с бронхиальной астмой. Современные технологии в медицине 2012; 3: 41–45.
- Modrzynski M., Zawisza E. An analysis of the incidence of adenoid hypertrophy in allergic children. Int J Pediatr Otorhinolaryngol 2007; 71(5): 713–719, http://dx.doi.org/10.1016/j.ijporl.2006.12.018.
- Pagella F., De Amici M., Pusateri A., Tinelli G., Matti E., Benazzo M., Licari A., Nigrisoli S., Quaglini S., Ciprandi G., Marseglia G.L. Adenoids and clinical symptoms: epidemiology of a cohort of 795 pediatric patients. Int J Pediatr Otorhinolaryngol 2015; 79(12): 2137–2141, http://dx.doi.org/10.1016/j.ijporl.2015.09.035.
- Sadeghi-Shabestari M., Jabbari Moghaddam Y., Ghaharri H. Is there any correlation between allergy and adenotonsillar tissue hypertrophy? Int J Pediatr Otorhinolaryngol 2011; 75(4): 589–591, http://dx.doi.org/10.1016/j.ijporl.2011.01.026.
- Карпова Е.П., Соколова М.В., Пампура А.Н. Влияние аденотомии на качество жизни детей с бронхиальной астмой в сочетании с аллергическим ринитом. Российская ринология 2007; 1: 39–42.
- Пухлик С.М., Неверт Э.Г., Карпович Д.В. Аденоиды и аллергический ринит. Новости медицины и фармации 2011; 380.
- Zhang L., Mendoza-Sassi R.A., César J.A., Chadha N.K. Intranasal corticosteroids for nasal airway obstruction in children with moderate to severe adenoidal hypertrophy. Cochrane Database Syst Rev 2008; 3: CD006286, http://dx.doi.org/10.1002/14651858.CD006286.pub2.
- Anfuso A., Ramadan H., Terrell A., Demirdag Y., Walton C., Skoner D.P., Piedimonte G. Sinus and adenoid inflammation in children with chronic rhinosinusitis and asthma. Ann Allergy Asthma Immunol 2015; 114(2): 103–110, http://dx.doi.org/10.1016/j.anai.2014.10.024.
- Undem B.J., McAlexander M., Hunter D.D. Neurobiology of the upper and lower airways. Allergy 1999; 54 (Suppl 57): 81–93, http://dx.doi.org/10.1111/j.1398-9995.1999.tb04409.x.
- Braunstahl G.J. United airways concept: what does it teach us about systemic inflammation in airways disease? Proc Am Thorac Soc 2009; 6(8): 652–654, http://dx.doi.org/10.1513/pats.200906-052DP.
- Passali D., Benedetto de F., Benedetto de M., Chiaravalloti F., Damiani V., Passali F.M., Bellussi L.M.; Working Group. Rhino-Bronchial Syndrome. The SIO-AIMAR (Italian Society of Otorhinolaryngology, Head Neck Surgery-Interdisciplinary Scientific Association for the Study of the Respiratory Diseases) survey. Acta Otorhinolaryngol Ital 2011; 31(1): 27–34.
- Saedi B., Sadeghi M., Mojtahed M., Mahboubi H. Diagnostic efficacy of different methods in the assessment of adenoid hypertrophy. Am J Otolaryngol 2011; 32(2): 147–151, http://dx.doi.org/10.1016/j.amjoto.2009.11.003.
- Национальная программа «Бронхиальная астма у детей. Стратегия лечения и профилактика». Т. 4. М; 2012.
- GINA, Global Strategy for Asthma Management and Prevention. 2015. URL: http://www.ginasthma.org.
- Международная статистическая классификация болезней и проблем, связанных со здоровьем Десятого пересмотра (МКБ-10). 2015. URL: http://мкб11.рф.
- Bousquet J., Schünemann H.J., Samolinski B., Demoly P., Baena-Cagnani C.E., Bachert C., Bonini S., Boulet L.P., Bousquet P.J., Brozek J.L., Canonica G.W., Casale T.B., Cruz A.A., Fokkens W.J., Fonseca J.A., van Wijk R.G., Grouse L., Haahtela T., Khaltaev N., Kuna P., Lockey R.F., Lodrup Carlsen K.C., Mullol J., Naclerio R., O’Hehir R.E., Ohta K., Palkonen S., Papadopoulos N.G., Passalacqua G., Pawankar R., Price D., Ryan D., Simons F.E., Togias A., Williams D., Yorgancioglu A., Yusuf O.M., Aberer W., Adachi M., Agache I., Aït-Khaled N., Akdis C.A., Andrianarisoa A., Annesi-Maesano I., Ansotegui I.J., Baiardini I., Bateman E.D., Bedbrook A., Beghé B., Beji M., Bel E.H., Ben Kheder A., Bennoor K.S., Bergmann K.C., Berrissoul F., Bieber T., Bindslev Jensen C., Blaiss M.S., Boner A.L., Bouchard J., Braido F., Brightling C.E., Bush A., Caballero F., Calderon M.A., Calvo M.A., Camargos P.A., Caraballo L.R., Carlsen K.H., Carr W., Cepeda A.M., Cesario A., Chavannes N.H., Chen Y.Z., Chiriac A.M., Chivato Pérez T., Chkhartishvili E., Ciprandi G., Costa D.J., Cox L., Custovic A., Dahl R., Darsow U., De Blay F., Deleanu D., Denburg J.A., Devillier P., Didi T., Dokic D., Dolen W.K., Douagui H., Dubakiene R., Durham S.R., Dykewicz M.S., El-Gamal Y., El-Meziane A., Emuzyte R., Fiocchi A., Fletcher M., Fukuda T., Gamkrelidze A., Gereda J.E., González Diaz S., Gotua M., Guzmán M.A., Hellings P.W., Hellquist-Dahl B., Horak F., Hourihane J.O., Howarth P., Humbert M., Ivancevich J.C., Jackson C., Just J., Kalayci O., Kaliner M.A., Kalyoncu A.F., Keil T., Keith P.K., Khayat G., Kim Y.Y., Koffi N’goran B., Koppelman G.H., Kowalski M.L., Kull I., Kvedariene V., Larenas-Linnemann D., Le L.T., Lemière C., Li J., Lieberman P., Lipworth B., Mahboub B., Makela M.J., Martin F., Marshall G.D., Martinez F.D., Masjedi M.R., Maurer M., Mavale-Manuel S., Mazon A., Melen E., Meltzer E.O., Mendez N.H., Merk H., Mihaltan F., Mohammad Y., Morais-Almeida M., Muraro A., Nafti S., Namazova-Baranova L., Nekam K., Neou A., Niggemann B., Nizankowska-Mogilnicka E., Nyembue T.D., Okamoto Y., Okubo K., Orru M.P., Ouedraogo S., Ozdemir C., Panzner P., Pali-Schöll I., Park H.S., Pigearias B., Pohl W., Popov T.A., Postma D.S., Potter P., Rabe K.F., Ratomaharo J., Reitamo S., Ring J., Roberts R., Rogala B., Romano A., Roman Rodriguez M., Rosado-Pinto J., Rosenwasser L., Rottem M., Sanchez-Borges M., Scadding G.K., Schmid-Grendelmeier P., Sheikh A., Sisul J.C., Solé D., Sooronbaev T., Spicak V., Spranger O., Stein R.T., Stoloff S.W., Sunyer J., Szczeklik A., Todo-Bom A., Toskala E., Tremblay Y., Valenta R., Valero A.L., Valeyre D., Valiulis A., Valovirta E., Van Cauwenberge P., Vandenplas O., van Weel C., Vichyanond P., Viegi G., Wang D.Y., Wickman M., Wöhrl S., Wright J., Yawn B.P., Yiallouros P.K., Zar H.J., Zernotti M.E., Zhong N., Zidarn M., Zuberbier T., Burney P.G., Johnston S.L., Warner J.O.; World Health Organization Collaborating Center for Asthma and Rhinitis. Allergic Rhinitis and its Impact on Asthma (ARIA): achievements in 10 years and future needs. J Allergy Clin Immunol 2012; 130(5): 1049–1062, http://dx.doi.org/10.1016/j.jaci.2012.07.053.
- International Consensus Report on the diagnosis and management of rhinitis. International Rhinitis Management Working Group. Allergy 1994; 49(19 Suppl): 1–34.
- Fokkens W.J., Lund V.J., Mullol J., Bachert C., Alobid I., Baroody F., Cohen N., Cervin A., Douglas R., Gevaert P., Georgalas C., Goossens H., Harvey R., Hellings P., Hopkins C., Jones N., Joos G., Kalogjera L., Kern B., Kowalski M., Price D., Riechelmann H., Schlosser R., Senior B., Thomas M., Toskala E., Voegels R., Wang de Y., Wormald P.J. EPOS 2012: European position paper on rhinosinusitis and nasal polyps 2012. A summary for otorhinolaryngologists. Rhinology 2012; 50(1): 1–12.
- Богомильский М.Р., Чистякова В.Р. Детская оториноларингология. М: ГЭОТАР-Медиа; 2012.
- Wang D., Clement P., Kaufman L., Derde M.P. Fiberoptic examination of the nasal cavity and nasopharynx in children. Int J Pediatr Otorhinolaryngol 1992; 24(1): 35–44, http://dx.doi.org/10.1016/0165-5876(92)90064-v.
- РАДАР. Аллергический ринит у детей: рекомендации и алгоритм при детском аллергическом рините. М: Оригинал-макет; 2015.