Декомпрессивная трепанация черепа в лечении злокачественного ишемического инсульта полушарий головного мозга (обзор)
Рассмотрены возможности декомпрессивной трепанации черепа в лечении злокачественного ишемического инсульта. Под злокачественным понимают инсульт с обширной зоной ишемии головного мозга, с образованием постишемического отека и наличием латерального и/или аксиального смещения головного мозга, что чаще всего обусловливается окклюзией проксимального отдела средней мозговой артерии. Освещены этиология и патогенез данного вида нарушения мозгового кровообращения. Подробно описаны предикторы заболевания (клинические, рентгенологические, лабораторные) и выделены среди них наиболее значимые. На основании рандомизированных многоцентровых исследований определены показания, противопоказания и критерии отбора пациентов при использовании данного хирургического метода лечения злокачественного ишемического инсульта. Показано, что хирургический метод позволяет добиться снижения летальности, улучшает функциональные исходы и результаты. Подробно описаны техника и особенности выполнения декомпрессивной трепанации черепа при данной патологии, а также основные осложнения, возникающие при хирургическом лечении. Рассмотрен вопрос оптимального времени выполнения оперативного вмешательства и предложен оригинальный алгоритм лечения пациентов с данной патологией.
Цереброваскулярные заболевания продолжают оставаться одной из важных медико-социальных проблем современности. Ежегодно в России регистрируются 400–450 тыс. новых случаев острых нарушений мозгового кровообращения (ОНМК) [1–9], а во всем мире — более 7 млн. ОНМК [10]. Смертность от инсультов в экономически развитых странах занимает 3-е место в структуре общей смертности [2, 5, 10–14]. На долю ишемических инсультов (ИИ) приходится 70–85% от всех ОНМК [2, 3, 5, 10, 13, 15, 16]. Около 31% пациентов, перенесших ИИ, нуждаются в постоянной посторонней помощи, а 20% не способны самостоятельно передвигаться [1, 3, 4, 6]. Только около 20% пациентов, оставшихся в живых после ИИ, способны вернуться к прежней работе [1, 4, 6].
Особую группу пациентов с ОНМК составляют больные с так называемым злокачественным ишемическим инсультом (ЗИИ), который наблюдается в 10–15% случаев [17–25]. Под ЗИИ понимают инсульт с обширной зоной ишемии головного мозга с образованием постишемического отека и наличием латерального и/или аксиального смещения головного мозга [22, 25, 26]. ЗИИ обычно связан с окклюзией проксимального отдела средней мозговой артерии (СМА), вызывающей инфаркт в области более 50% зоны ее кровоснабжения [26, 27]. ЗИИ развивается чаще у молодых пациентов из-за отсутствия атрофии и меньшей толерантности головного мозга. Установлено, что пациенты со злокачественным течением заболевания в среднем на 10 лет моложе, чем пациенты с обычным течением ИИ [18]. Смертность у больных с ЗИИ составляет 70–80%, а инвалидизация среди выживших — 80% [17–21, 23, 24, 26, 28–34]. Летальный исход у таких больных связан с прогрессированием отека головного мозга, неконтролируемым повышением внутричерепного давления (ВЧД) и дислокацией срединных мозговых структур [24, 25, 34–37].
Патогенез злокачественного ишемического инсульта
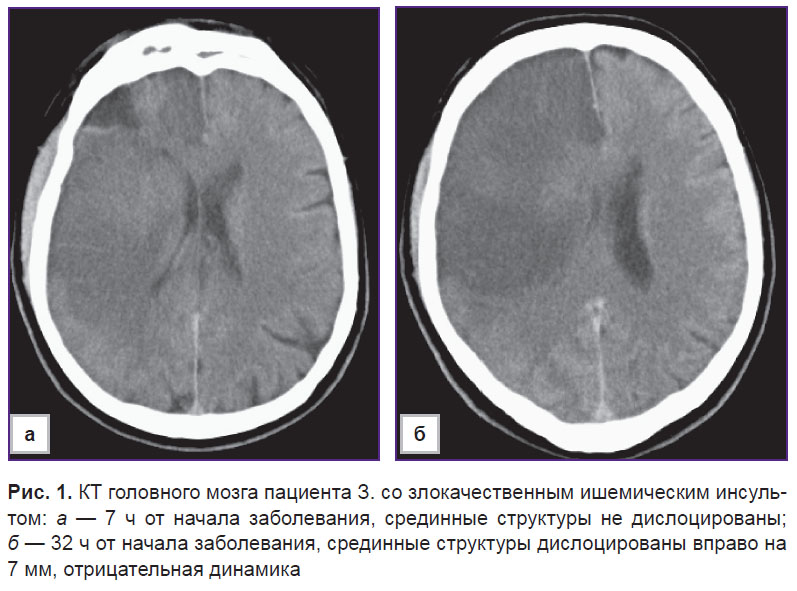
Прекращение поступления крови и кислорода по тромбированному сосуду в головной мозг приводит к развитию сложных патофизиологических и патобиохимических сдвигов. Нарушается аэробный гликолиз, что приводит к переходу метаболизма глюкозы на анаэробный путь и, как следствие, к лактатацидозу и накоплению ионов кальция. В свою очередь это ведет за собой нарушение функционирования ионных насосов, приводит к поступлению в клетки ионов натрия и хлора, а затем к развитию цитотоксического отека [1]. Отечная мозговая ткань вызывает локальное ВЧД. Когда локальное давление становится выше резистентности окружающего мозгового вещества, развивается дислокация головного мозга (рис. 1). Дислокация вызывает смещение срединных структур головного мозга, приводит сначала к сдавлению вен и локальному нарастанию венозной гипертензии, а затем к дополнительному локальному увеличению объема и обструкции ликворопроводящих путей, что вызывает резкое повышение ВЧД. В дальнейшем это приводит к сдавлению артерий и снижению перфузии мозговой ткани, причем не только в зоне инфаркта. Все это способствует увеличению зоны инфаркта и прогрессированию патологического процесса по принципу «порочного круга» [5, 26, 38]. Другими сателлитными реакциями являются нарушение микрососудистого тонуса, отек эндотелиальных клеток, активация тромбоцитов, лейкоцитов и коагуляционной системы крови [18]. Транстенториальное вклинение служит основной причиной летального исхода при ЗИИ. У таких пациентов летальность в течение первых 48 ч от начала заболевания достигает 47%, а в течение 49–96 ч — еще 34%, т.е. общая летальность при транстенториальном вклинении составляет 81% [26].
Прогностические факторы злокачественного ишемического инсульта
В некоторых работах обнаружена прямая связь между повышением ВЧД и последующим развитием транстенториального вклинения [29], причем дислокация мозга развивается тем раньше, чем значительнее повышается ВЧД, что служит причиной ухудшения клинического состояния больного [17]. Быстрое нарастание неврологической симптоматики, нарушение уровня сознания, фиксация взора в сторону инсульта, гемиплегия в течение первых 6 ч после дебюта заболевания в сочетании с окклюзией в проксимальном отделе СМА — неблагоприятные прогностические факторы [26].
Доказанными предикторами неблагоприятных исходов являются: гиподенсность более 50% мозгового вещества в бассейне СМА, объем ишемического очага более 145 см3, боковая дислокация срединных структур более 7–10 мм, наличие аксиальной дислокации II степени и более по Н.Н. Корниенко, гиподенсность более 70% в лобной и теменной долях и более 80% — в височной доле, развитие асимметричной окклюзионной гидроцефалии, уменьшение конвекситальных ликворных пространств, сглаживание кортикальных борозд, деформация боковых желудочков, компрессия базальных цистерн, снижение церебральной перфузии более чем на 66%, отсутствие накопления препарата при позитронно-эмиссионной томографии в зоне объемом 160 см3 [18, 24, 26, 27, 29, 35, 39, 40–42].
Уровень белка астроглии S100B, который высвобождается из клеток после их гибели, является потенциально полезным лабораторным способом диагностики ЗИИ [26]. При инсульте этот специфический для нервной ткани протеин поступает в кровь, достигая максимального уровня концентрации на 2–4-е сутки, причем его количество зависит от объема зоны ишемии. Объем зоны инфаркта взаимосвязан с уровнем S100B.Через 24 ч от дебюта заболевания значение белка в сыворотке составляет 1,03 мкг/л, что вкупе с чувствительностью 94%, специфичностью 84% может служить признаком массивного отека головного мозга [18]. К сожалению, в данное время этот способ диагностики доступен не в каждой больнице и его достоверность в прогнозировании должна быть подтверждена в более крупных исследованиях.
M.A. Moro с соавт. [43] провел исследование по определению концентрации молекулярных маркеров прорыва гематоэнцефалического барьера (ГЭБ) у пациентов с ЗИИ. В плазме крови больных в течение первых 24 ч от дебюта заболевания определяли уровень глутамата, альфа-фактора некроза опухолей, глицина, ИЛ-10, ГАМК, ИЛ-6, матриксной металлопротеиназы-9 (ММП-9) и клеточного фибронектина (c-Fn). Было выявлено, что в группе больных со злокачественным инсультом ММП-9 приблизительно в 2 раза выше, а уровень c-Fn примерно в 6 раз выше, чем в группе контроля. Авторы продемонстрировали, что сывороточный уровень c-Fn, равный 16,6 мг/мл (норма — 0,4 мг/мл), является предиктором ЗИИ с чувствительностью 90% и специфичностью около 100%.
Таким образом, астроглиальный протеин S100B (>0,4 мкг/л, норма <0,105 мкг/л), матриксная металлопротеиназа-9 (>140 нг/мл, норма <25 нг/мл) и клеточный фибронектин (≥16,6 мг/мл, норма — 0,4 мг/мл) могут служить молекулярными маркерами ЗИИ.
Лечение злокачественного ишемического инсульта
Место декомпрессивной трепанации черепа в лечении злокачественного ишемического инсульта. В 1905 г. Cushing предложил технику декомпрессивной трепанации черепа (ДТЧ) в качестве паллиативного метода лечения опухолей головного мозга путем снижения внутричерепной гипертензии. Первые декомпрессивные гемикраниоэктомии при ЗИИ начали выполняться в 1930-х годах [44, 45].
Результаты, достигнутые при использовании данного метода, подробно представлены в табл. 1 [46–52].
 Таблица 1. Результаты выполнения декомпрессионной трепанации черепа при злокачественном ишемическом инсульте Таблица 1. Результаты выполнения декомпрессионной трепанации черепа при злокачественном ишемическом инсульте
|
В дальнейшем проводилось большое количество исследований, сравнивающих результаты хирургического и консервативного лечения ЗИИ. Во множестве работ показано преимущество хирургического лечения данной патологии. Все результаты исследований, сопоставляющих хирургическое и консервативное лечение, представлены в табл. 2 [53–59].
 Таблица 2. Сравнение результатов хирургического и консервативного лечения злокачественного ишемического инсульта Таблица 2. Сравнение результатов хирургического и консервативного лечения злокачественного ишемического инсульта
|
До конца не изучен вопрос оптимальных сроков выполнения оперативного вмешательства у пациентов с данной патологией. Одни хирурги предлагают выполнять операцию в сверхраннем периоде — до развития отека и дислокации головного мозга, другие — в отсроченном — в период их наибольшего развития. Результаты исследований, определяющих благоприятное время для проведения хирургического лечения (ультрараннее или отсроченное), представлены в табл. 3 [60, 61].
 Таблица 3. Сравнение результатов хирургического (сверхраннего и отсроченного) лечения злокачественного ишемического инсульта Таблица 3. Сравнение результатов хирургического (сверхраннего и отсроченного) лечения злокачественного ишемического инсульта
|
Существует ряд исследований на животных, в которых доказывается эффективность ДТЧ при ЗИИ [62–66].
Таким образом, по данным большинства проведенных исследований, при выполнении ДТЧ при ЗИИ достоверно уменьшается летальность и улучшаются функциональные исходы лечения, особенно у молодых пациентов [22, 23, 28, 32–34, 39, 67–82].
Критерии отбора пациентов на операцию. В рекомендательном протоколе ведения больных с инсультом [83], опубликованном в 2008 г., указаны следующие критерии включения пациентов в группу для рассмотрения вопроса о возможности проведения ДТЧ:
1) возраст 18–60 лет;
2) признаки инфаркта СМА на КТ 50% или более, или >145 см3 по диффузно-взвешенным изображениям МРТ;
3) неврологический статус по шкале NIHSS >15 баллов;
4) угнетение уровня сознания на 1 балл и более по пункту 1а шкалы NIHSS (соответствует уровню сознания «оглушение» и ниже);
5) проведение операции не позднее 48 ч от начала заболевания.
Один из главных факторов успешности хирургического лечения ЗИИ — это время выполнения операции. Оперативное лечение должно быть превентивным и опережать развитие дислокационного синдрома [18, 29]. Хирургия не может воскресить «мертвые» нейроны. Операцию лучше всего проводить в первые 48 ч от начала заболевания [18, 32, 40, 75], однако эффективность возможна и в случае вмешательства до 96 ч [17]. Сверхраннее выполнение оперативного вмешательства (в течение 6 ч после появления симптомов) дает еще больший эффект [61]. Поэтому все пациенты с ЗИИ с давностью заболевания менее 48 ч должны осматриваться нейрохирургом для оценки возможности хирургического лечения [18]. Возраст 18–60 лет — прогностически более благоприятный, но доказана эффективность оперативного лечения и у больных старше 60 лет [19, 52, 84]. Смещение срединных структур более 7–10 мм также является показанием к операции [19, 27, 75]. После проведенного системного фибринолиза оперативное лечение также эффективно и не отличается в отдаленном послеоперационном периоде по функциональным исходам [85]. Рекомендуется выполнение ДТЧ при появлении одностороннего мидриаза или при прогрессирующем снижении уровня сознания [26].
Нецелесообразно проведение ДТЧ при инсульте вне бассейна кровоснабжения СМА, длительности заболевания более 48 ч, углублении уровня сознания до глубокой комы (менее 6 баллов) с двухсторонним мидриазом, при длительно существующей стволовой симптоматике, системных заболеваниях крови и тяжелой сопутствующей соматической патологии [17, 18, 26, 32, 40]. Вопрос о проведении ДТЧ при ЗИИ должен решаться индивидуально в каждом случае, основываясь на желании пациента и/или его семьи, а также на возможных функциональных исходах. Немаловажное значение при выборе оперативного лечения в качестве первичного имеет возраст больного, наличие сопутствующей патологии и т.д. Примерная схема отбора пациентов на ДТЧ при ЗИИ выглядит следующим образом (рис. 2).
 Рис. 2. Схема отбора пациентов на декомпрессивную трепанацию черепа при злокачественном ишемическом инсульте Рис. 2. Схема отбора пациентов на декомпрессивную трепанацию черепа при злокачественном ишемическом инсульте
|
Техника выполнения операции. Оперативное вмешательство заключается в резекции лобно-височно-теменно-затылочного фрагмента, вскрытии и свободной пластике твердой мозговой оболочки [17, 26]. Трепанационное окно должно быть не менее 12 см в диаметре, так как меньший размер приводит к ущемлению мозгового вещества, что снижает выживаемость с 80 до 55% [86]. Так, в проспективных исследованиях (DESTINY I, DECIMAL, HAMLET) размер трепанационного окна составлял не менее 12 см в диаметре.
В исследовании J. Chung [87] продемонстрировано, что максимальный размер декомпрессии (более 14–16 см в диаметре или более 399 см2) по сравнению с бóльшим размером (12 см или 308 см2) повышает процент благоприятного исхода (по шкале Рэнкина ≤3) через 3 мес после инсульта и снижает число неудовлетворительных результатов лечения и послеоперационную летальность.
Одним из видов кожного разреза при выполнении ДТЧ является разрез мягких тканей в лобно-теменно-височной области в виде «вопросительного знака» с основанием, располагающимся у козелка уха (рис. 3).
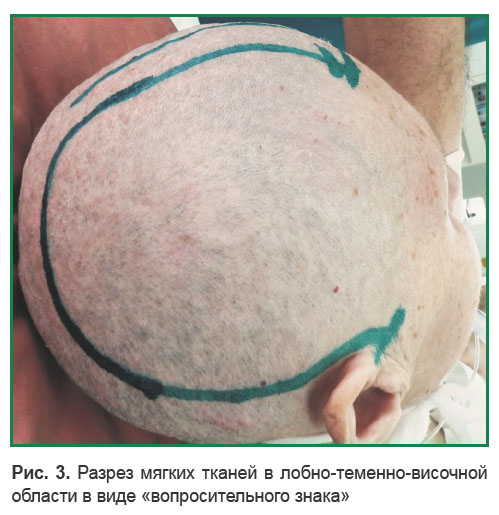 Рис. 3. Разрез мягких тканей в лобно-теменно-височной области в виде «вопросительного знака» Рис. 3. Разрез мягких тканей в лобно-теменно-височной области в виде «вопросительного знака»
|
Другим видом — разрез в виде большой «подковы» (рис. 4). Такой вариант разреза обладает меньшей длиной, отличается меньшей кровоточивостью, позволяет сохранить основные стволы поверхностной височной артерии, мягкотканный этап операции проводится быстрее [29].
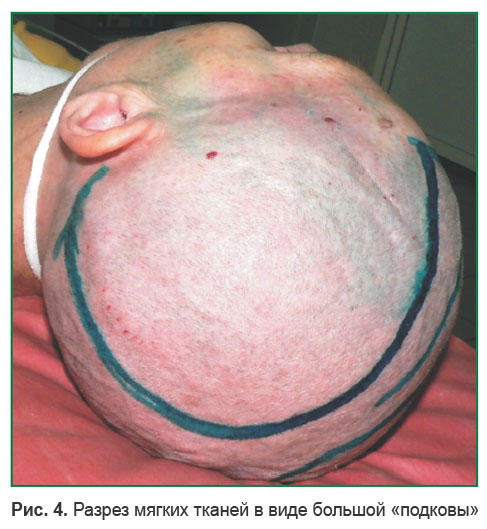 Рис. 4. Разрез мягких тканей в виде большой «подковы» Рис. 4. Разрез мягких тканей в виде большой «подковы»
|
Границами костной резекции являются: передняя (лобная) — по линии зрачка; задняя — 4 см кзади от наружного слухового прохода; верхняя — до уровня верхнего сагиттального синуса; нижняя — дно средней черепной ямки (рис. 5). Особенно важно выполнить резекцию чешуи височной кости в базальном направлении, потому что на этом уровне локализуется пахионово отверстие, в котором при височно-тенториальной дислокации ущемляется ствол мозга [17, 26, 88].
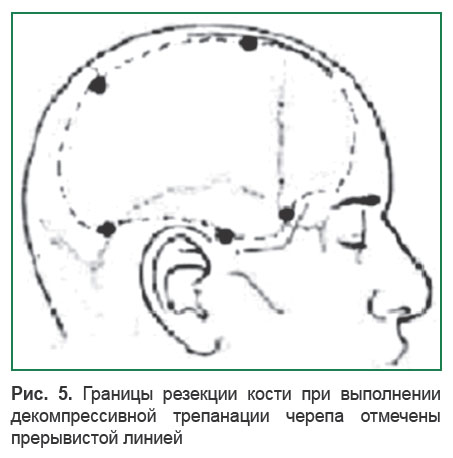 Рис. 5. Границы резекции кости при выполнении декомпрессивной трепанации черепа отмечены прерывистой линией Рис. 5. Границы резекции кости при выполнении декомпрессивной трепанации черепа отмечены прерывистой линией
|
После трепанации черепа выполняется дугообразный разрез твердой мозговой оболочки по периметру костного окна с подшиванием ее к надкостнице с целью профилактики образования эпидуральной гематомы [17, 26, 88]. Ишемизированную мозговую ткань не резецируют [17, 26]. Далее выполняют свободную пластику твердой мозговой оболочки трансплантатом (обычно синтетическим), который фиксируют в нескольких местах вверху раны для предотвращения дислокации трансплантата. Особенно тщательно и послойно следует ушивать мягкие ткани для создания герметичности раны и предупреждения послеоперационной раневой ликвореи [17]. Ряд исследователей сочетают ДТЧ с ункопарагиппокампэктомией, парциальной лобэктомией, удалением некротического мозгового вещества и установкой датчика ВЧД [26, 29, 49].
Наиболее оптимальные сроки выполнения последующей краниопластики — 1,5–6 мес после ДТЧ [17, 18, 89]. При этом число осложнений достигает 26%: эпиприпадки — 15,6%, поверхностные раневые инфекции — 3,1%, гидроцефалия — 3,1%, транзиторные неврологические дефициты — 3,1% и остеомиелит — 2,1% [90]. D. Wachter с соавт. сообщили о частоте осложнений в 30% случаев: 17,4% — асептический некроз кости, 5% — раневые инфекции, 2,5% — гематомы, 2,7% — гигромы и 1,7% — плохие косметические результаты [91].
Влияние декомпрессивной трепанации черепа на исходы лечения. Многие авторы отмечают лучшую эффективность ДТЧ при выполнении ее в случае ЗИИ, чем в случае тяжелой черепно-мозговой травмы [69, 92]. Это связано с меньшим пролабированием мозгового вещества в трепанационный дефект за счет сниженного артериального притока и меньшего масс-эффекта за счет одностороннего поражения, тогда как при черепно-мозговой травме обычно отмечается диффузный отек мозга [13]. У пациентов, которым была выполнена ДТЧ при ЗИИ, снижается ВЧД, происходит улучшение церебральной гемодинамики, что подтверждается данными КТ-перфузии [29, 68, 93–96].
Неблагоприятными факторами для церебральной гемодинамики являются следующие: операция, проведенная более чем через 48 ч после дебюта заболевания, смещение срединных структур более 10 мм и возраст больного более 55 лет [68]. В настоящее время отсутствуют убедительные доказательства о необходимости проведения мониторинга ВЧД больным с уже выполненной ДТЧ [29, 97].
Факторами неблагоприятного исхода при проведении ДТЧ у пациентов с ЗИИ считаются: смещение срединных структур более 10 мм, возраст старше 60 лет, анизокория, нарушение уровня сознания до комы. В ряде случаев таким фактором служит инфаркт на всей территории кровоснабжения внутренней сонной артерии [29]. До сих пор не определено, влияет ли на исход заболевания у оперированных больных вовлечение в зону инфаркта бассейнов передней и задней мозговой артерий.
Основными осложнениями ДТЧ при ЗИИ являются: послеоперационная эпидуральная гематома, менингит, раневая инфекция, паренхиматозное повреждение головного мозга, ликворрея, гигрома, геморрагическая трансформация зоны инфаркта, косметические дефекты [24, 89, 98]. Все эти осложнения ухудшают течение и прогноз ЗИИ, а в некоторых случаях могут определять основную тяжесть основного заболевания. Так, удаление костного лоскута в послеоперационном периоде приводит к возникновению «синдрома трепанированных» или «синдрома запавшего кожного лоскута», что вызывает снижение качества жизни, косметические дефекты и увеличение процента инвалидизации [99].
К основным причинам смерти таких больных относят пневмонию, тромбоз глубоких вен нижних конечностей, тромбоэмболию легочной артерии, сепсис, синдром полиорганной недостаточности [89, 100].
Заключение
Проведенный анализ результатов ДТЧ при ЗИИ позволяет сделать убедительные выводы о снижении летальности и улучшении функциональных исходов при ее проведении и дает возможость рекомендовать данный метод к использованию у определенных групп больных. Особенно это касается пациентов моложе 60 лет, которым возможно выполнение раннего оперативного лечения (менее 48 ч от дебюта заболевания), хотя и у пожилых пациентов констатировано снижение процента смертности и тяжелой инвалидизации. В ходе применения ДТЧ имеет значение правильная техника выполнения: с трепанационным окном диаметром не менее 12 см, резекцией базальных отделов височной кости, широким вскрытием твердой мозговой оболочки с ее последующей свободной пластикой. Также нужно помнить, что само оперативное вмешательство несет в себе определенный риск осложнений: инфекционных, геморрагических, косметических.
Данная тема нуждается в проведении исследований, которые должны быть направлены на выявление предикторов ЗИИ, дальнейшее уточнение показаний и противопоказаний к проведению оперативного вмешательства и определение оптимального времени выполнения и объема операции.
Финансирование исследования и конфликт интересов. Исследование не финансировалось какими-либо источниками, и конфликты интересов, связанные с данным исследованием, отсутствуют.
Литература
- Гусев Е.И., Мартынов М.Ю., Камчатнов П.Р. Ишемический инсульт. Современное состояние проблемы. Доктор.Ру 2013; 5(83): 7–12.
- Неврология. Национальное руководство. Под. ред. Гусева Е.И., Коновалова А.Н., Скворцовой В.И., Гехт А.Б. М: ГЭОТАР-Медиа; 2009; 1040 с.
- Муравьева В.Н., Карпова Е.Н. Современные представления о факторах риска и профилактики ОНМК. Международный журнал экспериментального образования 2014; 3(часть 2): 59–64.
- Ширяева Е.А., Федерко Н.Л. Долечивание и ранняя реабилитация пациентов после острого нарушения мозгового кровообращения в условиях санатория «Жемчужина». Здоровье. Медицинская экология. Наука 2011; 45(2): 16–18.
- Монгуш Х.Д., Ондар А.Б., Чылбакоол Р.Ч. Медицинская помощь больным с инсультом на этапах скорой помощи. Сибирский медицинский журнал (Иркутск) 2013; 118(3): 81–84.
- Тишин А.Н. Анализ заболеваемости инсультом в Курской области. Журнал научных статей Здоровье и образование в XXI веке 2010; 12(3): 356.
- Суслина З.А., Чечеткин А.О., Кунцевич Г.И., Кротенкова М.В. Алгоритм применения методов ангиовизуализации сонных артерий. Нервные болезни 2013; 1: 6–9.
- Ахмедов А.Д., Усачев Д.Ю., Лукшин В.А., Шмигельский А.В., Беляев А.Ю., Соснин А.Д. Каротидная эндартерэктомия у пациентов с высоких хирургическим риском. Вопросы нейрохирургии им. Н.Н. Бурденко 2013; 4: 36–42.
- Кадыков А.С., Шахпаронова Н.В. Ранняя реабилитация больных, перенесших инсульт. Роль медикаментозной терапии. Нервные болезни 2014; 1: 22–25.
- Михайлов В.Б. Непсихотические психические расстройства у лиц, перенесших ишемический мозговой инсульт. Український вісник психоневрології 2011; 1(66): 72–78.
- Крючкова О.Н., Турна Э.Ю. Ведение пациентов, перенесших ишемический инсульт. Крымский терапевтический журнал 2011; 1(16): 20–25.
- Прекина В.И., Самолькина О.Г. Ишемический инсульт и вариабельность ритма сердца. Современные проблемы науки и образования 2014; 5: 443.
- Куликов А.Ю., Комаров И.А. Фармакоэкономическое исследование применения церебролизина при терапии острого нарушения мозгового кровообращения по ишемическому типу. Фармакоэкономика. Современная фармакоэкономика и фармакоэпидемиология 2013; 6(4): 38–45.
- Kernan W.N., Ovbiagele B., Black H.R., Bravata D.M., Chimowitz M.I., Ezekowitz M.D., Fang M.C., Fisher M., Furie K.L., Heck D.V., Johnston S.C., Kasner S.E., Kittner S.J., Mitchell P.H., Rich M.W., Richardson D., Schwamm L.H., Wilson J.A.; American Heart Association Stroke Council, Council on Cardiovascular and Stroke Nursing, Council on Clinical Cardiology, and Council on Peripheral Vascular Disease. Guidelines for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke 2014; 45(7): 2160–2236, http://dx.doi.org/10.1161/STR.0000000000000024.
- Неверовский Д.В. Курение и ишемический инсульт. Неврология, нейропсихиатрия, психосоматика 2010; 4: 42–47.
- Кузовлев О.П., Афонина Н.С. Применение структурно-резонансной электро- и электромагнитной терапии в лечение больных, перенесших ишемический инсульт. Клиническая практика 2011; 3(7): 15–19.
- Дашьян В.Г., Талыпов А.Э. Декомпрессивная краниотомия в лечении инфарктов больших полушарий головного мозга. Нейрохирургия 2011; 4: 8–15.
- Ronchetti G., Panciani P.P., Stefini R., Spena G., Fontanella M.M. Acute supratentorial ischemic stroke: when surgery is mandatory. Biomed Res Int 2014; 2014: 624126, http://dx.doi.org/10.1155/2014/624126.
- Yu J.W., Choi J.H., Kim D.H., Cha J.K., Huh J.T. Outcome following decompressive craniectomy for malignant middle cerebral artery infarction in patients older than 70 years old. J Cerebrovasc Endovasc Neurosurg 2012; 14(2): 65–74, http://dx.doi.org/10.7461/jcen.2012.14.2.65.
- Wang D.Z., Nair D.S., Talkad A.V. Acute decompressive hemicraniectomy to control high intracranial pressure in patients with malignant MCA ischemic strokes. Curr Treat Options Cardiovasc Med 2011; 13(3): 225–232, http://dx.doi.org/10.1007/s11936-011-0121-1.
- Rabadán A.T., Sposato L., Mazia C. Update on interventional treatment of acute ischemic stroke. Medicina (B Aires) 2010; 70(5): 463–468.
- Taylor B., Appelboom G., Connolly E.S. Jr. Age selection for decompressive craniectomy in malignant middle cerebral artery infarction. World Neurosurg 2015; 83(3): 301–302, http://dx.doi.org/10.1016/j.wneu.2014.05.012.
- Winston K.R., Beauchamp K.M. Letter to the editor: decompression for ischemia. J Neurosurg 2013; 118(6): 1382–1383, http://dx.doi.org/10.3171/2012.11.JNS121653.
- Flechsenhar J., Woitzik J., Zweckberger K., Amiri H., Hacke W., Jüttler E. Hemicraniectomy in the management of space-occupying ischemic stroke. J Clin Neurosci 2013; 20(1): 6–12, http://dx.doi.org/10.1016/j.jocn.2012.02.019.
- Gautschi O.P., Cadosch D., Stienen M.N., Steiner L.A., Schaller K. Decompressive craniectomy in acute stroke — the different perspective. Anasthesiol Intensivmed Notfallmed Schmerzther 2012; 47(1): 8–13, http://dx.doi.org/10.1055/s-0032-1301374.
- Джинджихадзе Р.С., Древаль О.Н., Лазарев В.А. Декомпрессивная гемикраниэктомия при обширном ишемическом инсульте в бассейне средней мозговой артерии. Вопросы нейрохирургии им. Н.Н. Бурденко 2012; 76(3): 69–74.
- Буров С.А., Никитин А.С., Асратян С.А., Крылов В.В. Факторы риска развития злокачественного течения массивного ишемического инсульта. Нейрохирургия 2012; 3: 18–25.
- Godoy D., Piñero G., Cruz-Flores S., Alcalá Cerra G., Rabinstein A. Malignant hemispheric infarction of the middle cerebral artery. Diagnostic considerations and treatment options. Neurologia 2016; 31(5): 332–343, http://dx.doi.org/10.1016/j.nrl.2013.02.009.
- Буров С.А., Никитин А.С. Возможности декомпрессивной краниотомии в лечении злокачественных форм массивного ишемического инсульта. Нейрохирургия 2011; 3: 82–87.
- Giossi A., Volonghi I., Del Zotto E., Costa P., Padovani A., Pezzini A. Large middle cerebral artery and panhemispheric infarction. Front Neurol Neurosci 2012; 30: 154–157, http://dx.doi.org/10.1159/000333628.
- Vibbert M., Mayer S.A. Early decompressive hemicraniectomy following malignant ischemic stroke: the crucial role of timing. Curr Neurol Neurosci Rep 2010; 10(1): 1–3, http://dx.doi.org/10.1007/s11910-009-0081-y.
- Merenda A., DeGeorgia M. Craniectomy for acute ischemic stroke: how to apply the data to the bedside. Curr Opin Neurol 2010; 23(1): 5–58, http://dx.doi.org/10.1097/WCO.0b013e328334bdf4.
- Hwang D.Y., Matouk C.C., Sheth K.N. Management of the malignant middle cerebral artery syndrome. Semin Neurol 2013; 33(5): 448–455, http://dx.doi.org/10.1055/s-0033-1364211.
- Subramaniam S., Hill M.D. Decompressive hemicraniectomy for malignant middle cerebral artery infarction: an update. Neurologist 2009; 15(4): 178–184, http://dx.doi.org/10.1097/NRL.0b013e3181963d19.
- Cho S.Y., Oh C.W., Bae H.J., Han M.K., Park H., Bang J.S. The prognostic factors that influence long-term survival in acute large cerebral infarction. J Korean Neurosurg Soc 2011; 49(2): 92–96, http://dx.doi.org/10.3340/jkns.2011.49.2.92.
- van der Worp H.B., Kappelle L.J. Early decompressive hemicraniectomy in older patients with nondominant hemispheric infarction does not improve outcome. Stroke 2011; 42(3): 845–846, http://dx.doi.org/10.1161/STROKEAHA.110.603605.
- Jeon S.B., Koh Y., Choi H.A., Lee K. Critical care for patients with massive ischemic stroke. J Stroke 2014; 16(3): 146–160, http://dx.doi.org/10.5853/jos.2014.16.3.146.
- Schwab S. Treatment of malignant MCA infarction. Журнал Гродненского государственного медицинского университета 2010; 3(31): 3–8. Schwab S. Treatment of malignant MCA infarction. Zhurnal Grodnenskogo gosudarstvennogo meditsinskogo universiteta 2010; 3(31): 3–8.
- Mostofi K. Neurosurgical management of massive cerebellar infarct outcome in 53 patients. Surg Neurol Int 2013; 4: 28, http://dx.doi.org/10.4103/2152-7806.107906.
- Wartenberg K.E. Malignant middle cerebral artery infarction. Curr Opin Crit Care 2012; 18(2): 152–163, http://dx.doi.org/10.1097/MCC.0b013e32835075c5.
- Dohmen C., Galldiks N., Bosche B., Kracht L., Graf R. The severity of ischemia determines and predicts malignant brain edema in patients with large middle cerebral artery infarction. Cerebrovasc Dis 2012; 33(1): 1–7, http://dx.doi.org/10.1159/000330648.
- Thomalla G., Hartmann F., Juettler E., Singer O.C., Lehnhardt F.G., Köhrmann M., Kersten J.F., Krützelmann A., Humpich M.C., Sobesky J., Gerloff C., Villringer A., Fiehler J., Neumann-Haefelin T., Schellinger P.D., Röther J.; Clinical Trial Net of the German Competence Network Stroke. Prediction of malignant middle cerebral artery infarction by magnetic resonance imaging within 6 hours of symptom onset: a prospective multicenter observational study. Ann Neurol 2010; 68(4): 435–445, http://dx.doi.org/10.1002/ana.22125.
- Serena J., Blanco M., Castellanos M., Silva Y., Vivancos J., Moro M.A., Leira R., Lizasoain I., Castillo J., Dávalos A. The prediction of malignant cerebral infarction by molecular brain barrier disruption markers. Stroke 2005; 36(9): 1921–1926.
- Brown M.M. Surgical decompression of patients with large middle cerebral artery infarcts is effective: not proven. Stroke 2003; 34(9): 2305–2306, http://dx.doi.org/10.1161/01.str.0000089298.19012.9b.
- Ким А.В., Антонов Г.И., Лазарев В.А., Джинджихадзе Р.С., Миклашевич Э.Р., Мельничук С.В., Гладышев С.Ю., Курносенко В.Ю. Хирургическое лечение больных с ишемическим инсультом в бассейне средней мозговой артерии в остром периоде. Нейрохирургия 2014; 1: 126–131.
- Ivamoto H.S., Numoto M., Donaghy R.M. Surgical decompression for cerebral and cerebellar infarcts. Stroke 1974; 5(3): 365–370, http://dx.doi.org/10.1161/01.str.5.3.365.
- Kondziolka D., Fazl M. Functional recovery after decompressive craniectomy for cerebral infarction. Neurosurgery 1988; 23(2): 143–147, http://dx.doi.org/10.1227/00006123-198808000-00002.
- Gupta R., Connolly E.S., Mayer S., Elkind M.S. Hemicraniectomy for massive middle cerebral artery territory infarction: a systematic review. Stroke 2004; 35(2): 539–543, http://dx.doi.org/10.1161/01.str.0000109772.64650.18.
- Curry W.T. Jr., Sethi M.K., Ogilvy C.S., Carter B.S. Factors associated with outcome after hemicraniectomy for large middle cerebral artery territory infarction. Neurosurgery 2005; 56(4): 681–692, http://dx.doi.org/10.1227/01.neu.0000156604.41886.62.
- Świat M., Targosz-Gajniak M., Arkuszewski M., Pięta M., Gamrot J., Wojtacha M., Bażowski P., Opala G. Decompressive hemicraniectomy in ischaemic stroke. Neurol Neurochir Pol 2010; 44(2): 131–138, http://dx.doi.org/10.1016/s0028-3843(14)60004-9.
- Крылов В.В., Никитин А.С., Буров С.А., Петриков С.С., Асратян С.А., Аверин А.Ю., Кольяк Е.В. Декомпрессивная краниотомия в комплексной интенсивной терапии злокачественных форм массивного ишемического инсульта. Журнал неврологии и психиатрии им. C.C. Корсакова 2013; 113(1): 15–22.
- Suyama K., Horie N., Hayashi K., Nagata I. Nationwide survey of decompressive hemicraniectomy for malignant middle cerebral artery infarction in Japan. World Neurosurg 2014; 82(6): 1158–1163, http://dx.doi.org/10.1016/j.wneu.2014.07.015.
- Holtkamp M., Buchheim K., Unterberg A., Hoffmann O., Schielke E., Weber J.R., Masuhr F. Hemicraniectomy in elderly patients with space occupying media infarction: improved survival but poor functional outcome. J Neurol Neurosurg Psychiatry 2001; 70(2): 226–228, http://dx.doi.org/10.1136/jnnp.70.2.226.
- Jüttler E., Schwab S., Schmiedek P., Unterberg A., Hennerici M., Woitzik J., Witte S., Jenetzky E., Hacke W.; DESTINY Study Group. Decompressive surgery for the treatment of malignant infarction of the middle cerebral artery (DESTINY): a randomized, controlled trial. Stroke 2007; 38(9): 2518–2525, http://dx.doi.org/10.1161/strokeaha.107.485649.
- Hofmeijer J., Kappelle L.J., Algra A., Amelink G.J., van Gijn J., van der Worp H.B.; HAMLET investigators. Surgical decompression for space-occupying cerebral infarction (the hemicraniectomy after middle cerebral artery infarction with life-threatening edema trial [HAMLET]): a multicentre, open, randomised trial. Lancet Neurol 2009; 8(4): 326–333, http://dx.doi.org/10.1016/S1474-4422(09)70047-X.
- Mitchell P., Gregson B.A., Crossman J., Gerber C., Jenkins A., Nicholson C., Todd N.V., Ross N., Bhattathiri P., Nissen J., Crawford P.J., Wynne-Jones G., Sengupta R.P., Graham L., Gani A., Davis M., Gray C., Barer D., Dorman P., Millar D., Williamson J., Durham H., Jones A., Hastie H., Mendelow A.D. Reassessment of the HAMLET study. Lancet Neurol 2009; 8(7): 602–604, http://dx.doi.org/10.1016/S1474-4422(09)70157-7.
- Jüttler E., Unterberg A., Woitzik J., Bösel J., Amiri H., Sakowitz O.W., Gondan M., Schiller P., Limprecht R., Luntz S., Schneider H., Pinzer T., Hobohm C., Meixensberger J., Hacke W.; DESTINY II Investigators. Hemicraniectomy in older patients with extensive middle-cerebral-artery stroke. N Engl J Med 2014; 370(12): 1091–1100, http://dx.doi.org/10.1056/NEJMoa1311367.
- Jüttler E., Bösel J., Amiri H., Schiller P., Limprecht R., Hacke W., Unterberg A.; DESTINY II Study Group. DESTINY II: decompressive surgery for the treatment of malignant infarction of the middle cerebral artery II. Int J Stroke 2011; 6(1): 79–86, http://dx.doi.org/10.1111/j.1747-4949.2010.00544.x.
- Raffiq M.A., Haspani M.S., Kandasamy R., Abdullah J.M. Decompressive craniectomy for malignant middle cerebral artery infarction: impact on mortality and functional outcome. Surg Neurol Int 2014; 5: 102, http://dx.doi.org/10.4103/2152-7806.135342.
- Schwab S., Steiner T., Aschoff A., Schwarz S., Steiner H.H., Jansen O., Hacke W. Early hemicraniectomy in patients with complete middle cerebral artery infarction. Stroke 1998; 29(9): 1888–1893, http://dx.doi.org/10.1161/01.str.29.9.1888.
- Cho D.Y., Chen T.C., Lee H.C. Ultra-early decompressive craniectomy for malignant middle cerebral artery infarction. Surg Neurol 2003; 60(3): 227–233, http://dx.doi.org/10.1016/s0090-3019(03)00266-0.
- Sakai K., Iwahashi K., Terada K., Gohda Y., Sakurai M., Matsumoto Y. Outcome after external decompression for massive cerebral infarction. Med Chir (Tokyo) 1998; 38(3): 131–136, http://dx.doi.org/10.2176/nmc.38.131.
- Doerfler A., Forsting M., Reith W., Staff C., Heiland S., Schäbitz W.R., von Kummer R., Hacke W., Sartor K. Decompressive craniectomy in a rat model of “malignant” cerebral hemispheric stroke: experimental support for an aggressive therapeutic approach. J Neurosurg 1996; 85(5): 853–859, http://dx.doi.org/10.3171/jns.1996.85.5.0853.
- Engelhorn T., Dörfler A., Egelhof T., Schwab S., Heiland S., Sartor K., Forsting M. Follow-up monitoring with magnetic resonance tomography after decompressive trephining in experimental “malignant” hemispheric infarct. Zentralbl Neurochir 1998; 59(3): 157–165.
- Engelhorn T., Doerfler A., Kastrup A., Beaulieu C., de Crespigny A., Forsting M., Moseley M.E., Faraci F.M. Decompressive craniectomy, reperfusion, or a combination for early treatment of acute “malignant” cerebral hemispheric stroke in rats? Potential mechanisms studied by MRI. Stroke 1999; 30(7): 1456–1463, http://dx.doi.org/10.1161/01.str.30.7.1456.
- Doerfler A., Schwab S., Hoffmann T.T., Engelhorn T., Forsting M. Combination of decompressive craniectomy and mild hypothermia ameliorates infarction volume after permanent focal ischemia in rats. Stroke 2001; 32(11): 2675–2681, http://dx.doi.org/10.1161/hs1101.098369.
- Uhl E., Kreth F.W., Elias B., Goldammer A., Hempelmann R.G., Liefner M., Nowak G., Oertel M., Schmieder K., Schneider G.H. Outcome and prognostic factors of hemicraniectomy for space occupying cerebral infarction. J Neurol Neurosurg Psychiatry 2004; 75(2): 270–274.
- Amorim R.L., de Andrade A.F., Gattás G.S., Paiva W.S., Menezes M., Teixeira M.J., Bor-Seng-Shu E. Improved hemodynamic parameters in middle cerebral artery infarction after decompressive craniectomy. Stroke 2014; 45(5): 1375–1380, http://dx.doi.org/10.1161/STROKEAHA.113.003670.
- Shao A., Guo S., Chen S., Sun C., Wu H., Hong Y., Zhang J. Comparison between routine and improved decompressive craniectomy on patients with malignant cerebral artery infarction without traumatic brain injury. J Craniofac Surg 2013; 24(6): 2085–2088, http://dx.doi.org/10.1097/SCS.0b013e3182a2435a.
- Shah S., Murthy S.B., Whitehead W.E., Jea A., Nassif L.M. Decompressive hemicraniectomy in pediatric patients with malignant middle cerebral artery infarction: case series and review of the literature. World Neurosurg 2013; 80(1–2): 126–133, http://dx.doi.org/10.1016/j.wneu.2013.06.001.
- Bhattacharya P., Kansara A., Chaturvedi S., Coplin W. What drives the increasing utilisation of hemicraniectomy in acute ischaemic stroke? J Neurol Neurosurg Psychiatry 2013; 84(7): 727–731, http://dx.doi.org/10.1136/jnnp-2012-303610.
- Neugebauer H., Heuschmann P.U., Jüttler E. Decompressive surgery for the treatment of malignant infarction of the middle cerebral artery — registry (DESTINY-R): design and protocols. BMC Neurol 2012; 12: 115, http://dx.doi.org/10.1186/1471-2377-12-115.
- Montgomery A.K., Maixner W.J., Wallace D., Wray A., Mackay M.T. Decompressive craniectomy in childhood posterior circulation stroke: a case series and review of the literature. Pediatr Neurol 2012; 47(3): 193–197, http://dx.doi.org/10.1016/j.pediatrneurol.2012.05.005.
- Kim H., Jin S.T., Kim Y.W., Kim S.R., Park I.S., Jo K.W. Predictors of malignant brain edema in middle cerebral artery infarction observed on CT angiography. J Clin Neurosci 2015; 22(3): 554–560, http://dx.doi.org/10.1016/j.jocn.2014.08.021.
- Никитин А.С., Буров С.А., Петриков С.С., Асратян С.А., Завалишин Е.Е., Крылов В.В. Декомпрессивная краниотомия у больных со злокачественным течением массивного ишемического инсульта. Нейрохирургия 2014; 3: 23–29.
- Agarwalla P.K., Stapleton C.J., Ogilvy C.S. Craniectomy in acute ischemic stroke. Neurosurgery 2014; 74(Suppl 1): S151–S162, http://dx.doi.org/10.1227/NEU.0000000000000226.
- Arnaout O.M., Aoun S.G., Batjer H.H., Bendok B.R. Decompressive hemicraniectomy after malignant middle cerebral artery infarction: rationale and controversies. Neurosurg Focus 2011; 30(6): E18, http://dx.doi.org/10.3171/2011.3.FOCUS1160.
- Kelly A.G., Holloway R.G. Health state preferences and decision-making after malignant middle cerebral artery infarctions. Neurology 2010; 75(8): 682–687, http://dx.doi.org/10.1212/WNL.0b013e3181eee273.
- Alshekhlee A., Horn C., Jung R., Alawi A.A., Cruz-Flores S. In-hospital mortality in acute ischemic stroke treated with hemicraniectomy in US hospitals. J Stroke Cerebrovasc Dis 2011; 20(3): 196–201, http://dx.doi.org/10.1016/j.jstrokecerebrovasdis.2009.11.019.
- Nakagawa K., Bianchi M.T., Nakagawa S.S., Sorond F.A. Aggressive care after a massive stroke in young patients: is that what they want? Neurocrit Care 2010; 13(1): 118–122, http://dx.doi.org/10.1007/s12028-010-9340-7.
- Allahtavakoli M., Kahnouei M.H., Rezazadeh H., Roohbakhsh A., Mahmoodi M.H., Moghadam-Ahmadi A., Zarisfi M. Delayed combination therapy of local brain hypothermia and decompressive craniectomy on acute stroke outcome in rat. Iran J Basic Med Sci 2014; 17(7): 476–482.
- Никитин А.С., Асратян С.А., Аверин А.Ю., Камчатнов П.Р. Эффективная декомпрессивная краниотомия у молодого пациента с массивным ишемическим инсультом. Журнал неврологии и психиатрии имени С.С. Корсакова 2013; 2013; 12(2): 12–26.
- European Stroke Organisation (ESO) Executive Committee; ESO Writing Committee. Guidelines for management of ischaemic stroke and transient ischaemic attack 2008. Cerebrovasc Dis 2008; 25(5): 457–507, http://dx.doi.org/10.1159/000131083.
- Neugebauer H., Jüttler E. Hemicraniectomy for malignant middle cerebral artery infarction: current status and future directions. Int J Stroke 2014; 9(4): 460–467, http://dx.doi.org/10.1111/ijs.12211.
- Takeuchi S., Wada K., Nawashiro H., Arimoto H., Ohkawa H., Masaoka H., Otani N., Takasato Y. Decompressive craniectomy after intravenous tissue plasminogen activator administration for stroke. Clin Neurol Neurosurg 2012; 114(10): 1312–135, http://dx.doi.org/10.1016/j.clineuro.2012.03.044.
- Wagner S., Schnippering H., Aschoff A., Koziol J.A., Schwab S., Steiner T. Suboptimum hemicraniectomy as a cause of additional cerebral lesions in patients with malignant infarction of the middle cerebral artery. J Neurosurg 2001; 94(5): 693–696, http://dx.doi.org/10.3171/jns.2001.94.5.0693.
- Chung J., Bang O.Y., Lim Y.C., Park S.K., Shin Y.S. Newly suggested surgical method of decompressive craniectomy for patients with middle cerebral artery infarction. Neurologist 2011; 17(1): 11–15, http://dx.doi.org/10.1097/NRL.0b013e3181f4ec88.
- Demchuk A.M. Hemicraniectomy is a promising treatment in ischemic stroke. Can J Neurol Sci 2000; 27(4): 274–277, http://dx.doi.org/10.1017/s0317167100000986.
- Zweckberger K., Juettler E., Bösel J., Unterberg W.A. Surgical aspects of decompression craniectomy in malignant stroke: review. Cerebrovasc Dis 2014; 38(5): 313–323, http://dx.doi.org/10.1159/000365864.
- Sobani Z.A., Shamim M.S., Zafar S.N., Qadeer M., Bilal N., Murtaza S.G., Enam S.A., Bari M.E. Cranioplasty after decompressive craniectomy: an institutional audit and analysis of factors related to complications. Surg Neurol Int 2011; 2(1): 123, http://dx.doi.org/10.4103/2152-7806.85055.
- Wachter D., Reineke K., Behm T., Rohde V. Cranioplasty after decompressive hemicraniectomy: underestimated surgery-associated complications? Clin Neurol Neurosurg 2013; 115(8): 1293–1297, http://dx.doi.org/10.1016/j.clineuro.2012.12.002.
- Rengachary S.S., Batnitzky S., Morantz R.A., Arjunan K., Jeffries B. Hemicraniectomy for acute massive cerebral infarction. Neurosurgery 1981; 8(3): 321–328, http://dx.doi.org/10.1097/00006123-198103000-00004.
- Vassileva E., Stoyanov P., Vavrek E., Stamenova P. Unexpected arterial recanalization after decompressive hemicraniectomy. J Stroke Cerebrovasc Dis 2013; 22(8): e661–e663, http://dx.doi.org/10.1016/j.jstrokecerebrovasdis.2013.05.023.
- Pérez-Bárcena J., Goedhart P., Ibáñez J., Brell M., García R., Llinás P., Jiménez C., Ince C. Direct observation of human microcirculation during decompressive craniectomy after stroke. Crit Care Med 2011; 39(5): 1126–1129, http://dx.doi.org/10.1097/CCM.0b013e31820ead5e.
- Woitzik J., Hecht N., Pinczolits A., Sandow N., Major S., Winkler M.K., Weber-Carstens S., Dohmen C., Graf R., Strong A.J., Dreier J.P., Vajkoczy P.; COSBID study group. Propagation of cortical spreading depolarization in the human cortex after malignant stroke. Neurology 2013; 80(12): 1095–1102, http://dx.doi.org/10.1212/WNL.0b013e3182886932.
- Smith E.R., Carter B.S., Ogilvy C.S. Proposed use of prophylactic decompressive craniectomy in poor-grade aneurysmal subarachnoid hemorrhage patients presenting with associated large sylvian hematomas. Neurosurgery 2002; 51(1): 117–124, http://dx.doi.org/10.1097/00006123-200207000-00018.
- Poca M.A., Benejam B., Sahuquillo J., Riveiro M., Frascheri L., Merino M.A., Delgado P., Alvarez-Sabin J. Monitoring intracranial pressure in patients with malignant middle cerebral artery infarction: is it useful? J Neurosurg 2010; 112(3): 648–657, http://dx.doi.org/10.3171/2009.7.JNS081677.
- Arch A.E., Sheth K.N. Malignant cerebral edema after large anterior circulation infarction: a review. Curr Treat Options Cardiovasc Med 2014; 16(1): 275, http://dx.doi.org/10.1007/s11936-013-0275-0.
- Тихомиров С.Е., Цыбусов С.Н., Кравец Л.Я. Использование материала «Реперен»® для пластики дефектов свода черепа. Сибирский медицинский журнал (Иркутск) 2010; 2(93): 121–124.
- Крылов В.В., Никитин А.С., Дашьян В.Г., Буров С.А., Петриков С.С., Асратян С.А. Хирургия массивного ишемического инсульта. М: ГЭОТАР-Медиа; 2016; 136 с.