Новый подход к объемной реконструкции сложных дефектов альвеолярной кости
Цель исследования — оценить эффективность объемной реконструкции альвеолярной кости методом направленной костной регенерации на основе трехмерного компьютерного планирования с использованием резорбируемой каркасной мембраны.
Материалы и методы. В исследовании приняли участие 35 практически здоровых пациентов без выраженной сопутствующей соматической патологии с диагнозом «частичная потеря зубов, осложненная атрофией альвеолярной кости». Всем пациентам проводились реконструктивные операции, направленные на устранение дефектов и восстановление объема альвеолярной кости методом направленной костной регенерации с использованием резорбируемых каркасных мембран. Планирование и сами операции выполняли по разработанному унифицированному протоколу, включающему компьютерное 3D-планирование операции и изготовление интраоперационных шаблонов для каркасной мембраны методом объемного прототипирования.
Результаты. Разработанный метод трехмерного компьютерного планирования и изготовления интраоперационных шаблонов для каркасной мембраны методом объемного прототипирования показал эффективность по ряду показателей: уменьшение времени оперативного вмешательства, исключение риска формирования мембраны меньшего размера и неправильной формы, получение необходимого костного объема.
Заключение. Предложенный метод трехмерного компьютерного планирования и изготовления интраоперационных шаблонов для каркасной мембраны с помощью объемного прототипирования позволяет повысить точность проведения операций по направленной костной регенерации, уменьшить интраоперационное время адаптации мембраны и исключить возможность ее неправильного позиционирования. Вместе с тем использование резорбируемой каркасной мембраны позволяет повысить эффективность объемной реконструкции альвеолярной кости.
Реконструктивные операции на костной ткани челюстей направлены на восстановление адекватного объема и качества костной ткани для последующей дентальной имплантации и протезирования зубных рядов [1, 2]. Основными причинами уменьшения ширины и высоты альвеолярного отростка верхней челюсти и альвеолярной части нижней челюсти (далее: «альвеолярной кости») являются резорбция кости при пародонтите, травматичное удаление зубов, атрофия вследствие уменьшения функциональной нагрузки на кость [3, 4].
Для описания нарушений строения челюстей в литературе встречаются термины «дефект» и «деформация». Слово «дефект» (от лат. defectus — изъян) имеет значения «изъян, недостаток, недочет», а слово «деформация» (от лат. deformatio — искажение) означает изменение размеров, формы твердого тела под действием внешних сил (обычно без изменения его массы) [5]. Исходя из этих определений к деформациям челюстей и альвеолярной кости целесообразно отнести врожденные состояния (макро- и микрогнатию), а к дефектам — все приобретенные изъяны челюстей вследствие удаления зубов, пародонтита, травм и атрофии.
Наиболее сложные случаи для лечения представляют дефекты альвеолярной кости в нескольких плоскостях (по ширине и высоте). Авторами ранее предложено несколько различных методик объемной костной реконструкции с использованием костных лоскутов (сэндвич-пластика ротационным лоскутом) и костных трансплантатов (Г-образная пластика) [6–8]. Между тем собственный опыт показал, что существует ряд клинических и анатомических условий, в которых применение упомянутых методов нецелесообразно. Прежде всего это выраженная степень атрофии, при которой показано увеличение костного объема более чем на 5 мм по высоте и ширине, при том что сэндвич-пластика или винирная Г-образная пластика позволяют увеличить высоту альвеолярной кости лишь в пределах 5 мм. Использование данных методов, например сэндвич-пластики, может быть невозможным в силу отсутствия исходного костного объема (близко расположен нижнеальвеолярный нерв), а винирной пластики — при выраженных неровностях реципиентного ложа, когда сложно добиться прилегания костного трансплантата. Другим ограничением служит дополнительная травматичность забора костного трансплантата при восстановлении ограниченных костных дефектов в пределах 1–3 зубов. В описанных ситуациях направленная костная регенерация с применением каркасных мембран может являться методом выбора. Этот метод лишен указанных выше ограничений, а именно: костный дефект ограничивается мембраной, определяющей форму и объем реконструкции; сформированная мембраной полость заполняется костной стружкой, обладающей всеми достоинствами аутогенной кости [9], и костным гидроксиапатитом, обеспечивающим матриксные свойства для костного регенерата [10]. В качестве материала для заполнения дефекта костной ткани можно также использовать пористые скаффолды [11–13] и микрочастицы из биоразлагаемых полимеров [14, 15], биополимерные гидрогели [14], а также композитные изделия и материалы [13, 14], в том числе обладающие терапевтической активностью за счет пролонгированного высвобождения загруженных в полимерную матрицу лекарственных веществ [15, 16], а барьерные мембраны [16–18] можно изготавливать из биоразлагаемых [19, 20] и биосовместимых полимеров [21–24].
Основным недостатком направленной костной регенерации при восстановлении дефектов альвеолярной кости является сложность адаптации и стабильной фиксации каркасной мембраны для ограничения зоны реконструкции. Для решения указанной проблемы авторами предложен метод трехмерного компьютерного планирования направленной костной регенерации на основе данных рентгеновской компьютерной томографии.
Цель исследования — оценить эффективность объемной реконструкции альвеолярной кости методом направленной костной регенерации на основе трехмерного компьютерного планирования с использованием резорбируемой каркасной мембраны.
Материалы и методы. В исследование были включены 35 практически здоровых некурящих пациентов без выраженной сопутствующей соматической патологии с диагнозом «частичная потеря зубов, осложненная атрофией альвеолярной кости» (по МКБ — K08.1, К08.2), из них 17 мужчин и 18 женщин, возраст 35–62 года. Всем пациентам проведены реконструктивные операции с целью устранения дефектов и восстановления объема альвеолярной кости методом направленной костной регенерации с использованием резорбируемых каркасных мембран Lamina (Osteobiol, Италия). 20 операций проведено на нижней челюсти, 15 — на верхней. Планирование и сами операции осуществляли по разработанному унифицированному протоколу.
Исследование проведено в соответствии с Хельсинкской декларацией, принятой в июне 1964 г. (Хельсинки, Финляндия) и пересмотренной в октябре 2000 г. (Эдинбург, Шотландия), и одобрено Этическим комитетом НижГМА. От каждого пациента получено информированное согласие.
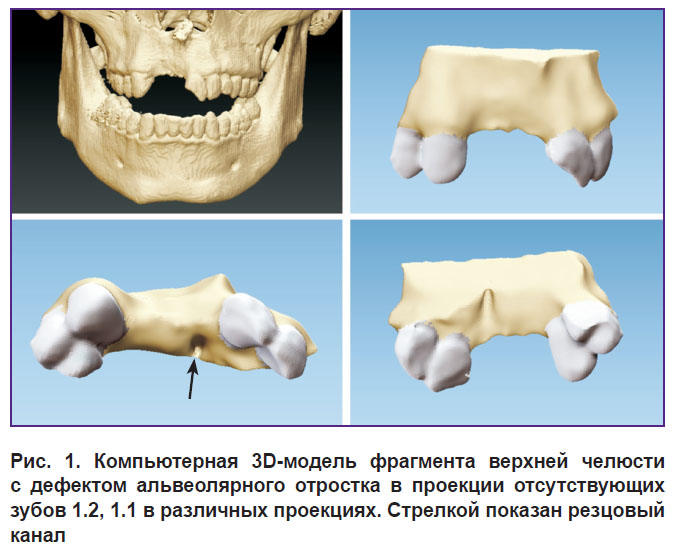
Компьютерное 3D-планирование операции. Всем пациентам проводили конусно-лучевую компьютерную томографию. При наличии металлокерамических ортопедических конструкций на зубах, прилегающих к области планируемой реконструкции, их предварительно снимали для уменьшения помех при рентгенологическом исследовании. На основе полученных DICOM-файлов выполняли реформацию 3D-модели челюсти (рис. 1), затем в программе ViSurgery (Россия) моделировали объем костной реконструкции (рис. 2).
|
Рис. 1. Компьютерная 3D-модель фрагмента верхней челюсти с дефектом альвеолярного отростка в проекции отсутствующих зубов 1.2, 1.1 в различных проекциях. Стрелкой показан резцовый канал |
|
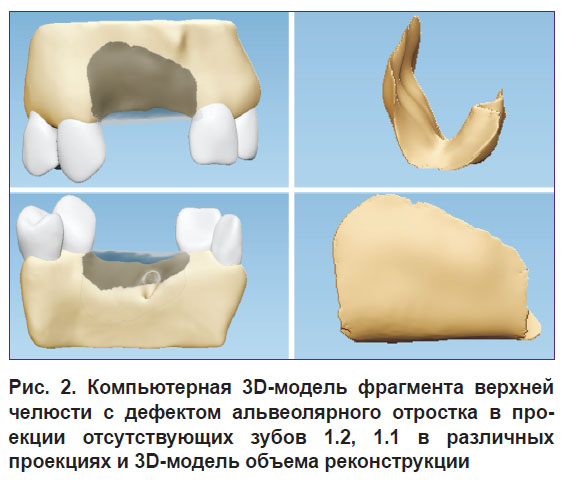
Рис. 2. Компьютерная 3D-модель фрагмента верхней челюсти с дефектом альвеолярного отростка в проекции отсутствующих зубов 1.2, 1.1 в различных проекциях и 3D-модель объема реконструкции |
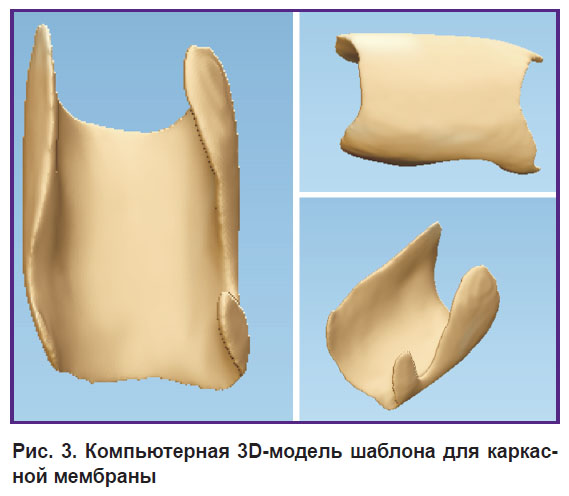
Моделирование верхней границы регенерата проводили по уровню костной ткани у шеек зубов, ограничивающих дефект. В случае концевых дефектов зубного ряда уровень реконструкции определяли по пришеечному уровню кости дистально расположенного зуба. Объем реконструкции рассчитывали в программе (в мм3), в дальнейшем этот показатель сравнивали с полученным объемом кости. Затем в программе моделировали шаблон каркасной мембраны (рис. 3).
|
Рис. 3. Компьютерная 3D-модель шаблона для каркасной мембраны |
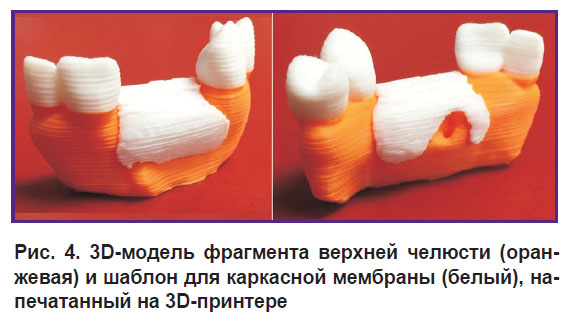
3D-модель альвеолярной кости и шаблон каркасной мембраны печатали на 3D-принтере Engineer V2 (3DExperts.ru, Россия) методом послойного наплавления (FDM) (рис. 4). Для печати использовали пруток из полилактида (диаметр — 1,75 мм, температура плавления — 225°С, плотность — 1,08–1,2 кг/м2, экологически чистый, не токсичен, производитель — Московский завод FDPlast, Россия). Толщина слоя модели — 100 мкм.
|
Рис. 4. 3D-модель фрагмента верхней челюсти (оранжевая) и шаблон для каркасной мембраны (белый), напечатанный на 3D-принтере |
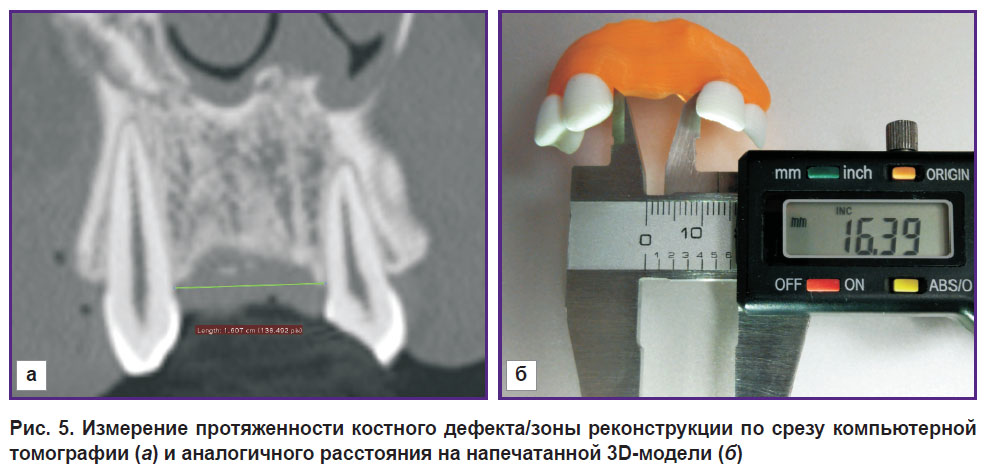
С целью контроля точности виртуального планирования и печати 3D-моделей измеряли протяженность костного дефекта на срезах компьютерной томографии и аналогичное расстояние на 3D-моделях челюстей и сравнивали значения (рис. 5). В каждом случае для определения повторяемости метода проводили по три повторных измерения на томограмме и на модели. Полученные результаты подвергали статистической обработке в программном обеспечении SAS Studio. Использовали F-критерий Фишера и t-критерий Стьюдента. Значения средних абсолютных отклонений результатов измерений протяженности костного дефекта по компьютерной томограмме и 3D-модели рассчитывали по формуле
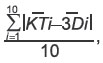
где 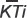 — i-е измерение по КТ-модели,
— i-е измерение по КТ-модели, 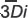 — это i-е измерение по 3D-модели. Полученные данные позволяют сравнить систематическую ошибку измерений, связанную с методом преобразования модели, с ошибками измерений по каждой модели.
— это i-е измерение по 3D-модели. Полученные данные позволяют сравнить систематическую ошибку измерений, связанную с методом преобразования модели, с ошибками измерений по каждой модели.
|
Рис. 5. Измерение протяженности костного дефекта/зоны реконструкции по срезу компьютерной томографии (а) и аналогичного расстояния на напечатанной 3D-модели (б) |
Шаблон мембраны стерилизовали и использовали во время операции для придания нужной формы каркасной мембране, ограничивающей зону реконструкции.
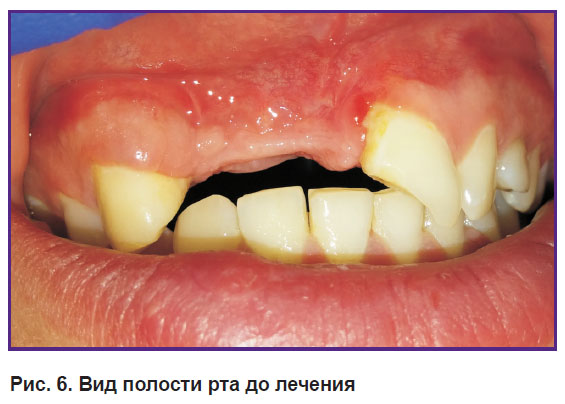
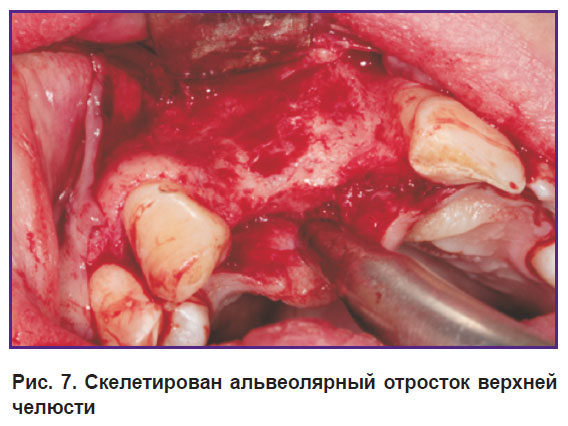
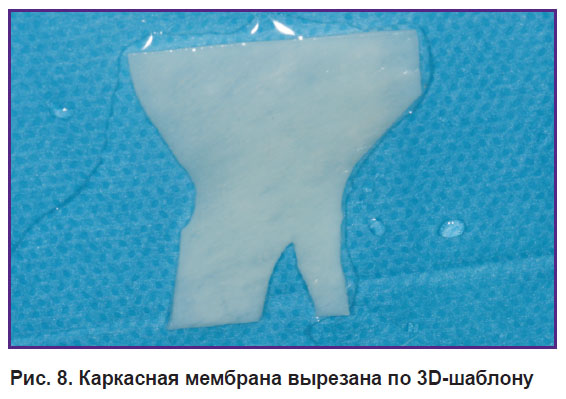
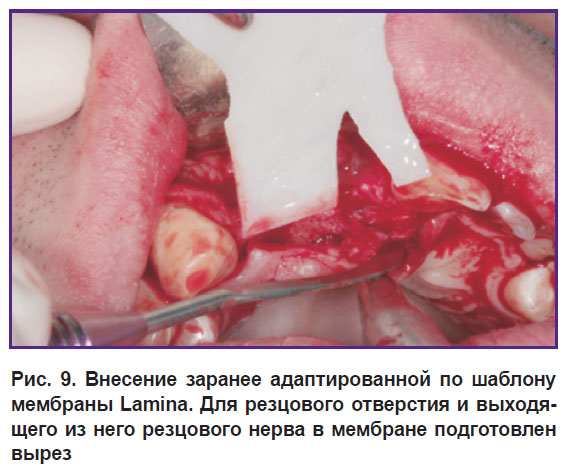
Протокол операции трехмерной реконструкции альвеолярной кости. Операцию костной пластики выполняли под сбалансированной анестезией (рис. 6). Производили разрез слизистой оболочки, отслаивали слизисто-надкостничный лоскут и скелетировали область дефекта альвеолярной кости (рис. 7). Затем мембрану Lamina совмещали с простерилизованным шаблоном и придавали ей нужную форму (рис. 8). С небной стороны мембрану фиксировали пинами или микровинтами («Конмет», Россия) (рис. 9, 10). В качестве материала для реконструкции использовали костную стружку, полученную из области косой линии нижней челюсти костным скребком. Стружку смешивали с депротеинизированным костным гидроксиапатитом (Биопласт-Дент, «ВладМиВа», Россия) в соотношении 1:1. Полученную массу укладывали в область дефекта и уплотняли (см. рис. 10). Потом мембраной Lamina плотно перекрывали область реконструкции и фиксировали пинами с вестибулярной стороны (рис. 11). После мобилизации лоскута герметично ушивали рану: накладывали внутренний П-образный шов на надкостницу вестибулярного и небного лоскутов, тем самым сводя края раны и дополнительно прижимая мембрану, края лоскутов ушивали матрацными и узловыми швами.
|
Рис. 6. Вид полости рта до лечения |
|
Рис. 7. Скелетирован альвеолярный отросток верхней челюсти |
|
Рис. 8. Каркасная мембрана вырезана по 3D-шаблону |
|
Рис. 9. Внесение заранее адаптированной по шаблону мембраны Lamina. Для резцового отверстия и выходящего из него резцового нерва в мембране подготовлен вырез |
|
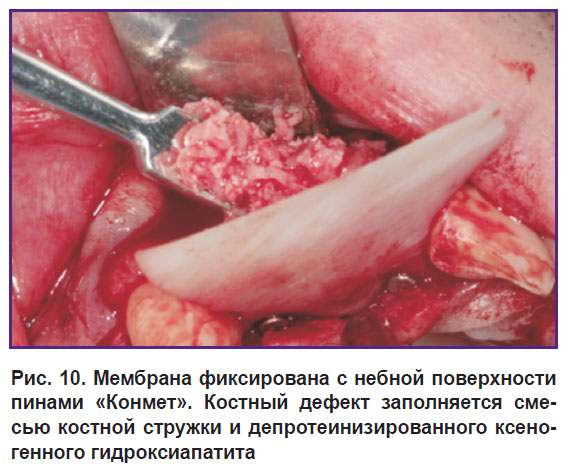
Рис. 10. Мембрана фиксирована с небной поверхности пинами «Конмет». Костный дефект заполняется смесью костной стружки и депротеинизированного ксеногенного гидроксиапатита |
|
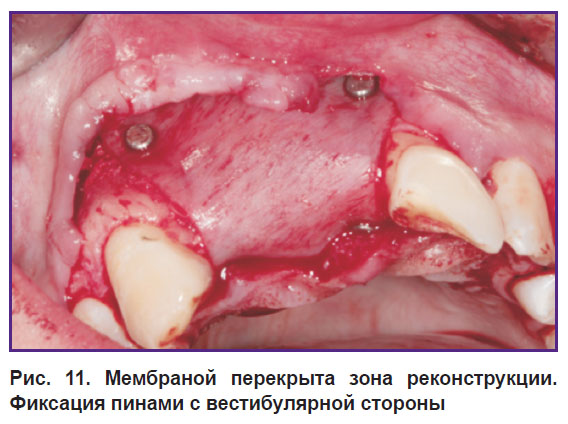
Рис. 11. Мембраной перекрыта зона реконструкции. Фиксация пинами с вестибулярной стороны |
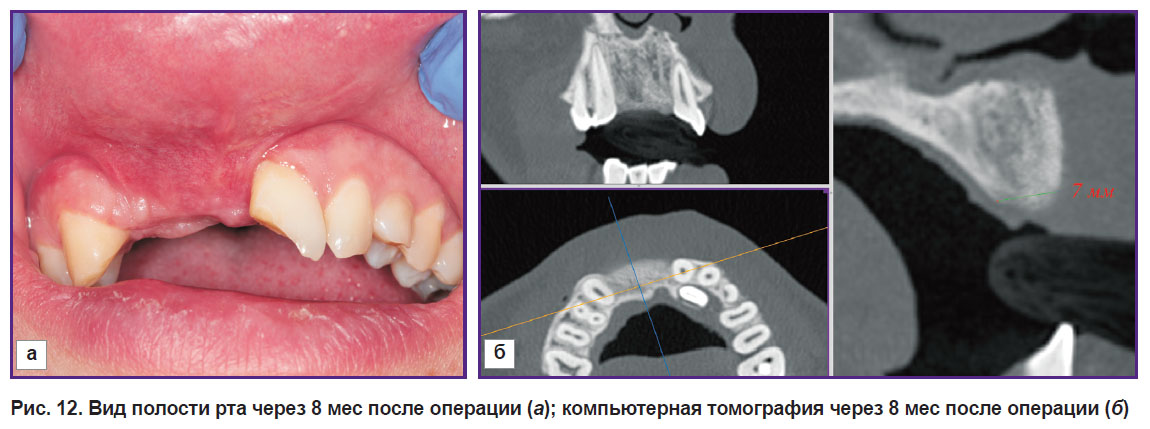
Через 8 мес после реконструкции (рис. 12, а) проводили повторную компьютерную томографию, измеряли размеры регенерата (рис. 12, б). По данным DICOM реформировали 3D-модель костного регенерата и сравнивали полученный и запланированный объемы костного регенерата.
|
Рис. 12. Вид полости рта через 8 мес после операции (а); компьютерная томография через 8 мес после операции (б) |
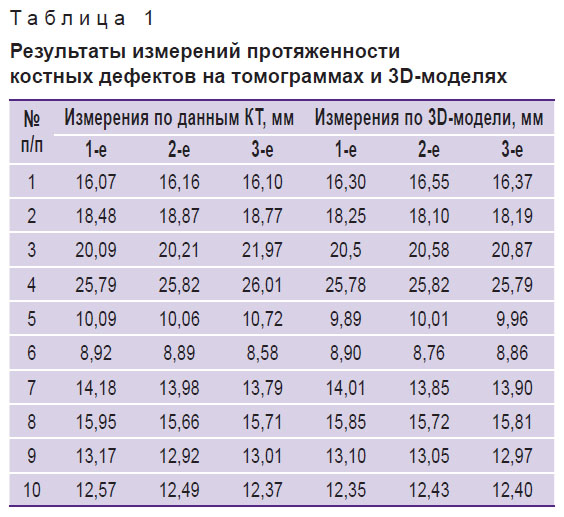
Результаты и обсуждение. Для оценки точности изготовления 3D-моделей челюстей и шаблонов каркасных мембран были измерены протяженности костных дефектов на томограммах и на 3D-моделях, изготовленных методом FDM. Для анализа были произвольно выбраны данные 10 пациентов (табл. 1).
|
Таблица 1. Результаты измерений протяженности костных дефектов на томограммах и 3D-моделях |
Анализ результатов измерений показал достаточно высокую точность полученных 3D-моделей. Критерий Фишера F=0,9923 свидетельствует о неразличимости дисперсий. Критерий Стьюдента для одинаковых дисперсий t=0,9715 также показал, что средние значения статистически неразличимы. Среднее модулей разности средних значений измерений составило 0,156 мм при среднеквадратичном отклонении 0,26 мм, что в пересчете на проценты дает погрешность не более 3,32%.
Стоит учесть, что источником отклонений могут служить следующие факторы: ошибки измерения (фактор исследователя); особенности алгоритмов восстановления 3D-модели по результатам КТ и их преобразования в 3D-модель для печати; точность калибровки 3D-принтера и погрешности печати методом FDM.
Полученные нами результаты отличаются от данных M. Salmi и соавт. [25], которые сравнивают различные технологии объемного прототипирования анатомических моделей черепа тремя различными методами: стереолитографией (SLA), порошковой печатью (3DP) и струйной 3D-печатью (PolyJet). Наилучшие результаты по точности показала технология PolyJet (ошибка — 0,18±0,12%) по сравнению с SLA (0,79±0,26%) и 3DP (0,67±0,43%). Расхождение наших результатов с значениями [25] можно объяснить тем, что технологии печати 3DP, PolyJet обладают более высокой точностью: PolyJet — 0,016 мм, 3DP — 0,09 мм. Высота слоя при печати SLA — 0,15 мм, а FDM — 0,1 мм. Расхождения можно также объяснить методологией измерения моделей и точностью измерительного аппарата. В любом случае полученная нами погрешность в 3,32% при пересчете на максимальную протяженность дефекта в 26 мм составит 0,86 мм, что допустимо при планировании реконструкции альвеолярной кости. Кроме того, использованная нами технология FDP отличается от указанных простотой печати и недорогими расходными материалами.
По описанной методике проведено лечение 35 пациентов (20 операций на нижней челюсти и 15 — на верхней). В послеоперационном периоде в трех случаях отмечалось частичное расхождение швов над каркасной мембраной. Заживление проходило вторичным натяжением. В остальных случаях осложнений не наблюдалось.
Время оперативного вмешательства незначительно сокращалось по сравнению со стандартным протоколом, в среднем на 5–7 мин, за счет более быстрого адаптирования каркасной мембраны, скроенной по шаблону, и отсутствия необходимости ее примерок. Более важным результатом явилось полное исключение риска формирования мембраны меньшего размера и неправильной формы, что может приводить к ошибке при формировании объема костной реконструкции.
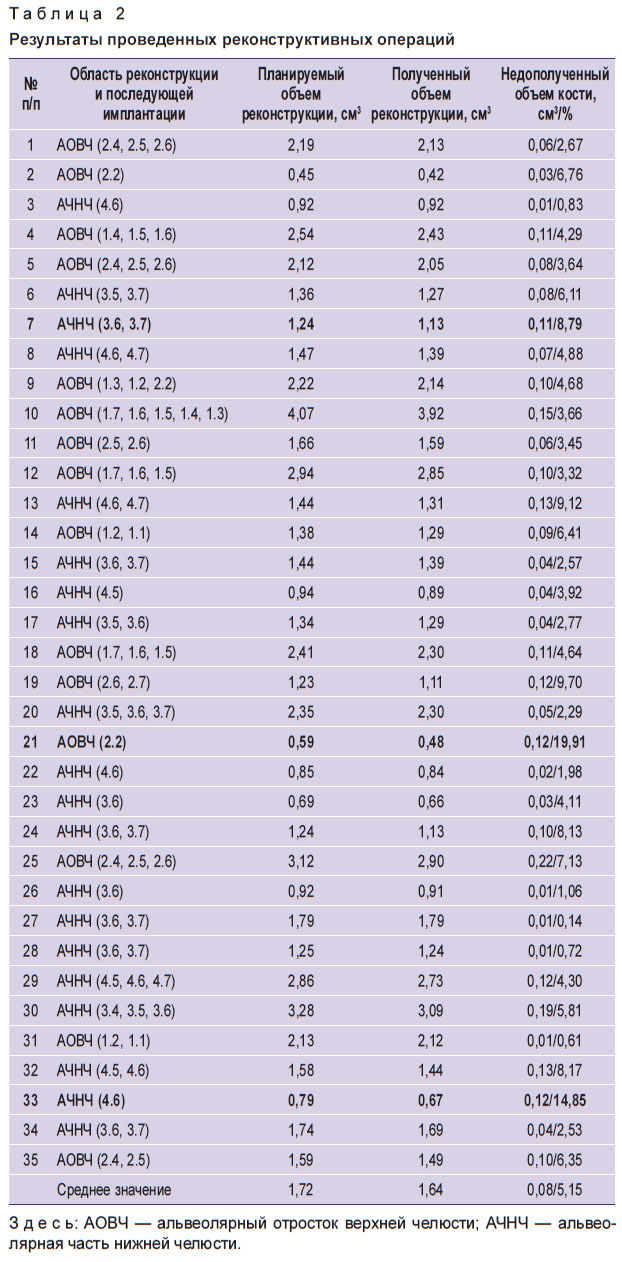
В табл. 2 приведены сведения о выполненных операциях: области реконструкции, планируемом и полученном в результате лечения объеме и недополученном объеме. Строки 7, 21, 33 соответствуют случаям, в которых отмечалось расхождение швов (выделены жирным).
|
Таблица 2. Результаты проведенных реконструктивных операций |
Среднее значение недополученного костного объема составило 0,08 см3 (0,0541–0,2228 см3), или 5,2% (0,3–19%) от планируемого костного объема. Максимальная потеря в объеме наблюдалась при расхождении швов и экспозиции мембраны в 3 случаях из 35, или в 8,57%. В работе G. Lizio с соавт. [26] проводилась оценка эффективности объемной реконструкции альвеолярной кости с использованием титановой сетки в качестве барьерной мембраны. Результаты показали, что объем потери костного регенерата коррелирует с площадью экспозиции титановой сетки и составляет до 30,2%, при том что экспозиция сетки наблюдалась в 80% случаев ее использования (12 из 15). Таким образом, с точки зрения риска экспозиции резорбируемая каркасная мембрана выгодно отличается от титановой сетки.
Заключение. Предложенный метод трехмерного компьютерного планирования и изготовления интраоперационных шаблонов для каркасной мембраны с помощью объемного прототипирования позволяет повысить точность проведения операций по направленной костной регенерации, уменьшить интраоперационное время адаптации мембраны и исключить возможность ее неправильного позиционирования. При этом использование резорбируемой каркасной мембраны позволяет повысить эффективность объемной реконструкции альвеолярной кости за счет снижения случаев экспозиции регенерата и получить 94,8% от запланированного костного объема.
Финансирование исследования. Работа выполнена при поддержке гранта Российского научного фонда (соглашение №15-15-10014 от 01.05.2015 г.).
Конфликт интересов. У авторов нет конфликта интересов. ООО «НЕКСТ» не финансировало исследование и не влияло на его результат.
Литература
- Параскевич В.Л. Возможности применения внутрикостной имплантации при значительной атрофии челюстей. В кн.: Материалы I международной конференции «Актуальные вопросы стоматологической имплантации». Минск; 1998; с. 15–23.
- Иванов С.Ю., Ямуркова Н.Ф., Мураев А.А. Устранение дефектов альвеолярной части нижней челюсти методом сэндвич-пластики. Стоматология 2010; 89(2): 42–47.
- Bassett C.A.L. Biologic significance of piezoelectricity. Calcif Tissue Res 1967; 1(1): 252–272, https://doi.org/10.1007/bf02008098.
- Boyne P.J., James R.A. Grafting of the maxillary sinus floor with autogenous marrow and bone. J Oral Surg 1980; 38(8): 613–616.
- Большая советская энциклопедия. Т. 30. Гл. ред. Прохоров А.М. М: Советская энциклопедия; 1969–1978.
- Иванов С.Ю., Ямуркова Н.Ф., Мураев А.А., Хасьянов И.Т. Обоснование применения различных методов реконструкции альвеолярной части нижней челюсти как этапа подготовки к стоматологической имплантации. Российский вестник дентальной имплантологии 2013; 2(28): 34–39.
- Ямуркова Н.Ф., Иванов С.Ю., Мураев А.А. «Винирная» пластика альвеолярной части челюсти перед проведением стоматологической имплантации. Стоматология 2010; 89(2): 36–41.
- Панин А.М., Малинецкий Г.Г., Цициашвили А.М., Анастос А. Математическое планирование операции сэндвич-пластики скользящим костно-надкостнично-слизистым лоскутом. Стоматология 2013; 92(3): 63–64.
- Khoury F., Hanser T. Mandibular bone block harvesting from the retromolar region: a 10-year prospective clinical study. Int J Oral Maxillofac Implants 2015; 30(3): 688–697, https://doi.org/10.11607/jomi.4117.
- Ломакин М.В., Филатова А.С., Солощанский И.И. Направленная костная регенерация при реконструкции альвеолярного костного объема в области дентальной имплантации. Российская стоматология 2011; 4(5): 15–18.
- Andreeva N.V., Bonartsev A.P., Zharkova I.I., Makhina T.K., Myshkina V.L., Kharitonova E.P., Voinova V.V., Bonartseva G.A., Shaitan K.V., Belyavskii A.V. Culturing of mouse mesenchymal stem cells on poly-3-hydroxybutyrate scaffolds. Bull Exp Biol Med 2015; 159(4): 567–571, https://doi.org/10.1007/s10517-015-3015-5.
- Bonartsev A.P., Zharkova I.I., Yakovlev S.G., Myshkina V.L., Makhina T.K., Zernov A.L., Kudryashova K.S., Feofanov A.V., Akulina E.A., Ivanova E.V., Zhuikov V.A., Andreeva N.V., Voinova V.V., Bessonov I.V., Kopitsyna M.V., Morozov A.S., Bonartseva G.A., Shaitan K.V., Kirpichnikov M.P. 3D-scaffolds from poly(3-hydroxybutyrate)poly(ethylene glycol) copolymer for tissue engineering. J Biomater Tissue Eng 2016; 6(1): 42–52, https://doi.org/10.1166/jbt.2016.1414.
- Muraev A.A., Bonartsev A.P., Gazhva Yu.V., Riabova V.M., Volkov A.V., Zharkova I.I., Stamboliev I.A., Kuznetsova E.S., Zhuikov V.A., Myshkina V.L., Mahina T.K., Bonartseva G.A., Yakovlev S.G., Kudryashova K.S., Voinova V.V., Mironov A.A., Shaitan K.V., Gazhva S.I., Ivanov S.Yu. Development and preclinical studies of orthotopic bone implants based on a hybrid construction from poly(3-hydroxybutyrate) and sodium alginate. Sovremennye tehnologii v medicine 2016; 8(4): 42–50, https://doi.org/10.17691/stm2016.8.4.06.
- Gazhva J.V., Bonartsev А.P., Mukhametshin R.F., Zharkova I.I., Andreeva N.V., Makhina T.К., Myshkina V.L., Bespalova A.E., Zernov А.L., Ryabova V.M., Ivanova E.V., Bonartseva G.А., Mironov А.А., Shaitan K.V., Volkov А.V., Muraev А.А., Ivanov S.Y. In vivo and in vitro development and study of osteoplastic material based on hydroxyapatite, poly-3-hydroxybutyrate and sodium alginate composition. Sovremennye tehnologii v medicine 2014; 6(1): 6–13.
- Livshits V.A., Bonartsev A.P., Iordanskii A.L., Ivanov E.A., Makhina T.A., Myshkina V.L., Bonartseva G.A. Microspheres based on poly(3-hydroxy)butyrate for prolonged drug release. Polymer Science Series B 2009; 51(7–8): 256–263, https://doi.org/10.1134/s1560090409070082.
- Bonartsev A.P., Bonartseva G.A., Makhina T.K., Myshkina V.L., Luchinina E.S., Livshits V.A., Boskhomdzhiev A.P., Markin V.S., Iordanskii A.L. New poly(3-hydroxybutyrate)-based systems for controlled release of dipyridamole and indomethacin. Appl Biochem Microbiol 2006; 42(6): 625–630, https://doi.org/10.1134/s0003683806060159.
- Иванов С.Ю., Бонарцев А.П., Гажва Ю.В., Жаркова И.И., Мухаметшин Р.Ф., Махина Т.К., Мышкина В.Л., Бонарцева Г.А., Воинова В.В., Андреева Н.В., Акулина Е.А., Харитонова Е.С., Шайтан К.В., Мураев А.А. Разработка и доклинические исследования изолирующей мембраны на основе сополимера поли-3-оксибутирата-со-3-оксивалерата для направленной костной регенерации. Биомедицинская химия 2015; 61(6): 717–723.
- Bonartsev A.P., Yakovlev S.G., Zharkova I.I., Boskhomdzhiev A.P., Bagrov D.V., Myshkina V.L., Makhina T.K., Kharitonova E.P., Samsonova O.V., Feofanov A.V., Voinova V.V., Zernov A.L., Efremov Y.M., Bonartseva G.A., Shaitan K.V., Kirpichnikov M.P. Cell attachment on poly(3-hydroxybutyrate)-poly(ethylene glycol) copolymer produced by Azotobacter chroococcum 7B. BMC Biochem 2013; 14(1): 12, https://doi.org/10.1186/1471-2091-14-12.
- Bonartsev A.P., Boskhomodgiev A.P., Iordanskii A.L., Bonartseva G.A., Rebrov A.V., Makhina T.K., Myshkina V.L., Yakovlev S.A., Filatova E.A., Ivanov E.A., Bagrov D.V., Zaikov G.E. Hydrolytic degradation of poly(3-hydroxybutyrate), polylactide and their derivatives: kinetics, crystallinity, and surface morphology. Molecular Crystals and Liquid Crystals 2012; 556(1): 288–300, https://doi.org/10.1080/15421406.2012.635982.
- Boskhomdzhiev A.P., Bonartsev A.P., Makhina T.K., Myshkina V.L., Ivanov E.A., Bagrov D.V., Filatova E.V., Iordanskii A.L., Bonartseva G.A. Biodegradation kinetics of poly(3-hydroxybutyrate)-based biopolymer systems. Biochemistry (Moscow) Supplement Series B: Biomedical Chemistry 2010; 4(2): 177–183, https://doi.org/10.1134/s1990750810020083.
- Myshkina V.L., Ivanov E.A., Nikolaeva D.A., Makhina T.K., Bonartsev A.P., Filatova E.V., Ruzhitsky A.O., Bonartseva G.A. Biosynthesis of poly(3-hydroxybutyrate-co-3-hydroxyvalerate) copolymer by Azotobacter chroococcum strain 7B. Appl Biochem Microbiol 2010; 46(3): 289–296, https://doi.org/10.1134/s0003683810030075.
- Bonartsev A.P., Iordanskii A.L., Bonartseva G.A., Zaikov G.E. Biodegradation and medical application of microbial poly (3-hydroxybutyrate). Journal of the Balkan Tribological Association 2008; 14(3): 359–395.
- Myshkina V.L., Nikolaeva D.A., Makhina T.K., Bonartsev A.P., Bonartseva G.A. Effect of growth conditions on the molecular weight of poly-3-hydroxybutyrate produced by Azotobacter chroococcum 7B. Appl Biochem Microbiol 2008; 44(5): 482–486, https://doi.org/10.1134/s0003683808050050.
- Bonartsev A.P., Bonartseva G.A., Shaitan K.V., Kirpichnikov M.P. Poly(3-hydroxybutyrate) and poly(3-hydroxybutyrate)-based biopolymer systems. Biochemistry (Moscow) Supplement Series B: Biomedical Chemistry 2011; 5(1): 10–21, https://doi.org/10.1134/s1990750811010045.
- Salmi M., Paloheimo K.-S., Tuomi J., Wolff J., Mäkitie A. Accuracy of medical models made by additive manufacturing (rapid manufacturing). Journal of Cranio-Maxillofacial Surgery 2013; 41(7): 603–609, https://doi.org/10.1016/j.jcms.2012.11.041.
- Lizio G., Corinaldesi G., Marchetti C. Alveolar ridge reconstruction with titanium mesh: a three-dimensional evaluation of factors affecting bone augmentation. Int J Oral Maxillofac Implants 2014; 29(6): 1354–1363,










