Ультраструктурные АСМ-маркеры эндогенной интоксикации при внебольничной пневмонии
Цель исследования — оценка информативности параметров атомно-силовой микроскопии для характеристики степени тяжести эндогенной интоксикации при внебольничной пневмонии по результатам исследования ультраструктурных показателей эритроцитов.
Материалы и методы. Методом атомно-силовой микроскопии исследованы наноанатомические и микромеханические показатели эритроцитов у 71 больного с тяжелой и нетяжелой внебольничной пневмонией в возрасте 18–23 года (средний возраст — 20,4±0,6 года) на фоне эндогенной интоксикации различной степени тяжести. Контрольную группу составили 20 добровольцев. Образцы эритроцитов были получены в 1, 3, 7 и 14-е сутки госпитализации. Для определения их морфологических свойств применяли контактный режим наномеханического картирования. Оценку тяжести эндогенной интоксикации проводили по общепринятым клинико-лабораторным параметрам, включающим гематологические, биохимические и иммунологические маркеры.
Результаты. Получены референсные значения микромеханических параметров мембран эритроцитов у здоровых лиц молодого возраста и больных внебольничной пневмонией с различной степенью тяжести эндогенной интоксикации, что может служить ориентиром для будущих исследований в аналогичных выборках. Установлено, что при данном заболевании упругоэластические свойства мембран эритроцитов тесно взаимосвязаны с выраженностью эндотоксикоза. Так, по мере его нарастания модуль упругости и сила адгезии мембраны эритроцитов снижались в 5,2 и 2,4 раза соответственно, а деформация повышалась в 2,6 раза. Корреляционный анализ выявил наличие тесных взаимосвязей между показателями, характеризующими тяжесть эндогенной интоксикации (молекулы средней массы, IL-10, фактор некроза опухоли, лейкоцитарный, ядерный, гематологический индексы интоксикации и др.), и микромеханическими параметрами клеточных мембран. Показатели, характеризующие геометрический «портрет» эритроцитов (площадь, диаметр, высота бортика и др.), существенно не изменялись, что может свидетельствовать о стабильности их цитоскелета.
Заключение. Проведенные исследования доказывают информативность оценки микромеханических параметров мембран эритроцитов методом атомно-силовой микроскопии для характеристики степени тяжести эндогенной интоксикации при внебольничной пневмонии. Полученные данные дополняют представления о патофизиологических последствиях эндогенной интоксикации, их влиянии на ультраструктуру клеток и адаптивный характер изменений микромеханических свойств мембран эритроцитов.
Синдром эндогенной интоксикации (ЭИ) является облигатным признаком большинства острых инфекционно-воспалительных процессов, в том числе внебольничной пневмонии (ВП), и нередко определяет тактику лечения и прогноз заболевания [1]. К основным патофизиологическим механизмам ЭИ относят стремительное накопление в организме бактериальных токсинов, продуктов клеточного распада, метаболитов оксидативного стресса, других физиологически активных веществ, а также избыточный протеолиз, которые происходят на фоне развивающегося несоответствия между чрезмерным поступлением токсических субстанций в ткани и кровоток и способностью биологических систем детоксикации организма их трансформировать, нейтрализовать и элиминировать [2]. Как показывает клиническая практика, у большинства больных ВП в разгар заболевания доминируют проявления синдрома ЭИ, которые иногда маскируют симптомы альвеолярного воспаления. Превалирование признаков эндотоксемии над симптоматикой воспаления легочной ткани чаще встречается при нетяжелой ВП, что в ряде случаев является причиной поздней диагностики заболевания. В дебюте тяжелой ВП почти всегда на первый план выходят проявления дыхательной недостаточности и артериальной гипоксемии, а симптоматика ЭИ лишь дополняет клиническую картину. Это не относится к особым вариантам эндотоксемии — инфекционно-токсическому шоку и полиорганной недостаточности, которые чаще всего развиваются на фоне септических состояний, осложняющих течение пневмонии.
Тяжесть ЭИ определяется уровнем концентрации в биологических средах организма бактериальных и метаболических эндотоксинов, оказывающих повреждающее действие на клеточные структуры с последующим каскадом обменных нарушений. В клинической практике для оценки тяжести ЭИ используют клинико-лабораторные тесты: лейкоцитарный (ЛИИ), гематологический (ГИИ), ядерный (ЯИИ) и другие индексы интоксикации [2]. К универсальным биохимическим маркерам ЭИ относят также молекулы средней массы (МСМ), являющиеся продуктом избыточного протеолиза. Вместе с тем имеются лишь единичные исследования наноструктуры клеток в условиях эндотоксемии. Использование для этих целей современных биомедицинских технологий открывает новые возможности для выяснения патофизиологических закономерностей формирования клинической картины заболевания у разных категорий больных [3].
Атомно-силовая микроскопия (АСМ) позволяет регистрировать силу взаимосвязей между атомами образца и атомом зонда (кантилевера) на расстояниях около одного ангстрема и оперирует наноразмерами. Это эффективно используется при изучении микрорельефа и структуры поверхности биологических тканей, фиксирует их трехмерные изображения на атомно-молекулярном уровне, что дает возможность изучать наноструктуру объекта. Кроме того, с помощью АСМ измеряют упругие и адгезивные свойства клеточных мембран, тесно взаимосвязанных с интра- и экстрацеллюлярными взаимодействиями [4]. Этот метод позволяет создавать как геометрический «образ» поверхности клетки, так и ее физико-механический (биомеханический) «образ», составленный из набора АСМ-параметров.
Цель исследования — оценка информативности параметров атомно-силовой микроскопии для характеристики степени тяжести эндогенной интоксикации при внебольничной пневмонии по результатам исследования ультраструктурных показателей эритроцитов.
Материалы и методы. Проанализированы результаты обследования 71 больного с ВП, лечившихся в 439 военном госпитале МО РФ в 2013–2014 гг. Возраст больных составлял 18–23 года, в среднем — 20,4±0,6 года. Все обследованные были лицами мужского пола, госпитализированными в стационар в первые сутки от начала заболевания. Никому из пациентов не проводилась антибактериальная терапия. Диагноз ВП во всех случаях устанавливали по результатам микробиологических, клинико-рентгенологических и лабораторных исследований с учетом рекомендаций Российского респираторного общества [5]. Нетяжелая ВП диагностирована у 45 больных и тяжелая — у 26. Контрольную группу составили 20 здоровых некурящих добровольцев аналогичного возраста.
Для больных с нетяжелой ВП было характерным наличие субсегментарной или в пределах нескольких сегментов очаговой воспалительной инфильтрации в легких. У больных тяжелой ВП фиксировали наличие долевых, бидолевых, билатеральных или полисегментарных двухсторонних легочных инфильтратов, у 8 из них диагностирован парапневмонический экссудативный плеврит. По данным мониторирования парциального напряжения кислорода в артериальной крови (РаО2) и ее сатурации кислородом (SpO2) у этой категории больных регистрировали гипоксемию со средним уровнем РаО2 — 90,71±0,68 мм рт. ст., SpO2 — 89,62±0,87%. Этиологическая структура нетяжелой и тяжелой ВП была следующей: Streptococcus pneumoniae — 64,4 и 61,5%, Haemophilus influenza — 17,8 и 23,1%, Mycoplasma pneumonia — 11,1 и 11,5%, Chlamydophila pneumonia — 4,4 и 7,7% соответственно.
С учетом клинико-лабораторных данных, характеризующих тяжесть эндотоксемии [2], было выделено три группы обследованных: 1-ю группу составили 25 больных с ЭИ I степени, 2-ю группу — 24 больных с ЭИ II степени и 3-ю группу — 22 больных с ЭИ III степени. При этом ЭИ I степени была характерна только для больных с нетяжелой ВП, II–III степени — как для больных с тяжелым течением ВП (26 человек), так и с нетяжелым (20 человек).
Забор крови всем обследованным производили из вены в количестве 3 мл в течение суток после поступления в стационар, а затем на 3, 7 и 14-е сутки. В качестве антикоагулянта использовали гепарин в количестве 10 ЕД/мл. Выделение эритроцитов осуществляли путем центрифугирования в течение 10 мин при 1500 об./мин. Всем больным выполняли стандартные лабораторные, микробиологические и иммунологические исследования, рассчитывали гематологические индексы интоксикации: ЛИИ, ГИИ, ЯИИ. Определяли концентрацию МСМ в плазме крови [2]. Уровень цитокинов в сыворотке крови оценивали методом иммуноферментного анализа с использованием тест-систем для определения IL-10, фактора некроза опухоли (TNF-α) по методике производителя DuoSet ELISA Development Systems (R&D Systems, Inc., США).
Анализ газового состава артериальной крови проводили на автоматическом анализаторе ABL-725 (Radiometer Copenhagen, Дания), SpO2 определяли на пульсоксиметре Nissei OX-700 (Nihon Seimitsu Sokki Co., Ltd., Япония).
Исследование наноструктуры эритроцитов осуществляли на сканирующем атомно-силовом микроскопе Bioscope Catalyst (Bruker, США) в сочетании с инвертированным микроскопом Axiovert 200 (Carl Zeiss, Германия). Изображение получали в контактном режиме Scan Asyst mode. Для контроля разрушения образцов при сканировании выборочно использовали полубесконтактный режим. Применяли датчики (кантилеверы) MSNL-10 (k: 0,07–0,107 Н/м, f0: 15–33 кГц) и SCANASYST-AIR (k: 0,3–0,4 Н/м, f0: 54–92 кГц) (Bruker, США).
Для определения микромеханических характеристик мембран эритроцитов (модуля упругости, эластической деформации, силы адгезии) использовали режим наномеханического картирования PFQNM (the peak force quantitative nano-mechanical mapping mode), разработанный ф. Bruker. Перед каждым микромеханическим картированием исследуемого образца проводили калибровку кантилевера по опорным материалам — эталонам ф. Bruker с известными механическими свойствами поверхности. При этом определяли чувствительность к отклонению по лейкосапфиру, модуль упругости — по полиэтилену: PDMS-SOFT1 (2,5 МПа) и PDMS-SOFT2 (3,5 МПа). Кроме того, измеряли радиус скругления кончика иглы кантилевера на специальной тестовой пластине с покрытием из оксида титана. Полученные калибровочные данные с помощью программы NanoScopev. 8.10 (Bruker, США) использовали для расчета истинной константы упругости (k) и построения изображения объекта в микромеханических размерах.
Исследование проведено в соответствии с Хельсинкской декларацией, принятой в июне 1964 г. (Хельсинки, Финляндия) и пересмотренной в октябре 2000 г. (Эдинбург, Шотландия), одобрено Этическим комитетом Тихоокеанского государственного медицинского университета. От пациентов получено информированное согласие на обработку персональных данных.
Результаты экспериментальных исследований обработаны методами вариационной статистики с использованием пакета анализа Microsoft Excel 14. При сравнении двух независимых групп применяли непараметрический критерий Манна–Уитни, анализ взаимосвязей выполняли непараметрическим методом корреляционного анализа Спирмена для ненормального распределения.
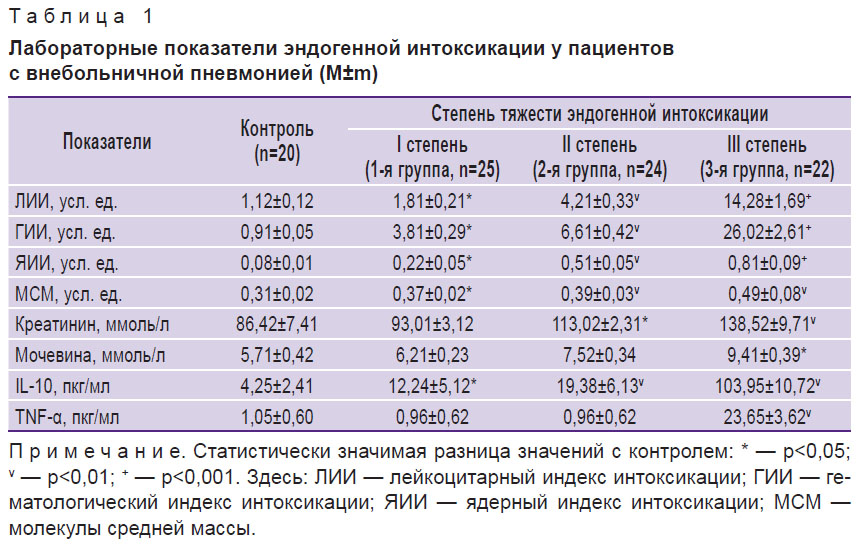
Результаты и обсуждение. Для более точного ранжирования больных по степени выраженности эндотоксикоза и последующего анализа влияния его факторов на ультраструктурные свойства эритроцитов были определены и рассчитаны стандартные лабораторные показатели и индексы интоксикации (табл. 1).
|
Таблица 1. Лабораторные показатели эндогенной интоксикации у пациентов с внебольничной пневмонией (M±m) |
Динамика изменений гематологических показателей продемонстрировала линейную направленность, которая ассоциировалась с достоверным увеличением их значений по мере нарастания ЭИ. Так, в 1-й группе значения ЛИИ, ГИИ и ЯИИ превышали значения контрольной группы в 1,6; 4,2 и 2,5 раза соответственно, во 2-й группе — в 3,8; 7,3 и 6,3 раза, а в 3-й группе — уже в 12,9; 28,8 и 10 раз. У всех больных 3-й группы зафиксирована токсическая зернистость в лейкоцитах, что также указывает на развитие тяжелой эндотоксемии. Одновременно выявлено статистически значимое повышение уровня МСМ в плазме крови на 19,4% при ЭИ I степени, на 25,8% — при II и на 58,1% — при III степени. Кроме того, тяжелая эндотоксемия характеризовалась значительным (почти в 1,6 раза) повышением в сыворотке крови концентрации креатинина и мочевины.
В ряде работ установлено прогностическое значение уровня цитокинов в развитии осложнений и исходов ВП [6]. Представлены доказательства того, что дисбаланс в системе цитокинов при остром воспалении провоцирует каскад метаболических нарушений, связанных с гиперпродукцией активных метаболитов кислорода, пероксинитрита, продуктов протеолиза. Это в значительной мере определяет тяжесть патологического процесса. Полученные в наших предыдущих исследованиях [7] результаты показали, что наиболее информативными параметрами цитокинового статуса для характеристики ЭИ при ВП являются IL-10 и TNF-α. Результаты настоящей работы демонстрируют значительное (почти в 20 раз по отношению к контролю) увеличение концентрации этих цитокинов при тяжелой ЭИ, что позволяет рассматривать их в качестве иммунологических маркеров данного синдрома.
Таким образом, комплексная оценка тяжести ЭИ существенно дополняет клиническую характеристику больных ВП и уточняет представления о выраженности метаболических нарушений и функциональном состоянии систем естественной биологической детоксикации.
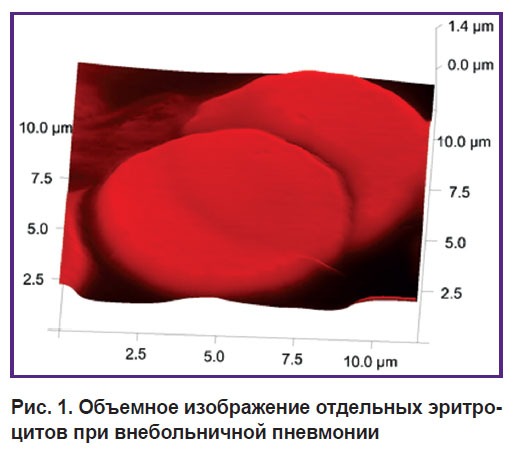
На следующем этапе была исследована наноструктура мембран эритроцитов у больных ВП с 3D-визуализацией отдельных клеток (рис. 1).
|
Рис. 1. Объемное изображение отдельных эритроцитов при внебольничной пневмонии |
Цветовая шкала дает возможность оценить профиль клетки и представить его в графическом виде. Диаметр эритроцита на данном изображении — 6816 нм, высота бортика — 530 нм, прогиб структуры дискоцита — 138 нм, ордината подъема края — 51,3 нм. Устанавливая курсор в любом интересующем исследователя направлении, можно с точностью до 0,1 нм определять любые необходимые размеры клетки.
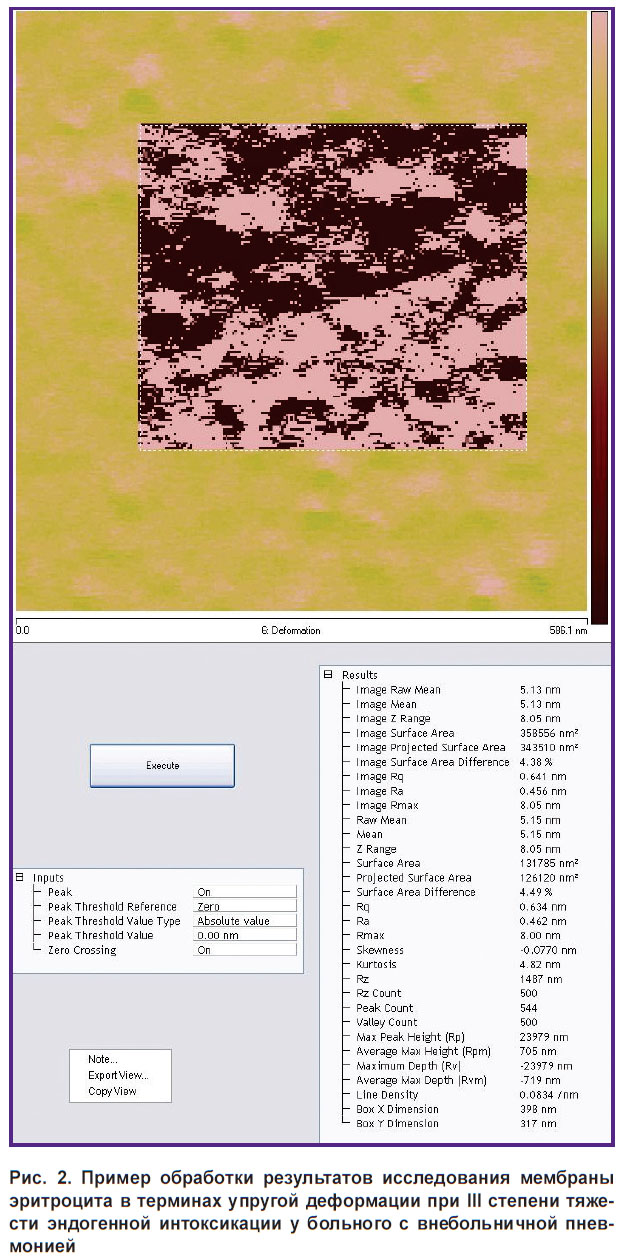
Одновременно с наноанатомическими параметрами эритроцитов были изучены микромеханические свойства поверхности мембраны клеток: модуль упругости, сила адгезии и упругая деформация (рис. 2).
|
Рис. 2. Пример обработки результатов исследования мембраны эритроцита в терминах упругой деформации при III степени тяжести эндогенной интоксикации у больного с внебольничной пневмонией |
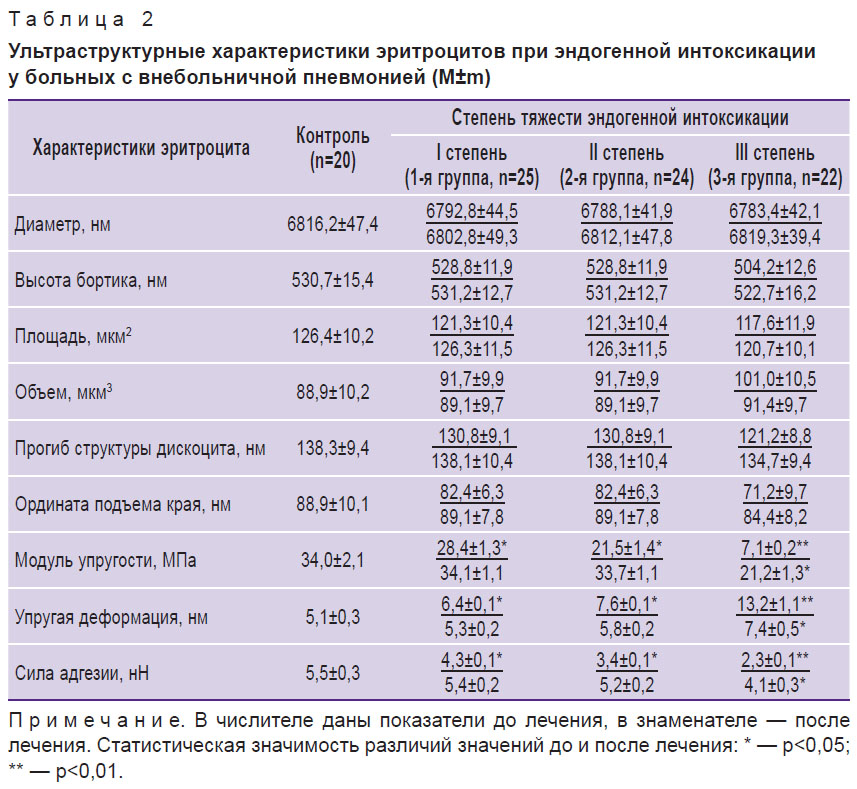
Полученные средние значения АСМ-параметров эритроцитов при различной степени тяжести ЭИ у больных ВП приведены в табл. 2. Установлено, что даже при ЭИ III степени диаметр, площадь, объем и другие параметры эритроцитов, описывающие их геометрический «образ», остаются стабильными у всех обследованных пациентов. Существенно изменялись только показатели, характеризующие упругоэластические свойства этих клеток. Выраженность данных изменений доминировала среди больных ВП с III степенью ЭИ. Так, модуль упругости клеточных мембран эритроцитов и сила их адгезии снижались в 5,2 и 2,4 раза соответственно, а показатель упругой деформации повышался в 2,6 раза. У больных с I и II степенью ЭИ уровень этих показателей также статистически значимо отличался от контрольных значений, но был менее заметным.
|
Таблица 2. Ультраструктурные характеристики эритроцитов при эндогенной интоксикации у больных с внебольничной пневмонией (М±m) |
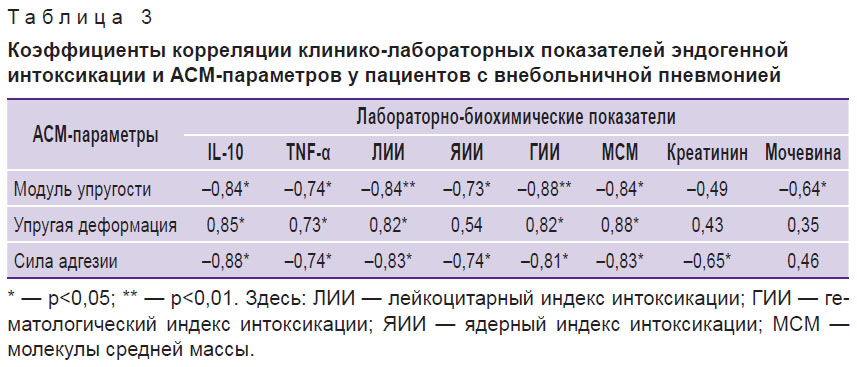
Результаты корреляционного анализа убедительно демонстрируют статистически значимые взаимосвязи между параметрами, характеризующими тяжесть ЭИ, и микромеханическими свойствами мембран (табл. 3). В частности, отмечены положительные корреляции высокой интенсивности между ЛИИ (r=0,82), ГИИ (r=0,84), МСМ (r=0,88) и показателем упругой деформации эритроцитов (во всех случаях p<0,01). Сильные обратные связи обнаружены между ЛИИ (r=–0,84), ГИИ (r=–0,88), МСМ (r=–0,84) и модулем упругости эритроцитарной мембраны, а также силой ее адгезии. При этом IL-10 и TNF-α показали сильную положительную связь с упругой деформацией и отрицательную зависимость от модуля упругости и силы адгезии клеточных мембран эритроцитов.
|
Таблица 3. Коэффициенты корреляции клинико-лабораторных показателей эндогенной интоксикации и АСМ-параметров у пациентов с внебольничной пневмонией |
Вместе с тем анализ этих показателей у больных с различной этиологической структурой ВП не выявил каких-либо количественных различий и направленности изменений корреляционных связей в зависимости от вида возбудителя.
У реконвалесцентов из 1-й и 2-й групп обследованных не удалось обнаружить отклонений микромеханических параметров эритроцитов от контрольных значений, что свидетельствует о транзиторном характере указанных изменений. У большинства пациентов 3-й группы сохранялись их статистически значимые отличия от уровня нормы, которые нивелировались при контрольном исследовании через 2,5–3 мес после выписки из стационара.
Результаты исследований показали, что наиболее чувствительными к проявлениям ЭИ при ВП оказались АСМ-параметры, характеризующие упругоэластические свойства мембран эритроцитов. Данные параметры могут существенно дополнить клинико-лабораторную характеристику эндотоксикоза при воспалительных заболеваниях легких.
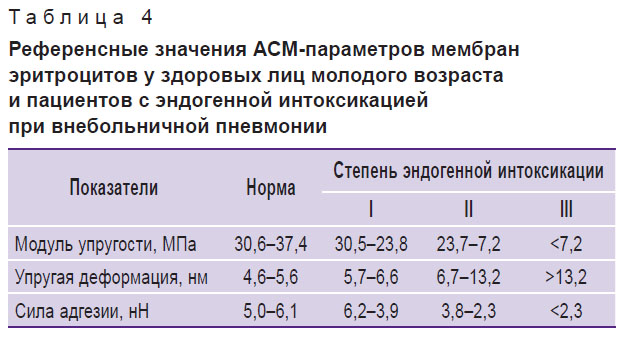
Статистическая обработка фактического материала позволила рассчитать референсные значения микромеханических показателей мембран эритроцитов у здоровых лиц молодого возраста и пациентов с ЭИ различной тяжести (табл. 4).
|
Таблица 4. Референсные значения АСМ-параметров мембран эритроцитов у здоровых лиц молодого возраста и пациентов с эндогенной интоксикацией при внебольничной пневмонии |
Представленные значения могут служить ориентиром при интерпретации АСМ-параметров в аналогичных выборках при дальнейших исследованиях, в том числе для мониторинга эффективности фармакокоррекции эндотоксикоза и полноты реконвалесценции.
Метод АСМ широко используется для оценки состояния различных объектов на ультраструктурном уровне, однако существует лишь небольшое число работ, где он использовался для анализа поверхности клеток при ВП [8, 9]. При этом мембрана эритроцитов в течение долгого времени представлялась исследователям лишь проницаемой для газов крови оболочкой, отделяющей гемоглобин от плазмы. Однако успехи, достигнутые в биоматериаловедении, позволяют считать мембрану эритроцита важнейшим элементом клетки, который одновременно является механической оболочкой с регулируемыми физическими свойствами и центральным элементом, осуществляющим координацию работы клетки в зависимости от физических и химических сигналов, поступающих к ней [4].
В условиях эндотоксикоза при ВП ключевую роль приобретает детоксикационная активность эритроцитов, которая связана с утилизацией эндогенных альдегидов, образующихся в процессе перекисного окисления липидов, в реакциях гликозилирования и при окислении радикалов некоторых свободных аминокислот [2]. Одновременно углеводы, локализованные в гликокаликсе, отвечают за адгезивные свойства красных клеток крови и являются специфическими рецепторами для связывания различных лигандов, вирусов, антител. Выявленное в нашей работе снижение значений модуля упругости и силы адгезии мембраны эритроцитов может указывать на адаптивный характер этой реакции, результатом которой является повышение пластичности клеток в условиях нарушенной микроциркуляции и гипоксемии. В циркуляторном русле эритроциты в силу своей эластичности принимают самую разнообразную конфигурацию, приспосабливаясь к форме сосуда. В связи с этим одним из основных свойств эритроцита следует считать способность к деформации. В норме эритроциты обладают высокой деформируемостью, что определяется упругими свойствами мембраны и низкой вязкостью внутриклеточного содержимого. Повышение у эритроцитов «текучести» липидного бислоя может способствовать росту резервных возможностей к быстрому восстановлению целостности мембраны в случае ее незначительного повреждения в условиях нарушения микроциркуляции на фоне тяжелой ЭИ [10]. По-видимому, это повышает эффективность газотранспортной функции красных клеток крови. Однако в ряде случаев при тяжелом эндотоксикозе у больных с ВП, а также у больных старших возрастных групп с сопутствующими заболеваниями продолжающееся снижение упругости мембран эритроцитов может служить своеобразным триггером, который запускает каскад необратимых ультраструктурных изменений клеток крови с повреждением их цитоскелета и нарушением газотранспортной функции [3]. Таким образом, у лиц молодого возраста транзиторные изменения микромеханических свойств мембран эритроцитов указывают на уникальную пластичность этих клеток и их высокий адаптивный потенциал, что позволяет использовать данные параметры в качестве дополнительных маркеров тяжести эндотоксикоза.
Заключение. Проведенные исследования доказывают информативность оценки микромеханических параметров мембран эритроцитов методом атомно-силовой микроскопии для характеристики степени тяжести эндогенной интоксикации при внебольничной пневмонии. Полученные данные дополняют представления о патофизиологических последствиях эндогенной интоксикации, их влиянии на ультраструктуру клеток и адаптивный характер изменений микромеханических свойств мембран эритроцитов.
Финансирование исследования. Исследование не финансировалось какими-либо источниками.
Конфликт интересов, связанный с данным исследованием, у авторов отсутствует.
Литература
- Musher D.M., Thorner A.R. Community-acquired pneumonia. N Engl J Med 2014; 371(17): 1619–1628, https://doi.org/10.1056/nejmra1312885.
- Бородин Е.А., Егоршина Е.В., Самсонов В.П. Биохимия эндотоксикоза. Механизмы развития и оценка степени тяжести при воспалительных заболеваниях легких. Благовещенск: АГМА; 2003; 129 c.
- Moeendarbary E., Harris A.R. Cell mechanics: principles, practices, and prospects. Wiley Interdiscip Rev Syst Biol Med 2014; 6(5): 371–388, https://doi.org/10.1002/wsbm.1275.
- Забиняков Н.А., Довгий П.Г., Полторацкий А.Н., Азаров К.С. Структурно-функциональные свойства эритроцитов и нейтрофилов людей с острой внебольничной пневмонией среднего, пожилого и старческого возраста. Геронтология 2014; 2(1): 23–33.
- Чучалин А.Г., Синопальников А.И., Козлов Р.С., Авдеев С.Н., Тюрин И.Е., Руднов В.А., Рачина С.А., Фесенко О.В. Клинические рекомендации по диагностике, лечению и профилактике тяжелой внебольничной пневмонии у взрослых. Пульмонология 2014; 4: 13–48.
- Кондрашова Н.М., Плехова Н.Г., Сомова Л.М., Костюшко А.В., Гельцер Б.И. Оптимизация оценки показателей функциональной активности клеток врожденного иммунитета при воспалительных заболеваниях легких. Тихоокеанский медицинский журнал 2012; 1: 83–86.
- Гельцер Б.И., Ким А.П., Котельников В.Н., Макаров А.Б. Особенности иммунного ответа у больных внебольничной пневмонией с различной степенью тяжести эндогенной интоксикации. Цитокины и воспаление 2015; 14(3): 35–41.
- Proshchaev K.I., Zabinyakov N.A., Azarov K.S., Dovgii P.G. Studies of the structure and functions of blood cells in senile patients with pneumonia on the biological model of hypoxia by scanning probe microscopy. Bull Exper Biol 2014; 158(2): 256–259, https://doi.org/10.1007/s10517-014-2735-2.
- Lamzin I.M., Khayrullin R.M. The quality assessment of stored red blood cells probed using atomic-force microscopy. Anat Res Int 2014; 2014: 869683, https://doi.org/10.1155/2014/869683.
- Иванов К.П. Современные медицинские проблемы микроциркуляции и гипоксического синдрома. Вестник РАМН 2014; 69(1–2): 57–63, https://doi.org/10.15690/vramn.v69.i1-2.943.










