Роль современных методов обследования в оценке влияния курения на течение бронхиальной астмы и развитие коморбидной метаболической патологии
Цель исследования — показать возможности использования современных методов обследования в оценке влияния курения на течение бронхиальной астмы (БА) и развитие коморбидной метаболической патологии.
Материалы и методы. Обследован 201 пациент с неконтролируемой БА. 1-я группу составили 152 некурящих пациента, 2-ю — 18 курильщиков, 3-ю — 31 «злостный» курильщик. Наряду с общеклиническими методами исследования проводилось исследование функции внешнего дыхания с оценкой форсированной жизненной емкости легких, объема форсированного выдоха за 1 с, индекса Тиффно. Для диагностики ожирения применяли биоэлектрический импедансный анализ, определяли индекс массы тела, объем талии. При изучении углеводного обмена оценивали уровень гликированного гемоглобина (HbA1c), а также иммунореактивного инсулина и С-пептида.
Результаты. Большую роль в диагностике коморбидной эндокринной патологии при БА играют определение объема талии, метод биоэлектрического импедансного анализа, исследование уровней HbA1с, иммунореактивного инсулина и С-пептида. Тяжесть таких больных усугубляют висцеральное ожирение и сахарный диабет, существенным фактором риска развития которых является курение сигарет. Длительно и интенсивно курящие пациенты с БА характеризуются присоединением хронической обструктивной болезни легких и развитием перекрестного синдрома с особо тяжелым течением.
В настоящее время бронхиальная астма (БА) является одним из наиболее актуальных заболеваний пульмонологического профиля. На территории РФ распространенность ее колеблется от 1 до 12% [1, 2]. В последние годы появилось много работ о частом сочетанном течении БА с гипертонической болезнью, ишемической болезнью сердца, сахарным диабетом (СД), ожирением и метаболическим синдромом [1–13]. Установлено, что БА у больных с ожирением развивается значительно чаще, чем в общей популяции [1–4].Различные исследования подтверждают дозозависимую ассоциацию между данными патологиями [1]. При коморбидности БА с метаболическим синдромом характерно более тяжелое клиническое течение ее с частыми обострениями и госпитализациями, выявляются достоверно более низкие спирометрические показатели и даже на фоне стационарного лечения нередко не удается достичь контроля над состоянием пациента [1–13].
Ведущим универсальным фактором риска бронхолегочной, сердечно-сосудистой и метаболической патологии принято считать курение сигарет. Данная вредная привычка ассоциируется с прогрессирующим снижением легочной функции, уменьшением ответа на терапию глюкокортикоидами [2, 11]. Увеличение дозы базисных препаратов, избыточное потребление β2-агонистов короткого действия, прогрессирующая артериальная гипоксемия в сочетании с множеством других факторов запускают порочные круги патогенеза коморбидных кардиоваскулярных и метаболических заболеваний, которые в свою очередь еще усугубляют течение БА. Особую актуальность имеет синдром перекреста БА и хронической обструктивной болезни легких (ХОБЛ), активно обсуждающийся в современной литературе [14–16]. Следует учитывать, что у многих курящих пациентов с БА резко ухудшается качество жизни за счет более частых обострений, быстрее снижается легочная функция и наступает смертельный исход. Однако все тонкости влияния курения на бронхолегочную и метаболическую патологию бывает сложно отследить. В данной работе нами предпринята попытка оценить влияние курения сигарет при БА, в том числе и при перекрестном синдроме, на развитие коморбидных нарушений и заболеваний с помощью дополнительных современных методов.
Цель исследования — показать возможности использования современных методов обследования больных в оценке влияния курения на течение бронхиальной астмы и развитие коморбидной метаболической патологии.
Материалы и методы. Обследован 201 пациент с неконтролируемой БА, проходивший стационарное лечение в специализированном пульмонологическом отделении Городской клинической больницы №10 Нижнего Новгорода. Верификация диагноза проводилась согласно критериям GINA [2, 14]. Все больные были разделены на три группы: 1-ю группу составили 152 некурящих пациента, 2-ю — 18 курильщиков (в том числе бывших), 3-ю — 31 «злостный» курильщик. Именно у пациентов последней группы и был представлен перекрестный синдром БА + ХОБЛ, а первые две группы были обследованы с целью сравнения. Исследование проведено в соответствии с Хельсинкской декларацией, принятой в июне 1964 г. (Хельсинки, Финляндия) и пересмотренной в октябре 2000 г. (Эдинбург, Шотландия), и одобрено Этическим комитетом НижГМА. От каждого пациента получено информированное согласие.
Наряду с общеклиническими методами исследования проводилось изучение функции внешнего дыхания с оценкой форсированной жизненной емкости легких (ФЖЕЛ), объема форсированного выдоха за 1 с (ОФВ1) и индекса Тиффно на спирометре ShillerSPIROVITSP-1 (Shiller, Швейцария). В настоящее время верификация висцерального ожирения базируется на применении компьютерной или магнитно-резонансной томографии [17]. Однако это — весьма дорогостоящие методы, поэтому для определения процентного содержания жировой ткани в организме, а также висцерального жира мы использовали биоэлектрический импедансный анализ с помощью BodyCompositionMonitorBF 508 (OMRON, Япония), данных о применении которого в подобных исследованиях в доступной литературе нам найти не удалось. Кроме того, всем пациентам проводили подсчет индекса массы тела, измеряли объем талии.
При изучении углеводного обмена наряду с показателями гликемии крови определяли уровень гликированного гемоглобина (HbA1c) с помощью автоматического анализатора D-10 (BIO-RAD, США), протестированного и сертифицированного в соответствии с NGSP (Национальная программа стандартизации гликозилированного гемоглобина) и являющегося, по данным некоторых авторов, наиболее точным прибором, используемым на территории РФ [18], а также иммунореактивного инсулина (ИРИ) и С-пептида на электрохемилюминесцентном анализаторе для иммунологических исследований Elecsys 2010 (ROCHE, Швейцария).
Статистическую обработкуосуществляли с помощью программ Minitab 16 и Statistica 7.0. В начале анализа данных проводили определение правильности распределения признака с помощью теста Андерсона–Дарлинга. Протяженные переменные были представлены в виде среднего арифметического (M) и стандартного отклонения (SD) или в виде медианы (Me) и квартилей (Q1; Q3). При сравнении двух несвязанных групп использовали t-тест Стьюдента и критерий Манна–Уитни. Для сопоставления частот применяли критерий χ2. С целью установления взаимосвязей между явлениями использовали линейную корреляцию Пирсона (r), ранговую корреляцию Спирмена (RS), а также критерий Gamma. При недостоверном значении «р» в таблицах применялось сокращение Н/д.
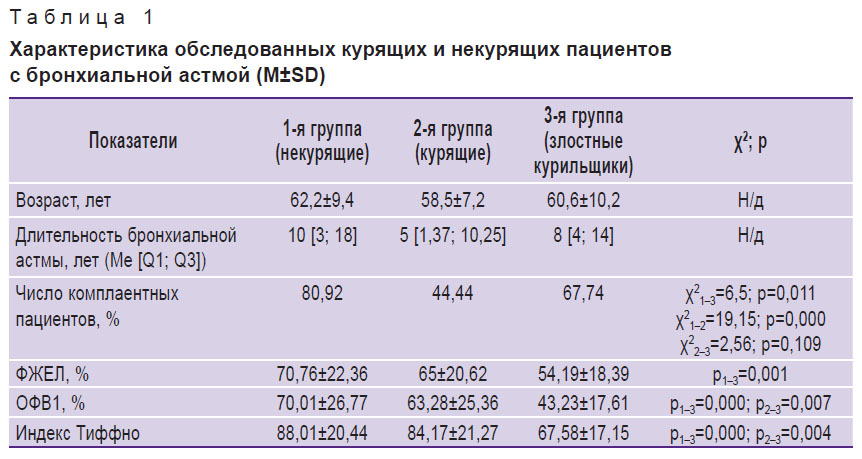
Результаты и обсуждение. У большинства обследованных нами пациентов наблюдались существенные смешанные нарушения функции внешнего дыхания (табл. 1). При этом интенсивное курение способствовало достоверному снижению всех вентиляционных констант. Наиболее комплаентными оказались некурящие больные с БА (получали регулярную поддерживающую терапию ингаляционными глюкокортикоидами). Во 2-й группе правильное лечение установлено только в 44% случаев. Длительное и интенсивное курение приводило к развитию тяжелых смешанных нарушений легочной вентиляции, побуждающих слушать советы врачей и принимать поддерживающую терапию, при этом распространенность комплаентных пациентов достигла в 3-й группе 68%, однако она все равно оказалась статистически значимо более низкой, чем у некурящих астматиков (χ21–3=6,5; р=0,011).
|
Таблица 1. Характеристика обследованных курящих и некурящих пациентов с бронхиальной астмой (M±SD) |
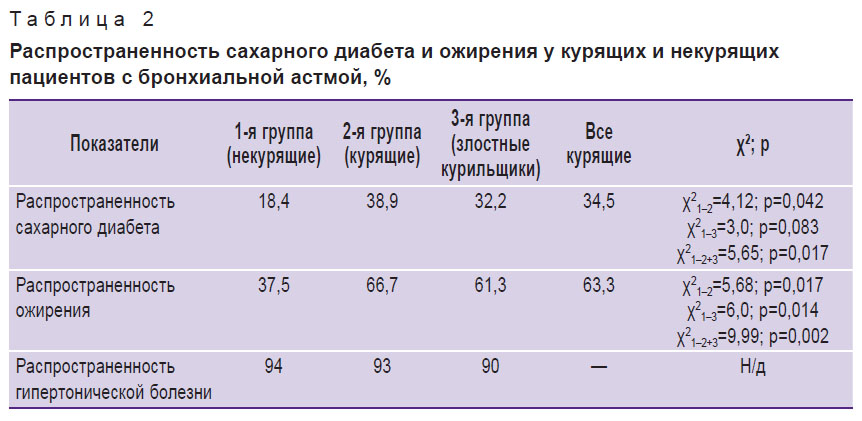
На следующем этапе были детально изучены метаболические нарушения у курящих и некурящих больных БА. Распространенность СД у всех пациентов оказалась выше, чем в популяции (табл. 2). При этом у курящих больных она достигала 34,5% (2-я группа + 3-я группа). Благодаря проведению анализов на постпрандиальную гликемию и HbA1c диагноз СД впервые установлен у 4,5% пациентов 1-й группы.
|
Таблица 2. Распространенность сахарного диабета и ожирения у курящих и некурящих пациентов с бронхиальной астмой, % |
Перекрестный синдром БА + ХОБЛ (3-я группа) также статистически значимо чаще сопровождался коморбидным ожирением (определялось по индексу массы тела), достигшим в 3-й группе распространенности 61,3%. Некоторое статистически не значимое снижение частоты ожирения в 3-й группе по сравнению со 2-й, по нашему мнению, обусловлено присоединением ХОБЛ, которая имеет существенные системные проявления. Абсолютное большинство обследованных пациентов имели сопутствующую гипертоническую болезнь. Различия между группами оказались статистически не значимыми.
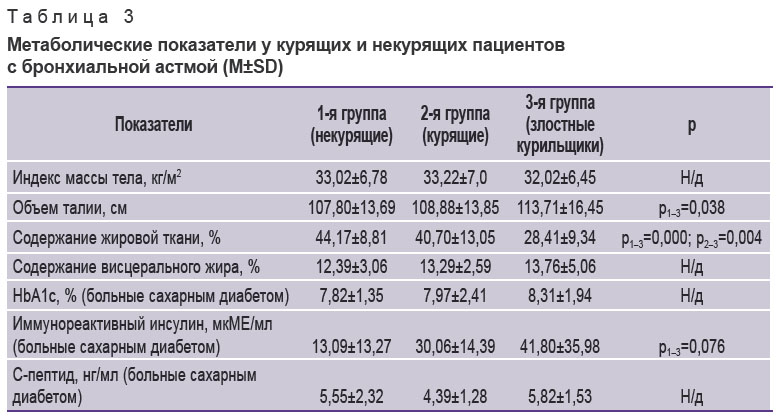
При анализе параметров питательного статуса во всех трех группах больных средние значения индекса массы тела соответствовали категории ожирения I степени (табл. 3). Интересную тенденцию демонстрировал показатель объема талии, который в 3-й группе (перекрестный синдром) достигал значения 113,71±16,45 см и оказался статистически значимо более высоким, чем в 1-й (р1–3=0,038). При этом отмечено статистически значимое снижение процентного содержания жировой ткани на фоне интенсивного курения. Таким образом, ожирение было типично для большинства больных БА. Длительно и интенсивно курящие пациенты характеризовались снижением общей массы жира, который, однако, перераспределялся в абдоминально-висцеральную область, что подтверждает наличие у них метаболического синдрома. Применение метода биоэлектрического импедансного анализа позволило более точно описать изменения питательного статуса при перекрестном синдроме.
|
Таблица 3. Метаболические показатели у курящих и некурящих пациентов с бронхиальной астмой (M±SD) |
Изучение углеводного обмена показало, что показатели гликемии (натощак и постпрандиальной) между группами существенно не различались, поэтому мы решили здесь их не приводить. Значения HbA1c и ИРИ у пациентов с СД несколько нарастали от 1-й группы к 3-й, однако разница между группами достигала лишь уровня статистической тенденции и только в случае ИРИ (р1–3=0,076). Следует отметить, что большинство обследованных больных имели выраженную гиперинсулинемию.
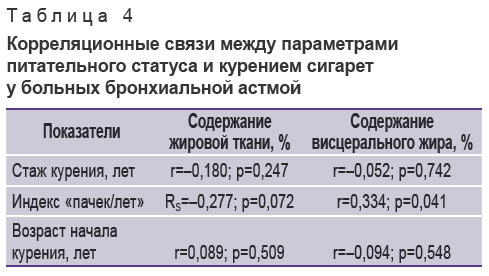
С целью более детального анализа метаболического профиля при БА применяли и другие статистические методики. Так, корреляционный анализ выявил статистически значимую положительную связь между индексом «пачек/лет» и объемом висцерального жира (r=0,334; p=0,041), что еще раз подтверждает влияние курения на развитие метаболического синдрома (табл. 4). Установлена отчетливая статистическая тенденция к наличию отрицательной корреляции между индексом «пачек/лет» и процентным содержанием в организме жировой ткани (RS=–0,277; p=0,072). Возраст начала и стаж курения с параметрами питательного статуса не коррелировали. При анализе углеводного обмена установлены несколько другие тенденции. Так, у курящих пациентов 2-й и 3-й групп без сопутствующего СД выявлена статистически значимая отрицательная связь возраста начала курения с HbA1c (RS=–0,381; p=0,049).
|
Таблица 4. Корреляционные связи между параметрами питательного статуса и курением сигарет у больных бронхиальной астмой |
Установлено, что степень артериальной гипертензии увеличивалась на фоне повышения индекса «пачек/лет» (табл. 5). Выявлена отрицательная корреляция между возрастом начала курения и уровнем артериального давления.

|
Таблица 5. Корреляционные связи между показателями интенсивности курения сигарет и степенью артериальной гипертензии |
Таким образом, ожирение, метаболический синдром, СД и гипертоническая болезнь являются частыми спутниками БА у курящих пациентов, что приводит к увеличению общей тяжести заболевания и требует пересмотра программ лечения. Длительно и интенсивно курящие пациенты с астмой характеризуются присоединением ХОБЛ и развитием перекрестного синдрома, отличающегося особо тяжелым течением. Наряду с бронхолегочными явлениями общую тяжесть заболевания у таких пациентов усугубляют частые коморбидные состояния, к которым следует отнести абдоминально-висцеральное ожирение, СД и гипертоническую болезнь. Выявление тонких механизмов формирования сочетанной патологии невозможно без применения достаточного арсенала современных статистических методик.
Заключение. Большую роль в диагностике коморбидной эндокринной патологии при бронхиальной астме играют некоторые современные, легко доступные в клинической практике методы обследования. Для диагностики висцерального ожирения целесообразно определение объема талии, применение метода биоэлектрического импедансного анализа. С целью оценки состояния углеводного обмена и его регуляции, а также диагностики гиперинсулинемии и сахарного диабета недостаточно измерения показателей гликемии крови — в данном случае будет полезным изучение уровней HbA1с, иммунореактивного инсулина и С-пептида.
Финансирование исследования. Исследование не финансировалось какими-либо источниками.
Конфликт интересов. Авторы подтверждают отсутствие конфликта интересов.
Литература
- Астафьева Н.Г., Гамова И.В., Удовиченко Е.Н., Перфилова И.А. Ожирение и бронхиальная астма (часть 1). Лечащий врач 2014; 4: 8.
- Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких (пересмотр 2011 г.). Под ред. Белевского А.С. М: Российское респираторное общество; 2012.
- Будневский А.В., Чернов А.В., Ермолова А.В., Трибунцева Л.В. Бронхиальная астма в сочетании с метаболическим синдромом: возможности достижения контроля над заболеванием. Пульмонология 2014; 5: 39–45.
- Астафьева Н.Г., Гамова И.В., Удовиченко Е.Н., Перфилова И.А. Ожирение и бронхиальная астма (часть 2). Лечащий врач 2014; 5: 100.
- Минеев В.Н., Лалаева Т.М., Васильева Т.С., Трофимов В.И. Фенотип бронхиальной астмы с ожирением. Пульмонология 2012; 2: 102–107.
- Сысоева М.С., Соловьева А.В., Никифоров А.А., Ракита Д.Р. Влияние наличия метаболического синдрома на клиническое течение бронхиальной астмы. Российский медико-биологический вестник им. академика И.П. Павлова 2011; 4: 93–98.
- Урясьев О.М., Панфилов Ю.А. Бронхиальная астма и метаболический синдром: некоторые аспекты сочетанного течения. Международный эндокринологический журнал 2008; 3(15): 15–25.
- Ермолова А.В., Будневский А.В., Дробышева Е.С. Бронхиальная астма и метаболический синдром: клинико-патогенетические взаимосвязи. Молодой ученый 2014; 6: 291–294.
- Beyther D.A., Sutherland E.R. Over weight, obesity and incident asthma: a meta-analysis of prospective epidemiologic studies. Am J Resp Crit Care Med 2007; 175: 661–667, https://doi.org/10.1164/rccm.200611-1717OC.
- Yeh K.H., Skowronski M.E., Coreno A.J., Seitz R.E., Villalba K.D., Dickey-White H., McFadden E.R. Impact of obesity on the severity and therapeutic responsiveness of acute episodes of asthma. J Asthma 2011; 8(6): 546–552, https://doi.org/10.3109/02770903.2011.581733.
- Цибулькина В.Н., Цибулькин Н.А. Бронхиальная астма и ожирение: совпадение или закономерность? Практическая медицина 2011; 6(54): 36–41.
- Shore S.A. Obesity and asthma: possible mechanisms. J Allergy Clin Immunol 2008; 121(5): 1087–1093, https://doi.org/10.1016/j.jaci.2008.03.004.
- Saint-Pierre P., Bourdin A., Chanez P., Daures J.-P., Godard P. Are overweight asthmatics more difficult to control? Allergy 2006; 61(1): 79–84, https://doi.org/10.1111/j.1398-9995.2005.00953.x.
- Глобальная стратегия лечения и профилактики бронхиальной астмы (пересмотр 2014 г.). Под ред. Белевского А.С. М: Российское респираторное общество; 2015.
- Белевский А.С. Синдром перекреста бронхиальной астмы и хронической обструктивной болезни легких (по материалам совместного документа рабочих групп экспертов GINA и GOLD). Практическая пульмонология 2014; 2: 12–19.
- Трофимов В., Миронова Ж., Белаш В. Overlap-cиндpoм: перекрестный синдром ХОБЛ–астма. Врач 2013; 2: 20–21.
- Проект рекомендаций экспертов Российского кардиологического общества по диагностике и лечению метаболического синдрома (3-й пересмотр). М; 2013; 103 с.
- Лихоносова А.П., Лихоносов Н.П., Кузнецова О.Г. Анализ методов определения уровня гликозилированного гемоглобина в лечебно-профилактических учреждениях города Санкт-Петербурга. Международный эндокринологический журнал 2010; 6(30): 23–27.










