Оптимизация хирургического лечения объемных образований головки поджелудочной железы
Цель исследования — улучшить результаты панкреатодуоденальной резекции путем применения алгоритма выбора панкреатодигестивного анастомоза (ПДА) и двух новых способов формирования панкреатоеюнального соустья.
Материалы и методы. При разработке алгоритма выбора ПДА учитывали основные факторы риска развития осложнений: консистенцию ткани железы, диаметр панкреатического протока и соответствие размеров плоскости среза железы и тощей кишки. На основании сочетания этих факторов выделили пять степеней готовности культи поджелудочной железы к анастомозированию и определили оптимальные для каждой степени ПДА. В рамках указанного алгоритма применили два оригинальных способа панкреатоеюнального анастомоза: инвагинационный конце-концевой со сквозными П-образными швами и конце-петлевой с инвагинацией культи поджелудочной железы в тонкокишечный резервуар. У 48 человек основной группы применили пять видов ПДА, у 58 больных группы сравнения в 52 случаях — конце-концевые панкреатоеюнальные анастомозы.
Результаты. Обе группы сопоставимы по основным факторам риска развития осложнений: состоянию ткани поджелудочной железы и диаметру панкреатического протока. Частота несостоятельности ПДА составила 4 случая в основной группе и 10 — в группе сравнения. В основной группе случаев острого панкреатита и летальных исходов, обусловленных техническими особенностями формирования ПДА, не выявлено. В группе сравнения отмечено 6 случаев острого панкреатита, летальность составила 3 случая. Оригинальный конце-концевой панкреатоеюнальный анастомоз согласно алгоритму применен у 10 больных основной группы, конце-петлевой — у 14. Разработанный алгоритм дает возможность выбрать оптимальный способ формирования соустья в зависимости от морфометрических особенностей анастомозируемых культи поджелудочной железы и тощей кишки.
Заключение. Индивидуализированный подход к выбору ПДА и примененные в рамках алгоритма оригинальные способы формирования соустья позволяют уменьшить число тяжелых осложнений и летальность после панкреатодуоденальной резекции.
Единственным методом радикального лечения рака поджелудочной железы (ПЖ) является панкреатодуоденальная резекция. За последние десятилетия удалось снизить летальность после этой операции до 0–2% [1, 2]. В то же время частота осложнений не имеет тенденции к снижению и остается на уровне 27–54% [2–4]. Наиболее частым осложнением после панкреатодуоденальной резекции является несостоятельность панкреатодигестивных анастомозов (ПДА), которая развивается в 9–14% случаев [3, 5]. В свою очередь несостоятельность ПДА является основной причиной жизнеугрожающих осложнений и летальных исходов [6–10]. Для снижения частоты несостоятельности анастомозов и, соответственно, улучшения результатов панкреатодуоденальной резекции предложено много способов ПДА, часто они позиционируются как универсальные. Однако возможность применения одного способа ПДА во всех случаях сомнительна по причине вариабельности состояния культи ПЖ и анатомических особенностей анастомозируемых тощей кишки или желудка [11, 12]. Поэтому актуальным в плане уменьшения несостоятельности ПДА является индивидуализированный подход к формированию соустья.
Цель исследования — улучшить результаты панкреатодуоденальной резекции путем применения алгоритма выбора панкреатодигестивных анастомозов и разработки новых способов формирования этого вида соустья.
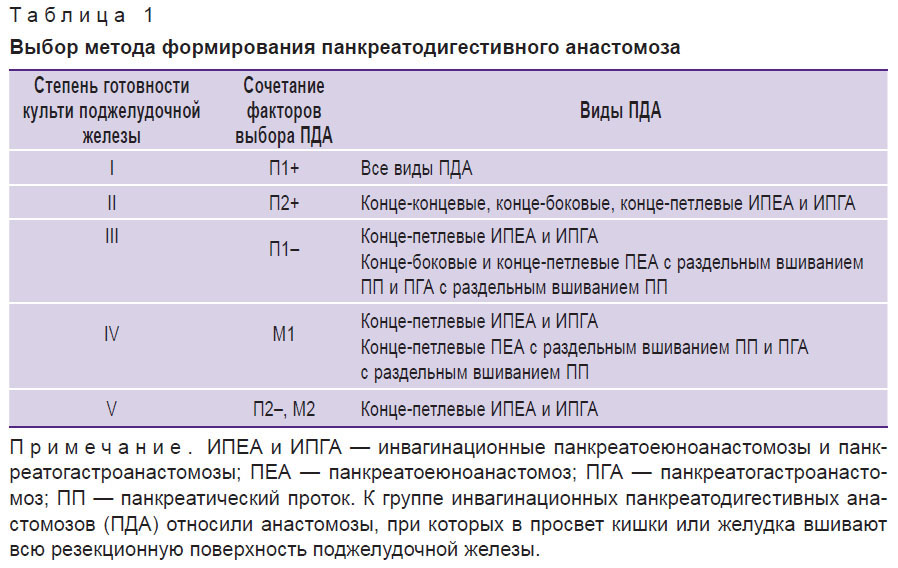
Материалы и методы. Алгоритм выбора ПДА основан на трех факторах риска развития специфических для панкреатоеюнального соустья осложнений: состоянии ткани культи ПЖ, диаметре панкреатического протока (ПП) и соответствии размеров резекционной плоскости культи ПЖ и анастомозируемой петли тощей кишки [13]. Ткань железы определяли как плотную (П) или мягкую (М) по критерию «прорезывание ткани ПЖ лигатурой». Вариантом П считали случаи, когда при затягивании узла нить не прорезала ткань ПЖ, вариант М — если нить прорезала ткань ПЖ. Возможный диаметр ПП разделили на два варианта: при диаметре протока 3 мм и более ставили цифру 1; при диаметре менее 3 мм — цифру 2. Стентирование ПП считали возможным только при диаметре протока 3 мм и более. При диаметре менее 3 мм проток стентировали на период проведения гемостаза культи ПЖ и выполнения ПДА. При плотной железе и размерах просвета тощей кишки больше диаметра резекционной плоскости культи ПЖ к варианту ткани железы П и диаметру протока добавляем знак «+». Если размеры равны или просвет кишки меньше, добавляем знак «–». На основании сочетания указанных факторов выделили пять степеней готовности культи ПЖ к анастомозированию и оптимальные для каждой степени ПДА (табл. 1). Алгоритм выбора ПДА применяется с 2007 г.
|
Таблица 1. Выбор метода формирования панкреатодигестивного анастомоза |
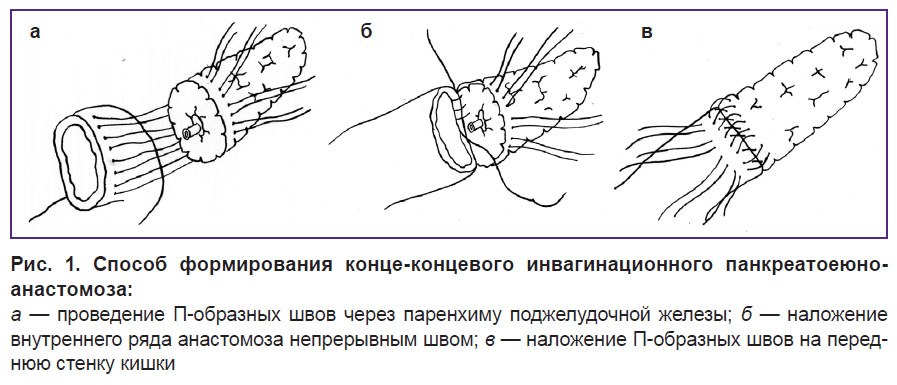
В рамках алгоритма использовали два оригинальных способа панкреатоеюноанастомоза (ПЕА): конце-концевой и конце-петлевой. Конце-концевой инвагинационный панкреатоеюноанастомоз (ИПЕА) (патент РФ на изобретение 2432126 от 11 января 2010 г.) выполняют следующим образом [14]. Стентируют катетером вирсунгов проток. На заднюю стенку тощей кишки параллельно просвету и на 1,5–2 см от ее края накладывают четыре-пять П-образных серозно-мышечных швов монофиламентной нитью. Обе нити каждого шва проводят через паренхиму ПЖ (рис. 1, а). Накладывают внутренний непрерывный шов между просветом кишки и резекционной поверхностью ПЖ (рис. 1, б). Нитями каждого ранее наложенного П-образного шва накладывают серозно-мышечные швы на переднюю поверхность тощей кишки перпендикулярно на расстоянии 1 см от края непрерывного шва (рис. 1, в). Культю ПЖ инвагинируют в просвет тощей кишки и завязывают швы. Боковые стенки анастомоза укрепляют узловым швом.
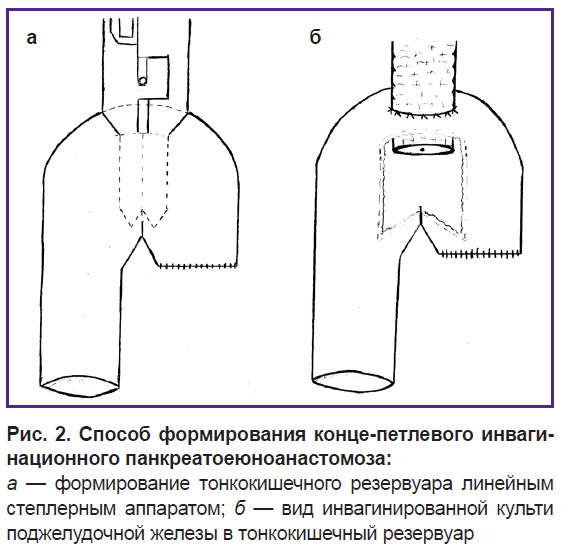
Второй способ — конце-петлевой резервуарный ИПЕА (патент РФ на изобретение 2552670 от 22 апреля 2014 г.) — применим при всех степенях готовности культи ПЖ к анастомозированию. Для формирования этого способа анастомоза свободный конец тощей кишки складывают в виде двустволки длиной 6–8 см. На противобрыжеечном крае двустволки выполняют продольный разрез примерно 3 см. Через созданное отверстие в оба колена кишечной двустволки вводят бранши линейного степлерного аппарата (рис. 2, а) и формируют тонкокишечный резервуар. При необходимости на кишечном резервуаре удлиняют разрез для его соответствия диаметру культи ПЖ. На расстоянии 1,0–1,5 см дистально от края резекции железы накладывают первый ряд узловых швов между ПЖ и задней стенкой кишечного резервуара. Выполняют внутренний непрерывный шов между просветом кишки и периметром среза ПЖ. Накладывают второй ряд узловых швов между железой и передней стенкой кишечного резервуара на расстоянии 1,0–1,5 см от внутреннего ряда швов (рис. 2, б). После выполнения продольного разреза кишки может образоваться избыток ее стенки в области скрепочных швов, который эвагинирует из резервуара и затрудняет формирование передней губы анастомоза. В этом случае достаточно иссечь его для лучшей адаптации железы и стенки кишки.
С 2004 по 2014 г. в хирургических отделениях Коми республиканской больницы и Коми республиканского онкологического диспансера (Сыктывкар) выполнено 106 панкреатодуоденальных резекций. Пациенты были разделены на две группы. В основную группу вошли 48 пациентов (22 женщины и 26 мужчин), которым ПДА формировали согласно предложенному алгоритму. Группу сравнения составили 58 пациентов (24 женщины и 34 мужчины). Средний возраст больных основной группы составил 54,5±9,2 года (от 35 до 80 лет) лет, группы сравнения — 55,1±8,7 года (от 30 до 76 лет).
Исследование проведено в соответствии с Хельсинкской декларацией, принятой в июне 1964 г. (Хельсинки, Финляндия) и пересмотренной в октябре 2000 г. (Эдинбург, Шотландия), и одобрено Этическим комитетом Коми республиканской больницы. От каждого пациента получено информированное согласие.
Оригинальный конце-концевой ИПЕА применяли в обеих группах с 2005 г. В рамках алгоритма его выполняли при I степени готовности культи ПЖ к анастомозированию. Оригинальный конце-петлевой ИПЕА применяли с 2012 г. и только в основной группе. С целью профилактики послеоперационного панкреатита вводили октреотид в дозе 0,3 мг/сутки в течение 3–5 дней.
Проведен сравнительный анализ морфометрических параметров культи ПЖ и осложнений, непосредственно связанных с методикой формирования ПДА. Такими осложнениями считали деструктивный панкреатит (ДП) и/или несостоятельность соустья. Послеоперационный ДП диагностировали при проведении КТ или МРТ брюшной полости и/или последующей релапаротомии. Несостоятельность ПДА определяли в соответствии с критериями, предложенными S.M. Strasberg [15]. Согласно этим критериям несостоятельностью ПДА считают количество отделяемого по дренажу более 50 мл в сутки и повышение уровня активности амилазы в полученной жидкости более чем в 3 раза по сравнению с верхней границей нормы уровня амилазы в сыворотке крови с десятого дня после операции.
Для анализа статистической значимости различий значений между группами и признаков в группах с учетом числа объектов по каждому признаку использовали непараметрические методы: тесты Манна–Уитни и хи-квадрат (χ2) с поправкой Йетса, точный критерий Фишера. Статистически значимыми считали различия при р<0,05.
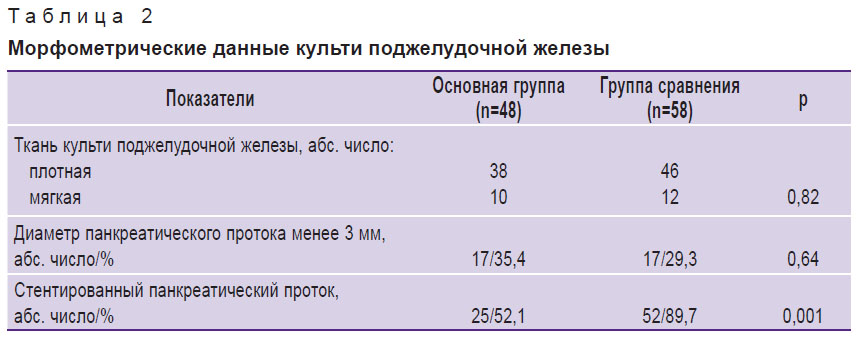
Результаты. Морфометрические данные культи ПЖ в группах пациентов приведены в табл. 2.
|
Таблица 2. Морфометрические данные культи поджелудочной железы |
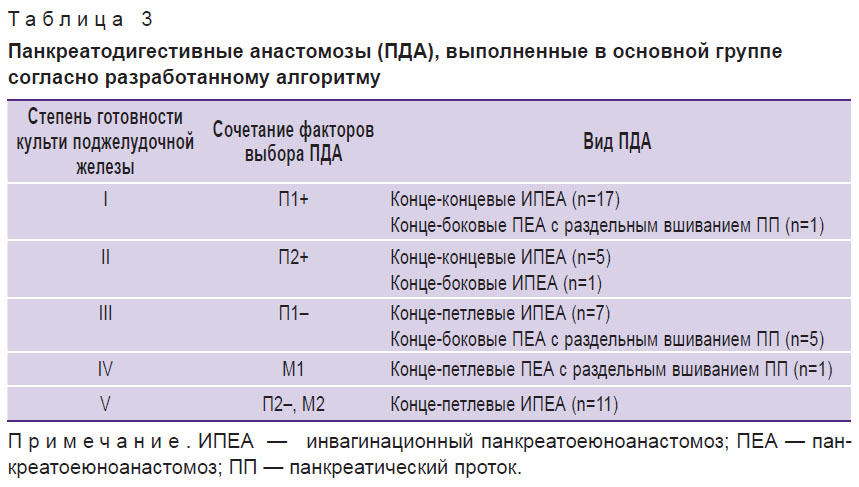
В табл. 3 указаны степени готовности культи ПЖ к анастомозированию согласно предложенной классификации и примененные виды ПДА в основной группе.
|
Таблица 3. Панкреатодигестивные анастомозы (ПДА), выполненные в основной группесогласно разработанному алгоритму |
В основной группе по оригинальной методике выполнено 14 конце-петлевых и 10 конце-концевых ИПЕА. В группе сравнения при формировании ПДА применяли следующие виды соустий: конце-концевые ИПЕА в 52 случаях (89,7%), из них по оригинальной методике — в 14 (26,9%); конце-боковые ПЕА с раздельным вшиванием ПП — в 2; инвагинационный панкреатогастроанастомоз (ИПГА) — в 4 случаях.
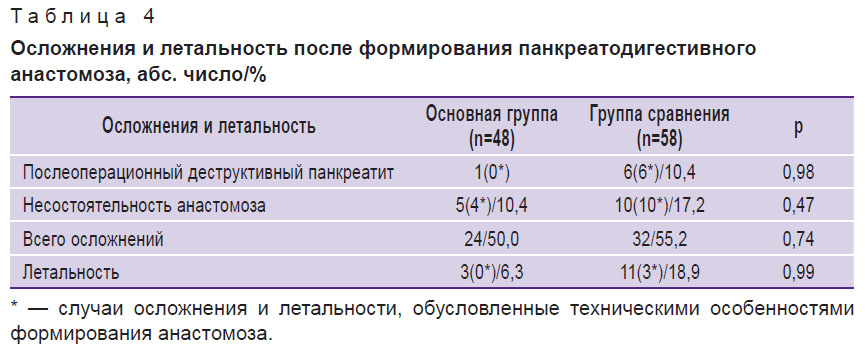
Частота осложнений непосредственно после операции и летальность приведены в табл. 4.
|
Таблица 4. Осложнения и летальность после формирования панкреатодигестивного анастомоза, абс. число/% |
В обеих группах при развитии ДП вирсунгов проток был стентирован.
Изолированная несостоятельность ПЕА в основной группе отмечена у 4 пациентов: М2 с оригинальным конце-петлевым ИПЕА — 2 случая; П2+ с оригинальным конце-концевым ИПЕА (ПП стентирован) — 1; М1 — 1 случай. Свищи закрылись самостоятельно через 6–10 нед.
Три случая летальных исходов в основной группе непосредственно с ПДА не связаны. У одного пациента (П2+, оригинальный конце-концевой ИПЕА) во время проведения лимфодиссекции была повреждена селезеночная артерия. При релапаротомии выявлены некроз всей культи ПЖ, парапанкреатической и забрюшинной клетчатки слева, несостоятельность ИПЕА, выпот брюшной полости с примесью кишечного содержимого. Травма селезеночной артерии и стандартная мобилизация желудка, предполагающая разобщение коллатерального тока крови, явились причиной некроза культи ПЖ с развитием несостоятельности ИПЕА. Еще двое больных (П2+, оригинальный конце-концевой ИПЕА; М2, конце-петлевой ИПЕА с циркулярной резекцией воротной вены) умерли в первые сутки после операции от острой сердечной недостаточности и внутрибрюшного кровотечения на фоне ДВС-синдрома.
Изолированная несостоятельность ПДА (6 случаев) в группе сравнения отмечена после конце-концевых ИПЕА, из них 2 случая — по оригинальной методике. При этом мягкая ткань железы диагностирована у 5 пациентов. ПП стентирован в 5 из 6 случаев несостоятельности ПДА, в том числе у 4 больных с мягкой тканью ПЖ. У 4 из 6 больных с ДП в группе сравнения отмечена несостоятельность ПДА, у 2 человек смерть наступила в раннем послеоперационном периоде от эндогенной интоксикации до развития вероятной несостоятельности анастомоза. ДП у этих больных развился после наложения конце-концевых ИПЕА (5 случаев) и конце-бокового ПЕА с раздельным вшиванием ПП (1 случай). Мягкая ткань железы отмечена у 2 пациентов с ДП. В 3 случаях из 11 смерть наступила от ДП. Остальные причины смерти непосредственно с методикой формирования ПДА не связаны: внутрибрюшное кровотечение — 4 случая, перфорация острых язв желудка — 1, желудочно-кишечное кровотечение с развитием несостоятельности гастроеюноанастомоза — 1, гастростаз с развитием необратимых электролитных нарушений — 1, острая печеночно-почечная недостаточность — 1.
Обсуждение. Среди факторов риска развития несостоятельности ПДА наиболее значимыми являются состояние ткани культи ПЖ и диаметр ПП [16–18]. Для снижения частоты развития несостоятельности ПДА авторы [6, 19–21] предлагают индивидуальный подход к формированию соустья, который определяется прежде всего состоянием ткани железы и диаметром ПП. В настоящее время не существует прижизненной морфометрической оценки состояния паренхимы ПЖ. В литературе имеются лишь единичные сообщения относительно критериев определения состояния ПЖ. Так, Y. Suzuki и соавт. [21] определяют состояние паренхимы ПЖ (плотная или мягкая), основываясь на трудности или легкости диссекции ткани железы ультразвуковым скальпелем. Нами предложен критерий «прорезывание ткани лигатурой». Несмотря на субъективность данного критерия — зависимость от индивидуального восприятия хирурга (прилагаемое усилие, техника завязывания шва) — объективизация достигается тем, что, определив состояние ткани железы, хирург выбирает оптимальный, по его мнению, вариант ПДА. Нередко очевидность выбора проявляется при выполнении гемостаза по резекционной плоскости культи ПЖ прошиванием мест кровотечения. При прорезывании ткани железы лигатурой хирург сужает для себя круг возможных ПДА. Так, при мягкой ткани ПЖ считаем показанными только конце-петлевые ИПЕА и ИПГА. Надежность инвагинационных ПДА достигается широкой зоной перитонизации соустья за счет увеличения площади контакта стенки кишки или желудка и поверхности культи ПЖ. Предложенный оригинальный конце-петлевой ИПЕА позволяет наложить соустье при любом диаметре тонкой кишки. Соответствие диаметров формирующих анастомоз образований регулируется длиной продольного разреза на кишке. Расположение инвагинированной культи ПЖ в просвете образованного тонкокишечного резервуара исключает сдавление культи ПЖ стенкой кишки, что способствует свободному оттоку панкреатического секрета. Полученные данные подтверждают обоснованность применения инвагинационных конце-петлевых ПДА при состоянии железы М. В основной группе при таком состоянии железы случаев ДП не было.
Важным при выборе вида ПДА является диаметр ПП. При диаметре менее 3 ммвыполнение ПДА с изолированным вшиванием ПП нецелесообразно. При таком диаметре ПП не стентируем, поскольку площадь сечения протока становится меньше за счет стенки катетера. Кроме того, в случаях с сохраненной функцией ПЖ нельзя исключить затруднение оттока секрета железы [22]. У 2 больных основной группы после временного стентирования ПП в конце операции развился субкапсулярный отек культи ПЖ. После удаления стентов из ПП под давлением выделился панкреатический секрет. Считается, что сохраняющийся субкапсулярный отек после наложения ПДА служит предиктором развития ДП [23]. В группе сравнения ДП после операции развился у 6 больных, которым был стентирован ПП.
В предлагаемом алгоритме при мягкой железе мы не указываем на соотнесение размеров просвета и диаметра резекционной плоскости культи ПЖ, поскольку состояние культи ПЖ М1 встречается крайне редко. В нашем наблюдении только в 1 случае (основная группа) отмечено прорезывание ткани ПЖ лигатурой при диаметре ПП более 3 мм. Операция была выполнена по поводу рака большого дуоденального сосочка через 6 нед после перенесенного панкреатита. Во время вмешательства в парапанкреатической клетчатке вскрыты 3 небольших (до 2 см) абсцесса с секвестрами. Воспаление ПЖ возникло после чрескожного чреспеченочного транспапиллярного наружно-внутреннего дренирования, выполненного с целью декомпрессии желчных путей.
Важным условием выбора ПДА является соответствие размера резекционной поверхности культи ПЖ и диаметра анастомозируемой тощей кишки. Как и другие авторы [12], полагаем, что размеры культи ПЖ и тощей кишки могут быть ограничением в применении некоторых видов ПДА. Прежде всего это связано с опасением сдавления инвагинированной культи ПЖ и ПП стенкой кишки в случаях, когда диаметр культи железы на уровне среза равен или превышает диаметр кишки. Одной из причин двух случаев ДП в группе сравнения стало ошибочное наложение конце-концевых ИПЕА при диаметре тощей кишки, равном диаметру культи ПЖ.
После оригинального конце-концевого ИПЕА отмечены 3 случая изолированной несостоятельности соустья: 1 — в основной группе; 2 — в группе сравнения, из них 1 — при мягкой железе. ДП с летальным исходом после оригинального конце-концевого ИПЕА развился в 1 случае основной группы и не был связан с особенностями формирования ПДА. При конце-петлевых ИПЕА, примененных только в основной группе, отмечено 2 случая несостоятельности анастомоза при железе М2. Отсутствие ДП и самостоятельное закрытие панкреатических свищей на фоне консервативной терапии считаем приемлемым результатом для неблагоприятных условий формирования ПДА. Один случай летального исхода после применения оригинального конце-петлевого ИПЕА непосредственно с формированием соустья не связан.
Оригинальный конце-петлевой ИПЕА согласно разработанному алгоритму подходит для всех степеней готовности железы. Тем не менее мы не выполняем его в случаях, когда при одинаковой надежности есть более простая в техническом плане альтернатива. Это связанно с тем, что при формировании резервуара может появиться полоска ишемии стенки кишки в проекции стыка скрепочного шва у изгиба кишечной петли протяженностью до 2–3 см и шириной до 0,5–1 см, хотя данная проблема легко устраняется наложением серо-серозных швов. Кроме того, обязательным условием для выполнения предлагаемого вида анастомоза является наличие линейного степлерного аппарата (НЖКА, GIA и аналоги), так как ручное формирование тонкокишечного резервуара сделает формирование предлагаемого вида соустья неоправданно громоздким.
По изолированной несостоятельности ПДА значимых различий в группах не получено (р=0,95). Однако в основной группе не было случаев ДП и летальных исходов, непосредственно связанных с особенностями формирования ПДА.
Заключение. Предлагаемый алгоритм, в который адаптированы оригинальные способы ИПЕА, позволяет выбрать оптимальный метод формирования соустья в зависимости от морфометрических особенностей анастомозируемых культи поджелудочной железы и тощей кишки и улучшить результаты панкреатодуоденальной резекции. Дифференцированный подход к выбору панкреатодигестивного анастомоза позволяет уменьшить количество случаев деструктивного панкреатита, являющегося основной причиной развития жизнеугрожающих осложнений и летальных исходов после резекции железы.
Финансирование исследования и конфликт интересов. Исследование не финансировалось какими-либо источниками, и конфликты интересов, связанные с данным исследованием, отсутствуют.
Литература
- Orr R.K. Outcomes in pancreatic cancer surgery. Surg Clin North Am 2010; 90(2): 219–234, https://doi.org/10.1016/j.suc.2009.12.007.
- Walters D.M., McGarey P., LaPar D.J., Strong A., Good E., Adams R.B., Bauer T.W. A 6-day clinical pathway after a pancreaticoduodenectomy is feasible, safe and efficient. HPB 2013; 15(9): 668–673, https://doi.org/10.1111/hpb.12016.
- Addeo P., Delpero J.R., Paye F., Oussoultzoglou E., Fuchshuber P.R., Sauvanet A., Sa Cunha A., Le Treut Y.P., Adham M., Mabrut J.Y., Chiche L., Bachellier P. Pancreatic fistula after a pancreaticoduodenectomy for ductal adenocarcinoma and its association with morbidity: a multicentre study of the French Surgical Association. HPB 2014; 16(1): 46–55, https://doi.org/10.1111/hpb.12063.
- Grobmyer S.R., Pieracci F.M., Allen P.J., Brennan M.F., Jaques D.P. Defining morbidity after pancreaticoduodenectomy: use of a prospective complication grading system. J Am Coll Surg 2007; 204(3): 356–364, https://doi.org/10.1016/j.jamcollsurg.2006.11.017.
- Fernández-del Castillo C., Morales-Oyarvide V., McGrath D., Wargo J.A., Ferrone C.R., Thayer S.P., Lillemoe K.D., Warshaw A.L. Evolution of the Whipple procedure at the Massachusetts General Hospital. Surgery 2012; 152(3 Suppl 1): S56–S63, https://doi.org/10.1016/j.surg.2012.05.022.
- Щастный А.Т. Послеоперационные осложнения проксимальных резекций поджелудочной железы у пациентов с хроническим панкреатитом. Новости хирургии 2011; 19(3): 30–43.
- Callery M.P., Pratt W.B., Vollmer C.M. Jr. Prevention and management of pancreatic fistula. J Gastrointest Surg 2009; 13(1): 163–173, https://doi.org/10.1007/s11605-008-0534-7.
- Hong T.H., Youn Y.C., You Y.K., Kim D.G. An easy and secure pancreaticogastrostomy after pancreaticoduodenectomy: transpancreatic suture with a buttress method through an anterior gastrotomy. J Korean Surg Soc 2011; 81(5): 332–338, https://doi.org/10.4174/jkss.2011.81.5.332.
- Lai E.C., Lau S.H., Lau W.Y. Measures to prevent pancreatic fistula after pancreatoduodenectomy: a comprehensive review. Arch Surg 2009; 144(11): 1074–1080, https://doi.org/10.1001/archsurg.2009.193.
- Pecorelli N., Balzano G., Capretti G., Zerbi A., Di Carlo V., Braga M. Effect of surgeon volume on outcome following pancreaticoduodenectomy in a high-volume hospital. J Gastrointest Surg 2012; 16(3): 518–523, https://doi.org/10.1007/s11605-011-1777-2.
- Патютко Ю.И., Котельников А.Г. Хирургия рака органов билиопанкреатодуоденальной зоны. М: Медицина; 2007; 448 с.
- Zhang B., Xu J., Liu C., Long J., Liu L., Xu Y., Wu C., Luo G., Ni Q., Li M., Yu X. Application of “papillary-like main pancreatic duct invaginated” pancreaticojejunostomy for normal soft pancreas cases. Sci Rep 2013; 3: 2068, https://doi.org/10.1038/srep02068.
- Барванян Г.М. Выбор способа панкреатодигестивного соустья при панкреатодуоденальной резекции. Вестник хирургии им. И.И. Грекова 2014; 173(6): 27–30.
- Барванян Г.М. Способ формирования панкреатоеюноанастомоза при панкреатодуоденальной резекции. Хирургия. Журнал им. Н.И. Пирогова 2014; 8: 28–31.
- Strasberg S.M., Linehan D.C., Clavien P.A., Barkun J.S. Proposal for definition and severity grading of pancreatic anastomosis failure and pancreatic occlusion failure. Surgery 2007; 141(4): 420–426, https://doi.org/10.1016/j.surg.2006.12.001.
- Inchauste S.M., Lanier B.J., Libutti S.K., Phan G.Q., Nilubol N., Steinberg S.M., Kebebew E., Hughes M.S. Rate of clinically significant postoperative pancreatic fistula in pancreatic neuroendocrine tumors. World J Surg 2012; 36(7): 1517–1526, https://doi.org/10.1007/s00268-012-1598-9.
- Katsaragakis S., Larentzakis A., Panousopoulos S.G., Toutouzas K.G., Theodorou D., Stergiopoulos S., Androulakis G. A new pancreaticojejunostomy technique: a battle against postoperative pancreatic fistula. World J Gastroenterol 2013; 19(27): 4351–4355, https://doi.org/10.3748/wjg.v19.i27.4351.
- Machado N.O. Pancreatic fistula after pancreatectomy: definitions, risk factors, preventive measures, and management — review. Int J Surg Oncol 2012; 2012: 60247, https://doi.org/10.1155/2012/602478.
- Запорожченко Б.С., Качанов В.Н., Зубков О.Б., Бородаев И.Е., Горбунов А.А., Шевченко В.Г. Различные варианты наложения панкреатодигестивных анастомозов при выполнении панкреатодуоденальных резекций. Вестник неотложной и восстановительной медицины 2012; 13(2): 270–272.
- Касаткин В.Ф. Пути улучшения непосредственных результатов панкреатодуоденальных резекций при периампулярном раке. Хирургия. Журнал им. Н.И. Пирогова 2008; 10: 10–16.
- Suzuki Y., Fujino Y., Tanioka Y., Hiraoka K., Takada M., Ajiki T., Takeyama Y., Ku Y., Kuroda Y. Selection of pancreaticojejunostomy techniques according to pancreatic texture and duct size. Arch Surg 2002; 137(9): 1044–10478, https://doi.org/10.1001/archsurg.137.9.1044.
- Чернявский А.А., Лавров Н.А., Стражнов А.В., Пенин С.В. Резекционные вмешательства на поджелудочной железе при операциях по поводу рака желудка. Вестник хирургической гастроэнтерологии 2013; 3: 4–13.
- Кригер А.Г., Кубышкин В.А., Кармазановский Г.Г., Свитина К.А., Кочатков А.В., Берелавичус С.В., Козлов И.А., Королев С.В., Горин Д.С. Послеоперационный панкреатит при хирургических вмешательствах на поджелудочной железе. Хирургия. Журнал им. Н.И. Пирогова 2012; 4: 14–19.