Параметры дисфункции автономной нервной системы у пациентов кардиологического профиля с острой и хронической формами ишемической болезни сердца
Цель исследования — определить клиническую значимость новых параметров вариабельности сердечного ритма у пациентов с острым инфарктом миокарда и хронической ишемической болезнью сердца.
Материалы и методы. В исследование включено 83 пациента мужского пола, которые разделены на три группы: 1-я группа — 30 человек с диагнозом острого коронарного синдрома с исходом в инфаркт миокарда; 2-я группа — 30 пациентов с хроническими формами ишемической болезни сердца; 3-я группа (контрольная) — 23 практически здоровых пациента без изменений на ЭКГ. Регистрацию ЭКГ проводили с помощью сертифицированного компьютерного электрокардиографа ЭК-01 (ЗАО «Новые приборы», Самара). Полученные записи анализировали в пакете прикладных программ MATLAB. Оценивали показатели мониторирования ЭКГ (SDNN, RMSSD, LF/HF, коэффициент флюктуации α, общую мощность спектра, коэффициент акселерации/децелерации сердечного ритма — AC/DC) в состоянии покоя и при физической нагрузке (тест 6-минутной ходьбы).
Результаты. Отличия параметров вариабельности сердечного ритма, имеющиеся в покое, исчезают во время выполнения теста 6-минутной ходьбы (за исключением сниженного SDNN и общей мощности спектра у пациентов с острым инфарктом миокарда), который приводит к однонаправленному уменьшению вариабельности сердечного ритма как у здоровых, так и у больных. Выявлено уменьшение фрактальных свойств сердечного ритма у пациентов с ишемической болезнью сердца и острым инфарктом миокарда на коротких фрагментах записи ЭКГ (коэффициент флюктуации α), не зависящее от физической нагрузки.
Заключение. При изучении дисфункции автономной нервной системы наряду с классическим показателем RMSSD необходимо учитывать параметры, отражающие замедление (DС) и ускорении (АС) вариабельности сердечного ритма в состоянии покоя, фрактальную закономерность (α), не зависящую от физической нагрузки, а также значение SDNN и общей мощности спектра.
Вариабельность сердечного ритма (ВСР) — известный инструмент изучения дисфункции автономной нервной системы. Считается, что изменения сердечного цикла от сокращения к сокращению отражают баланс между симпатическими и парасимпатическими влияниями на сердце, причем последним приписывается кардиопротективная роль [1]. Острый инфаркт миокарда (ОИМ), нестабильная стенокардия — наиболее изученные формы ишемической болезни сердца (ИБС), при которых получены доказательства о взаимосвязи низкой ВСР как с клиническим прогнозом внезапной смерти [2], так и с прогрессированием хронической сердечной недостаточности [3].
Цель исследования — определить клиническую значимость параметров вариабельности сердечного ритма у пациентов с острым инфарктом миокарда и хронической ишемической болезнью сердца.
Материалы и методы. Проведено сравнение классических параметров ВСР с параметрами, характеризующими симметричность вариабельности (коэффициенты акселерации и децелерации — AC и DC) и степень фрактальности сердечного ритма (коэффициент флюктуации α) у больных с ОИМ и хронической ишемической болезнью сердца (ХИБС) в покое. Изучены влияние физической нагрузки (тест 6-минутной ходьбы) на показатели вариабельности R–R-интервалов, ускорение и замедление ВСР, а также степень фрактальности в группах пациентов с ХИБС, ОИМ и в группе контроля.
В исследование включено 83 пациента мужского пола, которые были разделены на три группы. В 1-ю группу вошли 30 пациентов с ОИМ (с зубцом Q — 21 человек, без зубца Q — 9). 2-ю группу составили 30 пациентов с различными формами ХИБС (18 человек — с верифицированным диагнозом нестабильной стенокардии в фазе стабилизации, 12 — со стабильной стенокардией напряжения I–II функционального класса), поступивших в кардиологическое отделение Самарской областной клинической больницы им. В.Д. Середавина. В 3-ю (контрольную) группу вошли 23 практически здоровых пациента без изменений на ЭКГ.
Исследования проводились в условиях Самарской областной клинической больницы им. В.Д. Середавина. В работе руководствовались Хельсинкской декларацией (принятой в июне 1964 г., Хельсинки, Финляндия и пересмотренной в октябре 2000 г., Эдинбург, Шотландия) и разрешением Этического комитета больницы. Все испытуемые были проинформированы о содержании и целях исследования и дали добровольное письменное согласие на участие.
Всем пациентам перед исследованием были выполнены измерения массы тела, роста и артериального давления.
Критериями исключения служили: хроническая сердечная недостаточность выше II функционального класса, артериальная гипертензия выше II степени, тяжелые хронические заболевания, в том числе онкологические, хроническая болезнь почек более II стадии, хроническая обструктивная болезнь легких II степени и выше, показатель гемоглобина крови менее 110 г/л, любые нарушения ритма, включая атриовентрикулярные блокады более I степени, частая экстрасистолия — более 30 в час.
Все пациенты обследованы перед выпиской из стационара, но не ранее, чем через 10 дней после поступления.
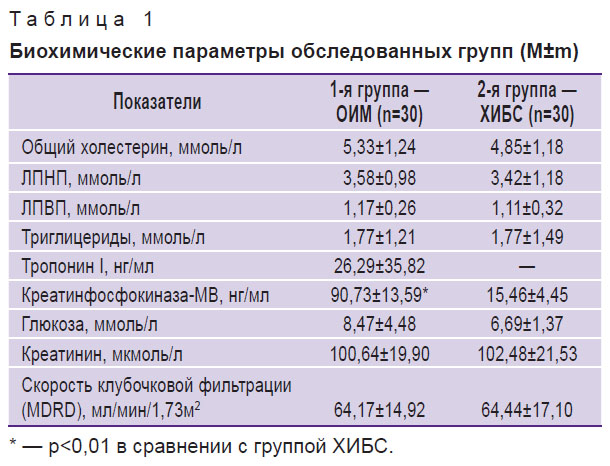
В группе ХИБС средний возраст составил 59,3±11,5 года, в группе ОИМ — 59,5±8,4 года. Группы были сопоставимы по индексу массы тела: 28,26±3,94 и 28,14±3,57 соответственно. Параметр фракции выброса левого желудочка показал отсутствие систолической дисфункции и составил в группе ХИБС 58,13±8,65%, в группе ОИМ — 56,1±7,55%. По параметрам липидного профиля, гликемии, фильтрационной функции почек значимых различий не выявлено (табл. 1). Концентрация тропонина крови и креатинфосфокиназы в 1-й группе (см. табл. 1) отражает некроз кардиомиоцитов, подтверждая ОИМ у всех пациентов этой группы.
|
Таблица 1. Биохимические параметры обследованных групп (M±m) |
В группе контроля средний возраст был статистически значимо меньше и составил 49,5±4,6 года.
Регистрация ЭКГ-сигнала выполнена пациентам во II стандартном отведении в состоянии покоя с последующим проведением функционального теста 6-минутной ходьбы. Регистрацию осуществляли с помощью сертифицированного компьютерного электрокардиографа ЭК-01 (ЗАО «Новые приборы», Самара), имеющего стандартные технические характеристики: полоса пропускания по уровню –3 дБ составляла 0,05–100 Гц; частота дискретизации — 1000 Гц; разрядность аналого-цифрового преобразования — 16 бит. Компьютерная обработка ЭКГ-сигнала, включая этапы цифровой фильтрации сигнала, обнаружения характерных точек, формирования массива длительностей кардиоинтервалов и определения показателей ВСР, проводилась в пакете инженерных вычислений MATLAB R2013a.
В ходе исследования оценивали спектральные и частотные показатели мониторирования ЭКГ (SDNN, RMSSD, высокочастотные (HF) и низкочастотные (LF) компоненты, коэффициент флюктуации α, общую мощность спектра TP, AC/DC) в покое и при физической нагрузке.
SDNN — среднеквадратичное отклонение длительностей кардиоинтервалов (КИ), мс:
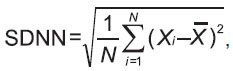
где Xi — значение длительности i-го КИ; 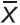 — среднее значение длительности КИ; N — размер исследуемой выборки КИ.
— среднее значение длительности КИ; N — размер исследуемой выборки КИ.
Статистический показатель RMSSD — квадратный корень из суммы квадратов разности величин последовательных пар КИ, мс:
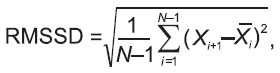
где Xi+1 — значение длительности (i+1)-го КИ; 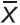 i — значение длительности i-го КИ; N — размер выборки КИ.
i — значение длительности i-го КИ; N — размер выборки КИ.
Коэффициент флюктуации α определяется с помощью флюктуационного анализа с устранением трендов (DFA: detrended fluctuation analysis) [4]. Метод DFA позволяет проводить изучение структуры различных процессов, в том числе и нестационарных, с точки зрения статистического самоподобия.
Алгоритм вычисления коэффициента флюктуации α состоит в следующем [4]. На первом этапе из временной последовательности длительностей КИ X формируется кумулятивнаясумма Wt:
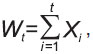
где Xi — значение длительности i-го КИ; t — переменная, изменяющаяся от 1 до величины размера исходной выборки КИ X.
На втором этапе кумулятивная сумма Wt разбивается на временные окна равного размера L; для каждого временнóго окна составляется интерполяционный полином, в случае использования метода DFA первого порядка это линейный полином Z.
На третьем этапе для каждого значения размера временнóго окна L вычисляется среднеквадратичное отклонение F:
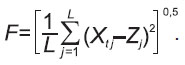
На четвертом этапе вычисления 2 и 3 повторяются при различных размерах временнóго окна L.
На пятом этапе определяют коэффициент флюктуации первого порядка α как отношение логарифмов изменения F в зависимости от изменения L.
Коэффициенты акселерации и децелерации (AC и DC) сердечного ритма имеют высокую чувствительность к определению риска внезапной сердечной смерти и служат значимыми предикторами выживания пациентов после перенесенного инфаркта миокарда [5]. Данные показатели являются нелинейными и определяют интенсивность квазипериодических трендов в сердечном ритме на основе усреднения сигналов с устранением фазы (phase-rectified signal averaging) [6].
Коэффициенты акселерации и децелерации сердечного ритма определяют следующим образом. На первом этапе из последовательности длительностей КИ выделяют якорные узлы акселерации и децелерации. КИ считается якорной точкой децелерации, если значение его длительности превосходит длительность предыдущего КИ. КИ является якорной точкой акселерации, если длительность текущего КИ меньше длительности предыдущего. Для увеличения помехоустойчивости определения показателей акселерации/децелерации на этом этапе могут вводиться дополнительные условия, например, задаваться максимально допустимая величина между длительностями двух последовательных КИ.
На втором этапе для каждой якорной точки акселерации или децелерации из исходной последовательности КИ формируется опорный фрагмент, в середине которого должна находиться якорная точка. Оптимальный размер ширины окна опорного фрагмента зависит от исходной выборки КИ и обычно берется в пределах от 12 до 60 КИ [5].
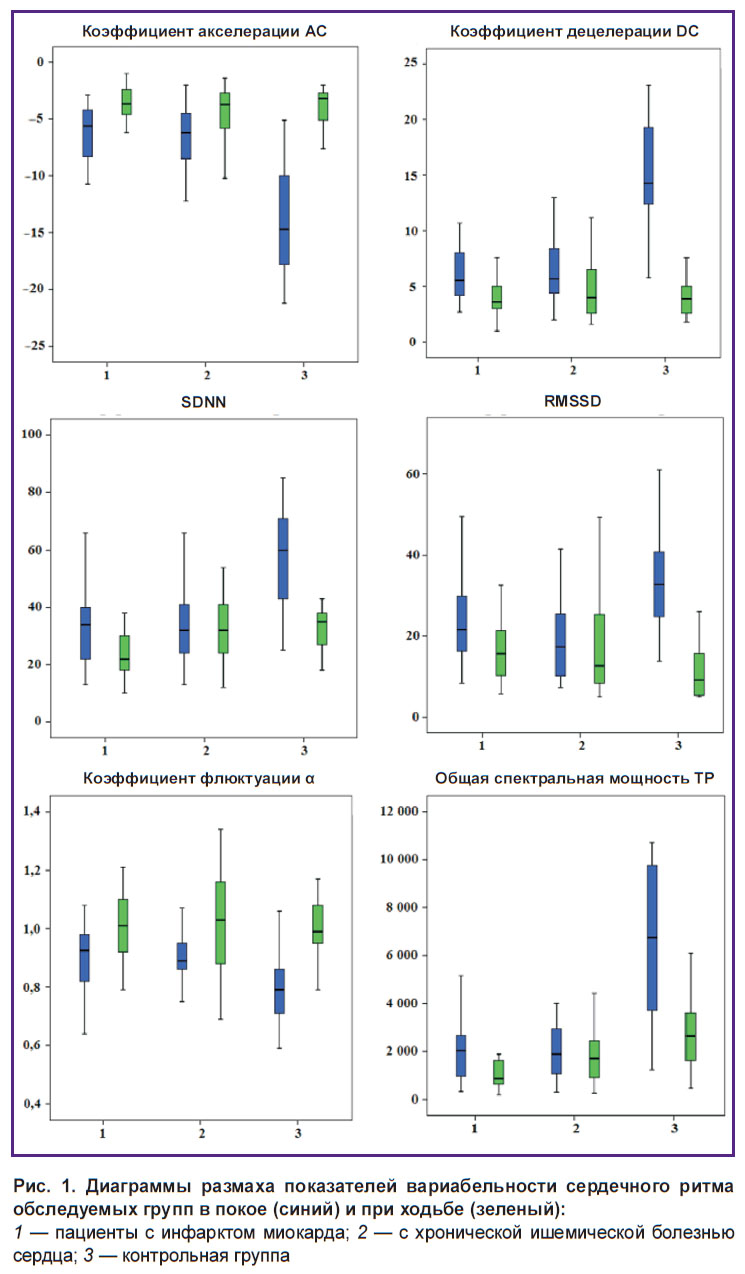
На третьем этапе сформированные опорные сегменты усредняют отдельно для всех якорных точек акселерации и децелерации, в результате чего формируются две интегральные кривые (рис. 1).
На заключительном этапе вычисляют коэффициенты AC и DC:
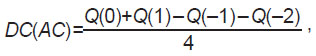
где Q — значение усредненной длительности соответствующих КИ на интегральной кривой акселерации или децелерации; Q(0) — усредненное значение длительности всех КИ, соответствующих якорным точкам акселерации или децелерации.
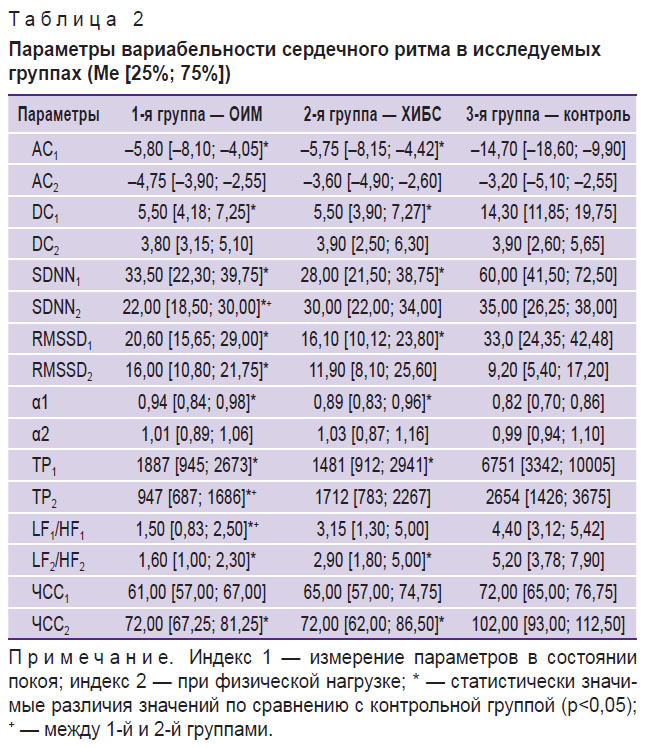
Результаты. В табл. 2 приведены значения показателей ВСР для всех исследуемых групп в покое и в ходе теста 6-минутной ходьбы. Статистическая обработка полученных результатов проводилась с помощью компьютерной программы Statistica 6.0. Для оценки достоверности средних показателей в сравниваемых группах применялся непараметрический критерий U Манна–Уитни, различия считались статистически значимыми при р<0,05.
|
Таблица 2. Параметры вариабельности сердечного ритма в исследуемых группах (Me [25%; 75%]) |
На рис. 1 приведены диаграммы размаха (box-and-whisker plot), на которых указаны медиана, 75-й и 25-й перцентили, а также максимальные и минимальные значения показателей ВСР для всех групп.
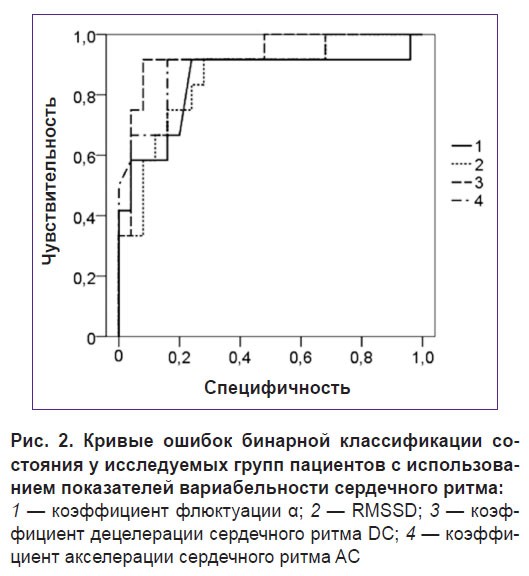
Оценена чувствительность и специфичность используемых показателей ВСР по бинарной шкале «патология/норма» (рис. 2). Для количественной оценки качества бинарной классификации рассчитано значение площади под ROC-кривой (receiver operating characteristic) для каждого показателя ВСР: для коэффициента флюктуации α оно составляло 0,845; для RMSSD — 0,857; для коэффициента децелерации DC — 0,930;для коэффициента акселерации AC — 0,898.
Обсуждение. При анализе частотных и спектральных показателей кардиоинтервалов ЭКГ в покое отмечены статистически значимые изменения показателей SDNN, RMSSD в обеих группах с ИБС, что согласуется с классическими закономерностями [1–3]: ВСР уменьшается при острых и хронических формах ИБС. Уменьшение общей ВСР (о чем свидетельствует SDNN) совпадает с уменьшением общего спектра мощности TP, а также мощности по всем компонентам TP, включая высокочастотную составляющую — HF. Поскольку высокие частоты колебаний R–R-интервалов связаны с частотой дыхания и, соответственно, с периодическим возбуждением блуждающего нерва, не удивительно, что RMSSD, являясь вариабельностью разности последовательных интервалов и отражая их быстрые изменения, также реагирует уменьшением. Эти данные соответствуют результатам, полученным нами ранее [7], что свидетельствует об утрате рефлексогенных влияний парасимпатической системы на синусовый узел. Существует и другое объяснение уменьшения ВСР при увеличении частоты сердечных сокращений (ЧСС) [8]. Согласно простому математическому правилу одна и та же вариабельность требует большего изменения интервалов при редком ритме, чем при частом. Поэтому требуется нормализация ВСР к ЧСС, чтобы отделить физиологическое влияние от чисто математической зависимости.
Известно, что уменьшение ВСР является значительным фактором риска пациентов, перенесших инфаркт миокарда. Фазовое усреднение сигнала позволяет выделить периодику из временных отрезков записи, которая может включать нестационарные шумы и артефакты, также как и периодические компоненты, с исключением непериодических компонентов. При этом можно выделить коэффициент децелерации DC, который описывает усредненную характеристику замедления сердечного ритма, обусловленную модуляциями тонуса вагуса. Исследованиe A. Bauer с соавт. [5] показало, что способность к замедлению ритма имеет большее клиническое значение, чем способность к ускорению ритма. Из общего количества пациентов, перенесших недавний инфаркт миокарда, авторами были выделены пациенты, составившие 15% от общего количества обследованных, у которых параметр DC был снижен асимметрично, т.е. гораздо больше, чем AC. Данное проспективное исследование показало, что выраженное снижение замедления ритма имеет наибольшую прогностическую ценность в выявлении пациентов с риском внезапной аритмической смерти в сравнении с уменьшением общей вариабельности по SDNN и уменьшением коэффициента акселерации. Это дает основание говорить о том, что механизмы, ответственные за ускорение и замедление ритма, различны. В нашей работе у всех обследованных явной асимметрии этих показателей не было, т.е. коэффициенты акселерации и децелерации были существенно ниже в группах с ИБС в сравнении с контрольной группой, отражая существенное уменьшение общей ВСР.
При физической нагрузке (тест 6-минутной ходьбы) ВСР существенно падает во всех исследованных нами группах и все параметры изменяются однонаправленно, хотя степень изменения ВСР в контрольной группе больше, чем в группах с ИБС. В результате статистические различия исчезают по большинству параметров. Очевидно, это связано с увеличением симпатических влияний при физической нагрузке, что является доказанным механизмом [9]. Следует отметить значительное уменьшение общей спектральной мощности ТР у пациентов с ОИМ при физической нагрузке, что обусловило статистическое отличие от группы с ХИБС по аналогичному параметру, в то время как в покое группы не отличались.
Обращает на себя внимание различная степень уменьшения RMSSD и SDNN в группах больных при физической нагрузке. У пациентов с ИБС падение общей ВСР сопровождалось незначительным уменьшением RMSSD в сравнении с параметром, зафиксированным в покое, а у здоровых RMSSD уменьшился настолько выраженно, что в абсолютном значении стал меньше, чем в группах с ИБС. Это говорит о том, что быстрые изменения ВСР при физической нагрузке не характерны для здоровых. Способность к ускорению и замедлению ритма сердца в обследованных группах закономерно симметрично уменьшалась, не отличаясь по средним значениям (АС2 и DC2) в группах.
Большая методологическая сложность оценки ВСР связана с нестационарным характером кардиоинтервалов. Флюктуации ритма сердца обладают свойством временного самоподобия (фрактальными характеристиками), поэтому в основном используются длительные записи ЭКГ, предоставляемые холтеровским мониторированием.
В нашей работе проанализированы 6-минутные фрагменты ЭКГ. Наличие длительно существующих фрактальных эпизодов говорит о том, что изменения ВСР происходят не только под действием сиюминутной причины, но и объясняются своеобразной памятью. Снижение степени фрактальности ритма сердца отмечено при хронической сердечной недостаточности [10]. Исследование [8] показало, что нелинейный анализ ВСР может превосходить классические методы анализа в способности предсказывать внезапную кардиальную смерть у пациентов с аритмогенным субстратом, например после перенесенного инфаркта миокарда. Выявлено, что коэффициент флюктуации α не изменяется, в то время как ВСР, определяемая классическими методами, снижается [11]. Это подтверждается и в нашей работе.
Периодические компоненты ВСР традиционно оцениваются с помощью частотного анализа [1]. Считается, что высокие частоты отражают парасимпатический, а низкие — симпатический тонус. Соответственно отношение LF/HF отражает баланс автономной нервной системы. R. Perine с соавт. [9] исследовали эти параметры у здоровых во время выполнения физической нагрузки, управляемом дыхании и изменении положения тела. Авторы считают, что спектральные показатели не отражают увеличения симпатического и уменьшения парасимпатического вклада во время физической нагрузки. Мощность HF-спектра отмечена во всем диапазоне физических нагрузок и при больших нагрузках обусловливает наибольшую часть мощности ВСР. Мощность LF-спектра не изменяется под действием небольшой нагрузки в положении сидя, а при ее увеличении существенно падает, демонстрируя полное несоответствие с увеличением симпатической активности при физической нагрузке. При этом статистически значимых различий значений уровня физической подготовки и возраста обследованных не выявлено. Мощность LF значительно возрастала при нагрузках средней интенсивности, если нагрузка совершалась в положении лежа. Вероятно, в этих ситуациях задействуются разные механизмы контроля артериального давления. Известно, что LF обусловлены отчасти активностью барорефлекса, при которой замедляется темп сердечных сокращений при увеличении давления в аорте [9]. В работе G.E. Billman [12] указывается на невозможность физиологической интерпретации этого широко распространенного индекса. Также существуют трудности в интерпретации влияния физической нагрузки на ВСР у больных и здоровых, поскольку ее интенсивность в ходе 6-минутного теста не нормирована.
В работе [13] не выявлено зависимости LF/HF от уровня физической нагрузки, в то время как SDNN и коэффициент флюктуации α закономерно уменьшались при исследовании коротких интервалов ЭКГ пропорционально усилию педалирования. Эти данные отражают противоречия, возникающие при физиологической интерпретации параметров ВСР. Некоторые исследователи [14] полагают, что существуют концептуальные отличия между понятиями тонуса автономной нервной системы и автономной модуляцией. Авторы считают, что простое толкование симпатовагального баланса как суммы влияний на синусовый узел двух ветвей автономной нервной системы не состоятельно. Система регуляции сердечного ритма представляется многоуровневой и сложной, с этих позиций фрактальные закономерности более адекватно отражают расстройства регуляции, не объясняя их механизмы, а фиксируя сам факт нарушений.
Проведенные нами исследования показали, что отличия параметров ВСР, имеющиеся в покое, исчезают во время теста 6-минутной ходьбы, который приводит к однонаправленному уменьшению ВСР как у здоровых, так и у больных. Однако у пациентов с ОИМ значительно снижается SDNN и общая мощность спектра.
Вариабельность, связанная с ускорением темпа сердечного ритма и его замедлением при ИБС, в основном изменяется симметрично. При этом у пациентов с ИБС общая ВСР значительно ниже по сравнению с группой контроля.
Выявлено, что уменьшение степени фрактальности сердечного ритма у пациентов с ИБС на коротких фрагментах записи ЭКГ (коэффициент флюктуации α) не зависит от физической нагрузки.
В нашей работе продемонстрирована сопоставимая специфичность новых параметров нелинейной динамики сердечного ритма (α, AC, DC) в сравнении с классическими параметрами статистического анализа в выявлении автономной дисфункции у пациентов с ИБС. В этом контексте отсутствие тесных корреляций коэффициента флюктуации α с параметрами ВСР у пациентов с ХИБС и ОИМ свидетельствует о потенциальной клинической пользе этого параметра. Отсутствие значительных различий в ВСР между группами с ОИМ и ХИБС, очевидно, объясняется тем, что современные методы лечения пациентов с ОИМ обладают большой клинической эффективностью, уменьшая размер некроза — морфологического субстрата аритмогенности и хронической сердечной недостаточности [15]. В результате параметры дисфункции автономной нервной системы при ОИМ приближаются к параметрам пациентов с хроническими формами ИБС.
Заключение. При изучении дисфункции автономной нервной системы наряду с классическими показателями вариабельности сердечного ритма необходимо учитывать параметры характеризующие симметричность вариабельности в состоянии покоя у пациентов с острой и хронической формами ишемической болезни сердца, коэффициент флюктуации α, не зависящий от физической нагрузки, а также значение SDNN и общей мощности спектра у пациентов с острым инфарктом миокарда.
Финансирование исследования. Работа выполнена при поддержке Министерства образования и науки Российской Федерации в рамках проектной части государственного задания в сфере научной деятельности (код проекта 12.2013.2014/К, номер государственной регистрации 114121670017).
Конфликт интересов. Авторы не имеют конфликта интересов, связанных с исследованием.
Литература
- Schwartz P.J., La Rovere M.T., Vanoli E. Autonomic nervous system and sudden cardiac death. Experimental basis and clinical observations for post-myocardial infarction risk stratification. Circulation 1992; 85(1 Suppl): I77–I91.
- Kiviniemi A.M., Tulppo M.P., Wichterle D., Hautala A.J., Tiinanen S., Seppänen T. Mäkikallio T.H., Huikuri H.V. Novel spectral indexes of heart rate variability as predictors of sudden and non-sudden cardiac death after an acute myocardial infarction. Ann Med 2007; 39(1): 54–62, https://doi.org/10.1080/07853890600990375.
- Shah S.A., Kambur T., Chan C., Herrington D.M., Liu K., Shah S.J. Relation of short-term heart rate variability to incident heart failure (from the Multi-Ethnic Study of Atherosclerosis). Am J Cardiol 2013; 112(4): 533–540, https://doi.org/10.1016/j.amjcard.2013.04.018.
- Peng C.K., Buldyrev S.V., Havlin S., Simons M., Stanley H.E., Goldberger A.L. Mosaic organization of DNA nucleotides. Phys Rev E 1994; 49(2): 1685–1689, https://doi.org/10.1103/physreve.49.1685.
- Bauer A., Kantelhardt J.W., Barthel P., Schneider R., Mäkikallio T., Ulm K., Hnatkova K., Schömig A., Huikuri H., Bunde A., Malik M., Schmidt G. Deceleration capacity of heart rate as a predictor of mortality after myocardial infarction: cohort study. Lancet 2006; 367(9523): 1674–1681, https://doi.org/10.1016/s0140-6736(06)68735-7.
- Bauer A., Kantelhardt J.W., Bunde A., Barthel P., Schneider R., Malik M., Schmidt G. Phase-rectified signal averaging detects quasi-periodicities in non-stationary data. Physica A: Statistical Mechanics and its Applications 2006; 364: 423–434, http://dx.doi.org/10.1016/j.physa.2005.08.080.
- Поваляева Р.А., Лебедев П.А., Калакутский Л.И., Бубнова М.Г., Аронов Д.М. Методы компьютерной фотоплетизмографии в оптимизации оценки реабилитационных мероприятий у постинфарктных пациентов. CardioСоматика 2012; 3(2): 5–10.
- Huikuri H.V., Stein P.K. Heart rate variability in risk stratification of cardiac patients. Prog Cardiovasc Dis 2013; 56(2): 153–159, https://doi.org/10.1016/j.pcad.2013.07.003.
- Perini R., Veicsteinas A. Heart rate variability and autonomic activity at rest and during exercise in various physiological conditions. Eur J Appl Physiol 2003; 90(3–4): 317–325, https://doi.org/10.1007/s00421-003-0953-9.
- Peng C.K., Havlin S., Stanley H.E., Goldberger A.L. Quantification of scaling exponents and crossover phenomena in nonstationary heartbeat time series. Chaos 1995; 5(1): 82–87, https://doi.org/10.1063/1.166141.
- Weippert M., Behrens K., Rieger A., Kumar M., Behrens M. Effects of breathing patterns and light exercise on linear and nonlinear heart rate variability. Appl Physiol Nutr Metab 2015; 40(8): 762–768, https://doi.org/10.1139/apnm-2014-0493.
- Billman G.E. The LF/HF ratio does not acurately measure cardiac sympatho-vagal balance. Front Physiol 2013; 4, https://doi.org/10.3389/fphys.2013.00026.
- Chen S.W., Liaw J.W., Chang Y.J., Chuang L.L., Chien C.T. Combined heart rate variability and dynamic measures for quantitatively characterizing the cardiac stress status during cycling exercise. Comput Biol Med 2015; 63: 133–142, https://doi.org/10.1016/j.compbiomed.2015.05.026.
- Nicolini P., Ciulla M.M., De Asmundis C., Magrini F., Brugada P. The prognostic value of heart rate variability in the elderly, changing the perspective: from sympathovagal balance to chaos theory. Pacing Clin Electrophysiol 2012; 35(5): 622–638, https://doi.org/10.1111/j.1540-8159.2012.03335.x.
- Huikuri H.V., Stein P.K. Clinical application of heart rate variability after acute myocardial infarction. Front Physiol 2012; 3, https://doi.org/10.3389/fphys.2012.00041.