Опыт диагностики и хирургического лечения тромбоэмболии легочных артерий у беременных
Тромбоэмболия легочных артерий (ТЭЛА) — серьезное и часто встречающееся экстрагенитальное осложнение беременности, а описаний случаев его лечения очень мало.
В статье рассмотрены три клинических случая хирургического лечения беременных с диагнозом массивной критической ТЭЛА, развившейся на фоне тромбоза глубоких вен нижних конечностей и малого таза с рецидивирующим эмболическим синдромом. Диагнозы подтверждены с помощью инструментальных методов (эхоКГ, МСКТ-ангиография). Было проведено оперативное вмешательство в объеме открытой тромбоэмболэктомии из легочных артерий на работающем сердце.
Установлено, что показания и сроки проведения различных лечебных мероприятий определяются объемом поражения и локализацией тромбоэмболов в легочном сосудистом русле. Оптимальным вариантом оперативного вмешательства служит эмболэктомия из легочных артерий в условиях искусственного кровообращения на работающем сердце без пережатия аорты с минимизацией времени перфузии, поддержанием высокой объемной скорости (2,4 л/мин/м2) и среднего артериального давления (70–75 мм рт. ст.), позволяющая быстро и достаточно полно восстановить легочную гемодинамику. Отказ от применения кардиоплегии при этом способствует адекватной доставке кислорода тканям и плоду; в двух случаях удалось обеспечить пролонгирование беременности с последующим родоразрешением, в одном случае экстренно проведено кесарево сечение.
Авторы отмечают важность полного обследования, подбора адекватной периоперационной терапии и необходимость экстренной хирургической операции у тяжелой категории больных. Результаты исследования показывают, что выполнение открытой эмболэктомии из легочных артерий при массивной критической ТЭЛА у беременных позволяет сохранить жизнь матери и обеспечить рождение здорового ребенка.
Тромбоэмболия легочных артерий (ТЭЛА) — одно из наиболее тяжелых экстрагенитальных осложнений беременности. Основными причинами материнской смертности при ТЭЛАявляются рефлекторное падение сердечного выброса, фибрилляция желудочков и острая дыхательная недостаточность. Все беременные с подозрением на тромбоэмболические осложнения должны быть госпитализированы в многопрофильные стационары. Выбор лечебной тактики у беременных с ТЭЛА — одна из наиболее сложных проблем, возникающих в хирургической и акушерской практике. Недостаточная верификация диагноза грозит неадекватным лечением, в то время как рентгенорадиологические методы диагностики, являющиеся «золотым стандартом» скрининговой оценки, не применимы на ранних сроках беременности и должны использоваться по строгим показаниям. Тромботическая настороженность и отсутствие пренебрежения к «эмболическим знакам» обеспечивают сбалансированный подход к верификации диагноза. Наиболее сложные проблемы возникают при массивной критической тромбоэмболии, что наблюдается при поражении ствола и главных ветвей легочной артерии, при ТЭЛА с мобильным тромбом правых отделов сердца, в случае возникновения кардиогенного шока и необходимости реанимации. Лечебные мероприятия (тромболитическая терапия и открытая эмболэктомия) у этих пациенток должны быть направлены на быстрое восстановление перфузии легочного артериального русла с нормализацией давления в легочной артерии и функции правого желудочка (ПЖ), а открытая эмболэктомия должна рассматриваться как последняя возможность для спасения жизни матери и ребенка [1–5]. Причем тактику ведения больных необходимо вырабатывать хирургу и акушеру-гинекологу совместно с анестезиологом исходя из тяжести состояния пациентки, локализации тромба, гестационного срока, жизнеспособности и степени зрелости плода.
Многочисленные данные [2–9] свидетельствуют о том, что часто такие пациентки не получают самую современную медицинскую помощь. Причина этого многофакторна и включает, как нам кажется, незнание последних принципиальных изменений в методиках кардиохирургических пособий и недоверие или недостаточное представление о возможностях современного хирургического лечения. В подавляющем большинстве случаев (более 95%) для успешного лечения ТЭЛА достаточно назначить антикоагулянты. Как правило, это пациентки с небольшим поражением легочного сосудистого русла без выраженной легочной гипертензии и дисфункции ПЖ. В случае же критического характера эмболии, с массивной дыхательной и сердечной недостаточностью, возникает необходимость скорейшего восстановления легочного кровотока и устранения опасной перегрузки правых отделов сердца. Это требует максимально быстрого осуществления хирургического вмешательства — эмболэктомии из легочных артерий — или тромболитической терапии. В настоящее время хирургическая интервенция и тромболитическая терапия считаются конкурирующими методами. Врачи выполняют либо исключительно открытую эмболэктомию, либо проводят лечение активаторами фибринолиза. По нашему мнению, только объективные показания в каждом конкретном случае могут служить гарантией успеха лечения.
Хирургическое лечение легочной эмболии подразумевает полное удаление тромбоэмболов из сосудистого русла легких. Показания к проведению открытой эмболэктомии у беременных с массивной ТЭЛА не отличаются от таковых у других категорий пациентов. К ним относятся неэффективность тромболитической терапии, абсолютные противопоказания к применению тромболитиков, отсутствие времени для проведения тромболизиса вследствие тяжелого состояния больных. При этом большое значение придается тактике анестезиологического и перфузионного обеспечения экстренных операций по поводу острой массивной ТЭЛА у беременных. В исследовании [10] показано, что материнская смертность у беременных женщин при операциях в условиях искусственного кровообращения (ИК) не превышает таковую у небеременных (1,47%) в случае выполнения плановых вмешательств. При выполнении экстренных операций у пациентов, находящихся в критическом состоянии, на фоне выраженной перегрузки правых отделов сердца и нестабильной гемодинамики показатели материнской летальности значительно возрастают. Однако основным риском ИК является его влияние на плод.
Все вышеизложенное определяет важность более критического подхода к лечению беременных женщин с ТЭЛА. Многоликость клинической картины, невозможность собрать достаточное для анализа число наблюдений в одном учреждении и, как следствие, отсутствие клинических рекомендаций создают серьезные трудности в своевременном определении показаний и выборе хирургической тактики. С целью иллюстрации специфики хирургического лечения разных по клиническому течению случаев массивной критической ТЭЛА у беременных приводим описание трех случаев успешного оперирования беременных по поводу острой массивной ТЭЛА (особенности диагностики, предоперационной подготовки, анестезиолого-перфузионного обеспечения операций, хирургической техники и послеоперационного ведения).
Исследование проведено в соответствии с Хельсинкской декларацией, принятой в июне 1964 г. (Хельсинки, Финляндия) и пересмотренной в октябре 2000 г. (Эдинбург, Шотландия), и одобрено Этическим комитетом НижГМА. От каждой пациентки получено информированное согласие.
Особенности диагностики тромбоэмболии легочной артерии у беременных
У всех трех пациенток ТЭЛА развилась на фоне тромбоза глубоких вен нижних конечностей и малого таза с рецидивирующим эмболическим синдромом.
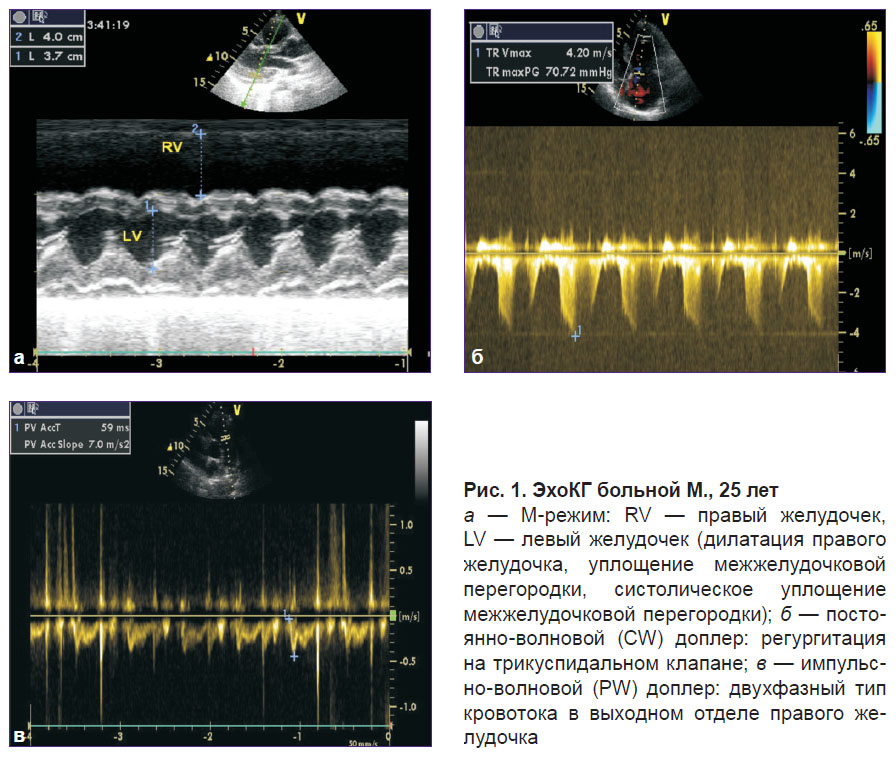
Больная М., 25 лет, 2-я беременность. Поступила в кардиохирургический центр на машине скорой помощи 08.11.2013 г. с диагнозом: «острая массивная ТЭЛА главных ветвей легочных артерий. Илеофеморальный тромбоз слева. Беременность 30 нед». Состояние больной — тяжелое: тахипноэ, тахикардия; кислородотерапия через маску, постоянно вводится Допмин. На эхоКГ при поступлении выявлены выраженные признаки перегрузки ПЖ: диастолический размер (парастернальная позиция) составил 40 мм; поперечный размер правого предсердия — 46 мм; отмечались систолическое уплощение межжелудочковой перегородки, регургитация II степени на трикуспидальном клапане. Максимальное систолическое давление в легочной артерии —
75 мм рт. ст., среднее давление — 52 мм рт. ст., в выходном отделе ПЖ регистрировался двухфазный кровоток с выраженной инцизурой и последующей низкоскоростной фазой (рис. 1). Тромботических масс в правых отделах сердца, стволе легочной артерии не выявлено.
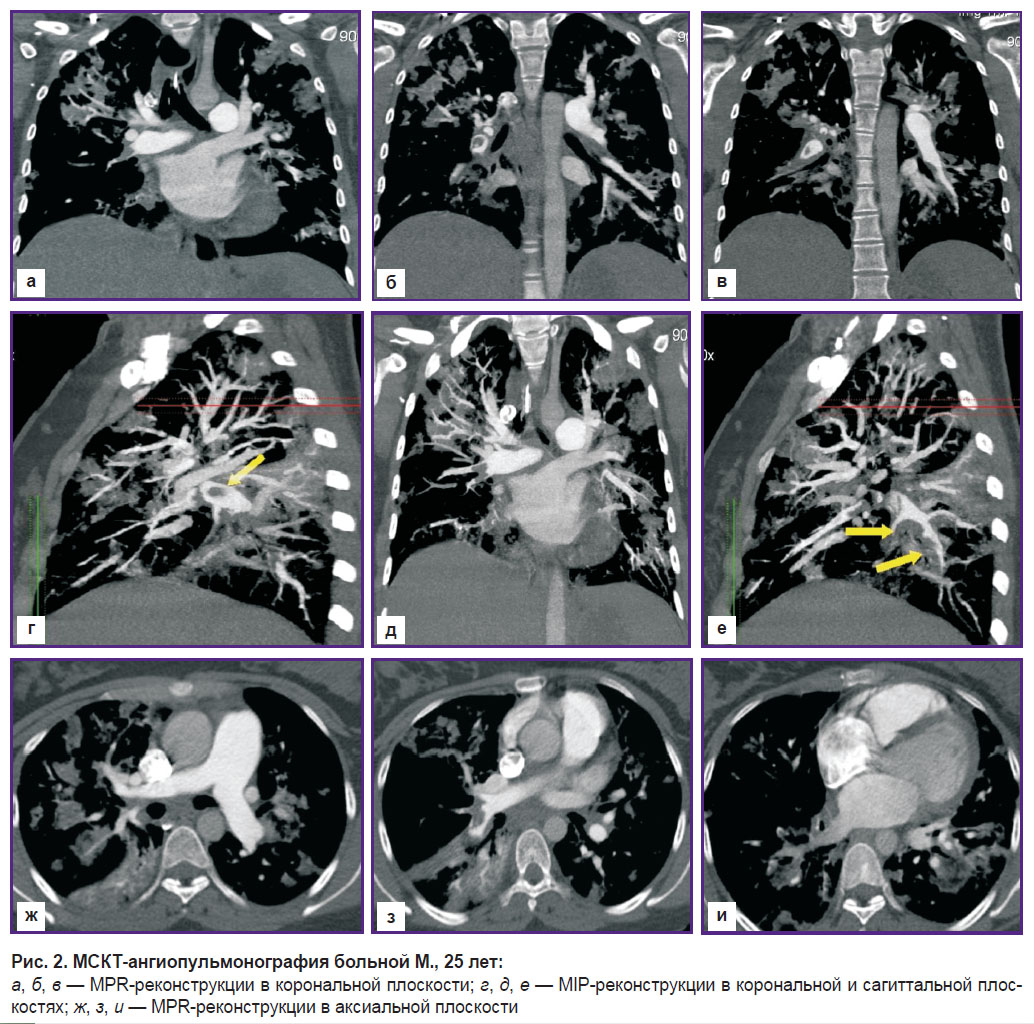
При МСКТ-ангиографии (рис. 2) визуализируются протяженные веретенообразные дефекты наполнения главных ветвей легочной артерии, суживающие просвет на 70%; разнокалиберные дефекты долевых и сегментарных ветвей правой и левой ветвей легочной артерии; расширение правых камер сердца (признаки перегрузки правых камер сердца, косвенные признаки легочной гипертензии).
Больная проконсультирована акушером-гинекологом: матка не возбуждена, сердцебиение плода — отчетливое, ЧСС — 145 в минуту, признаков гипоксического страдания плода не зарегистрировано. Акушерских показаний к прерыванию беременности нет.
Принято решение о выполнении экстренного оперативного вмешательства, направленного на восстановление легочной гемодинамики.
Больная Б., 41 год, 4-я беременность. Поступила в Специализированную кардиохирургическую клиническую больницу Н. Новгорода на машине скорой помощи 25.03.2016 г. с диагнозом: «острая массивная тромбоэмболия главных ветвей легочных артерий. Острое легочное сердце. Илеофеморальный тромбоз правой нижней конечности. Беременность — 25 нед». Доставлена в тяжелом состоянии с рецидивирующими приступами потери сознания, наличием тахипноэ и тахикардии в покое. Дробно получала дексаметазон (суммарно 24 мг), продолжалась кислородотерапия через маску. АД — 110/60 мм рт. ст., ЧСС — 100 в минуту, сатурация кислорода — 96%.
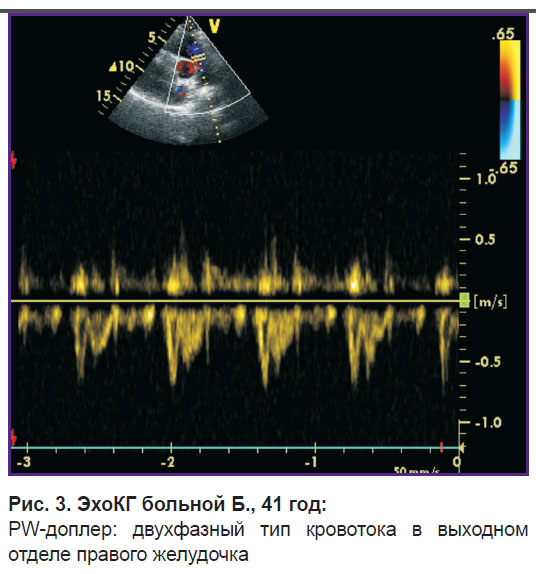
По данным эхоКГ выявлены выраженные признаки перегрузки ПЖ: диастолический размер (парастернальная позиция) составил 43 мм; поперечный размер правого предсердия — 50 мм; отмечены систолическое уплощение межжелудочковой перегородки, регургитация II степени на трикуспидальном клапане. Максимальное систолическое давление в легочной артерии — 65 мм рт. ст., среднее давление — 43 мм рт. ст., в выходном отделе ПЖ регистрировался двухфазный кровоток с выраженной инцизурой и последующей низкоскоростной фазой (рис. 3). Тромботических масс в правых отделах сердца, стволе легочной артерии не выявлено.
|
Рис. 3. ЭхоКГ больной Б., 41 год: PW-доплер: двухфазный тип кровотока в выходном отделе правого желудочка |
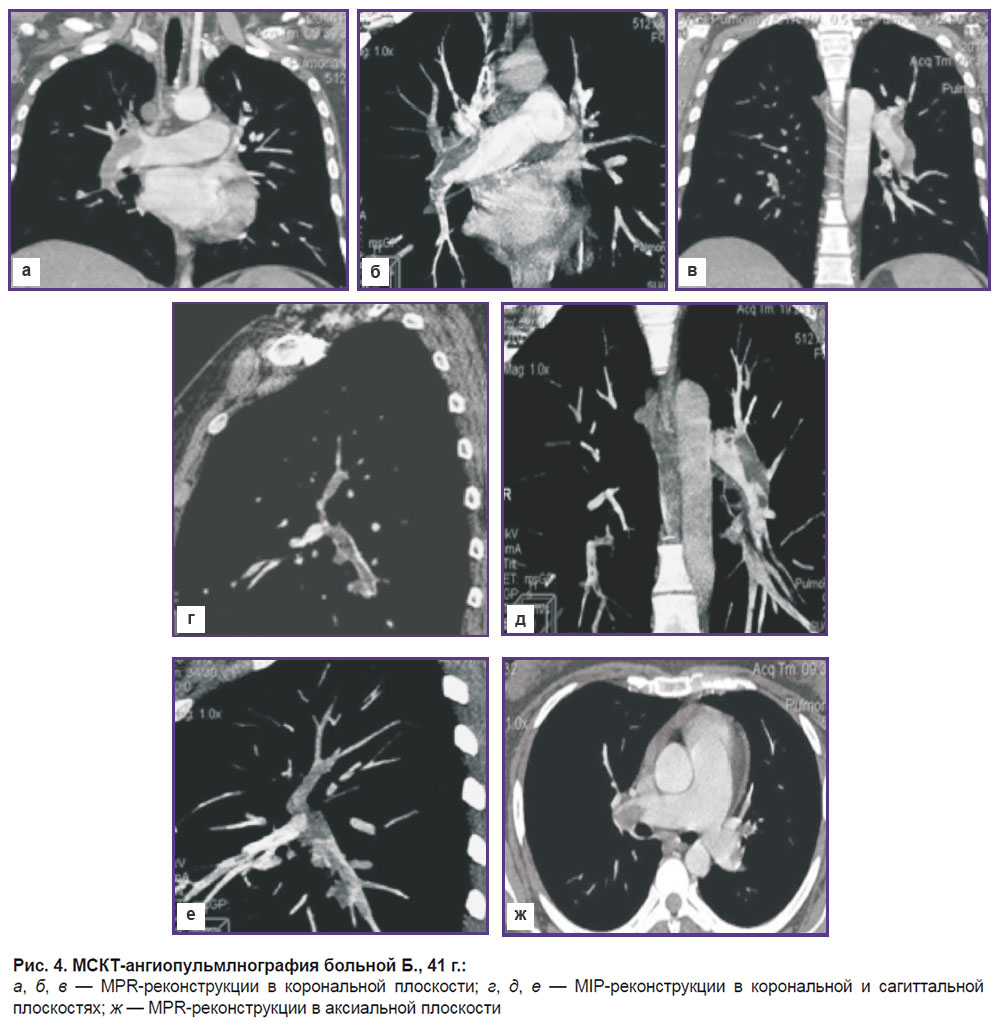
При МСКТ-ангиографии визуализируются разнокалиберные дефекты наполнения нижнедолевых ветвей правой и левой ветвей легочной артерии, резко выраженные застойные изменения по малому кругу кровообращения, сливные фокусы сегментарных пневмонических инфильтраций правого и левого легких (рис. 4).
Больная проконсультирована акушером-гинекологом: сердцебиение плода отчетливо, 140 в минуту, матка не возбуждена, признаков гипоксического повреждения плода не выявлено. Противопоказаний к пролонгированию беременности нет. Решено провести открытую эмболэктомию по жизненным показаниям. Риск операции оценивался как крайне высокий — III–IV по шкале ASA (Американской ассоциации анестезиологов, American Society of Anaesthesiologists).
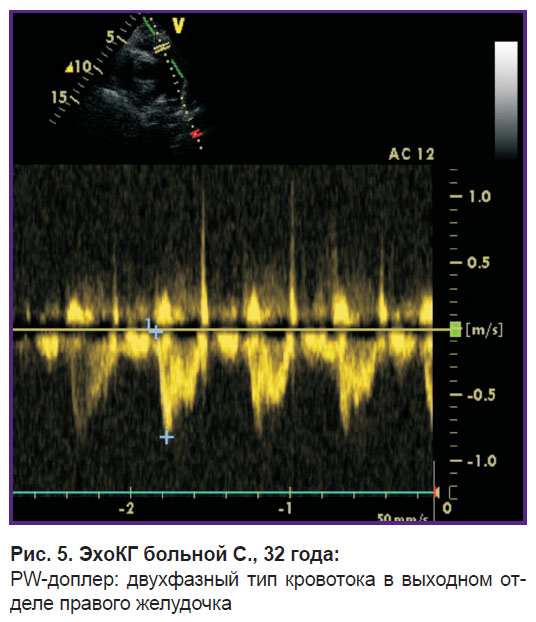
Больная С., 32 года, 1-я беременность. Поступила в клинику 15.06.2017 г. в связи с развитием 14.06 острой тромбоэмболии легочных артерий на фоне тромбофлебита глубоких вен левой нижней конечности и беременности 32 нед. Состояние больной при поступлении — тяжелое, отмечались слабость, тахипноэ и тахикардия в покое. При эхоКГ выявлены признаки перегрузки ПЖ и регургитация II степени на трикуспидальном клапане со средним расчетным давлением в легочной артерии 52 мм рт. ст., в выходном отделе ПЖ так же, как и в предыдущих случаях, регистрировался двухфазный кровоток (рис. 5).
|
Рис. 5. ЭхоКГ больной С., 32 года:
PW-доплер: двухфазный тип кровотока в выходном отделе правого желудочка |
При МСКТ-ангиографии выявлены дефекты наполнения главных ветвей легочной артерии — седловидный справа и пристеночный слева, суживающие просвет артерии на 55 и 30% соответственно. Также отмечаются окклюзирующие дефекты наполнения нижнедолевых ветвей легочной артерии и разнокалиберные дефекты наполнения сегментарных ветвей артерии обоих легких, имеются косвенные признаки легочной гипертензии (рис. 6).
Больная проконсультирована акушером-гинекологом, акушерских показаний к прерыванию беременности не установлено.
Принято решение о выполнении экстренной тромбэмболэктомии из легочных артерий.
Особенности предоперационной подготовки и анестезиолого-перфузионного обеспечения операций
Предоперационная подготовка беременных женщин включала оценку функции сердечно-сосудистой системы и ее необходимую оптимизацию; коррекцию метаболических нарушений (водно-электролитного баланса, кислотно-основного состояния, газов крови); оценку и оптимизацию маточно-плацентарного кровотока (акушер-гинеколог); назначение глюкокортикоидов (дексаметазон 4–8 мг/сут). В предоперационной подготовке обязательно принимал участие акушер-гинеколог для оценки состояния беременной и плода. Во всех случаях перед операцией беременные женщины имели жизнеспособный плод.
Две пациентки поступили непосредственно в операционную, одна — в отделение реанимации и интенсивной терапии. Предоперационное состояние женщин оценивалось как крайне тяжелое — IV класс по классификации ASA.
Мониторинг состояния матери включал в первую очередь контроль за состоянием сердечно-сосудистой и дыхательной систем: исследовали ЭКГ в 6 отведениях, выполнялись инвазивное измерение АД и центрального венозного давления, по показаниям — измерение давления в легочной артерии, насыщения крови гемоглобином, концентрации CO2, дыхательного объема и минутного объема дыхания, давления в дыхательных путях, минимальной альвеолярной концентрации, комплаенса легких. У всех больных исследовали в процессе операции и в ближайшем послеоперационном периоде кислотно-основное состояние, газы крови, гемоглобин, гематокрит, активированное время свертывания, коагулограмму, электролиты, общий белок, лактат. В послеоперационном периоде дополнительно исследовали маркеры повреждения миокарда (СК МВ, СК), оценивали функцию почек и печени, кислородо-транспортную функцию крови. Мониторинг состояния плода включал кардиотокографию, позволяющую мониторировать ЧСС плода и измерение TOCO-датчиком сократительной активности матки.
Премедикацию, учитывая экстренность ситуации и нестабильную гемодинамику, не проводили.
Для индукции в анестезию во всех случаях была использована комбинация диазепама (0,10±0,01 мг/кг) и пропофола (2,0±0,4 мг/кг). Трахею интубировали на фоне миорелаксации панкурония бромидом (0,1–0,12 мг/кг). После индукции для предупреждения смещения матки размещали пациентку лежа на боку с поворотом влево на 15° при помощи клина под правым бедром или путем левого бокового наклона стола. Поддержание анестезии до ИК, во время перфузии и в послеперфузионном периоде осуществляли севофлураном (1–3 об.%), на травматичных этапах операции дробно вводили 50–100 мкг фентанила, общая доза которого не превышала 10 мкг/кг. Нервно-мышечный блок поддерживали дробным введением панкурония бромида по 2 мг до достижения общей дозы 0,2 мг/кг.
Изменения центральной гемодинамики при индукции в анестезию были незначительными и сопровождались относительной стабильностью показателей АД, центрального венозного давления, сердечного выброса. При дальнейшем течении доперфузионного периода отмечено достоверное снижение АДср, рост ЧСС, снижение сердечного и ударного индексов сердца. Однако данные изменения мы связываем не столько с кардиодепрессивным действием применяемых анестетиков, сколько со значительным нарушением внутрисердечной гемодинамики в связи с основным заболеванием на фоне хирургических манипуляций.
Перед началом ИК проводили гепаринизацию в дозе 2–3 мг/кг массы тела. ИК выполняли на аппаратах Stockert (Sorin Group Deutschland, Германия) с применением мембранных оксигенаторов Medtronic (Medtronic Inc., США). Во всех случаях использовали непульсирующий поток в режиме нормотермии. Все перфузии проводили с повышенной (до 2,8 л/мин/м2) объемной скоростью, что позволяло поддерживать среднее АД выше 80 мм рт. ст. При всех операциях использовали ультрагемофильтрацию.
При проведении нормотермических перфузий было отмечено увеличение концентрации кислорода как в артериальной, так и в венозной крови на 10–15% со снижением артериовенозной разницы по кислороду и возрастанием транспорта кислорода при несущественных изменениях коэффициента тканевой экстракции, что, безусловно, указывает на более благоприятный кислородный режим перфузии как для матери, так и для плода.
В постперфузионном периоде для стабилизации гемодинамики и при явлениях острой сердечной недостаточности (у двух больных) мы использовали препараты β-адреномиметического ряда (Допмин в дозе 3–5 мкг/кг/мин) в сочетании с нитратами и глюкокортикоидами (Дексазон 12–20 мг). Коррекцию свертывающей системы крови выполняли протамин-сульфатом под контролем активированного времени свертывания. Проводимая во время ИК ультрагемофильтрация позволила контролировать степень гемодилюции: в конце ИК гемоглобин составлял 105,0±8,1 г/л, а гематокрит — 28,7±5,6%. Кроме этого, осуществляли мероприятия по снижению интраоперационной кровопотери: общая кровопотеря не превышала 576,0±65,0 мл.
В послеоперационном периоде у всех больных проводили пролонгированную искусственную вентиляцию легких, ее продолжительность составила от 10 до 48 ч. Особое внимание уделялось адекватной коррекции послеоперационных нарушений сократимости миокарда и поддержанию адекватного уровня показателей кислородо-транспортной функции крови. Мы отказались от применения α-агонистов (Норадреналин, Мезатон) для инотропной стимуляции, использовали комбинации β-агонистов (допамин, добутамин) с вазодилататорами (нитроглицерин, изосорбитдинитрат).
Ведение больных в послеоперационном периоде осуществляли с обязательным привлечением акушера-гинеколога. С первых суток проводили комплекс мероприятий по профилактике прерывания беременности. С этой целью назначали спазмолитики, сернокислую магнезию и нестероидные противовоспалительные препараты (индометацин), токолитик Гинипрал, витамин Е.
Осложнения послеоперационного периода
Всем пациенткам выполнена открытая эмболэктомия из главных и долевых легочных артерий в условиях нормотермии на работающем сердце без пережатия аорты. В первом случае (у больной М., 25 лет) операция проводилась по жизненным показаниям через 3 ч от момента поступления с удалением крупных неоднородных по срокам формирования эмболов (рис. 7).

|
Рис. 7. Эмболы, удаленные из главных и долевых легочных артерий |
Послеоперационный период протекал гладко, на следующие сутки после операции отмечено восстановление нормальных характеристик доплерограммы кровотока в выводном отделе ПЖ в виде равнобедренного треугольника, уменьшение степени регургитации на трикуспидальном клапане до I степени, снижение среднего давления в легочной артерии до 29 мм рт. ст. (рис. 8). Сохранялось увеличение полости ПЖ (37 мм), правого предсердия (43 мм).

|
Рис. 8. ЭхоКГ пациентки М., 25 лет: PW-доплер: изменение формы кровотока в выходном отделе правого желудочка в послеоперационном периоде |
На 12-е сутки послеоперационного периода в удовлетворительном состоянии больная выписана на амбулаторное лечение. В отдаленном периоде (через 1 мес после операции) отмечена нормализация размеров полости ПЖ и правого предсердия.
В 37 нед беременности выполнено родоразрешение путем кесарева сечения по акушерским показаниям (рубец на матке), пациентка родила здоровую девочку.
Во втором случае пациентка Б., 41 год, оперирована через 2 ч от момента поступления, послеоперационный период также протекал гладко. На следующие сутки после операции отмечено восстановление нормальных характеристик доплерограммы кровотока в выводном отделе ПЖ в виде равнобедренного треугольника, уменьшение степени регургитации на трикуспидальном клапане до I степени, снижение среднего давления в легочной артерии до 34 мм рт. ст. Сохранялось увеличение полости ПЖ (41 мм), правого предсердия (47 мм).
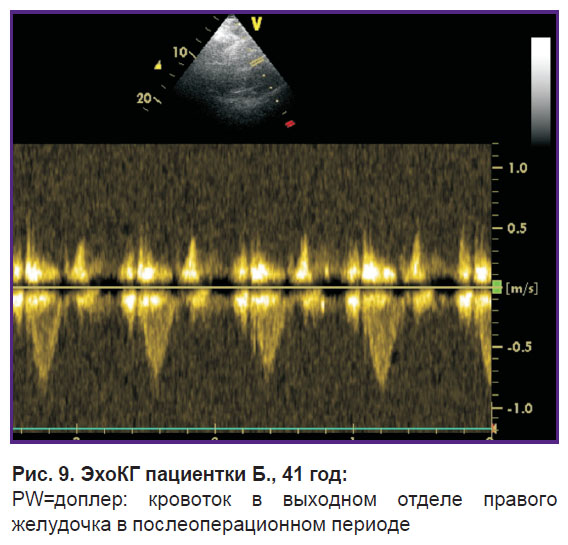
На 12-е сутки женщина выписана на амбулаторное лечение. В отдаленном периоде (через 1 мес после операции) отмечена нормализация всех параметров эхоКГ (рис. 9). В сроке 39 нед беременности родила здоровую девочку через естественные родовые пути.
|
Рис. 9. ЭхоКГ пациентки Б., 41 год:
PW=доплер: кровоток в выходном отделе правого желудочка в послеоперационном периоде |
В третьем случае пациентка С., 32 года, также оперирована сразу после поступления и определения локализации эмболов в легочных артериях с восстановлением хорошего ретроградного кровотока, однако в раннем послеоперационном периоде по данным КТ выявлена сформировавшаяся правосторонняя нижнедолевая инфаркт-пневмония, что стало одной из причин родоразрешения пациентки путем экстренного кесарева сечения. Послеоперационный период протекал без осложнений, и сама пациентка, и рожденный мальчик выписаны в удовлетворительном состоянии.
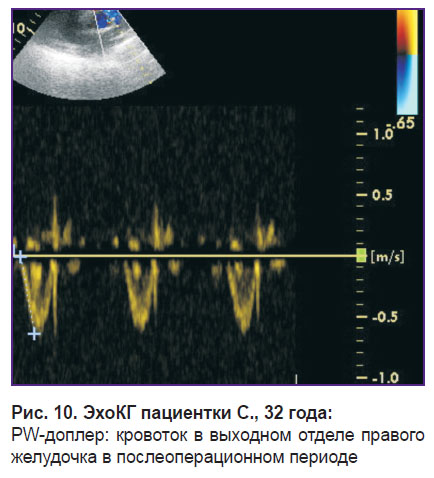
В отдаленном послеоперационном периоде у пациентки отмечено изменение формы кровотока в выводном отделе правого желудочка из двухфазного в монофазный, снижение среднего давления до 34 мм рт. ст. (рис. 10).
|
Рис. 10. ЭхоКГ пациентки С., 32 года:
PW-доплер: кровоток в выходном отделе правого желудочка в послеоперационном периоде |
Обсуждение результатов
Сложность задачи ведения беременных с ТЭЛА обусловлена особым медицинским и социальным статусом женщины, а также серьезными ограничениями, которые налагает на действия врача необходимость исключения или минимизации негативного влияния диагностических и лечебных манипуляций на плод. Приведенные примеры демонстрируют разные варианты клинического развития массивной критической ТЭЛА с выраженными угрожающими жизни гемодинамическими и дыхательными нарушениями. Общими для всех случаев являлись предшествующее ТЭЛА развитие тромбоза глубоких вен и необходимость проведения базисной антикоагулянтной терапии низкомолекулярным гепарином. Эти примеры также показали, что следует считать ошибочным мнение, будто у больных с тромботическим процессом в системе нижней полой вены достаточно ограничиться только антикоагулянтной терапией, не имея при этом представления о характере тромба и возможностях его перехода в эмболоопасные формы.
В большинстве случаев для подтверждения факта ТЭЛА и оценки объема эмболического поражения необходимо инструментальное обследование сосудистого русла легких.
Соответственно, важна предварительная клиническая оценка и ультразвуковое исследование с определением характера кровотока в легочной артерии и расчетом давления в ней, что позволяет обосновать необходимость МСКТ, связанной с лучевой нагрузкой на развивающийся плод в ранние сроки заболевания, поскольку последствия недиагностированной ТЭЛА могут быть фатальными [11].
Классическими признаками, описанными во множестве руководств и учебников, служат одышка, боли в грудной клетке, кровохарканье, синкопальные состояния, артериальная гипотензия, цианоз лица и верхней половины туловища. Однако сочетание «классических» признаков в клинической картине тромбоэмболии может быть названо «счастливым» случаем для диагностики, так как встречается менее чем у 10% больных [1]. Вероятность ТЭЛА повышается при наличии тромбоза глубоких вен и выраженной гипертензии малого круга кровообращения, верифицированных с помощью ультразвуковых методов. Объем поражения и локализация тромбоэмболов в легочном сосудистом русле, а также выраженность острой легочной гипертензии определяют показания и сроки проведения различных лечебных мероприятий. С особой тщательностью следует исследовать эти параметры у беременных.
Антикоагулянтная терапия — основа консервативного лечения ТЭЛА. В качестве средств антикоагулянтной терапии у беременных применяют нефракционированные низкомолекулярные гепарины, не проникающие через плаценту и не оказывающие отрицательного влияния на плод. При массивной критической ТЭЛА (объем поражения легочно-сосудистого русла более 70%) с развитием тяжелой сердечно-легочной недостаточности и высоким риском летального исхода рассматриваются возможности проведения тромболитической терапии, селективного внутриартериального тромболизиса с разрушением и аспирацией тромбоэмболов, а также открытой эмболэктомии. Публикации, анализирующие эти варианты лечения, в основном представляют собой серию описаний клинических наблюдений [12–14].
В связи с риском развития кровотечений тромболитическая терапия не является рутинным методом лечения массивной ТЭЛА. В работе [15] описано 13 случаев применения тромболитической терапии у беременных. Среди пациенток не было случаев материнской смерти, отмечены 4 кровотечения, 2 смерти плода и 5 преждевременных родов. Принято считать, что подобная частота осложнений намного ниже риска летального исхода при массивной критической легочной эмболии в отсутствие тромболизиса. Это служит «оправданием» для клинициста, выбравшего такую лечебную тактику [1].
В литературе встречаются упоминания успешных попыток проведения селективного тромболизиса с разрушением и аспирацией тромбоэмболов при массивной ТЭЛА во время беременности [16–18]. В этих сообщениях авторы подчеркивают преимущества такой тактики — уменьшение системных эффектов, предсказуемое удаление тромбоэмболов и снижение рисков для женщины и развивающегося плода. Однако нет однозначной уверенности в превосходстве катетерной тромболитической терапии перед проведением системного тромболизиса и гепаринотерапией. Транскатетерная тромбэктомия позволяет фрагментировать эмболический материал, который может в последующем с высокой вероятностью попасть в периферическую легочную систему и повысить риск легочной гипертензии и ее хронизации [19].
Хирургическое лечение легочной эмболии подразумевает полное удаление тромбоэмболов из сосудистого русла легких с нормализацией давления в легочной артерии и функции ПЖ.
Таким образом, на основании имеющихся данных трудно сделать вывод об оптимальном методе лечения массивной критической ТЭЛА у беременных. Авторами накоплен большой клинический опыт лечения ТЭЛА, в том числе выполнено более 150 операций у больных с острой и рецидивирующей обструкцией легочных артерий и высокой гипертензией малого круга. Анализ собственных данных (отсутствие летальности за последние 6 лет при более чем 120 эмболэктомиях), а также опыта российских и зарубежных коллег позволяет нам считать открытую эмболэктомию наиболее приемлемым методом лечения беременных, позволяющим не только сохранить жизнь женщине, но и пролонгировать беременность и родить здорового ребенка. Оптимальный вариант оперативного вмешательства — эмболэктомии из легочных артерий в условиях ИК на работающем сердце без пережатия аорты [19–21]. Несомненно, это требует проведения операции в условиях специализированного кардиохирургического стационара, врачами, обладающими большим опытом выполнения вмешательств на сердце.
Важное значение имеет положение беременной на операционном столе [22]. Так, для предупреждения смещения матки и развития аортокавальной компрессии целесообразно размещать пациентку лежа на боку с поворотом влево на 15° при помощи клина под правым бедром или левого бокового наклона стола. Такое положение на операционном столе должно быть придано для любой беременной со сроком более 20 нед с целью исключения ухудшения маточно-плацентарного кровотока [23]. При проведении всех операций мы использовали данное положение, что позволило избежать компрессии магистральных сосудов беременной маткой и тем самым поддержать адекватный маточно-плацентарный кровоток.
Связанные с беременностью изменения в функционировании органов приводят к изменению материнской фармакодинамики и фармакокинетики лекарственных препаратов [24]. Гемодилюция в начале ИК в дальнейшем изменяет фармакологию препарата и вызывает увеличенную вариабельность несвязанных концентраций препарата. Переход препарата через плаценту к плоду происходит согласно градиенту концентрации препарата от матери в фетальную циркуляцию и особенностей работы плацентарной мембраны. Препараты требуют более частого применения без изменения ежедневной дозировки. Все ингаляционные анестетики и большинство внутривенных анестезирующих препаратов являются высоко жирорастворимыми и свободно проникают через плаценту. Ингаляционные анестетики являются также мощными маточными релаксантами и способны уменьшать маточный кровоток. В наших исследованиях мы не отметили необходимости значимого увеличения дозировок применяемых препаратов для анестезии. Хотя считается, что большинство неблагоприятных материнских и эмбриональных результатов при операции на сердце во время беременности связано с эффектами ИК и состоянием сердечно-сосудистой системы матери, а не выбором препарата и дозы для анестезии [22].
По данным исследований, перфузия с высокой объемной скоростью, высоким перфузионным давлением, в нормотермическом режиме и, по возможности, короткая является наилучшей перфузионной стратегией для обеспечения адекватного плацентарного гомеостаза [22]. Использованная нами перфузионная тактика полностью соответствует данной стратегии: нормотермическое ИК, минимизация времени перфузии, поддержание высокой объемной скорости — 2,4 л/мин/м2 и среднего артериального давления — 70–75 мм рт. ст. Кроме того, отказ от применения кардиоплегии и выполнение операций на «бьющемся» сердце позволили не только поддерживать оптимальный уровень гемоглобина и гематокрита, но и обеспечили адекватную доставку кислорода тканям и плоду.
С 1970 по 2014 г. в доступной литературе мы нашли описание 13 случаев проведения эмболэктомии у беременных. Все пациентки имели массивную ТЭЛА с нарастанием легочно-сердечной недостаточности, что являлось показанием к операции [25]. Среди оперированных пациенток 2 погибли [26, 27], в 3 случаях произошла гибель плода [27–29]. Тем не менее мы согласны с мнением D.А. Cooley и соавт. [30] и J. Hajj-Chahine и соавт. [31], считающих, что только своевременная адекватная эмболэктомия из легочной артерии, возможная при ранней диагностике ТЭЛА, позволяет сохранить жизнь матери и пролонгировать беременность.
Заключение. Собственный опыт проведения трех успешных операций у беременных позволяет сформулировать следующие выводы. Хирургическое лечение тромбоэмболии легочных артерий у такой категории пациенток должно включать:
по возможности раннее диагностическое обследование пациенток с подозрением на тромбоэмболию легочных артерий, в которое должно входить ультразвуковое исследование с оценкой степени гемодинамических нарушений и МСКТ с точной верификацией местоположения эмболов в легочном русле;
выполнение операций на «бьющемся» сердце в условиях нормотермического искусственного кровообращения, отказ от проведения кардиоплегии, минимизацию времени перфузии, поддержание ее высокой объемной скорости — 2,4 л/мин/м2 и среднего артериального давления 70–75 мм рт. ст.;
максимально возможную дезоблитерацию легочных артерий с минимальной травматичностью и длительностью вмешательства на легочных сосудах.
Только при благоприятном течении послеоперационного периода с нормализацией давления в легочной артерии возможно пролонгирование беременности.
Финансирование исследования и конфликт интересов. Исследование не финансировалось какими-либо источниками, и конфликты интересов, связанные с данным исследованием, отсутствуют.
Литература
- Тромбоэмболия легочных артерий: как лечить и предотвращать. Под ред. Кириенко А.И., Чернявского А.М., Андрияшкина В.В. М: МИА; 2015; 280 с.
- Fukuda I., Taniguchi S., Fukui K., Minakawa M., Daitoku K., Suzuki Y. Improved outcome of surgical pulmonary embolectomy by aggressive intervention for critically ill patients. Ann Thorac Surg 2011; 91(3): 728–732, https://doi.org/10.1016/j.athoracsur.2010.10.086.
- Sareyyupoglu B., Greason K.L., Suri R.M., Keegan M.T., Dearani J.A., Sundt T.M. A more aggressive approach to emergency embolectomy for acute pulmonary embolism. Mayo Clin Proc 2010; 85(9): 785–790, https://doi.org/10.4065/mcp.2010.0250.
- Kadner A., Schmidli J., Schönhoff F., Krähenbühl E., Immer F., Carrel T., Eckstein F. Excellent outcome after surgical treatment of massive pulmonary embolism in critically ill patients. J Thorac Cardiovasc Surg 2008; 136(2): 448–451, https://doi.org/10.1016/j.jtcvs.2007.11.021.
- Amirghofran A.A., Emami Nia A., Javan R. Surgical embolectomy in acute massive pulmonary embolism. Asian Cardiovasc Thorac Ann 2007; 15(2): 149–153, https://doi.org/10.1177/021849230701500214.
- Leacche M., Unic D., Goldhaber S.Z., Rawn J.D., Aranki S.F., Couper G.S., Mihaljevic T., Rizzo R.J., Cohn L.H., Aklog L., Byrne J.G. Modern surgical treatment of massive pulmonary embolism: results in 47 consecutive patients after rapid diagnosis and aggressive surgical approach. J Thorac Cardiovasc Surg 2005; 129(5): 1018–1023, https://doi.org/10.1016/j.jtcvs.2004.10.023.
- Vohra H.A., Whistance R.N., Mattam K., Kaarne M., Haw M.P., Barlow C.W., Tsang G.M., Livesey S.A., Ohri S.K. Early and late clinical outcomes of pulmonary embolectomy for acute massive pulmonary embolism. Ann Thorac Surg 2010; 90(6): 1747–1752, https://doi.org/10.1016/j.athoracsur.2010.08.002.
- Konstantinov I.E., Saxena P., Koniuszko M.D., Alvarez J., Newman M.A. Acute massive pulmonary embolism with cardiopulmonary resuscitation: management and results. Tex Heart Inst J 2007; 34(1): 41–46.
- Goldhaber S.Z. Surgical pulmonary embolectomy: the resurrection of an almost discarded operation. Tex Heart Inst J 2013; 40(1): 5–8.
- Martin S.R., Foley M.R. Intensive care in obstetrics: an evidence-based review. Am J Obstet Gynecol 2006; 195(3): 673–689, https://doi.org/10.1016/j.ajog.2006.05.042.
- Kucher N., Rossi E., De Rosa M., Goldhaber S.Z. Massive pulmonary embolism. Circulation 2006; 113(4): 577–582, https://doi.org/10.1161/circulationaha.105.592592.
- Sato T., Kobatake R., Yoshioka R., Fuke S., Ikeda T., Saito H., Maekawa K., Hioka T. Massive pulmonary thromboembolism in pregnancy rescued using transcatheter thrombectomy. Int Heart J 2007; 48(2): 269–276, https://doi.org/10.1536/ihj.48.269.
- Torbicki A., Perrier A., Konstantinides S., Agnelli G., Galiè N., Pruszczyk P., Bengel F., Brady A.J., Ferreira D., Janssens U., Klepetko W., Mayer E., Remy-Jardin M., Bassand J.P.; ESC Committee for Practice Guidelines (CPG). Guidelines on the diagnosis and management of acute pulmonary embolism: the Task Force for the Diagnosis and Management of Acute Pulmonary Embolism of the European Society of Cardiology (ESC). Eur Heart J 2008; 29(18): 2276–2315, https://doi.org/10.1093/eurheartj/ehn310.
- Ahearn G.S., Hadjiliadis D., Govert J.A., Tapson V.F. Massive pulmonary embolism during pregnancy successfully treated with recombinant tissue plasminogen activator: a case report and review of treatment options. Arch Intern Med 2002; 162(11): 1221, https://doi.org/10.1001/archinte.162.11.1221.
- Te Raa G.D., Ribbert L.S.M., Snijder R.J., Biesma D.H. Treatment options in massive pulmonary embolism during pregnancy; a case-report and review of literature. Thromb Res 2009; 124(1): 1–5, https://doi.org/10.1016/j.thromres.2009.03.001.
- Weinberg L., Kay C., Liskaser F., Jones D., Tay S., Jaffe S., Seevanayagam S., Doolan L. Successful treatment of peripartum massive pulmonary embolism with extracorporeal membrane oxygenation and catheter-directed pulmonary thrombolytic therapy. Anaesth Intensive Care 2011; 39(3): 486–491.
- O’Keeffe S.A., McGrath A., Ryan J.M., Byrne B. Management of a massive pulmonary embolism in a pregnant patient with mechanical fragmentation followed by delayed catheter-directed thrombolysis in the early postpartum period. J Matern Fetal Neonatal Med 2008; 21(8): 591–594, http://dx.doi.org/10.1080/14767050802165604.
- Bechtel J.J., Mountford M.C., Ellinwood W.E. Massive pulmonary embolism in pregnancy treated with catheter fragmentation and local thrombolysis. Obstet Gynecol 2005; 106(5 Pt 2): 1158–1160.
- Dauphine C., Omari B. Pulmonary embolectomy for acute massive pulmonary embolism. Ann Thorac Surg 2005; 79(4): 1240–1244, https://doi.org/10.1016/j.athoracsur.2004.08.081.
- Nemirova S., Medvedev A., Pichugin V., Bhandari K. Surgical embolectomy in massive acute pulmonary embolism: our experience. Nepalese Heart Journal 2015; 12(2): 83, https://doi.org/10.3126/njh.v12i2.13387.
- Taniguchi S., Fukuda I., Minakawa M., Watanabe K., Daitoku K., Suzuki Y. Emergency pulmonary embolectomy during the second trimester of pregnancy: report of a case. Surg Today 2007; 38(1): 59–61, https://doi.org/10.1007/s00595-007-3570-0.
- Chandrasekhar S., Cook C.R., Collard C.D. Cardiac surgery in the parturient. Anesth Analg 2009; 108(3): 777–785, https://doi.org/10.1213/ane.0b013e31819367aa.
- John A.S., Gurley F., Schaff H.V., Warnes C.A., Phillips S.D., Arendt K.W., Abel M.D., Rose C.H., Connolly H.M. Cardiopulmonary bypass during pregnancy. Ann Thorac Surg 2011; 91(4): 1191–1196, https://doi.org/10.1016/j.athoracsur.2010.11.037. Qasqas S.A., McPherson C., Frishman W.H., Elkayam U. Cardiovascular pharmacotherapeutic considerations during pregnancy and lactation. Cardiol Rev 2004; 12(5): 240–261, https://doi.org/10.1097/01.crd.0000102421.89332.43.
- Saeed G., Möller M., Neuzner J., Gradaus R., Stein W., Langebrake U., Dimpfl T., Matin M., Peivandi A. Emergent surgical pulmonary embolectomy in a pregnant woman: case report and literature review. Tex Heart Inst J 2014; 41(2): 188–194, https://doi.org/10.14503/thij-12-2692.
- Girz B.A., Heiselman D.E. Fatal intrapartum pulmonary embolus during tocolysis. Am J Obstet Gynecol 1988; 158(1): 145–146, https://doi.org/10.1016/0002-9378(88)90798-3.
- Lau G. A case of sudden maternal death associated with resuscitative liver injury. Forensic Sci Int 1994; 67(2): 127–132, https://doi.org/10.1016/0379-0738(94)90327-1.
- Marcinkevicius A., Sirvydis V., Triponis V., Baublys A., Martinkenas G., Matulionis A. Pulmonary embolectomy during pregnancy. J Cardiovasc Surg (Torino) 1970; 11(5): 355–338.
- Duff P., Greene V.P. Pregnancy complicated by solid-papillary epithelial tumor of the pancreas, pulmonary embolism, and pulmonary embolectomy. Am J Obstet Gynecol 1985; 152(1): 80–81, https://doi.org/10.1016/s0002-9378(85)80182-4.
- Cooley D.A., Bell A.C. Jr., Alexander J.K. Acute massive pulmonary embolism. Successful surgical treatment using temporary cardiopulmonary bypass. JAMA 1961; 177(5): 283–286, https://doi.org/10.1001/jama.1961.03040310001001.
- Hajj-Chahine J., Jayle C., Tomasi J., Corbi P. Successful surgical management of massive pulmonary embolism during the second trimester in a parturient with heparin-induced thrombocytopenia. Interact Cardiovasc Thorac Surg 2010; 11(5): 679–681, https://doi.org/10.1510/icvts.2010.247460.