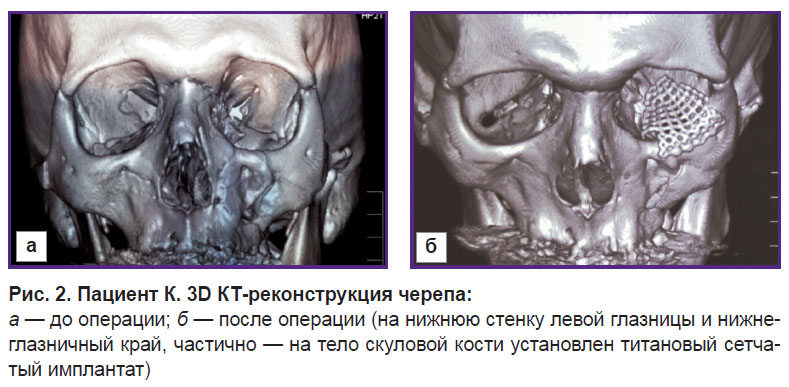
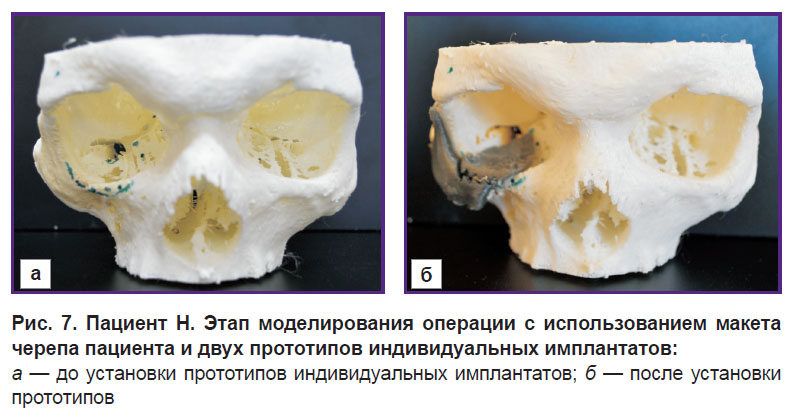
Цифровые технологии в хирургическом лечении посттравматических деформаций скулоорбитального комплекса
Цель исследования — определить эффективность использования цифровых технологий у пациентов с посттравматическими деформациями скулоорбитального комплекса (СОК) путем сравнения результатов с традиционными методами хирургического лечения.
Материалы и методы. Обобщен опыт хирургического лечения 231 пострадавшего с повреждениями СОК на клинических базах Приволжского исследовательского медицинского университета (Н. Новгород) в 2011–2019 гг. С посттравматической деформацией СОК пролечено 44,2% (102/231) пациентов, в том числе с посттравматическими дефектами и деформациями нижней стенки глазницы — 38,2% (39/102).
На основании клинико-рентгенологического планирования операций было выделено две группы исследуемых: в 1-ю группу вошли пациенты, которым не выполнялось виртуальное планирование операции, — 54,9% (56/102) случаев, во 2-ю группу — пациенты, которым виртуальное планирование проводилось (45,1% (46/102) случаев). 22 и 17 пациентов были с деформациями глазниц — в 1-й и 2-й группах соответственно.
Результаты. Оптимальное восстановление анатомии СОК у пациентов 1-й группы отмечено в 75% (42/56) случаев, у пациентов 2-й группы — в 93,5% (43/46) случаев. При реконструкции нижней стенки глазницы у пациентов 1-й группы были достигнуты успешные результаты в 68,2% (15/22) случаев, во 2-й группе — в 88,2% (15/17), в остальных случаях отмечены различные осложнения.
На основании анализа результатов хирургического лечения разработан персонифицированный подход к изготовлению имплантатов скуловой кости и нижней стенки глазницы с помощью технологий компьютерного моделирования и 3D-печати.
Заключение. Применение цифровых технологий в хирургическом лечении посттравматических деформаций СОК в отличие от использования традиционных методик позволяет избежать проблемных вопросов позиционирования имплантата и развития осложнений при реконструкции, значительно снизить травматичность операции и ускорить реабилитацию пациентов.
Введение
Одной из главных задач хирурга, выполняющего операции на средней зоне лица, является повышение эффективности лечения и улучшение качества жизни пациента после перенесенной травмы. Отсроченная и неспланированная операция или ее отсутствие при травме скулоорбитального комплекса (СОК), особенно при выраженных смещениях отломков, может приводить к усугублению повреждений глазницы, глазного яблока, глазодвигательных мышц, орбитальной клетчатки и зрительного нерва. В результате развиваются стойкие посттравматические деформации скуловой области и глазницы, функциональные и эстетические нарушения, обрекающие пациентов на длительное многоэтапное лечение [1–3]. По разным данным [2–4], на долю переломов скуловой кости приходится от 20 до 37,5% всех повреждений костей лицевого скелета, причем из этих переломов 35–40% составляют повреждения нижней стенки глазницы.
При переломах глазницы происходит нарушение ее анатомии и физиологии, в результате чего в раннем посттравматическом периоде развиваются офтальмологические и неврологические расстройства (деформация и изменение объема глазницы, диплопия, ограничение подвижности глаза, потеря или нарушение зрения, гипостезия по ходу подглазничного нерва). Затем при отсутствии лечения формируется гипо- и энофтальм, прогрессируют диплопия и косметические нарушения [4–6]. Перечисленные изменения позволяют считать повреждения СОК наиболее сложными в плане реконструкции и восстановления нарушенных функций.
До настоящего времени не разработан оптимальный алгоритм лечения пациентов с переломами и деформациями СОК: применяются различные оперативные доступы и методики, используются разнообразные материалы и имплантаты для реконструкции скуловой кости и нижней стенки глазницы [5, 7–9]. «Золотым стандартом» хирургического лечения повреждений скуловой кости и стенок глазницы по-прежнему является применение аутокости, а также широко используются металлические пластины или сетка и полимерные имплантаты [2, 3, 8–12]. Все это относится к традиционным (классическим) хирургическим методам лечения пациентов с травмой скулоглазничного комплекса, которые имеют свои достоинства и недостатки. К недостаткам следует отнести увеличение длительности операции при заборе аутокости или интраоперационном моделировании металлических и полимерных протезов; резорбцию аутокости; гипер- или гипокоррекцию скуловой зоны; сохранение гипофтальма или энофтальма; атрофию орбитальной клетчатки; развитие металлоза или прорезывание титановых имплантатов; сохранение функциональных и косметических проблем [3, 6, 12–14].
Первое десятилетие XXI в. характеризуется активным внедрением цифровых технологий в работу челюстно-лицевых хирургов. Прежде всего это связано с появлением новых методов компьютерного моделирования, повышением доступности и снижением стоимости оборудования для визуализации данных КТ и МРТ, развитием аддитивного производства индивидуальных имплантатов с использованием 3D-печати для восстановления анатомии костных структур лицевого скелета [3, 15–18]. Тщательная предоперационная подготовка пациента, виртуальное планирование вмешательства, изготовление персонифицированных имплантатов позволяют выполнять реконструктивно-пластические операции на скулоглазничном комплексе с применением минимально-инвазивных технологий [17, 18].
Цель исследования — определить эффективность использования цифровых технологий у пациентов с посттравматическими деформациями скулоорбитального комплекса путем сравнения результатов с традиционными методами хирургического лечения.
Материалы и методы
Обобщен опыт хирургического лечения 231 пострадавшего с повреждениями СОК на клинических базах кафедры хирургической стоматологии и челюстно-лицевой хирургии с курсом пластической хирургии Приволжского исследовательского медицинского университета (Н. Новгород) в 2011–2019 гг.: в Университетской клинике, в отделениях челюстно-лицевой хирургии Нижегородской областной клинической больницы им. Н.А. Семашко и клинической больницы №3 Приволжского окружного медицинского центра ФМБА России. Средний возраст пациентов составил 33,6 года (от 20 до 60 лет). Среди них было 80% (188/231) мужчин и 20% (43/231) женщин. Письменные согласия пациентов на использование данных и публикацию фотографий имеются в историях болезней.
Сроки хирургического лечения были разными: в 1-е сутки после травмы прооперированы 1,7% (4/231) пациентов, с 7-х по 14-е сутки — 19,5% (45/231), с 15-х по 30-е сутки — 33,8% (78/231), через 1–2 мес — 27,3% (63/231), спустя 4 мес — 12,5% (29/231), через 6 мес — 4,3% (10/231) больных. Из всех исследуемых с посттравматической деформацией СОК пролечено 44,2% (102/231) пациентов, в том числе с посттравматическими дефектами и деформациями нижней стенки глазницы — 38,2% (39/102). У всех больных имелась деформация скуловой зоны и орбиты, гипофтальм и/или энофтальм, диплопия различного характера.
Всем пациентам проводили стандартное клиническое обследование и мультиспиральную компьютерную томографию (МСКТ) черепа в аксиальной, сагиттальной и фронтальной плоскостях с построением 3D КТ-моделей до и после операции. Врачом-офтальмологом выполнялось обследование пациентов до и после операции: через 1, 3 и 6 мес, которое включало визометрию, тонометрию, офтальмоскопию и биомикроскопию. Аксиальное положение глаза в орбите (эно- или экзофтальм) определяли с помощью экзофтальмометра Hertel (Inami, Япония). Гипофтальм оценивали относительно горизонтальной линии, проходящей через центр зрачка здорового глаза. С помощью сферопериметра Гольдмана определяли характер и размер зоны бинокулярного двоения [3]. Данные перечисленной диагностики были крайне необходимы при планировании хирургического лечения и оценке результатов лечения орбиты [1, 3, 6].
Классические операции по устранению посттравматической деформации скуловой области (остеотомия и остеосинтез) выполнены в 85,3% (87/102) случаев, в 14,7% (15/102) проводили только контурную пластику скуловой области имплантатами и реконструкцию нижней стенки глазницы. При посттравматических дефектах и деформациях орбиты для реконструкции глазницы использовали в 38,4% (15/39) случаев полимерные имплантаты «Реперен» (Россия), в 30,8% (12/39) случаев — металлические имплантаты «Конмет» (Россия) и также в 30,8% (12/39) случаев — имплантаты Synthes (Швейцария) стандартных типоразмеров [12–14, 16].
Для оценки роли рентгенологического планирования операций по устранению посттравматической деформации СОК было сформировано две группы пациентов. В 1-й группе (54,9% (56/102) случаев) виртуальное планирование операции не выполняли. Во 2-ю группу (45,1% (46/102) случаев) вошли пациенты, которым проводили виртуальное планирование операции. 22 и 17 пациентов были с деформациями глазниц — в 1-й и 2-й группах соответственно.
Виртуальное планирование проводили с использованием многоплоскостных реформаций КТ-изображений и построением трехмерных реконструкций. Мы изучали характер посттравматической деформации СОК: определяли степень смещения костных структур и размер костного дефекта нижней стенки глазницы; выявляли сопутствующие изменения в орбите; измеряли линейные размеры поврежденной и неповрежденной глазниц; оценивали степень смещения глазного яблока; определяли оптимальное положение будущего имплантата.
В послеоперационном периоде всем пациентам назначали стандартное медикаментозное лечение. Швы снимали на 5–7-е сутки после операции. Контрольный осмотр осуществляли через 1, 3, 6 мес и 1, 3 года, 5 лет после операции.
Статистическая обработка цифрового материала результатов исследования была проведена с использованием программы Microsoft Office Excel 2010, пакета программ Statistica 10.0 (StatSoft, Inc.) в соответствии с общепринятыми современными методами статистического анализа. Непараметрический метод — тест Манна–Уитни (U) для несвязанных групп — использовали в тех случаях, когда значения анализируемых данных не соответствовали нормальному закону распределения.
Результаты и обсуждение
На основании проведенного анализа результатов хирургического лечения 231 пациента с повреждениями скулоглазничного комплекса была выделена группа больных (n=102), которым требовалось хирургическое лечение по поводу посттравматической деформации СОК, из них 39 человек нуждались в реконструкции нижней стенки глазницы. Оценка результатов хирургического лечения у пациентов с посттравматической деформацией проводилась на основании клинико-рентгенологических данных и анализа послеоперационных осложнений.
Оптимальное восстановление анатомии СОК отмечено у 75,0% (42/56) пациентов 1-й группы (без виртуального планирования операции) и у 93,5% (43/46) пациентов 2-й группы (рис. 1–4). После реконструкции нижней стенки глазницы успешные результаты были у 68,2% (15/22) пациентов 1-й группы и у 88,2% (15/17) — 2-й группы, в остальных случаях отмечены различные осложнения.
|
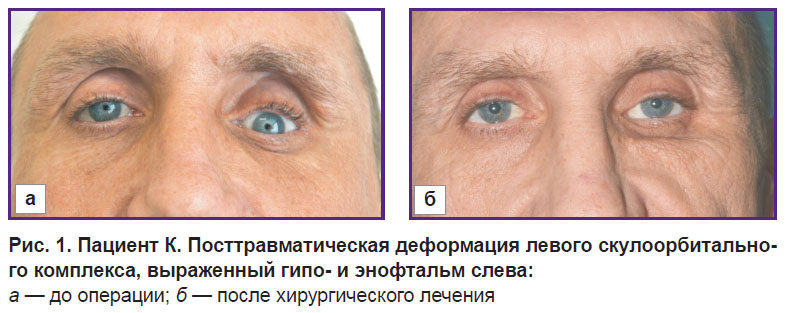
Рис. 1. Пациент К. Посттравматическая деформация левого скулоорбитального комплекса, выраженный гипо- и энофтальм слева:
а — до операции; б — после хирургического лечения |
|
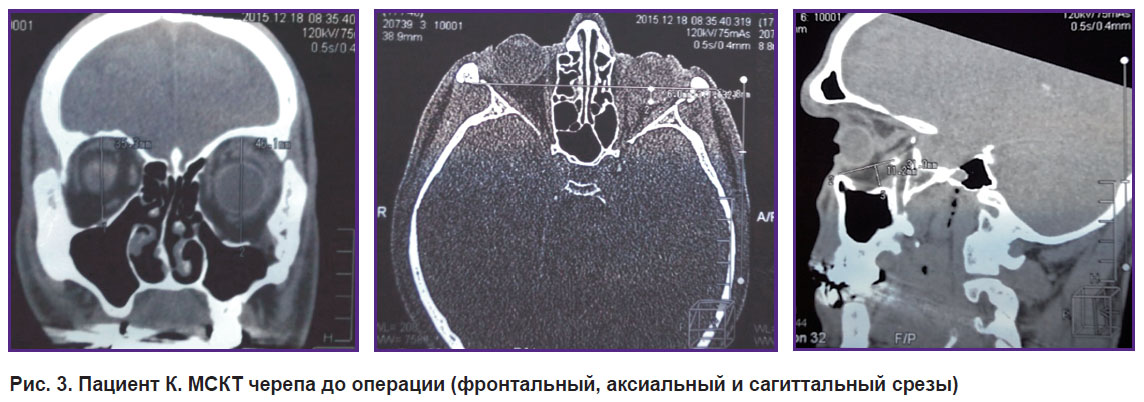
Рис. 3. Пациент К. МСКТ черепа до операции (фронтальный, аксиальный и сагиттальный срезы) |
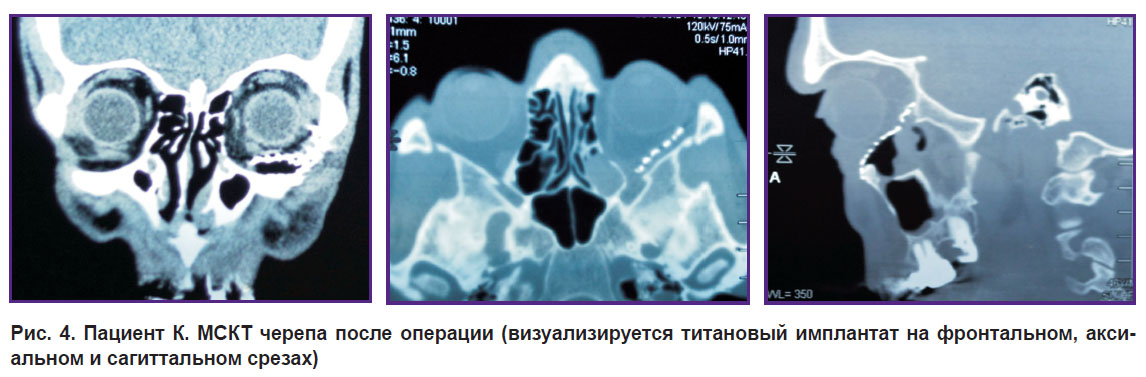
|
Рис. 4. Пациент К. МСКТ черепа после операции (визуализируется титановый имплантат на фронтальном, аксиальном и сагиттальном срезах) |
В отдаленном послеоперационном периоде у 3 из 22 пациентов 1-й группы отмечены гипофтальм и энофтальм (3–4 мм) и у 1 человека — гипофтальм (5 мм). При анализе МСКТ глазниц этих пациентов обнаружено пролабирование дистального края имплантата в сторону верхнечелюстной пазухи, что явилось причиной повторной операции.
У 1 из 17 пациентов 2-й группы отмечен гипофтальм и энофтальм (3–4 мм) в отдаленном периоде, что также обусловило повторную операцию. Энофтальм в пределах 1–2 мм не причинял дискомфорта пациентам обеих групп, хирургического лечения не проводилось.
Через 3 мес после вмешательства диплопия сохранялась у 4 из 22 пациентов 1-й группы и у 2 из 17 пациентов 2-й группы. Восстановление бинокулярного зрения у них продолжалось до 6 мес, что было связано с характером травмы и сроками хирургического лечения.
Степень выраженности гипофтальма и энофтальма различной степени представлена у пациентов с посттравматической деформацией глазницы (см. таблицу).
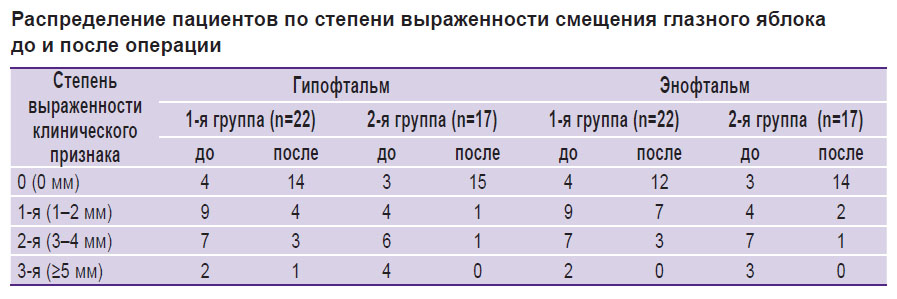
|
Распределение пациентов по степени выраженности смещения глазного яблока до и после операции |
При анализе отдаленных результатов лечения нами не отмечено воспалительных изменений вокруг имплантатов, а также потери зрения. Гиперофтальм наблюдался у 1 из 22 пациентов 1-й группы и у 1 из 17 пациентов 2-й группы, причем это были пациенты с выраженным посттравматическим гипофтальмом и энофтальмом. Во время операции у них проводилась умеренная гиперкоррекция по вертикали металлическими имплантатами с целью стабилизации положения глазного яблока в отдаленном периоде. Нормализация положения глаза по вертикали у пациентов произошла через 3 мес после реабилитации.
Смещение имплантата отмечено у 2 пациентов из 1-й группы спустя 6 мес после операции. Данное осложнение было обусловлено наличием обширного дефекта нижней стенки орбиты, рубцовыми изменениями орбитальной клетчатки и смещением полимерного имплантата вследствие рубцевания тканей в верхнечелюстную пазуху. Пациентам потребовалось повторное хирургическое вмешательство в связи с развитием прогрессирующей диплопии. Анализ причин смещения имплантата показал погрешности в планировании операции и в выборе видов и размеров имплантата, который не обеспечил достаточного перекрытия костного дефекта и жесткости опоры в дистальной зоне. Смещения имплантатов в сторону нижнего века не отмечено, так как все используемые полимерные и металлические конструкции стабильно фиксировались микровинтами к подлежащей кости.
В нашем исследовании усовершенствована методика анализа диагностических изображений при лучевом обследовании пациентов с травмой и разработан персонифицированный подход к изготовлению имплантатов. На практике технология была апробирована пока у 2 пациентов с выраженной посттравматической деформацией СОК, обусловленной смещением отломков и наличием обширных костных дефектов нижней стенки глазницы. Оперативное вмешательство выполнено с использованием двух индивидуальных имплантатов скуловой кости и нижней стенки глазницы, изготовленных с помощью технологий компьютерного моделирования и 3D-печати.
Применение стандартных имплантатов у данных пациентов было сопряжено с высоким риском их прецизионного несоответствия объемным параметрам костных дефектов; выраженного смещения отломков и деформации, обусловленной давностью травмы; возможной потери коррекции в послеоперационном периоде; сохранения диплопии и энофтальма (рис. 5).
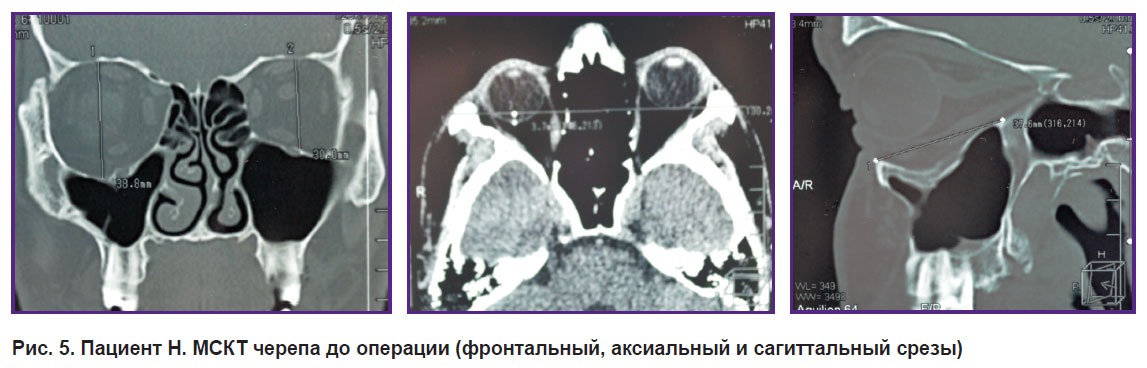
|
Рис. 5. Пациент Н. МСКТ черепа до операции (фронтальный, аксиальный и сагиттальный срезы) |
Для планирования хирургической реконструкции скулоглазничного комплекса были использованы современные цифровые технологии, позволяющие вычислить размеры дефектов и деформаций, рассчитать их объемные параметры и определить форму будущих имплантатов:
на первом этапе по данным МСКТ головы пациента в программном обеспечении 3D Slicer создавали компьютерную 3D-модель лицевого скелета;
на втором этапе в программном обеспечении Autodesk Meshmixer выполняли гибридное параметрическое моделирование, коррекцию деформации, замещение костных дефектов с использованием «зеркальной копии» неповрежденной контралатеральной стороны черепа;
на третьем этапе с целью последующего изготовления индивидуальных имплантатов были созданы их трехмерные модели и выполнена топологическая оптимизация (рис. 6).
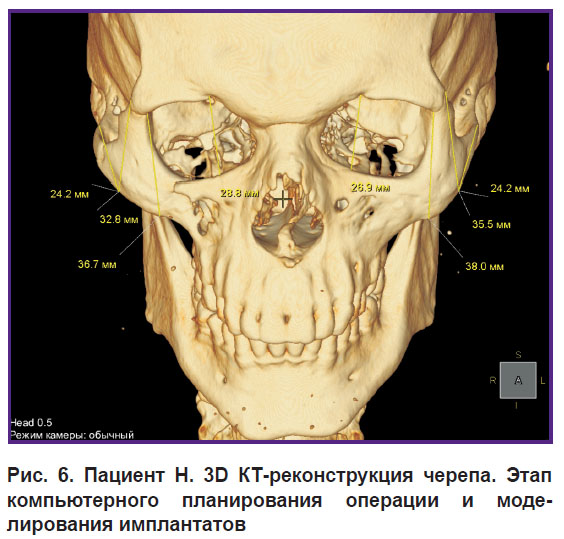
|
Рис. 6. Пациент Н. 3D КТ-реконструкция черепа. Этап компьютерного планирования операции и моделирования имплантатов |
Имплантат для реконструкции скуловой кости моделировали с учетом характера посттравматической деформации скуловой зоны, декомпрессии подглазничного нерва и с обязательным нанесением опорных пунктов для соединения с глазничным имплантатом. Его толщина в зависимости от зоны реконструкции варьировала от 0,1 до 0,8 мм. Имплантат для реконструкции нижней стенки глазницы полностью перекрывал дефект кости, опирался дистально на орбитальное возвышение и имел необходимую толщину для устранения энофтальма. Затем производили 3D-печать макета черепа и двух прототипов индивидуальных имплантатов. После этого с их помощью выполняли моделирование операции с использованием стандартного инструментария (рис. 7).
Далее на основе подготовленных прототипов индивидуальных имплантатов ф. «Экофлон» (С.-Петербург) были изготовлены имплантаты из политетрафторэтилена. При оперативном вмешательстве эти имплантаты фиксировали к подлежащим костным структурам титановыми микровинтами (рис. 8).
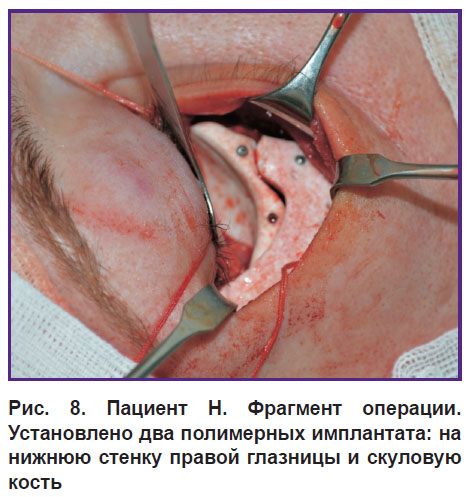
|
Рис. 8. Пациент Н. Фрагмент операции. Установлено два полимерных имплантата: на нижнюю стенку правой глазницы и скуловую кость |
Послеоперационный период протекал без особенностей. Все имплантаты хорошо интегрировались с тканями, нагноения и их отторжения не наблюдалось (рис. 9, 10).
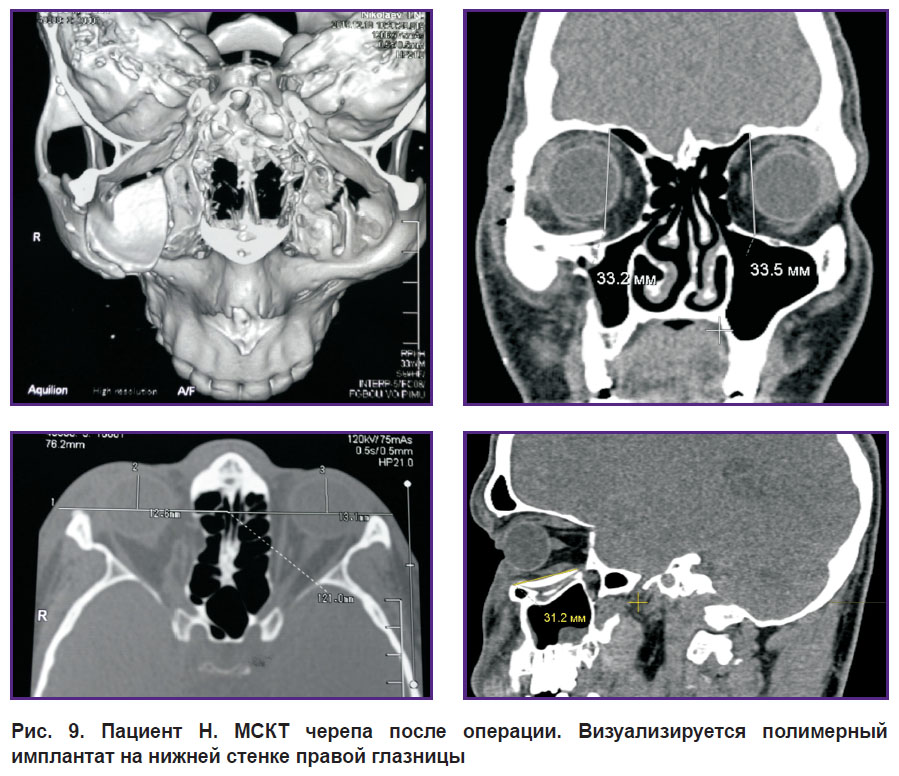
|
Рис. 9. Пациент Н. МСКТ черепа после операции. Визуализируется полимерный имплантат на нижней стенке правой глазницы |
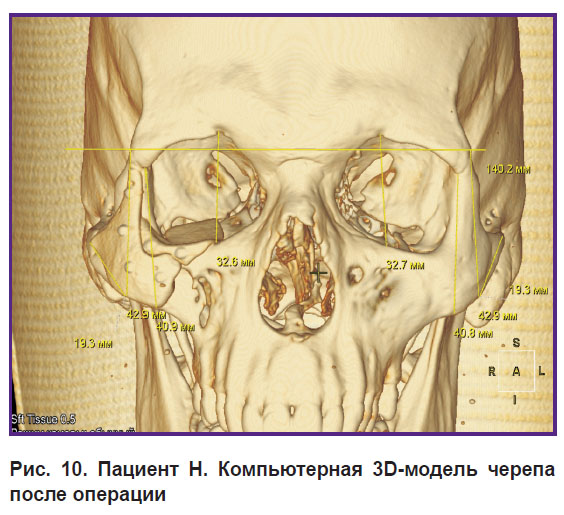
|
Рис. 10. Пациент Н. Компьютерная 3D-модель черепа после операции |
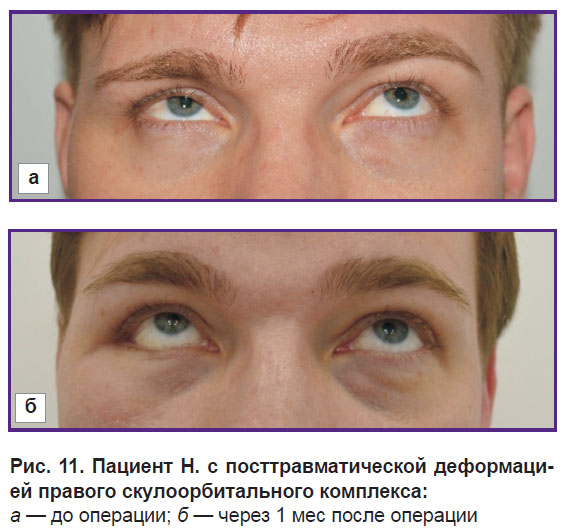
Использование в оперативном лечении пациентов цифровых технологий позволило оптимально устранить посттравматические деформации СОК, повысить точность реконструкции нижней стенки глазницы, снизить продолжительность вмешательства и его объем, получить прогнозируемый результат (рис. 11).
|
Рис. 11. Пациент Н. с посттравматической деформацией правого скулоорбитального комплекса:
а — до операции; б — через 1 мес после операции |
Заключение
Применение цифровых технологий в хирургическом лечении посттравматических деформаций скулоорбитального комплекса по сравнению с использованием традиционных методик позволяет избежать проблемных вопросов позиционирования имплантата и развития осложнений при реконструкции, значительно снизить травматичность операции и ускорить реабилитацию пациентов.
Финансирование исследования. Работа не получала финансовой поддержки.
Конфликт интересов отсутствует.
Литература
- Гундорова Р.А., Нероев В.В., Кашникова В.В. Травмы глаза. М: ГЭОТАР-Медиа; 2009.
- Дурново Е.А., Хомутинникова Н.Е., Мишина Н.В., Трофимов О.А. Особенности реконструкции стенок орбиты при лечении травматических повреждений лицевого скелета. Медицинский альманах 2013; 5(29): 159–161.
- Николаенко В.П., Астахов Ю.С. Орбитальные переломы. СПб: Эко-вектор; 2012; 436 с.
- Scolozzi P., Jacquier P., Courvoisier D.S. Can clinical findings predict orbital fractures and treatment decisions in patients with orbital trauma? Derivation of a simple clinical model. J Craniofac Surg 2017; 28(7): e661–e667, https://doi.org/10.1097/scs.0000000000003823.
- Ko M.J., Morris C.K., Kim J.W., Lad S.P., Arrigo R.T., Lad E.M. Orbital fractures: national inpatient trends and complications. Ophthalmic Plast Reconstr Surg 2013; 29(4): 298–303, https://doi.org/10.1097/IOP.0b013e318295f91d.
- Груша Я.О. Современные аспекты реконструктивной хирургии при травмах орбиты. Вестник офтальмологии 2014; 130(6): 50–55.
- Луцевич Е.Э., Альхумиди K. Современные аспекты диагностики и лечения переломов орбиты. Вестник офтальмологии 2013; 129(6): 89–95.
- Strong E.B. Orbital fractures: pathophysiology and implant materials for orbital reconstruction. Facial Plast Surg 2014; 30(5): 509–517, https://doi.org/10.1055/s-0034-1394099.
- Бакушев А.П., Сиволапов К.А. Хирургическое лечение пациентов с изолированными переломами стенок глазницы. Офтальмология 2015; 12(3): 48–52.
- Еолчиян C.А., Катаев М.Г., Карнаухова А.В. Устранение функциональных и эстетических нарушений при хирургическом лечении посттравматических дефектов и деформаций орбиты и периорбитальной области. Эстетическая медицина 2012; 11(4): 543–554.
- Митрошенков П.Н. Сравнительная оценка эффективности пластики тотальных и субтотальных дефектов верхней и средней зон лица с использованием перфорированных экранов из титана и костных аутотрансплантатов. Анналы пластической, реконструктивной и эстетической хирургии 2007; 4: 32–45.
- Хомутинникова Н.Е., Дурново Е.А., Мишина Н.В., Высельцева Ю.В. Ближайшие и отдаленные результаты лечения пациентов с переломами нижней стенки орбиты. Стоматология 2018; 97(5): 54–58, https://doi.org/10.17116/stomat20189705154.
- Clauser L., Galiè M., Pagliaro F., Tieghi R. Posttraumatic enophthalmos: etiology, principles of reconstruction, and correction. J Craniofac Surg 2008; 19(2): 351–359, https://doi.org/10.1097/SCS.0b013e3180534361.
- Груша О.В., Груша Я.О. 500 пластик орбиты: анализ осложнений. Вестник офтальмологии 2006; 122(1): 22–24.
- Лежнев Д.А., Давыдов Д.В., Костенко Д.И. Возможности современных томографических технологий в диагностике травм и посттравматических деформаций средней зоны лица. Вестник рентгенологии и радиологии 2013; 5: 005-008.
- Селезнев В.А, Буцан С.Б., Йигиталиев Ш.Н., Хохлачев С.Б., Ходячий А.Е., Черненький М.М. Виртуальное планирование костно-реконструктивных операций глазницы. Российский электронный журнал лучевой диагностики 2018; 8(3): 128–148.
- Карякин Н.Н., Горбатов Р.О. 3D-печать в медицине. М: ГЭОТАР-Медиа; 2019; 240 с., https://doi.org/10.33029/9704-5163-2-PRI-2019-1-240.
- Хассан М.А., Ховрин А.А., Митрошенков П.Н., Кантемиров О.И., Щербовских А.Е. Трехмерное моделирование рентгенологического изображения лицевого скелета в реконструктивной хирургии дефектов лица. Голова и шея 2017; 1: 13–17.