Исследование биомеханики створчатого аппарата протеза клапана сердца методом численного моделирования
Цель исследования — с помощью метода численного моделирования, воспроизводящего качественные и количественные результаты стендовых испытаний, исследовать комплексную биомеханику протеза клапана аорты и проанализировать влияние подвижности каркаса на напряженно-деформированное состояние и геометрию створчатого аппарата клапана.
Материалы и методы. В качестве объекта исследования использован коммерческий биопротез клапана «ЮниЛайн» («НеоКор», Россия), трехмерная сетка которого была получена на основе компьютерной микротомографии, с последующим анализом его напряженно-деформированного состояния в цикле «систола–диастола» методом конечных элементов в среде Abaqus/CAE. Моделирование было валидировано на основе сравнения результатов численного моделирования со стендовыми на гидродинамическом стенде ViVitro Labs (ViVitro Labs Inc., Канада).
Результаты. Метод моделирования имитации подвижности комиссуральных стоек за счет включения в расчет эластичных коннекторов регулируемой жесткости позволил воспроизвести качественные эффекты работы створок клапана, наблюдаемые в стендовом эксперименте. Площадь отверстия биопротеза в систолическую фазу соответствовала значениям, полученным на стенде, на протяжении всего цикла «систола–диастола». Анализ напряженно-деформированного состояния продемонстрировал принципиальное различие в распределении полей напряжения по Мизесу в зависимости от постановки численного эксперимента: концентрацию высоких амплитуд в области комиссуральных стоек и в области центральной части свободного края. Тем не менее количественно максимальные значения напряжения достигали 0,850–0,907 МПа (в среднем — 0,141–0,156 МПа), что ниже предела прочности биологического материала.
Заключение. Выполненное исследование с учетом проведенной валидации позволяет заключить, что адекватные результаты моделирования биомеханики створчатого аппарата биопротеза клапана сердца на основе метода конечных элементов могут быть достигнуты за счет использования модели высокого разрешения с наложением эластичных коннекторов в зоне комиссуральных стоек. Учет подвижности стоек каркаса протеза клапана сердца является определяющим в отношении конечной геометрии створчатого аппарата и может выступать негативным фактором в случае высокоэластичного материала створчатого аппарата. Представленный метод моделирования может быть использован для оптимизации геометрии створчатого аппарата протезов клапанов сердца с позиции оценки распределения напряженно-деформированного состояния.
Введение
В современной медицинской науке активно применяются численные методы моделирования работы биопротезов клапанов сердца на этапе их проектирования и оптимизации как высоко зарекомендовавшие себя инструменты глубокого инженерного анализа [1–4]. Основной мотивацией in silico исследований является увеличение сроков службы протезов [5, 6] в условиях длительной нагрузки в организме реципиента и повышение гемодинамической эффективности протезов [1, 2, 7]. В литературе показана прямая взаимосвязь развития патологической минерализации и усталостного разрушения створчатого аппарата от значений амплитуд напряжений и деформации в его материале [8–11]. Поэтому оптимизация распределения данных характеристик способна увеличить усталостную прочность и повысить сроки развития дисфункции, которые сегодня составляют 10–15 лет [12–14]. Кроме того, моделирование in silico позволяет выявить потенциал для улучшения гемодинамических характеристик протезов (повышения площади открытия, снижения транспротезного градиента, уменьшения объема регургитации) за счет возможности рассчитывать работу разнообразных геометрий створчатого аппарата до этапа натурного прототипирования [1, 7]. Результаты оптимизации и понимание взаимосвязи в системе «дизайн–эффект» являются основой для появления новых, более эффективных моделей биопротезов [15] и, в конечном счете, для улучшения результатов процедуры вмешательства на клапанах сердца с позиции клинических показателей.
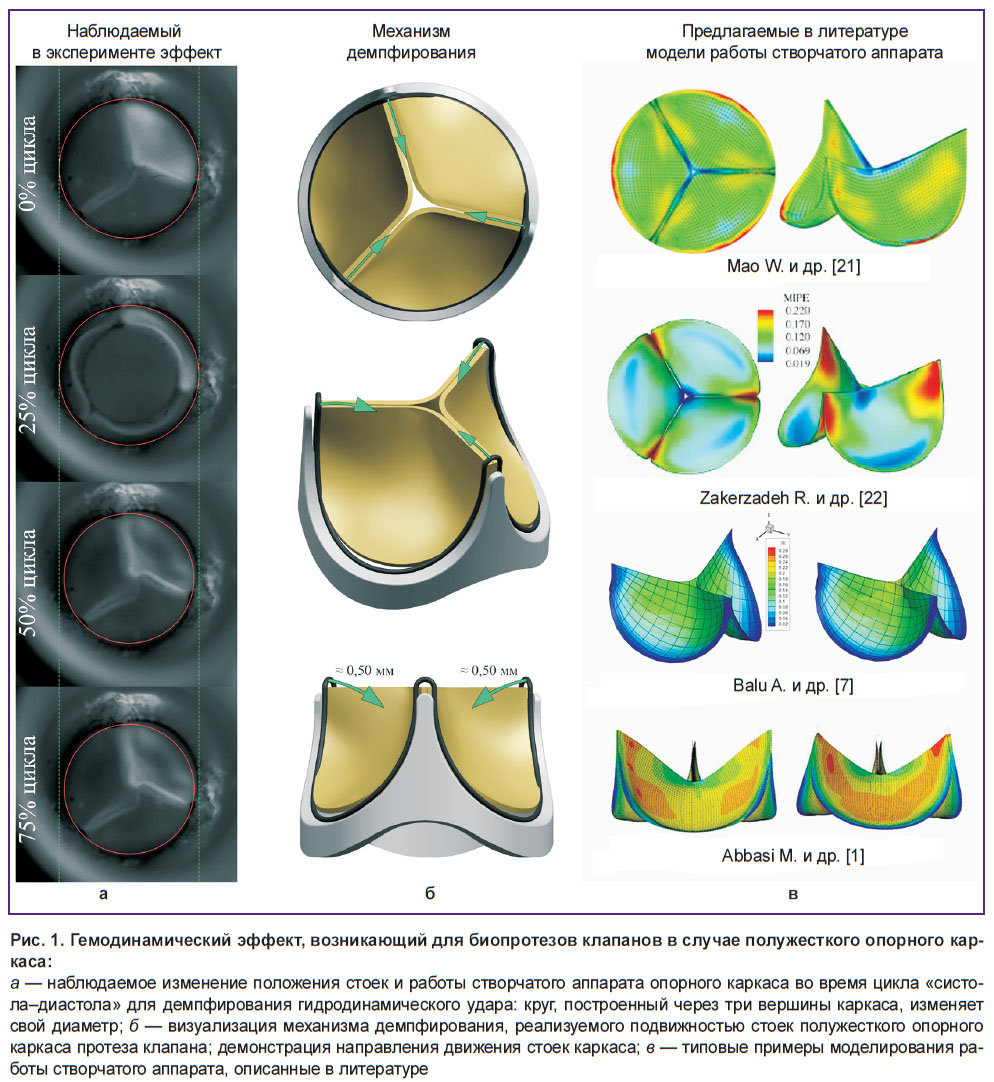
Численное моделирование требует непременного упрощения постановки задачи: некоторых допущений поведения материала; редукции граничных условий и геометрии, валидность применения которых должна быть обоснована качественно и количественно в сравнении с натурным in vitro или in vivo экспериментом [16, 17]. Ряд статей по численному моделированию, направленных на поиск оптимальной геометрии створчатого аппарата протезов клапанов сердца, воспроизводят базовый функционал его работы [1, 2, 7, 18, 19], однако не позволяют обеспечить детальное качественное повторение сложных эффектов и показывают качественное расхождение результатов с экспериментом. К таким сложным моментам можно отнести биомеханику работы компонентов биопротеза клапана по демпфированию гидродинамического удара в фазу диастолы [20]. Такое поведение характерно для протезов с полужестким опорным каркасом, который в момент запирания протеза способен обратимо (эластически) деформироваться в области комиссуральных стоек и снижать растягивающую нагрузку на створку (рис. 1). Однако большинство современных in silico численных расчетов не подразумевают такую возможность, полностью ограничивая перемещения створчатого аппарата по краю пришивания.
Описанные постановки экспериментов [1, 21–23] (рис. 1, в) искажают картину поведения створчатого аппарата и, следовательно, полученные таким образом количественные результаты анализа напряженно-деформированного состояния могут быть некорректными. В связи с этим целью исследования явилась модификация существующих подходов к численному моделированию работы створчатого аппарата биопротеза клапана сердца для воспроизведения особенностей биомеханики его работы с валидацией расчета в эксперименте in vitro.
Материалы и методы
Объект исследования. В качестве объекта исследования в настоящей работе использован биопротез клапана аорты «ЮниЛайн» («НеоКор», Россия) типоразмером 23 мм. Для данного биопротеза характерно возникновение демпфирующего эффекта работы створчатого аппарата за счет подвижного полужесткого опорного каркаса. Трехмерная модель клинического образца биопротеза была реконструирована методом компьютерной микротомографии на экспериментальной установке Томского политехнического университета «Орел-МТ»: получение 880 срезов формата DICOM с разрешением 2,54 мкм в 256 градациях серого. Затем с использованием средств анализа медицинских графических данных была получена пространственная трехмерная модель, состоящая из треугольных фасетов, формирующих единое полигональное тело формата STL. Данная модель была импортирована в среду автоматизированного проектирования NX (Siemens, Германия) и реконструирована в твердотельную модель створчатого аппарата на основе криволинейной поверхности. Затем поверхности придавали толщину 0,5 мм — среднее значение для коммерческого ксеноперикарда крупного рогатого скота, используемого при производстве данного биопротеза.
Численное моделирование — анализ сходимости. Полученные таким образом твердотельные модели створок импортировали в среду инженерного анализа «Abaqus/CAE» (Abaqus Inc., США) и осуществляли численное моделирование их биомеханики методом конечных элементов. Для этого каждая створка была интерполирована сеткой конечных элементов. Определение размера конечного элемента осуществляли в предварительном эксперименте сходимости, в рамках которого на упрощенной трехстворчатой модели работы створчатого аппарата оценивали напряжение по Мизесу и максимальную деформацию в материале в открытом состоянии створки. Референсной моделью служила наиболее подробная конечно-элементная сетка с длиной ребра элемента 0,1 мм и суммарным количеством элементов 371 775. Размер ребра изменяли в последовательности 0,1; 0,2; 0,3; 0,4; 0,5 мм, моделируя одинаковые условия работы протеза. Критерием отбора оптимального размера элемента явилось 5% отклонение по данным параметрам от наиболее точной конечно-элементной сетки с длиной ребра 0,1 мм.
Итогом подбора стала следующая характеристика модели: тип элемента — шестигранный элемент первого порядка C3D8; средняя длина грани — 0,4 мм; общее количество элементов на трехстворчатую модель — 7224; общее количество узлов — 11 376.
Численное моделирование — биомеханика створки. Основной эксперимент in silico моделирования работы створчатого аппарата проводили, используя решатель Abaqus/Explicit, включающий явную интеграцию по времени — для максимально физиологичного воспроизведения работы створок. В ходе моделирования рассчитывали работу створок в течение двух циклов «систола–диастола», каждый длительностью 0,857 с, что соответствует частоте сердечных сокращений 70 в минуту. Предполагается, что первый цикл служит для стабилизации расчета, второй — для непосредственного получения количественных результатов.
Модель материала для створчатого аппарата выбирали по результатам физико-механического тестирования в условиях одноосного растяжения ксеноперикардиальных лоскутов крупного рогатого скота (n=5) на установке Zwick Z50 (Zwick/Roell, Германия). Полученные кривые «напряжение–деформация» импортировали в виде данных для построения полиномиальной модели второго порядка — reduced polynomial. Контактные взаимодействия створок друг с другом описывали попарно на основе модели трения Колумба: в касательном направлении — по методу штрафов (penalty) с коэффициентом трения 0,2; в нормальном — с линейным коэффициентом жесткости 0,2. Моделью нагрузки, имитирующей воздействие на створчатый аппарат, выступило давление, прикладываемое раздельно к желудочковой и к аортальной поверхностям створчатого аппарата. При этом амплитуда давления воспроизводила результаты натурного испытания данного биопротеза «ЮниЛайн», полученные в испытании на гидродинамическом стенде (см. раздел «Валидация»). Всего моделировали два случая работы створчатого аппарата:
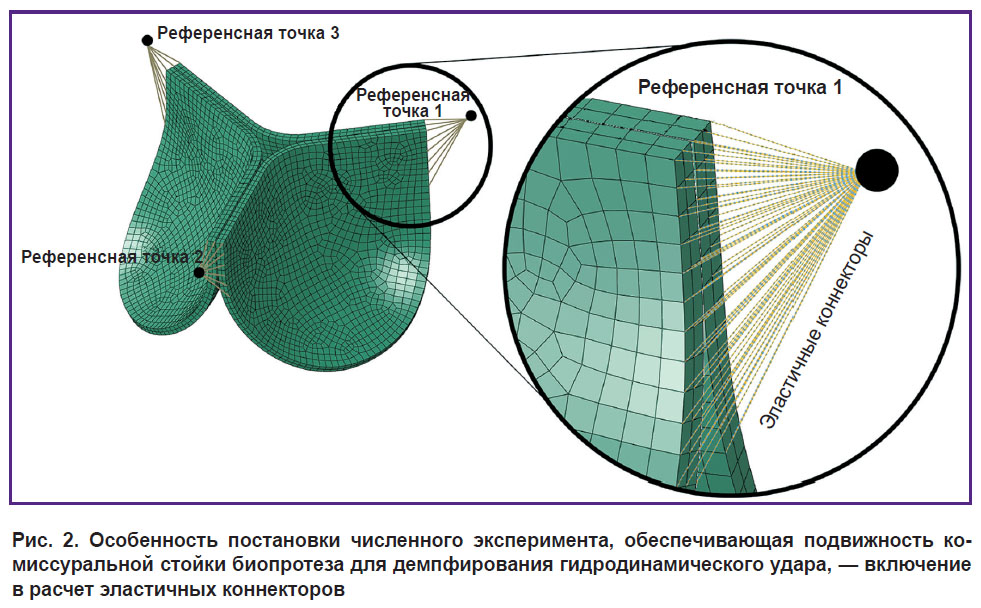
а) с подвижными комиссуральными стойками — для имитации подвижности стоек опорного каркаса, демпфирующих гидродинамический удар, использовали эластичные коннекторы, которыми соединяли референсные зафиксированные точки и отдельные узлы створчатого аппарата в области комиссур (рис. 2). Данные коннекторы обеспечивают контролируемую подвижность створчатого аппарата в радиальном направлении по оси ρ и по оси z (для цилиндрической системы координат) за счет своего типа — Radial-thrust;
б) с неподвижными комиссуральными стойками — в качестве варианта сравнения использовали более «традиционную» постановку эксперимента: по аналогии с описанными в литературе — без возможности перемещений комиссуральных стоек [1, 21, 22].
Сравнение двух случаев моделирования проводили по показателям напряженно-деформированного состояния — амплитуде напряжения по Мизесу и логарифмической деформации, а также по особенностям их локализации в участках створки.
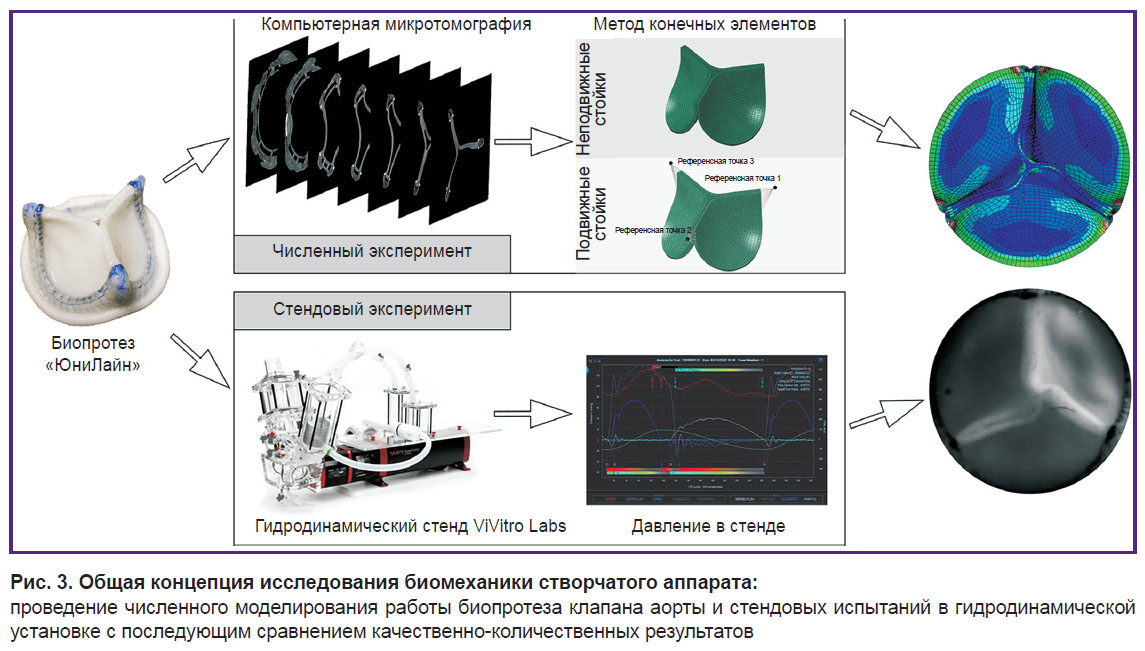
Валидация. Ключевым этапом, определяющим состоятельность предложенного подхода моделирования, является этап валидации — качественно-количественного сравнения показателей биомеханики протеза с результатами стендовых испытаний (рис. 3). Для валидации расчета экземпляр биопротеза «ЮниЛайн», подвергнутый оцифровке, исследовали на установке гидродинамического тестирования ViVitro Labs (ViVitro Labs Inc., Канада) в условиях имитации нормального режима функционирования клапана аорты. Ударный объем составил 5 л/мин, частота «сокращений» — 70 в минуту, давление в аорте — 120/80 мм рт. ст. Работу биопротеза снимали на видеокамеру ускоренной записи Fastvideo-250 (Fastvideo, Россия) с частотой 250 кадров/с. В качестве критериев сравнения результатов численного моделирования и стендового эксперимента выступили:
а) количественно — площадь открытия створчатого аппарата, определяемая как площадь проходного отверстия на каждом кадре замедленной видеосъемки в стенде и на каждом кадре при моделировании; наличие статистических различий оценивали попарным сравнением независимых выборок с использованием критерия Манна–Уитни; достоверными считали различия с уровнем значимости p<0,05;
б) качественно — поведение створчатого аппарата и возникающие эффекты на ключевых кадрах движения створок: начало открытия, максимум открытия, запирание створчатого аппарата, максимальное закрытие створок.
Результаты исследования
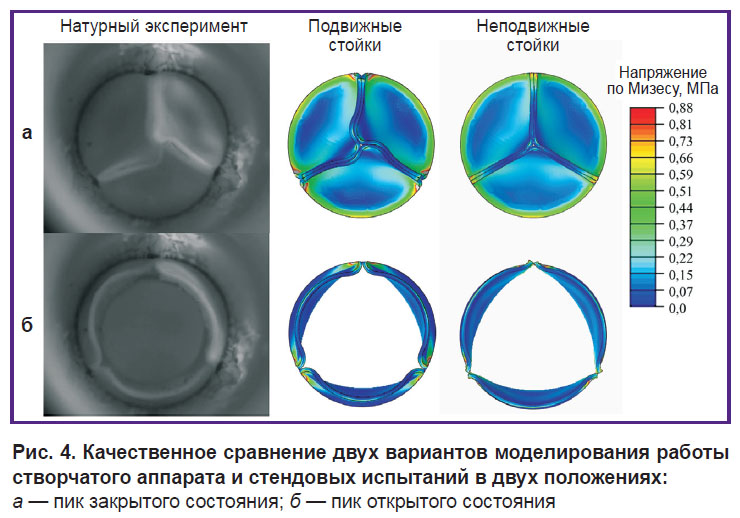
В ходе численного моделирования установлено, что включение в расчет эластичных коннекторов, обеспечивающих подвижность комиссуральных стоек створчатого аппарата, значительно изменяет поведение модели и количественные результаты. Такая in silico постановка успешно воспроизводит закрытие и открытие створок, соответствующие стендовой валидации. Напротив, в случае запрета перемещений комиссуральных стоек биомеханика в численной модели кардинально отличается от результатов гидродинамического испытания. Данный результат наглядно продемонстрирован графически (рис. 4), особенно для фазы запертого створчатого аппарата. Полностью открытое состояние работы створок в целом качественно не различалось.
|
Рис. 4. Качественное сравнение двух вариантов моделирования работы створчатого аппарата и стендовых испытаний в двух положениях: а — пик закрытого состояния; б — пик открытого состояния |
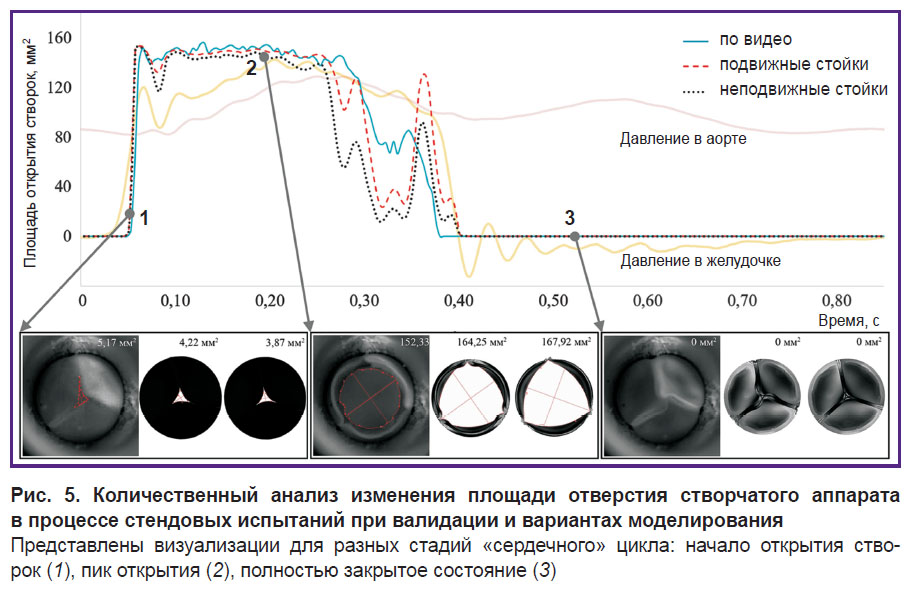
Анализ площади открытия, осуществленный покадрово для двух случаев моделирования, продемонстрировал незначительное расхождение с результатами валидации (рис. 5). Статистически значимых различий площадей открытия не обнаружено.
Количественные характеристики напряженно-деформированного состояния также различались незначительно. Так, для случая подвижных комиссуральных стоек амплитуда напряжения в биологическом материале сравнима с вариантом полностью неподвижных стоек. В первом случае максимум напряжения составил 0,850 МПа, во втором — 0,907 МПа. Среднее напряжение по Мизесу составило 0,141±0,094 и 0,156±0,075 МПа соответственно. Показатель логарифмической деформации у вариантов моделирования также не различался, для случая подвижных стоек составив 0,27 м/м, для неподвижных — 0,24 м/м. Среднее значение составило 0,078±0,0001 м/м и 0,082±0,0003 м/м соответственно.
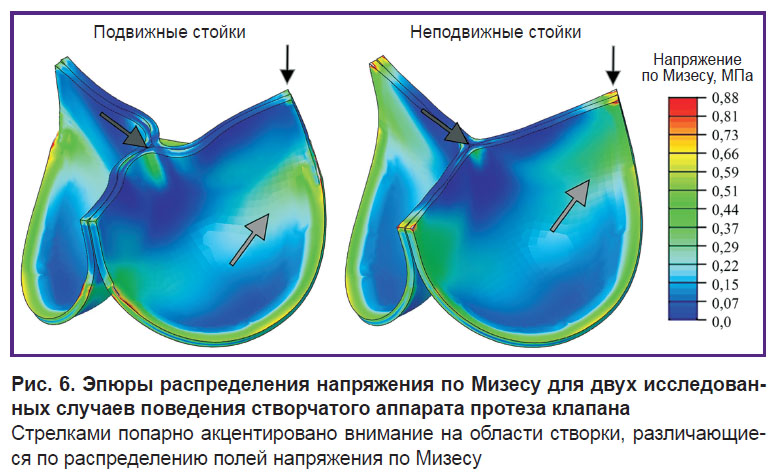
Качественные характеристики — эпюры распределения данных показателей — имели различия, прежде всего обусловленные эффектом демпфирования и складчатости центральной области свободного края створки. В случае использования эластичных коннекторов наблюдали более равномерное распределение напряжения по объему створок, в то время как для неподвижных стоек основные поля напряжения концентрировались в области комиссур (рис. 6). Таким образом, в результате расчетов неподвижных стоек наблюдали области, испытывающие значительные нагрузки — прежде всего растяжения. С другой стороны, возникающий эффект закручивания створок в закрытом состоянии для случая подвижных комиссур формировал перегибы в центральной части свободного края, что приводило к росту напряжения в данной области до 0,52 МПа. В альтернативном случае данный перегиб не формировался, а напряжение достигало 0,35–0,40 МПа.
Обсуждение
Результаты численного моделирования в значительной мере зависимы от настроек его проведения и степени детализации воспроизводимого поведения объекта [23]. Касательно компьютерного анализа работы сложных многокомпонентных систем — в данном случае биологических протезов клапана сердца — такая особенность может становиться причиной серьезных искажений результатов, на основании которых принимают выводы о безопасности и эффективности медицинского изделия. Именно поэтому вопрос валидации численного эксперимента для подобных устройств стоит остро. К сожалению, не всегда исследователи уделяют должное внимание сравнению предлагаемых численных расчетов биомеханики биопротезов с натурными стендовыми испытаниями, что приводит к парадоксальной ситуации. С одной стороны, в литературе описано достаточное количество высокоуровневых подходов к in silico исследованию створчатого аппарата биопротезов клапанов сердца, многие из которых моделируют и сложные многодисциплинарные взаимодействия (мультифизику). Наиболее детальные из таких исследований воспроизводят процессы «жидкость–твердое тело» с комплексным описанием материалов [24, 25], детальным подбором граничных условий и имитацией поведения сложной жидкости — крови [5, 26], однако в большинстве своем не приводят сравнений с результатами стендовых испытаний или сознательно не воспроизводят при моделировании важные эффекты, наблюдаемые в эксперименте in vitro [27, 28]. При этом в таких работах делаются выводы о взаимосвязи геометрии створок и гидродинамики [2, 29], формы створки и размера зоны кооптации [7], т.е. свойств, напрямую ассоциированных с рисками и эффективностью применения биопротезов. Насколько безопасно опираться на подобные выводы, полученные без должной валидации, при проектировании медицинского изделия наивысшего класса риска (биопротеза клапана сердца), остается серьезным вопросом.
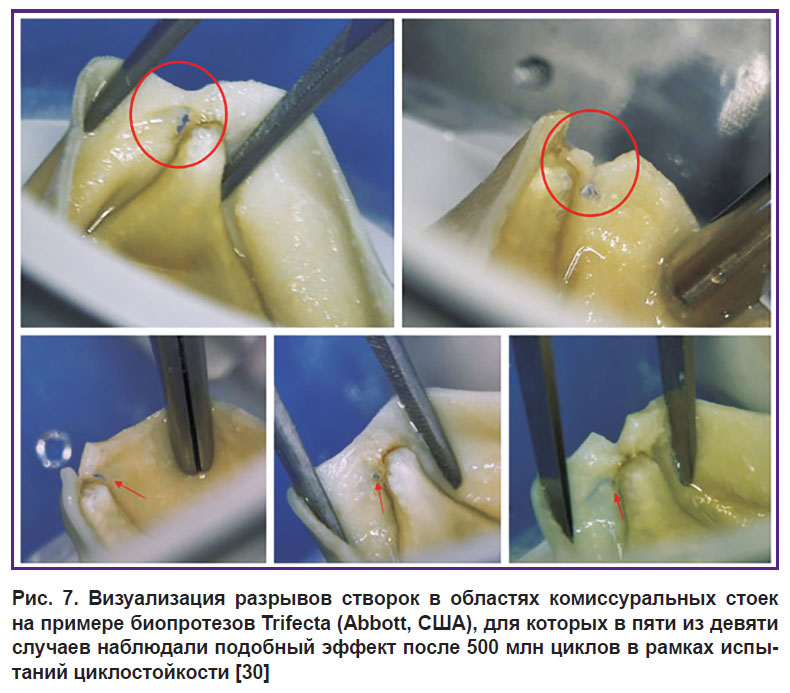
Данная проблема значительно обостряется при возникновении в эксперименте in vitro нетиповых особенностей работы биопротезов, характерных, например, для нашего объекта исследования: опорный каркас демпфирует гидродинамический удар за счет подвижности своих стоек. Такая концепция демпфирования обоснована [17] и представляет собой попытку решения проблемы отрыва створки биопротеза от комиссуральной стойки в результате воздействия на нее длительных нагрузок для случая жесткого неподвижного каркаса (рис. 7) [30]. Однако практически все представленные в литературе модели, несмотря на глубокую проработку других аспектов — нелинейных материалов, комплексных нагрузок, физики жидкости, не имеют возможностей и инструментов для имитации такого специфического поведения.
Стоит отметить, что в литературе все же описаны два in silico исследования, которые учитывают демпфирующий эффект и именно в разрезе моделирования долговечности створчатого аппарата [6, 31]. В данных работах имитируют различные варианты отклонения комиссуральных стоек в биопротезе Carpentier-Edwards PERIMOUNT (США), однако не проводят валидацию такого поведения. Тем не менее примечательно, что авторы обеих статей приходят к схожему выводу, наблюдаемому и в нашем исследовании: подвижность стоек протеза устраняет усталостное повреждение створки в области комиссур, но увеличивает повреждение свободного края. По-видимому, именно с этой позиции — уменьшения амплитуд напряжения в области свободного края — необходимо проводить дальнейшую оптимизацию исследованного нами протеза «ЮниЛайн». Несмотря на успешную историю применения данного изделия в клинике [32–34], его створчатый аппарат имеет потенциал для улучшения, а предложенная постановка in silico эксперимента может стать ценным инструментом для оценки эффективности таких улучшений путем численного анализа.
Заключение
Представлен подход к моделированию работы створчатого аппарата протеза клапана сердца с учетом подвижности комиссуральных стоек и демпфирования гидродинамического удара. Реализация подхода осуществлена путем введения в модель дополнительных эластичных коннекторов регулируемой жесткости, которые обеспечивают ограниченное контролируемое перемещение комиссур створок. Показано, что использование данного подхода значительно уточняет распределение полей напряжения и деформации в материале створчатого аппарата, а также воспроизводит качественно-количественные результаты валидации в стендовых условиях имитации работы протеза клапана, т.е. имеет натурное обоснование.
Результаты моделирования биомеханики протеза «ЮниЛайн» продемонстрировали, что подвижность стоек каркаса протеза клапана сердца является определяющим аспектом при оценке эффективности геометрии створчатого аппарата и может выступать негативным фактором в случае высокоэластичного материала створок.
Представленный метод моделирования может быть использован для оптимизации геометрии створчатого аппарата протезов клапанов сердца, выполненных на основе как ксеногенных консервированных биоматериалов, так и синтетических полимерных, с позиции оценки распределения напряженно-деформированного состояния.
Финансирование. Исследование выполнено за счет гранта Российского научного фонда №21-75-10128, https://rscf.ru/project/21-75-10128/.
Конфликт интересов отсутствует.
Литература
- Abbasi M., Azadani A.N. A geometry optimization framework for transcatheter heart valve leaflet design. J Mech Behav Biomed Mater 2020; 102: 103491, https://doi.org/10.1016/j.jmbbm.2019.103491.
- Dabiri Y., Ronsky J., Ali I., Basha A., Bhanji A., Narine K. Effects of leaflet design on transvalvular gradients of bioprosthetic heart valves. Cardiovasc Eng Technol 2016; 7(4): 363–373, https://doi.org/10.1007/s13239-016-0279-5.
- Li K., Sun W. Simulated transcatheter aortic valve deformation: a parametric study on the impact of leaflet geometry on valve peak stress. Int J Numer Method Biomed Eng 2017; 33(3): e02814, https://doi.org/10.1002/cnm.2814.
- De Gaetano F., Bagnoli P., Zaffora A., Pandolfi A., Serrani M., Brubert J., Stasiak J., Moggridge G.D., Costantino M.L. A newly developed tri-leaflet polymeric heart valve prosthesis. J Mech Med Biol 2015; 15(02): 1540009, https://doi.org/10.1142/s0219519415400096.
- Hsu M.C., Kamensky D., Xu F., Kiendl J., Wang C., Wu M.C.H., Mineroff J., Reali A., Bazilevs Y., Sacks M.S. Dynamic and fluid–structure interaction simulations of bioprosthetic heart valves using parametric design with T-splines and Fung-type material models. Comput Mech 2015; 55(6): 1211–1225, https://doi.org/10.1007/s00466-015-1166-x.
- Martin C., Sun W. Comparison of transcatheter aortic valve and surgical bioprosthetic valve durability: a fatigue simulation study. J Biomech 2015; 48(12): 3026–3034, https://doi.org/10.1016/j.jbiomech.2015.07.031.
- Balu A., Nallagonda S., Xu F., Krishnamurthy A., Hsu M.C., Sarkar S. A deep learning framework for design and analysis of surgical bioprosthetic heart valves. Sci Rep 2019; 9(1): 18560, https://doi.org/10.1038/s41598-019-54707-9.
- Глушкова Т.В., Овчаренко Е.А., Батранин А.В., Клышников К.Ю., Кудрявцева Ю.А., Барбараш Л.С. Клинический случай дисфункции биопротеза клапана сердца в трикуспидальной позиции у пациента дошкольного возраста: оценка вклада паннуса и кальцификации. Вестник трансплантологии и искусственных органов 2018; 20(3): 45–53, https://doi.org/10.15825/1995-1191-2018-3-45-53.
- Глушкова Т.В., Овчаренко Е.А., Рогулина Н.В., Клышников К.Ю., Кудрявцева Ю.А., Барбараш Л.С. Дисфункции эпоксиобработанных биопротезов клапанов сердца. Кардиология 2019; 59(10): 49–59, https://doi.org/10.18087/cardio.2019.10.n327.
- Мухамадияров Р.А., Рутковская Н.В., Мильто И.В., Васюков Г.Ю., Барбараш Л.С. Патогенетические параллели кальцификации нативных клапанов аорты и ксеногенных биопротезов клапанов сердца. Гены и Клетки 2016; 11(3): 72–79.
- Караськов А.М., Железнев С.И., Назаров В.М., Лавинюков С.О., Ларионов П.М., Богачев-Прокофьев А.В., Глотова Н.И., Матюгин М.П. Клинико-морфологические изменения при дисфункциях биологических протезов сердца. Патология кровообращения и кардиохирургия 2006; 2: 21–26.
- Foroutan F., Guyatt G.H., O’Brien K., Bain E., Stein M., Bhagra S., Sit D., Kamran R., Chang Y., Devji T., Mir H., Manja V., Schofield T., Siemieniuk R.A., Agoritsas T., Bagur R., Otto C.M., Vandvik P.O. Prognosis after surgical replacement with a bioprosthetic aortic valve in patients with severe symptomatic aortic stenosis: systematic review of observational studies. BMJ 2016; 354: i5065, https://doi.org/10.1136/bmj.i5065.
- Одаренко Ю.Н., Рутковская Н.В., Рогулина Н.В., Стасев А.Н., Кокорин С.Г., Каган Е.С., Барбараш Л.С. Анализ 23-летнего опыта использования ксеноаортальных эпоксиобработанных биопротезов в хирургии митральных пороков сердца. Исследование факторов реципиента с позиций влияния на развитие кальциевой дегенерации. Комплексные проблемы сердечно-сосудистых заболеваний 2015; 4: 17–25.
- Рогулина Н.В., Одаренко Ю.Н., Журавлева И.Ю., Барбараш Л.С. Отдаленные результаты применения механических и биологических протезов у пациентов различных возрастов. Journal of Siberian Medical Sciences 2014; 3: 47.
- Журавлева И.Ю., Богачев-Прокофьев А.В., Тимченко Т.П., Требушат Д.В., Майоров А.П., Гончаренко А.М., Астапов Д.А., Нуштаев Д.В., Демидов Д.П. Модель биопротеза аортального клапана для бесшовной имплантации. Медицинская техника 2017; 3: 15–18.
- Abbasi M., Qiu D., Behnam Y., Dvir D., Clary C., Azadani A.N. High resolution three-dimensional strain mapping of bioprosthetic heart valves using digital image correlation. J Biomech 2018; 76: 27–34, https://doi.org/10.1016/j.jbiomech.2018.05.020.
- Abbasi M., Barakat M.S., Vahidkhah K., Azadani A.N. Characterization of three-dimensional anisotropic heart valve tissue mechanical properties using inverse finite element analysis. J Mech Behav Biomed Mater 2016; 62: 33–44, https://doi.org/10.1016/j.jmbbm.2016.04.031.
- Abbasi M., Barakat M., Dvir D., Azadani A. Detailed stress analysis of Edwards-SAPIEN and Medtronic CoreValve devices. Is leaflet stress comparable to surgical Carpentier-Edwards PERIMOUNT Magna bioprosthesis? Struct Heart 2019; 3(Suppl 1): 192, https://doi.org/10.1080/24748706.2019.1591103.
- Liang L., Sun B. A proof of concept study of using machine-learning in artificial aortic valve design: from leaflet design to stress analysis. Bioengineering (Basel) 2019; 6(4): 104, https://doi.org/10.3390/bioengineering6040104.
- Vesely I. The evolution of bioprosthetic heart valve design and its impact on durability. Cardiovasc Pathol 2003; 12(5): 277–286, https://doi.org/10.1016/s1054-8807(03)00075-9.
- Mao W., Li K., Sun W. Fluid–structure interaction study of transcatheter aortic valve dynamics using smoothed particle hydrodynamics. Cardiovasc Eng Technol 2016; 7(4): 374–388, https://doi.org/10.1007/s13239-016-0285-7.
- Zakerzadeh R., Hsu M.C., Sacks M.S. Computational methods for the aortic heart valve and its replacements. Expert Rev Med Devices 2017; 14(11): 849–866, https://doi.org/10.1080/17434440.2017.1389274.
- Zhuravleva I.Y., Nushtaev D.V., Timchenko T.V., Trebushat D.V., Mayorov А.P., Zheleznev S.I., Demidov D.P., Bogachev-Prokophiev А.V. The concept of a device for the redo transcatheter mitral valve implantation. Sovremennye tehnologii v medicine 2017; 9(3): 7–14, https://doi.org/10.17691/stm2017.9.3.01.
- Zhang W., Rossini G., Kamensky D., Bui-Thanh T., Sacks M.S. Isogeometric finite element-based simulation of the aortic heart valve: integration of neural network structural material model and structural tensor fiber architecture representations. Int J Numer Method Biomed Eng 2021; 37(4): e3438, https://doi.org/10.1002/cnm.3438.
- Smuts A.N., Blaine D.C., Scheffer C., Weich H., Doubell A.F., Dellimore K.H. Application of finite element analysis to the design of tissue leaflets for a percutaneous aortic valve. J Mech Behav Biomed Mater 2011; 4(1): 85–98, https://doi.org/10.1016/j.jmbbm.2010.09.009.
- Soares J.S., Feaver K.R., Zhang W., Kamensky D., Aggarwal A., Sacks M.S. Biomechanical behavior of bioprosthetic heart valve heterograft tissues: characterization, simulation, and performance. Cardiovasc Eng Technol 2016; 7(4): 309–351, https://doi.org/10.1007/s13239-016-0276-8.
- Serrani M., Brubert J., Stasiak J., De Gaetano F., Zaffora A., Costantino M.L., Moggridge G.D. A computational tool for the microstructure optimization of a polymeric heart valve prosthesis. J Biomech Eng 2016; 138(6): 061001, https://doi.org/10.1115/1.4033178.
- Abbasi M., Barakat M.S., Dvir D., Azadani A.N. A non-invasive material characterization framework for bioprosthetic heart valves. Ann Biomed Eng 2019; 47(1): 97–112, https://doi.org/10.1007/s10439-018-02129-5.
- Lee J.H., Rygg A.D., Kolahdouz E.M., Rossi S., Retta S.M., Duraiswamy N., Scotten L.N., Craven B.A., Griffith B.E. Fluid–structure interaction models of bioprosthetic heart valve dynamics in an experimental pulse duplicator. Ann Biomed Eng 2020; 48(5): 1475–1490, https://doi.org/10.1007/s10439-020-02466-4.
- Vriesendorp M.D., de Lind van Wijngaarden R.A.F., Rao V., Moront M.G., Patel H.J., Sarnowski E., Vatanpour S., Klautz R.J.M. An in vitro comparison of internally versus externally mounted leaflets in surgical aortic bioprostheses. Interact Cardiovasc Thorac Surg 2020; 30(3): 417–423, https://doi.org/10.1093/icvts/ivz277.
- Martin C., Sun W. Simulation of long-term fatigue damage in bioprosthetic heart valves: effects of leaflet and stent elastic properties. Biomech Model Mechanobiol 2014; 13(4): 759–770, https://doi.org/10.1007/s10237-013-0532-x.
- Fedorov S.A., Chiginev V.A., Zhurko S.A., Gamzaev A.B., Medvedev A.P. Clinical and hemodynamic results of applying different biological prosthesis models for correction of calcific aortic valve disease. Sovremennye tehnologii v medicine 2016; 8(4): 292–296.
- Барбараш Л.С., Рогулина Н.В., Рутковская Н.В., Одаренко Ю.Н., Стасев А.Н., Левадин Ю.В., Кокорин С.Г. Пятилетний опыт применения биологического протеза ЮниЛайн при митральном пороке. Кардиология и сердечно-сосудистая хирургия 2015; 8(5): 49–54, https://doi.org/10.17116/kardio20158549-54.
- Караськов А.М., Железнев С.И., Рогулина Н.В., Сапегин А.В., Одаренко Ю.Н., Левадин Ю.В., Рутковская Н.В., Барбараш Л.С. Отечественный биологический протез нового поколения «Юнилайн» в хирургии митрального порока: первый опыт. Грудная и сердечно-сосудистая хирургия 2017; 59(2): 98–104, https://doi.org/10.24022/0236-2791-2017-59-2-98-104.