Радиомика при раке молочной железы: использование глубокого машинного анализа МРТ-изображений метастатического поражения позвоночника
Обработка изображений с использованием математических критериев (радиомика) позволяет более точно оценивать характер изменений под влиянием терапии, определять места максимального ответа. Полученные количественные данные при сопоставлении с клиническими могут выступать в качестве поддержки принятия решения врачом-рентгенологом.
Цель исследования — оценка возможностей программных операторов глубокого машинного анализа изображений метастатического поражения позвоночника при раке молочной железы.
Материалы и методы. В работе использовались данные МРТ трех пациенток с диагнозом «рак молочной железы T2N2–3M1», получающих лечение в соответствии с принятыми клиническими протоколами. Метастазы в позвоночник были оценены рентгенологом и с помощью машинного анализа с использованием программного оператора «вариации Арцелы». Было проанализировано 12 МРТ-исследований (по 4 на каждую пациентку), не включая исходное, с периодом выполнения приблизительно 3 мес.
Результаты. Посегментно проанализирована структура метастатически измененного позвоночника в сагиттальной и аксиальной проекциях с использованием машинных операторов анализа изображений. Обнаружены быстрые изменения сложности изображений позвонков, позволяющие предполагать эффективность лечения по одному из трех параметров — стабилизация, улучшение, прогрессирование. Отслежены изменения структуры позвонков при положительном ответе на проводимое лечение в виде формирования костных объектов — кальдер, снижения циркуляции контрастного препарата на микроуровне, подтвержденные математическим анализом. Установлена корреляционная связь между обнаруженными изменениями и уровнем опухолевого маркера CA 15-3.
Заключение. Исследование показало высокую эффективностьиспользования алгоритмов машинного анализа изображений, хорошую корреляцию полученных результатов с заключением врача-рентгенолога и с клинико-лабораторными данными в 9 из 12 случаев, коэффициент корреляции Пирсона между классическим маркером и кривой матричного фильтра составил 0,8.
Введение
Важной задачей лечения рака молочной железы является оценка его эффективности, максимально раннее выявление достоверных критериев стабилизации или прогрессирования заболевания, что позволяет вовремя корректировать план терапии [1]. Использование принципов радиомики открывает широкие возможности для контроля заболевания методами визуализации, преимуществом которых является малоинвазивность, — такими как МРТ с контрастным усилением [2, 3]. Сложность диагностики при использовании таких методов заключается в том, что процессы патологического остеолизиса и реактивного остеосклероза на микроуровне идут параллельно, и это дает большую вариабельность результатов, особенно в процессе лечения. По стандартно представляемым данным трудно ответить на такие вопросы: какова скорость и глубина этих изменений, где происходит максимальный ответ на терапию. Результаты интерпретации радиологических паттернов напрямую зависят от опыта врача-рентгенолога и являются качественной или полуколичественной характеристикой. Глубокая машинная обработка изображений с использованием математических критериев позволит получить достоверные количественные данные, которые могут выступать в качестве поддержки принятия решения [4]. В силу сложности рабочего процесса данная тема требует дальнейшего изучения.
Цель исследования — оценка возможностей программных операторов глубокого машинного анализа изображений метастатического поражения позвоночника при раке молочной железы.
Материалы и методы
Клиническая характеристика больных. В работе использовали данные МРТ трех пациенток с диагнозом «рак молочной железы T2N2–3M1», которым было проведено комплексное лечение, включающее неоадъювантную химиотерапию, мастэктомию и адъювантную химиотерапию в сочетании с дистанционной лучевой терапией до СОД 56 Гр.
По данным диагностических методов (остеосцинтиграфия и КТ и/или МРТ), у всех больных определялось метастатическое поражение скелета. После установки диагноза дальнейший контроль состояния очагов в позвоночнике осуществляли с помощью МРТ с внутривенным контрастным усилением препаратами гадолиния. Интервалы наблюдения составляли около 3 мес, каждой пациентке было выполнено не менее 4 исследований, максимально — 12 исследований. Общее количество проанализированных МРТ-исследований — 15, из которых 3 являлись исходной картиной в каждом наблюдении, в остальных случаях оценивали эффект терапии.
Моделирование процесса радиомики. Был сформулирован основной принцип исследования: теоретическое обоснование происходящих процессов, получение их практического (физического) подтверждения и сопоставление с клиническими данными.
Таким образом, рабочий процесс включал в себя два основных этапа: оценка диагностических изображений врачом-рентгенологом и с помощью машинного анализа. Для объективизации результатов все данные были анонимизированы, наблюдениям были присвоены условные номера Osteo-1, Osteo-2, Osteo-3 с порядковым номером очередности исследования, где МРТ-0 — первичное исследование, а МРТ-1, МРТ-2 и далее — диагностические исследования в процессе терапии. Важно отметить, что оба процесса оценки шли параллельно, по окончании формировался отчет, в котором заключительный диагноз имел трехзначную шкалу: улучшение, стабилизация, прогрессирование. Полученные результаты оценивали как простым сопоставлением, так и с помощью коэффициента корреляции Пирсона.
Система машинного анализа представляет собой Dicom Viewer с расширенными функциями анализа и представления результатов. Она написана на языке Java, поэтому является независимой от операционной системы используемого компьютера.
Математический анализ изображений был привязан к трем основным элементам микроуровня и включал в себя разработку следующих методов:
1) анализ сложности рисунка — на том основании, что опухолевые рост и ангиогенез хаотичны и поэтому характеризуются более низкой сложностью, чем упорядоченная структура здоровых тканей;
2) анализ контраста —на том основании, что накопление контраста уменьшается при успешном лечении;
3) анализ микрофокусов, или микроочагов (кальдер), — на том основании, что положительный эффект терапии в позвонках вызывает процессы склерозирования в местах раковых поражений.
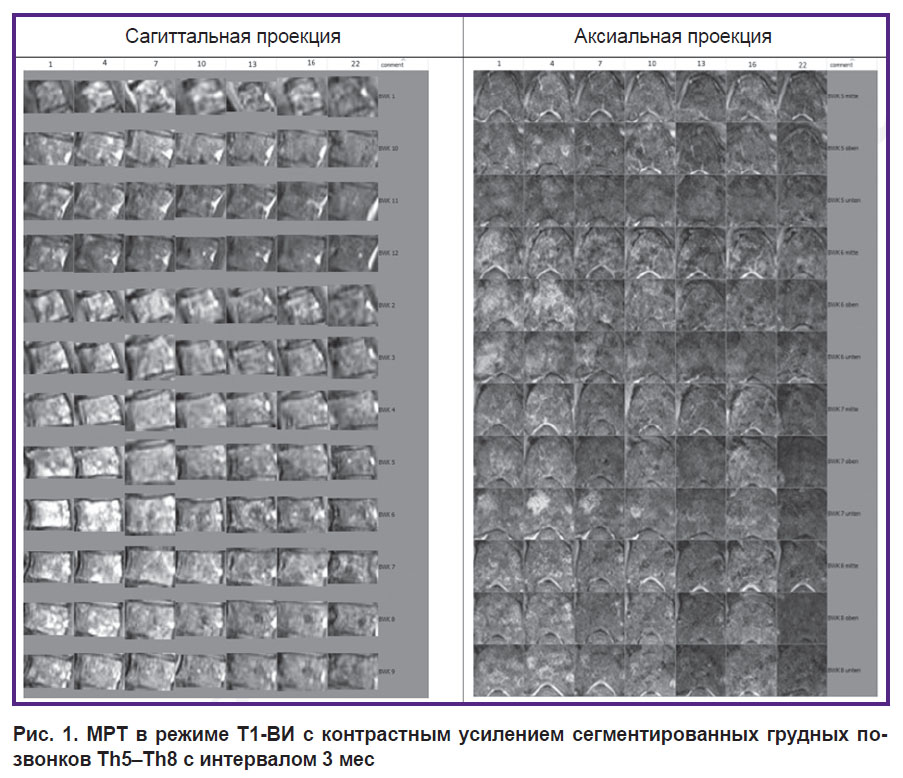
Методы анализа изображений. Технический анализ МРТ-изображений также включал несколько этапов. В работе были использованы серии сагиттальных (sagittal) и аксиальных (axial) МРТ в режиме Т1- и Т2-взвешенных изображений (Т1-ВИ, Т2-ВИ axial, sag) с введением и без введения контрастного вещества, с выделением тела позвонка как исследуемого сегмента изображения. При таком процессе возможно привлечение автоматизации, однако ее результаты при всем развитии технологии еще не достаточны [5], поэтому в нашей работе мы применили ручную сегментацию. Были построены карты динамики изменений на основании выполненных МРТ грудного отдела позвоночника в процессе лечения (например, рис. 1). Такие карты легли в основу всех трех разработанных методов.
|
Рис. 1. МРТ в режиме T1-ВИ с контрастным усилением сегментированных грудных позвонков Th5–Th8 с интервалом 3 мес |
1. Анализ сложности изображений начнем с замечания по расчету энтропии. Теоретико-информационный подход к оценке сложности изображений как потока сообщений, представленных в дискретной форме, часто основан на вычислении энтропии. Такой вариант предполагает независимость значений пикселей, тогда как изображение любого МРТ-паттерна рака имеет сильную корреляцию пикселей. Поэтому подходы, используемые для оценки сложности потока независимых сообщений, как, например, энтропия, часто оказываются недостаточными [6].
По этой причине для оценки контуров, или границ (сложности), изображений все они были преобразованы в монохромный серый цвет, при этом мы использовали программное обеспечение, которое позволило работать в рамках текстурного и проекционного анализа одновременно [7]. Существует несколько операторов для вычисления контуров объектов [8], нами были опробованы наиболее часто используемые операторы Sobel, Prewitt, Scharr, Arzela (рис. 2).

|
Рис. 2. Варианты различных фильтров для выделения контуров на изображении На снимках — МРТ T1-ВИ axial с контрастным усилением, верхнее сечение грудного позвонка Th6 |
По данным предварительного анализа, лучшие результаты показал оператор Arzela — метод, который хорошо отображает внутренние контуры. Вариации Арцелы (далее AV — Arzela variations) рассчитываются по следующей формуле для каждой проекции:
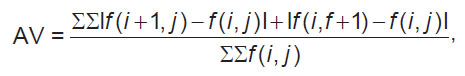
где f (i + 1, j), f (i, j + 1), f (i, j) — значения интенсивности серого для индексированного (i, j) пикселя.
Оценка сложностей изображения основывается на том, что оно будет сложнее другого изображения, если сумма границ объектов, его составляющих, больше. Усиленные контрастом изображения рака менее структурированы, чем нормальная костная ткань, в частности из-за хаотичного ангиогенеза, как уже упоминалось. Это приводит к уменьшению длины границ контура или к меньшей сумме градиентов, т.е., иначе, к низкой сложности изображения. Другими словами, воспаление вокруг опухоли увеличивает сумму градиентов интенсивности контраста, наблюдаемых как ангиогенез в патологических условиях, например во время заживления ран, делая общее изображение более сложным и, таким образом, показывая действие терапии. Используя оператор Арцелы, мы пришли к выводу, что чем больше AV, чем выше сложность изображения, тем ближе оно к изображению нормальной, пусть даже воспаленной, ткани. AV дают достаточно хорошие контуры важных деталей и могут служить мерой сложности, по крайней мере во взятых проекциях и при поражениях, видимых на изображениях позвонка. Структурная часть (сложность) хорошо реагирует на переход из неупорядоченного состояния в упорядоченное, когда области имеют средние размеры от 0,5 до 2,0 см. Порог чувствительности еще предстоит исследовать.
Поскольку в начале терапии трудно одновременно разделить долгосрочное принятие контраста и быстрые изменения в аксиальной плоскости, мы будем усиливать эффект накопления контраста взвешивающим множителем. Так мы переходим к системе взвешенных вариаций (WV): в качестве весов возьмем интенсивность в соответствующей точке f (i, j). WV показывают интегральный ответ на терапию, в нашем случае это используемые грудные позвонки Th5–Th8. В начальной фазе сложность WV низкая и резко возрастает при активной терапии. Это связано с появлением некротических участков, где структура накопления контрастного вещества более сложная, чем в области опухоли. Затем процесс переходит в стабильную фазу, сложность которой (в направлении нормальной ткани) значительно выше, чем в начальной фазе.
2. Автоматизация измерений контраста. Использовано автоматическое обнаружение областей высокой контрастности (ярких областей). После некоторых экспериментов получен следующий простой алгоритм: экстраполяция объектов сегментации (обычно порядка 100×100 пикселей) кубическим сплайном до размера примерно 250 пикселей; расчет пороговых значений средней яркости изображения и, наконец, контурирование с помощью функции BinaryImageOps.contour из библиотеки BoofCV с последующим расчетом общей интенсивности в контурах (рис. 3).

|
Рис. 3. Автоматически выделенные контуры (BoofCV) для грудного позвонка Th7 на T1-ВИ sag с контрастным усилением |
Площадь контуров (в пикселях) суммируется, чтобы учесть влияние распределения интенсивности внутри контуров.
Contact=ΣΣP(i, j),
где P(i, j) — значение пикселя (0–255); i — индекс контура; j — количество пикселей в контуре.
В результате получается количественная кривая приема контрастного вещества как функция длительного времени на всем регистрируемом участке позвоночника.
3. Микрофокусы, или микроочаги. При переходе к последнему этапумы отталкивались от проведенных ранее патологоанатомических исследований [9], установивших, что при раке молочной железы превалируют объекты с радиальной и сферической симметрией. Исходя из этого, мы искали объекты поражения с такой симметрией на МРТ-изображениях грудного отдела. На этом этапе мы столкнулись с вопросами дифференциальной диагностики, которые требуют отдельного большого исследования. В нашей работе были обнаружены изменения по типу эностозов — у них наблюдалась такая же кольцевидная форма, однако с большей однородностью [10].
На первом этапе работы мы сформулировали стандартное заключение врача-рентгенолога с оценкой происходящих процессов, видимых глазу. При этом протокол был более детализирован за счет возможности проследить изменения на длительном этапе наблюдения с использованием доступных средств обработки изображений на рабочих станциях, таких как увеличение, сопоставление.
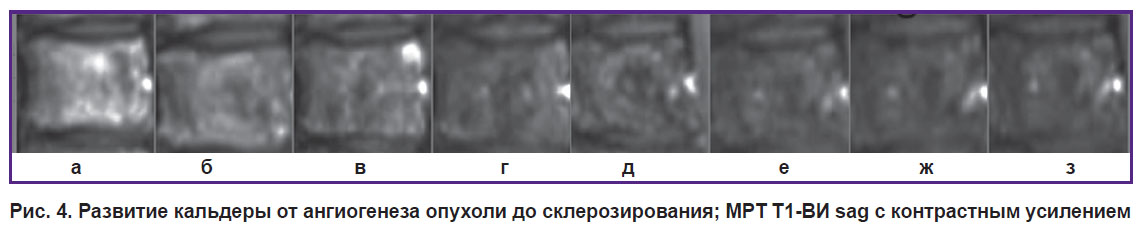
На рис. 4 показаны видимые изменения на МРТ-изображениях (T1-ВИ sag с контрастом) с течением времени для грудного позвонка Th6:
а) развитая опухоль — хаотично расположенные кровеносные сосуды сверху и снизу с интенсивным накоплением контрастного вещества;
б) разрушение ангиогенеза опухоли и воспаление — образование кальдеры;
в) хаотично расположенные сосуды в поражении почти не присутствуют, кальдера растет и структурируется;
г) вокруг кальдеры появляется «воспалительный ободок», она продолжает структурироваться;
д) воспалительный ободок сменяется «склеротическим» кольцом, дно кальдеры становится более однородным, происходит еще один небольшой прием контрастного вещества;
е) кальдера в центре закрывается, хорошо виден обод;
ж) кальдера теряет форму и еще больше сливается с общим фоном;
з) дальнейшая стабилизация процесса.
|
Рис. 4. Развитие кальдеры от ангиогенеза опухоли до склерозирования; МРТ T1-ВИ sag с контрастным усилением |
Такие же состояния наблюдаются и в других позвонках. На одном теле позвонка может происходить несколько таких процессов, и не всегда одновременно.
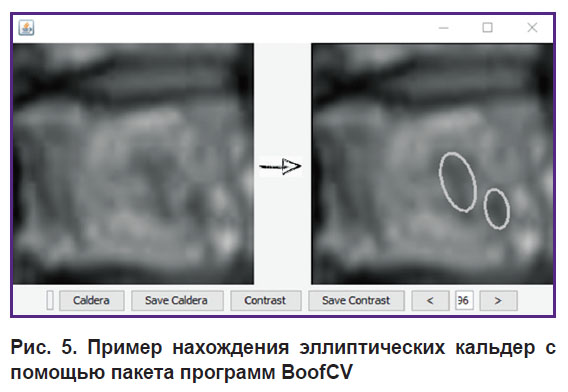
В процессе работы кальдерами было предложено называть все неясные сферически или радиально симметричные объекты (микрофокусы). Перед идентификацией кальдеры изображения растягивались до размера внутреннего стандарта (250×250) и выполнялась функция сглаживания. Для того чтобы провести обнаружение, необходимо установить порог, который варьировался в диапазоне от 1 до 254. Затем рассчитывалось среднее взвешенное значение, которое и принималось за пороговое, где весами являются значения площади кальдер. Из расчетов мы исключили примерно 20% границы изображения, которые выходили за поверхность позвонка. На рис. 5 приведен пример обнаружения кальдер системой.
|
Рис. 5. Пример нахождения эллиптических кальдер с помощью пакета программ BoofCV |
Количественное значение для кальдеры рассчитывали как общую площадь кальдеры на поверхности изучаемой части позвоночника:
Caldera=ΣS(i),
где S(i) — площадь отдельных кальдер. Эта величина выражена в процентах по отношению к исследуемой части поверхности позвонков.
Результаты исследования
По первому пункту анализа — оценке сложности — были проведены расчеты как по отдельным позвонкам, так и по группе тел позвонков одновременно.
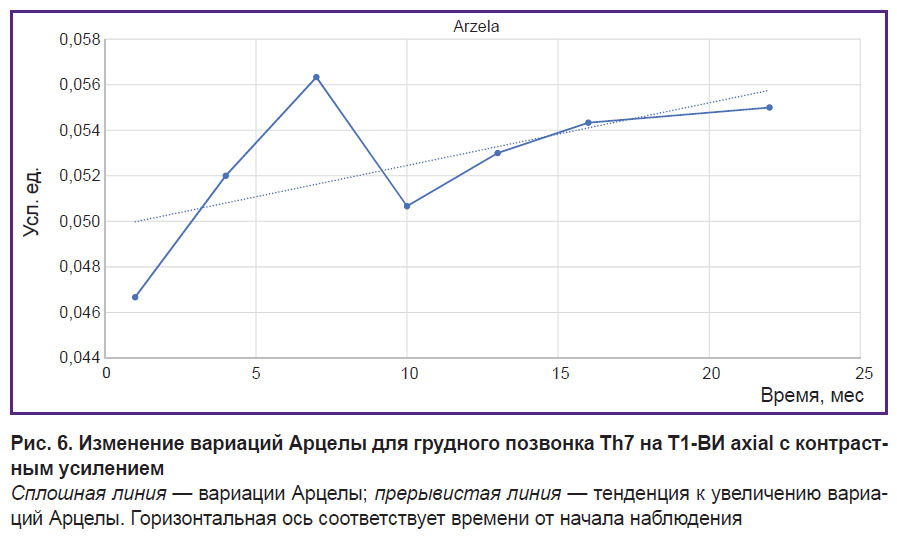
Рассмотрим общие изменения AV на аксиальной проекции на примере 7-го грудного позвонка Th7, рассчитав значения вариаций (рис. 6).
Видно, как AV (сложность) растет не только на начальном участке, но и асимптотически в целом, при этом возможен некоторый разброс значений за счет технических параметров МРТ. Первые значения наиболее чувствительно реагируют на терапию и поэтому могут служить дополнительным ориентиром при корректировке схемы лечения.
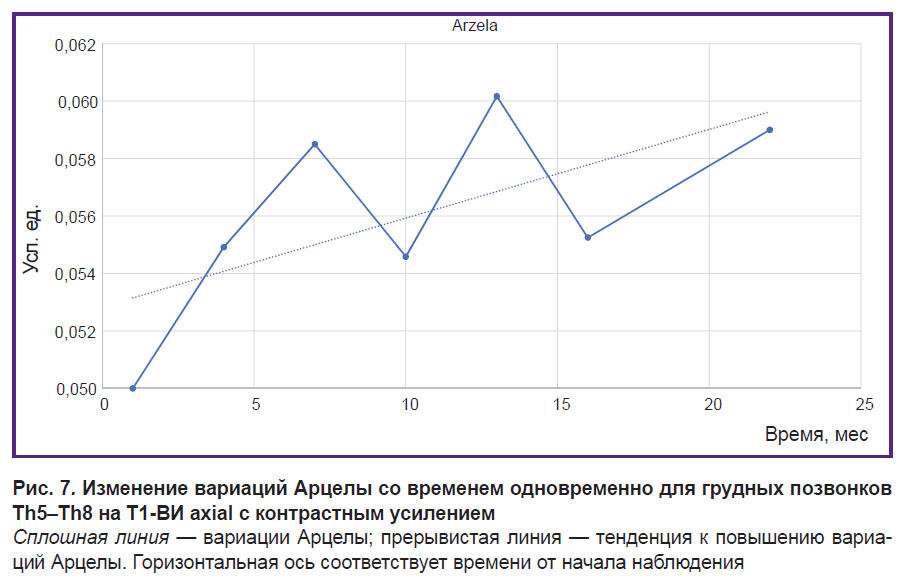
Для улучшения статистических результатов проанализированы разные сегменты нескольких позвонков одновременно, тем самым был нивелирован статистический разброс. Результаты AV для большого объема, включающие грудные позвонки Th5–Th8, представлены на рис. 7.
Видно, что поведение кривой при большем объеме позвонков аналогично поведению кривой для отдельных позвонков, что позволяет сделать важный вывод: увеличение исходных значений может быть использовано для быстрой оценки терапии. При этом асимптотическое поведение (пунктирная линия) может быть использовано для выявления положительного суммарного эффекта терапии в долгосрочной перспективе.
Результат расчета AV на сагиттальной проекции без контрастного вещества (T1-ВИ sag и T2-ВИ sag) оказался несколько неожиданным. В начале исследования предполагалось, что аксиальная проекция поверхностей позвонков является наиболее чувствительной, что в принципе и было подтверждено. Однако избирательность к опухоли оказалась ниже, чем в сагиттальной проекции. После подтверждения данной теории результаты будут представлены в наших последующих работах.
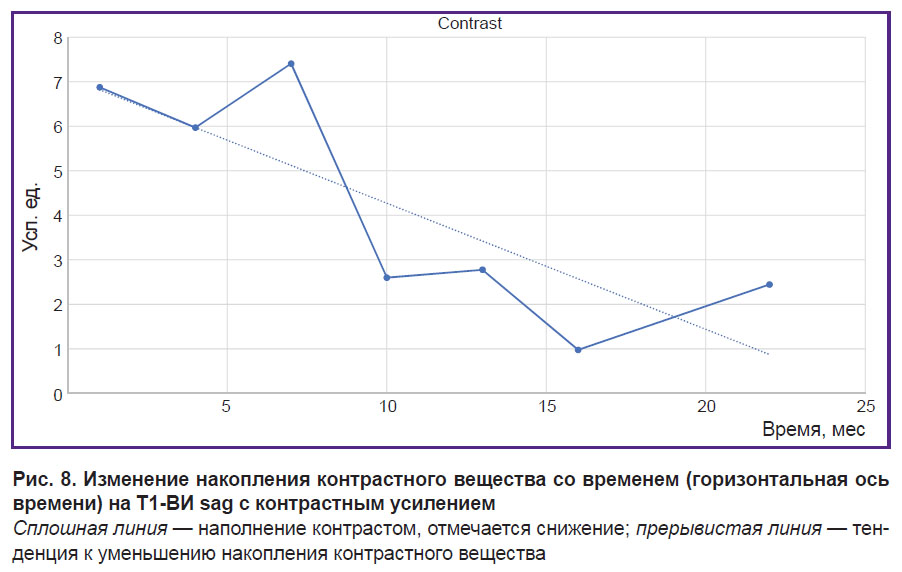
При измерении контраста на Т1-ВИ sag с контрастным усилениемполучается количественная кривая приема контрастного вещества как функция длительного времени на всем регистрируемом участке позвоночника (рис. 8).
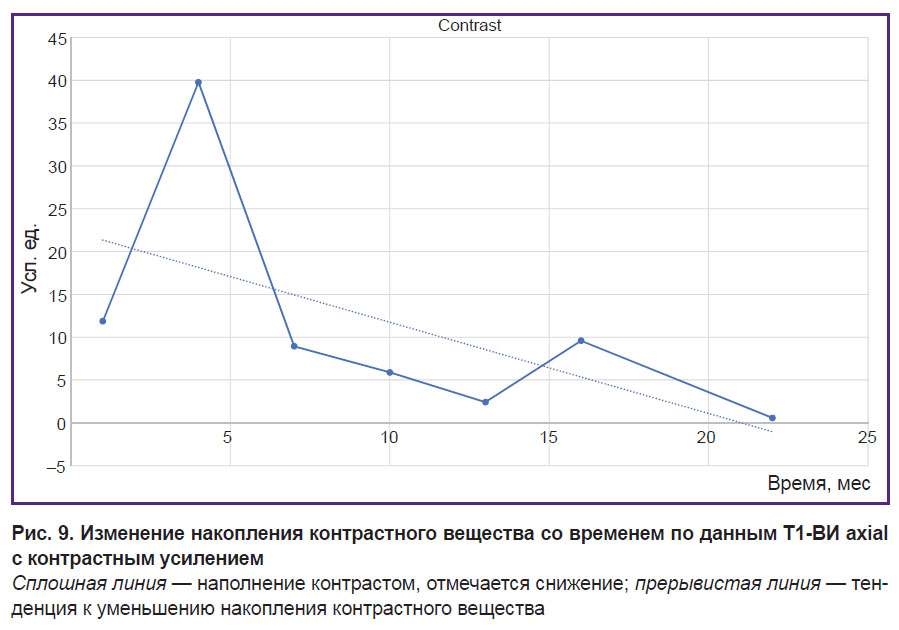
Полученные данные накопления контраста были проверены в аксиальной проекции с помощью того же метода, при этом все настройки оставались без изменений: пороговые значения средней интенсивности изображения (серое значение) (рис. 9).
Сравнение кривых в аксиальной и сагиттальной проекциях показывает, что они не принципиально изменяют свое локальное поведение и при этом сохраняют все глобальные свойства. Таким образом, мы наблюдаем в нашем случае падение накопления контраста до некоторого асимптотического значения. Такой анализ контрастного накопления позволяет количественно оценить долгосрочные изменения активности процессов в исследуемой зоне (тела позвонков) по данным МРТ.
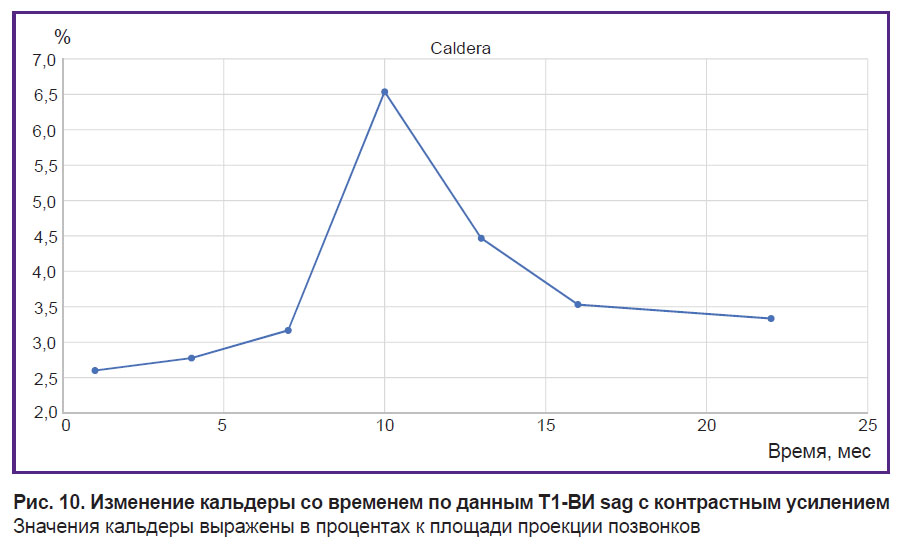
Микрофокусы, или микроочаги. Конечный результат при их анализе, как уже было сказано, является суммированием всех значений кальдеры для всех грудных позвонков. На представленном графике (рис. 10) максимум соответствует сферически- или радиально-симметричным ободкообразующим объектам, с большой вероятностью — с подавленными очагами. Таким образом, примерно через 10 мес после начала терапии достигается максимальное подавление очагов и со временем этот процесс сменяется склерозированием образовавшихся ниш.
|
Рис. 10. Изменение кальдеры со временем по данным T1-ВИ sag с контрастным усилением Значения кальдеры выражены в процентах к площади проекции позвонков |
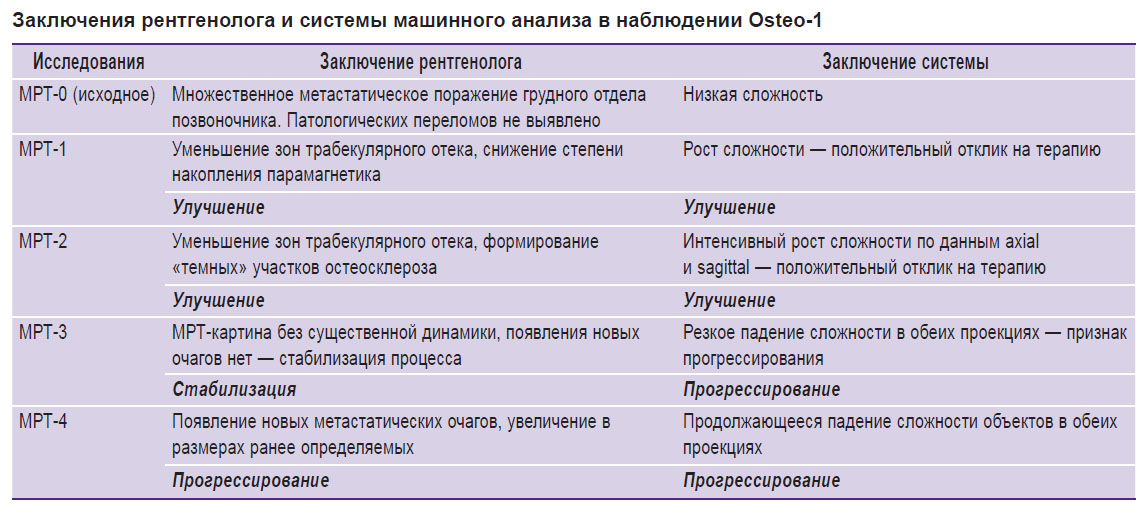
Интерпретация полученных данных. Достигнута высокая степень совпадения оценок радиолога и системы машинного анализа — 9 из 12. В двух случаях установлено несоответствие заключения рентгенолога как «стабилизация» с оценкой системы как «прогрессирование», дальнейшее наблюдение показало ухудшение. В одном случае отмечено расхождение заключения рентгенолога как «стабилизация» с оценкой системы как «улучшение» ввиду повышения сложности объектов. В качестве примера приводим форму отчета по наблюдению Osteo-1 (см. таблицу).
|
Заключения рентгенолога и системы машинного анализа в наблюдении Osteo-1 |
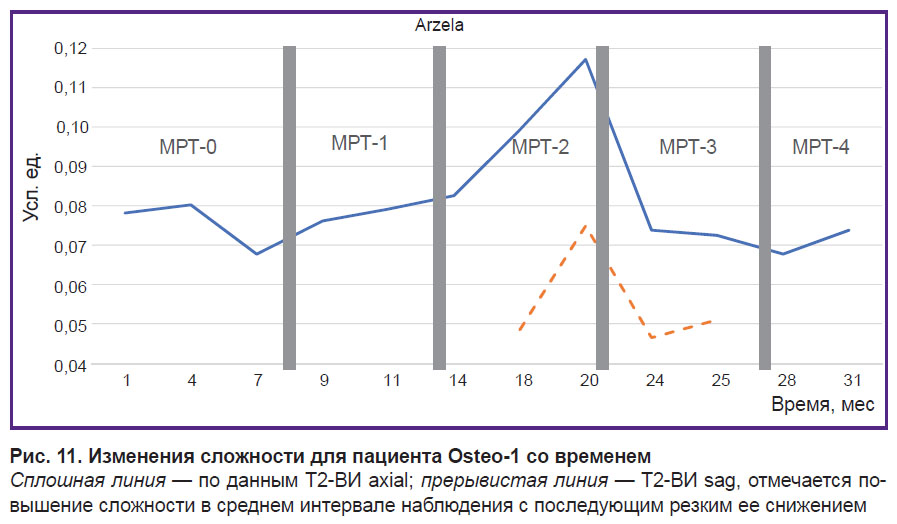
Для построения зависимости изменений были использованы 50 аксиальных срезов МРТ Т2-ВИ, всего около 600 измерений (рис. 11).
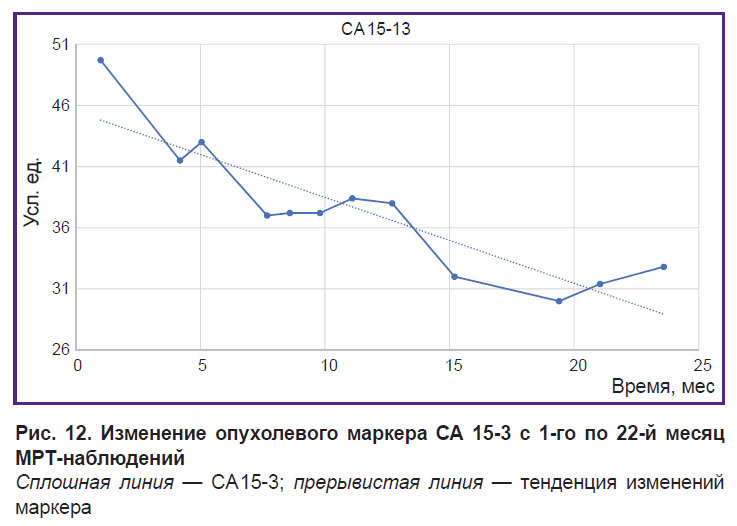
В качестве иллюстрации возможности дополнительного контроля за процессом терапии приводим изменения классического показателя — опухолевого маркера CA 15-3 — в случае пациента с установленным регрессом опухоли (рис. 12). Значения изменений маркера оценивали по принятым клиническим рекомендациям [11]. Из рисунков видно, что CA 15-3 хорошо коррелирует с AV, Contrast и Caldera в долгосрочной перспективе. Коэффициент Пирсона между AV и CA 15-3 составил в этом случае 0,8.
|
Рис. 12. Изменение опухолевого маркера СА 15-3 с 1-го по 22-й месяц МРТ-наблюдений
Сплошная линия — CA 15-3; прерывистая линия — тенденция изменений маркера |
Обсуждение
Подводя итог работе, еще раз отметим важный, на наш взгляд, и отраженный в литературе факт, от которого мы отталкивались в своих рассуждениях: на микроуровне при остеокластическом варианте рака молочной железы метастатическое поражение обычно представлено круглым или овальным дефектом, прослеживается эффект радиальной или сферической симметрии, изменяющейся под воздействием терапии [12]. По мере протекания лечения графическое изображение метастатического поражения меняется. Наиболее важным диагностическим признаком положительной тенденции лечения является повышение плотности костной структуры в месте поражения [13]. Широкий охват нашего алгоритма (работает при разных видах костных метастазов) обусловлен тем, что первое проявление репарации при остеокластических метастазах — появление склеротического ободка вокруг литического очага и последующее постепенное заполнение очага костной тканью — происходит у 93% пациентов в течение 3–6 мес после начала успешного лечения [14].
С помощью использованных в исследовании операторов нам удалось отследить ответ на терапию рака молочной железы с костными метастазами на трех схожих клинических наблюдениях. Мы понимаем, что этого недостаточно для получения однозначных выводов, поэтому постарались повысить достоверность за счет анализа одновременно нескольких позвонков у пациенток в нескольких режимах МРТ. В дальнейшем представленный алгоритм будет распространен на другие МРТ-последовательности, а также на данные КТ. В процессе исследования удалось установить несколько ограничений используемых методов.
Заключение
Проведенное исследование показало высокий процент совпадения врачебного и машинного анализа состояния рака молочной железы с метастатическим поражением позвоночника (в случае регресса корреляция достигла 0,8 по Пирсону). Подобный подход можно использовать в качестве поддержки принятия врачебного решения, однако сам процесс принятия решений требует дальнейшего развития, в первую очередь в направлении классификации результатов с помощью нейронных сетей, как мы ранее это использовали при автоматической классификации лейкоцитов [15].
Система машинного анализа позволяет глубже понять взаимосвязь между морфологией и характеристиками процессов при метастатическом раке молочной железы, более полно оценить эффект терапии.
Благодарности. Мы хотели бы поблагодарить компанию Devoteam GmbH (Weiterstadt, Германия) за поддержку публикации статьи и лично A. Klingel (Management of Devoteam GmbH), Prof. Dr. med. G. Hartung (руководителя онкологического центра в Groß-Gerau, Германия) за многочисленные конструктивные комментарии по онкологическим вопросам; к.м.н. Е.А. Власова (Лечебно-диагностический центр на Вернадского, Москва) — за многочисленные комментарии по МРТ. Мы также благодарим биоинформатика М. Steinhauer за терминологические замечания.
Источник финансирования. Работа не финансировалась никакими источниками.
Конфликт интересов отсутствует.
Литература
- Cardoso F., Kyriakides S., Ohno S., Penault-Llorca F., Poortmans P., Rubio I.T., Zackrisson S., Senkus E., ESMO Guidelines Committee. Early breast cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2019; 30(8): 1194–1220, https://doi.org/10.1093/annonc/mdz173.
- Tagliafico A.S., Piana M., Schenone D., Lai R., Massone A.M., Houssami N. Overview of radiomics in breast cancer diagnosis and prognostication. Breast 2020; 49: 74–80, https://doi.org/10.1016/j.breast.2019.10.018.
- Сергеев Н.И., Котляров П.М., Солодкий В.А., Близнюков О.П. Метастатическое поражение костей при раке молочной железы по данным высокопольной магнитно-резонансной томографии. Вестник Российского научного центра рентгенорадиологии 2012; 12(1): 15.
- Parekh V.S., Jacobs M.A. Integrated radiomic framework for breast cancer and tumor biology using advanced machine learning and multiparametric MRI. NPJ Breast Cancer 2017; 3: 43, https://doi.org/10.1038/s41523-017-0045-3.
- Hardisty M., Gordon L., Agarwal P., Skrinskas T., Whyne C. Quantitative characterization of metastatic disease in the spine. Part I. Semiautomated segmentation using atlas-based deformable registration and the level set method. Med Phys 2007; 34(8): 3127–3134, https://doi.org/10.1118/1.2746498.
- Chochia P.A., Milukova O.P. Two-dimensional variations comparison in the context of digital image complexity assessment. J Commun Technol Electron 2015; 60: 1443–1440, https://doi.org/10.1134/s1064226915120049.
- Image processing. BOOFCV; 2021. URL: https://boofcv.org/index.php?title=Main_Page.
- AlNouri M., Al Saei J., Younis M., Bouri F., Al Habash M.A., Shah M.H., Al Dosari M. Comparison of edge detection algorithms for automated radiographic measurement of the carrying angle. J Biomed Eng Med Imaging 2015; 12: 78–98, https://doi.org/10.14738/jbemi.26.1753.
- Даниленко В.И. Симметрия и рак. Методология и морфогенез. Саарбрюккен, Германия: LAP LAMBERT Academic Publishing; 2017; с. 85.
- Цориев А.Э. Опухоли позвоночника. Екатеринбург: УГМУ; 2021. URL: http://www.obtc.ru/spetsialistam/glavnyy- vneshtatnyy-spetsialist-po-luchevoy-i-instrumentalnoy- diagnostike/tsoriev_opuholi.pdf.
- Di Gioia D., Stieber P., Schmidt G.P., Nagel D., Heinemann V., Baur-Melnyk A. Early detection of metastatic disease in asymptomatic breast cancer patients with whole-body imaging and defined tumour marker increase. Br J Cancer 2015; 112(5): 809–818, https://doi.org/10.1038/bjc.2015.8.
- Najafi M., Mortezaee K., Ahadi R. Cancer stem cell (a)symmetry & plasticity: tumorigenesis and therapy relevance. Life Sci 2019; 231: 116520, https://doi.org/10.1016/j.lfs.2019.05.076.
- Сергеев Н.И., Котляров П.М., Нуднов Н.В. Оценка результатов химиолучевого лечения вторичного поражения костей по данным магнитно-резонансной томографии с динамическим контрастным усилением. Лучевая диагностика и терапия 2013; 3(4): 89–92.
- Петрова А.Д. Оценка эффективности лекарственного лечения метастазов в костях у больных раком молочной железы. Дис. … канд. мед. наук. М; 2014.
- Steinhauer V., Steinhauer L. Neuroph und DL4J. Einsatz in einer medizinischen Java-Anwendung. Java Magazin 2021; 06: 79–82.