Зависимость биологических свойств скаффолдов из фиброина шелка и желатина от состава и технологии изготовления
Цель исследования — сравнение биологических свойств скаффолдов из фиброина шелка и желатина в зависимости от способа их получения и состава субстрата.
Материалы и методы. Методами электроспиннинга и полива были изготовлены скаффолды из фиброина шелка и желатина, а также композитов с различным массовым соотношением фиброина и желатина. Изучение структуры изделий проведено методами световой микроскопии, сканирующей электронной микроскопии, лазерной конфокальной сканирующей микроскопии. Для проверки биосовместимости полученных изделий была изучена активность адгезии и пролиферации культуры мышиных фибробластов линии 3Т3 на их поверхности.
Результаты. Подобраны оптимальные параметры получения волокна из растворов фиброина шелка и желатина. Показано, что пролиферативная активность фибробластов 3Т3 на скаффолдах, изготовленных методом электроспиннинга, выше, чем на пленках, полученных методом полива. Добавление желатина в состав скаффолда увеличивает пролиферацию клеток.
Заключение. Композитные скаффолды, полученные методом электроспиннинга из фиброина шелка с желатином в соотношении 1:3 по массе, обладают большей способностью поддерживать пролиферацию фибробластов 3Т3, чем скаффолды из чистых полимеров.
Одной из важных задач, стоящих перед современной тканевой инженерией, является создание конструкций (скаффолдов), имитирующих микроархитектуру нативного внеклеточного матрикса тканей и органов и создающих благоприятную среду для культивирования клеток. При создании таких конструкций большое значение имеет правильный подбор материала. В настоящее время в тканевой инженерии и регенеративной медицине используются как синтетические полимеры, так и природные. К преимуществам природных полимеров можно отнести отсутствие у них токсичных продуктов распада и их включение в метаболические пути клеток. Природные полимеры, такие как коллаген, желатин, хитозан, альгинаты и т.д., успешно применяются в тканевой инженерии, однако ни один из них не является универсальным для создания конструкций с заданными свойствами, поскольку природные особенности полимеров (механические свойства, растворимость, уровень иммуногенности) накладывают ограничения на их использование.
Фиброин шелка тутового шелкопряда Bombyx mori является одним из наиболее перспективных природных полимеров для тканевой инженерии. Различными группами исследователей показано, что скаффолды на основе фиброина успешно поддерживают регенерацию кишечника, восстановление нервной и костной ткани [1]. Фиброин является фибриллярным белком с большим количеством повторов в первичной структуре. Вторичная структура фиброина представляет собой антипараллельные β-слои, объединенные водородными связями. Аморфные участки белка образуют α-спирали, доля которых возрастает при гидратации фиброина. Механические свойства и скорость биодеградации изделий из фиброина шелка можно контролировать, изменяя долю β-слоев в его структуре [2]. В третичной структуре фиброина выделяют две цепи: тяжелую и легкую с молекулярной массой 390 и 26 кДа соответственно, которые присутствуют в отношении 1:1 и соединены одной дисульфидной связью [3]. Такая структура фиброина шелка обеспечивает наличие свободных химических групп, которые могут быть использованы для создания конъюгатов и композитов с улучшенными свойствами [4–6].
Одним из современных методов получения скаффолдов является метод электроспиннинга [7]. Принцип его заключается в том, что под действием электрического поля из раствора полимера происходит вытягивание тонких волокон, которые затем попадают на катод, где происходит их окончательное высыхание. Установка для электроспиннинга состоит из трех основных компонентов: устройства для подачи раствора полимера, источника высокого напряжения и коллектора, являющегося катодом. В зависимости от выполняемой задачи применяют различные модификации установок, использующие изменение положения устройства подачи раствора, коллектора, расстояния между частями установки и др. При этом оптимальные параметры для получения волокон подбираются индивидуально для каждого материала в зависимости от целей эксперимента.
Электроспиннинг позволяет получать сети как с хаотичным, так и с ориентированным распределением волокон [8]. Ориентированная структура изделий дает возможность задавать направление роста клеток, что особенно важно при работе с мышечной или нервной тканью. Кроме того, этот метод позволяет создавать изделия со структурой, схожей с архитектурой костной ткани, что указывает на перспективы его использования в восстановлении кости [9]. К достоинствам изделий, полученных методом электроспиннинга, можно отнести высокое отношение поверхности к объему, значительную пористость, улучшенные физико-механические свойства, возможность варьирования толщины волокна.
Метод электроспиннинга широко применяется в современных исследованиях для создания искусственных сухожилий [10], восстановления нервной ткани [11], получения сосудистых имплантатов [12–14] и регенерации кости [15]. Изделия, синтезированные с помощью рассматриваемого метода, успешно испытаны в экспериментах как in vitro, так и in vivo [16]. В нашей работе впервые проведено сравнительное изучение биологических свойств полимеров и их композитов при использовании разных методов изготовления.
Цель исследования — сравнительный анализ биологических свойств скаффолдов из фиброина шелка, композита фиброина и желатина и оценка влияния способа их получения на способность поддерживать клеточную адгезию и пролиферацию.
Материалы и методы
Получение фиброина шелка. Фиброин шелка получали из коконов тутового шелкопряда B. mori, предоставленных Республиканской научно-исследовательской станцией шелководства Российской академии сельскохозяйственных наук. На первом этапе коконы подвергали очистке от серицина. Навеску шелка из коконов массой 1 г кипятили на водяной бане в 500 мл бидистиллированной воды с добавлением 1260 мг гидрокарбоната натрия (PanReac Applichem, Германия) в течение 40 мин. Затем промывали 3,6 л дистиллированной воды. Далее кипятили в 500 мл бидистиллированной воды 30 мин и промывали 3,6 л дистиллированной воды. Последнюю процедуру повторяли 3 раза. Очищенный фиброин шелка сушили на воздухе при комнатной температуре.
Получение водного раствора фиброина шелка. Для получения водного раствора фиброина навеску отмытого шелка переносили в раствор бромида лития (Sigma-Aldrich, США) с концентрацией 9,3 М из расчета 150 мг/мл и растворяли в течение 5 ч на водяной бане. Полученный раствор центрифугировали в течение 7 мин при 12100 g. Супернатант диализовали против 500 мл бидистиллированной воды, всего проводили 10 смен диализа по 30 мин. Раствор фиброина центрифугировали 7 мин при 12 100 g, концентрацию фиброина определяли спектрофотометрически при длине волны 280 нм, молярный коэффициент экстинкции принимали равным 473 480 М–1см–1, что соответствует теоретически рассчитанному коэффициенту экстинкции по аминокислотной последовательности тяжелой цепи фиброина шелка (номер в базе данных UniProt: P05790).
Получение раствора фиброина в 1,1,1,3,3,3-гексофторизопропаноле-2. Предварительно из фиброина получали высушенные пленки. Для изготовления пленки диаметром 1 см наносили 100 мкл водного раствора фиброина шелка на поверхность полированного тефлона и высушивали в течение двух дней при комнатной температуре. Общая концентрация белка в растворе для изготовления пленки составляла 20 мг/мл. Пленки снимали с поверхности тефлона с помощью скальпеля, предварительно инкубировав их в спирте в течение 15 мин, и хранили в 96% спирте при температуре 4°С. Раствор полимера получали путем растворения высушенной пленки из фиброина шелка в 1,1,1,3,3,3-гексофторизопропаноле-2 («ПиМ-инвест», Россия) при температуре 37°С до концентрации 75 мг/мл.
Получение раствора желатина в 1,1,1,3,3,3-гексофторизопропаноле-2. Для получения раствора желатина навеску сухого желатина типа А (Sigma-Aldrich, США) растворяли в 1,1,1,3,3,3-гексофторизопропаноле-2 при температуре 37°С до концентрации 75 мг/мл.
Изготовление скаффолдов из фиброина шелка и желатина. Скаффолды получали методом электроспиннинга из подготовленных растворов полимеров в 1,1,1,3,3,3-гексофторизопропаноле-2 с концентрацией 75 мг/мл. Было изготовлено 5 групп образцов по 5 штук, в каждой группе с разным соотношением используемых белков по массе: 1-я группа — фиброин; 2-я группа — фиброин и желатин — 1:3; 3-я группа — фиброин и желатин — 1:1; 4-я группа — фиброин и желатин — 3:1; 5-я группа — желатин. Полученные растворы полимеров непосредственно перед электроспиннингом центрифугировали в течение 10 мин при 12 100 g. Скаффолды получали на поверхности круглых стекол диаметром 2 см, обработанных 96% этиловым спиртом. Для подачи раствора использовали иглу калибра 22G, внутренний диаметр которой составлял 0,41 мм, внешний диаметр — 0,70 мм (Messe Düsseldorf Japan Ltd.).
При получении волокон из образцов 1-й и 5-й групп использовали следующие параметры: напряжение источника тока — 5,8 кВ («Научная электроника», Россия), скорость подачи раствора — 0,2 мл/ч; для образцов из остальных групп напряжение источника тока составляло 7 кВ, скорость подачи раствора — 0,3 мл/ч. Время напыления одного полимера — 20 мин. Стекла со скаффолдами высушивали при комнатной температуре в течение 2 ч. Образцы из 100% желатина с целью ковалентной перешивки дополнительно обрабатывали 0,3% раствором глутарового альдегида (Serva, Германия) в этиловом спирте в течение 12 ч в темноте при комнатной температуре. Все скаффолды окончательно обрабатывали 96% этиловым спиртом на протяжении 1 ч, после чего высушивали и хранили при комнатной температуре.
Изготовление пленок из полимеров методом полива. Для изготовления пленок методом полива раствор желатина или фиброина шелка в 1,1,1,3,3,3-гексофторизопропаноле-2 с концентрацией 75 мг/мл наносили на стекла диаметром 2 см и высушивали в течение 12 ч при комнатной температуре. Пленки из желатина дополнительно обрабатывали 0,3% раствором глутарового альдегида в этиловом спирте в течение 12 ч в темноте при комнатной температуре.
Анализ структуры скаффолдов методом сканирующей электронной микроскопии. Образцы скаффолдов фиксировали в 2,5% растворе глутарового альдегида в фосфатно-солевом буфере. Затем их дегидратировали возрастающими концентрациями этанола — 10, 30, 50, 70, 95% и помещали в ацетон («Химмед», Россия). После этого образцы высушивали методом перехода критической точки с помощью прибора HCP-2 (Hitachi Ltd., Япония). Высушенные образцы покрывали слоем хрома толщиной 20 нм в атмосфере аргона при ионном токе 6 мА и давлении 0,1 мм рт. ст. с использованием прибора IonCoater IB-3 (Eiko Engineering, Япония), затем анализировали с помощью сканирующего электронного микроскопа Camscan S2 (Cambridge Instruments, Великобритания) с разрешением 10 нм, рабочим напряжением 20 кВ. Изображения получали с использованием программного обеспечения MicroCapture.
Анализ адгезии и пролиферативной активности мышиных фибробластов линии 3Т3 на скаффолдах. Для исследования адгезии и пролиферативной активности образцы стекол с нанесенными скаффолдами переносили в культуральные чашки диаметром 35 мм. В качестве контроля использовали стекло без скаффолда. Перед проведением теста скаффолды в чашках подвергали стерилизации обработкой 70% спиртом в течение 12 ч. Затем в чашки вносили стерильный раствор фосфатно-солевого буфера на 30 мин, смену фосфатно-солевого буфера проводили 3 раза. Далее в чашки вносили по 1,5 мл среды инкубации, состоящей из Dulbecco’s Modified Eagle’s Medium — low glucose (Sigma-Aldrich, США) и Ham’s F12 (Flow laboratories, Великобритания) в соотношении 1:1, содержащей 10% эмбриональной телячьей сыворотки (HyClone, США), 40 мкг/мл гентамицина («Ферейн», Россия), 4 мМ глутамина («ПанЭко», Россия), и инкубировали в течение 15 мин.
Суспензию мышиных фибробластов 3Т3 в среде инкубации вносили в культуральные чашки по 2 мл, из расчета 9000 клеток на 1 см2 поверхности. Клетки инкубировали в термостате при 37°С, в среде 5% CO2. Анализ адгезии проводили через 12 ч после культивирования, а пролиферативную активность клеток оценивали на 3-и и 5-е сутки культивирования.
Оценку пролиферативной активности клеток проводили визуально с помощью микроскопа Carl Zeiss Axiovert 25 (Carl Zeiss, Германия). Изображения клеток на скаффолдах в проходящем свете и в режиме фазового контраста получали с помощью камеры AxioCam HRC (Carl Zeiss, Германия), далее изображения обрабатывали в программе AxioVision 3.1 (Carl Zeiss, Германия). По этим изображениям проводили подсчет клеток в поле зрения микроскопа. Полученное среднее значение количества клеток при данном увеличении пересчитывали на площадь скаффолда.
Анализ структуры скаффолдов методом лазерной конфокальной сканирующей микроскопии. Образцы скаффолдов фиксировали параформальдегидом (Sigma-Aldrich, США), отмывали от фиксатора фосфатно-солевым буфером в течение 10 мин, смену буфера проводили 3 раза. Затем готовили раствор красителя TRITC (Sigma-Aldrich, США) с концентрацией 10 мкг/мл в фосфатно-солевом буфере, после чего вносили его в культуральные чашки со скаффолдами в фосфатно-солевом буфере и инкубировали 1 ч при комнатной температуре. Реакцию останавливали, помещая образец в 0,1 М раствор трис(гидроксиметил) аминометана (Helicon, Россия) на 30 мин. Отмывку образцов проводили фосфатно-солевым буфером 3 раза по 10 мин, потом инкубировали их в 70% этиловом спирте в течение 30 мин. После этого снова проводили трехкратную отмывку образцов фосфатно-солевым буфером. Полученные образцы исследовали с помощью лазерного сканирующего конфокального микроскопа Axiovert 200M LSM510 META (Carl Zeiss Jena, Германия). Флюоресценцию в образцах возбуждали гелиево-неоновым лазером с длиной волны 543 нм. Анализ полученных изображений проводили с помощью программы LSM Image Browser (Carl Zeiss Jena, Германия).
Статистическая обработка данных. Данные обрабатывали методом дисперсионного анализа. Статистическую значимость результатов оценивали с помощью критерия Манна–Уитни. Уровень статистической значимости p принимали равным 0,05.
Результаты и обсуждение. Один из методов изготовления искусственных конструкций для тканевой инженерии — электроспиннинг, преимуществом которого является возможность получения структур, состоящих из микро- и нановолокон. Данные волокна имитируют структуру внеклеточного матрикса органов и тканей. Схема стандартной установки для изготовления скаффолдов методом электроспиннинга приведена на рис. 1.
|
|
Установка состоит из насоса, шприца с тупоконечной иглой, соединенной с источником высокого напряжения, а также отрицательно заряженного коллектора. В результате проведения ряда экспериментов были подобраны оптимальные параметры установки для работы с растворами фиброина шелка и желатина: насос располагали под углом 45° к плоскости опоры, расстояние между коллектором и концом иглы — 3 см. Варьирование параметров установки дает возможность изменять диаметр и плотность распределения волокна, что позволяет получать конструкции с заданным показателем пористости.
В качестве растворителя нами был выбран 1,1,1,3,3,3-гексафторизопропанол-2, являющийся одним из часто применяемых растворителей для электроспиннинга вследствие его высокой летучести, что позволяет обеспечить быстрое высыхание волокна в процессе его оседания на коллекторе.
В данной работе методом электроспиннинга на поверхности стекол были изготовлены скаффолды на основе двух полимеров — фиброина шелка и желатина, а также их композита с различным массовым соотношением фиброина и желатина. Каждый скаффолд представлял собой равномерно распределенные по поверхности стекла волокна, уложенные в несколько слоев (рис. 2).
|
|
Количественные характеристики скаффолда зависят от параметров получения волокна. К таким параметрам относятся скорость подачи раствора, напряжение, подаваемое на конец иглы, а также время нанесения волокна [7]. Кроме того, на свойства получаемого скаффолда оказывают влияние концентрация рабочего раствора полимера и диаметр иглы. Неправильный подбор параметров приводит к обрыву волокон полимера и формированию капель раствора полимера в составе скаффолда (рис. 3).
|
|
Такие дефекты негативно сказываются на характеристиках получаемой конструкции, что в свою очередь негативно влияет на адгезию и пролиферацию клеток. Параметры, подобранные в данной работе, не вызывают описанных выше процессов и не приводят к появлению дефектов.
Структуру полученных скаффолдов изучали методами микроскопии. Методом световой микроскопии установлено, что скаффолды представляют собой равномерно распределенные по поверхности стекла волокна, уложенные в несколько слоев (рис. 4, а). Полученная структура была подтверждена методом сканирующей электронной микроскопии (рис. 4, б). В ходе анализа образца было выявлено, что волокна фиброина шелка в составе скаффолда образуют многослойную пористую структуру. Это явление может способствовать пролиферации и миграции клеток внутри изделия, тем самым улучшая его свойства как имплантата [17]. Аналогичная структура была отмечена для образцов других групп.
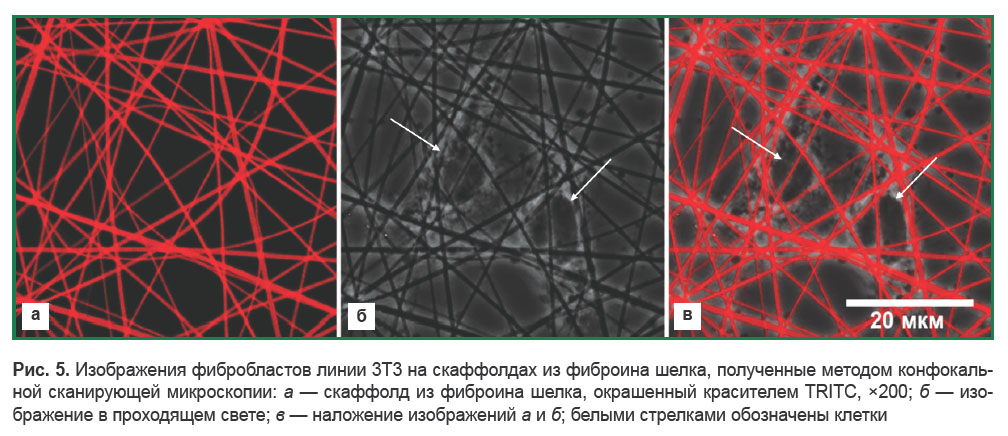
Для анализа структуры скаффолда из фиброина шелка в водной среде использован метод лазерной сканирующей конфокальной микроскопии. С целью измерения толщины волокна в составе скаффолдов, на которых предварительно культивировали фибробласты линии 3Т3 (рис. 5), получены изображения волокон фиброина шелка. Средняя толщина волокна составила 0,5±0,2 мкм.
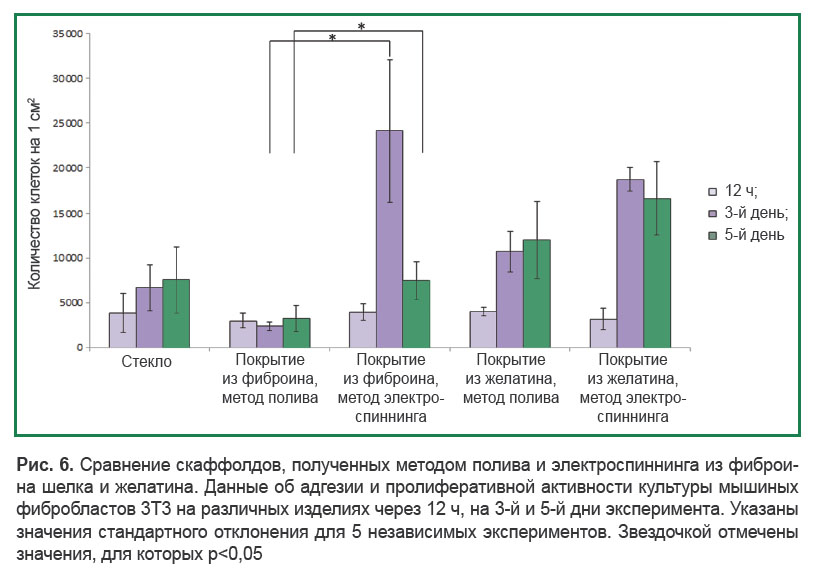
Для доказательства влияния структуры полученных конструкций, природы и состава используемых полимеров на адгезию и пролиферацию клеток проведено сравнение активности адгезии и пролиферации фибробластов линии 3Т3 на скаффолдах из фиброина шелка и желатина, изготовленных двумя разными способами: методом электроспиннинга и методом полива (рис. 6). В отличие от скаффолдов, выполненных методом электроспиннинга, конструкции, получаемые методом полива, характеризуются отсутствием пористости.
Адгезию оценивали через 12 ч после начала эксперимента. Выяснено, что количество фибробластов линии 3Т3, прикрепившихся к различным образцам скаффолдов, существенно не отличалось. Пролиферацию клеток оценивали на 3-и и 5-е сутки эксперимента. Количество клеток на скаффолдах, изготовленных из желатина методом электроспиннинга, на 3-и сутки эксперимента было незначительно больше, чем на покрытиях аналогичного состава, полученных методом полива. Однако на 5-е сутки эксперимента статистически значимых различий пролиферативной активности клеток между рассматриваемыми образцами не было. Это может объясняться тем, что желатин, являясь продуктом денатурации коллагена, содержит в своей структуре последовательность RGD, которая связывается с рецепторами-интегринами на мембранах фибробластов, тем самым запуская их пролиферацию [18]. Таким образом, в данном случае различия в пористости изделия не оказывают влияния на пролиферативную активность клеток. Желатин характеризуется хорошей способностью к поддержанию пролиферативной активности клеток [19].
Напротив, пролиферативная активность клеток на скаффолдах, изготовленных из фиброина шелка двумя различными методами, существенно различалась и была выше на изделиях, полученных методом электроспиннинга, поскольку такие конструкции характеризуются высокой пористостью и волокнистой структурой, которая создает благоприятные условия для пролиферации фибробластов, так как имитирует архитектуру нативного внеклеточного матрикса. Уменьшение пролиферативной активности клеток на скаффолдах, полученных методом электроспиннинга, на 5-е сутки эксперимента можно объяснить контактным торможением [20].
Количество клеток на изделиях из желатина увеличивалось в течение эксперимента, а распределение клеток в образцах было равномерным, что также подтверждает способность желатина поддерживать пролиферацию клеток. Это согласуется с большим количеством литературных данных о том, что использование желатина в качестве материала для культивирования клеток и изготовления конструкций для тканевой инженерии значительно повышает уровень клеточной адгезии [21–23], запускает пролиферацию и дифференцировку остеогенных клеток, действуя как натуральный компонент внеклеточного матрикса [24]. В то же время существуют работы, в которых отмечаются недостаточные для осуществления хирургических манипуляций значения механических характеристик изделий из желатина, что ограничивает возможное применение последних. Помимо этого, использование желатина ограничивается его высокой растворимостью в воде и быстрой биорезорбцией в организме [25].
В то же время фиброин шелка характеризуется уникальными механическими свойствами, однако пролиферативная активность клеток на изделиях из фиброина шелка ниже, чем на изделиях из желатина [26, 27].
Одним из возможных путей решения данной проблемы является создание композитных материалов с улучшенными адгезионными свойствами и оптимальными значениями механических показателей. Поэтому задача второго эксперимента заключалась в поиске оптимального соотношения желатина и фиброина в составе композита, которое бы обеспечивало адгезию и пролиферацию клеток, но при этом позволяло избежать быстрой резорбции волокна.
Нами были изготовлены три группы образцов с различным массовым соотношением фиброина шелка и желатина: 3:1, 1:1 и 1:3. Через 12 ч после начала эксперимента произошла успешная и примерно равная адгезия фибробластов ко всем образцам. Пролиферативная активность клеток на различных образцах оценивалась на 3-и и 5-е сутки эксперимента (рис. 7).
На 3-и сутки эксперимента произошло увеличение пролиферативной активности клеток на образцах, содержащих желатин, на 5-е сутки — увеличение количества клеток на всех композитных покрытиях. При этом была отмечена прямая зависимость пролиферативной активности клеток от содержания желатина в образце. Однако на скаффолдах из желатина количество клеток на 5-е сутки эксперимента не изменилось по сравнению с 3-ми сутками. Это можно объяснить тем, что образцы, полученные из желатина без композитной добавки, фиксировали 0,3% раствором глутарового альдегида, чтобы избежать нарушения их структуры вследствие растворения желатина в ходе эксперимента. Известно, что глутаровый альдегид является токсичным для клеток и негативно влияет на пролиферацию клеток в изделии [28].
Наибольшая пролиферативная активность клеток была выявлена на скаффолдах с массовым соотношением фиброина и желатина 1:3. Количество клеток на данных образцах было в 2,5 раза больше, чем на покрытиях из чистого желатина, и в 5 раз больше, чем на покрытиях из фиброина шелка. Достижение этого эффекта может быть связано с тем, что такое сочетание полимеров обеспечивает оптимальное распределение на поверхности волокна аминокислотной последовательности RGD в составе желатина, а также образование нерастворимого высокопористого скаффолда за счет наличия фиброина шелка в композите. Кроме того, на эффективность адгезии, жизнеспособность, скорость пролиферации и миграции клеток влияет заряд поверхности субстрата. Внесение желатина в состав пленок на основе несущего отрицательный заряд при нейтральном pH фиброина могло позволить улучшить эффективность адгезии клеток к такому субстрату. Так, пористые скаффолды и микрогели из рекомбинантного аналога спидроина — структурного белка шелка паутины, обладающего положительным зарядом при физиологических значениях pH, являются прекрасным субстратом для адгезии и пролиферации клеток in vitro, а также индуцируют нейро- и ангиогенез in vivo, что очень важно для регенерации различных типов тканей, включая полые органы желудочно-кишечного тракта, костную ткань, кожу и др. [29, 30].
Заключение. Сравнительный анализ биологических свойств скаффолдов из фиброина шелка и желатина, полученных разными способами, показал, что метод электроспиннинга позволяет изготавливать изделия с улучшенными физико-химическими свойствами, которые оказывают позитивное влияние на их биосовместимость. Оптимального сочетания структуры и биосовместимости можно достичь путем использования композитных скаффолдов с массовым соотношением фиброина и желатина 1:3, полученных методом электроспиннинга.
Благодарности. Авторы выражают благодарность директору Республиканской научно-исследовательской станции шелководства Российской академии сельскохозяйственных наук (Ставропольский край, Железноводск) В.В. Богословскому за предоставление коконов тутового шелкопряда B. mori.
Финансирование исследования. Работа выполнена при поддержке Минобрнауки РФ по Соглашению о предоставлении субсидии от 27 октября 2015 г. №14.607.21.0119 «Создание набора прототипов изделий из биоискусственной костной ткани и модуляторов остеогенеза для регенеративной медицины», уникальный идентификатор соглашения RFMEFI60715X0119.
Конфликт интересов. У авторов нет конфликта интересов.
Литература
- Vepari C., Kaplan D.L. Silk as a biomaterial. Prog Polym Sci 2007; 32(8–9), 99–1007, http://dx.doi.org/10.1016/j.progpolymsci.2007.05.013.
- Kasoju N., Bora U. Silk fibroin based biomimetic artificial extracellular matrix for hepatic tissue engineering applications. Biomed Mater 2012; 7(4): 045004, http://dx.doi.org/10.1088/1748-6041/7/4/045004.
- Kim U.J., Park J., Kim H.J., Wada M., Kaplan D.L. Three dimensional aqueous-derived biomaterial scaffold from silk fibroin. Biomaterials 2005; 26(15): 2775–2785, http://dx.doi.org/10.1016/j.biomaterials.2004.07.044.
- Baran E.T., Tuzlakoğlu K., Mano J.F., Reis R.L. Enzymatic degradation behavior and cytocompatibility of silk fibroin–starch–chitosan conjugate membranes. Mater Sci Eng C Mater Biol Appl 2012; 32(6): 1314–1322, http://dx.doi.org/10.1016/j.msec.2012.02.015.
- Moisenovich M.M., Arkhipova A.Y., Orlova A.A., Drutskaya M.S., Volkova S.V., Zacharov S.E., Agapov I.I., Kirpichnikov M.P. Composite scaffolds containing silk fibroin, gelatin, and hydroxyapatite for bone tissue regeneration and 3D cell culturing. Acta Naturae 2014; 6(1): 96–101.
- Agapov I.I., Moisenovich M.M., Druzhinina T.V., Kamenchuk Y.A., Trofimov K.V., Vasilyeva T.V., Konkov A.S., Arhipova A.Y., Sokolova O.S., Guzeev V.V., Kirpichnikov M.P. Biocomposite scaffolds containing regenerated silk fibroin and nanohydroxyapatite for bone tissue regeneration. Dokl Biochem Biophys 2011; 440: 228–230, http://dx.doi.org/10.1134/s1607672911050103.
- Ramakrishna S., Fujihara K., Teo W.E., Lim T.C., Ma Z. An introduction to electrospinning and nanofibers. Singapore: World Scientific; 2005, http://dx.doi.org/10.1142/9789812567611.
- Hu Z., Ma Z., Peng M., He X., Zhang H., Li Y., Qiu J. Composite film polarizer based on the oriented assembly of electrospun nanofibers. Nanotechnology 2016; 27(13): 135301, http://dx.doi.org/10.1088/0957-4484/27/13/135301.
- Vasita R., Katti D.S. Nanofibers and their applications in tissue engineering. Int J Nanomedicine 2006, 1(1): 15–30, http://dx.doi.org/10.2147/nano.2006.1.1.15.
- Orr S.B., Chainani A., Hippensteel K.J., Kishan A., Gilchrist C., Garrigues N.W., Ruch D.S., Guilak F., Little D. Aligned multilayered electrospun scaffolds for rotator cuff tendon tissue engineering. Acta Biomater 2015; 24: 117–126, http://dx.doi.org/10.1016/j.actbio.2015.06.010.
- Braghirolli D.I., Steffens D., Pranke P. Electrospinning for regenerative medicine: a review of the main topics. Drug Discov Today 2014; 19(6): 743–753, http://dx.doi.org/10.1016/j.drudis.2014.03.024.
- Zhou J., Cao C., Ma X., Lin J. Electrospinning of silk fibroin and collagen for vascular tissue engineering. Int J Biol Macromol 2010; 47(4): 514–519, http://dx.doi.org/10.1016/j.ijbiomac.2010.07.010.
- Catto V., Farè S., Cattaneo I., Figliuzzi M., Alessandrino A., Freddi G., Remuzzi A., Tanzi M.C. Small diameter electrospun silk fibroin vascular grafts: mechanical properties, in vitro biodegradability, and in vivo biocompatibility. Mater Sci Eng C Mater Biol Appl 2015; 54: 101–111, http://dx.doi.org/10.1016/j.msec.2015.05.003.
- Elsayed Y., Lekakou C., Labeed F., Tomlins P. Fabrication and characterisation of biomimetic, electrospun gelatin fibre scaffolds for tunica media-equivalent, tissue engineered vascular grafts. Mater Sci Eng C Mater Biol Appl 2015; 61: 473–483, http://dx.doi.org/10.1016/j.msec.2015.12.081.
- Moroni L., Schotel R., Sohier J., de Wijn J.R., van Blitterswijk C.A. Polymer hollow fiber three-dimensional matrices with controllable cavity and shell thickness. Biomaterials 2006; 27(35): 5918–5926, http://dx.doi.org/10.1016/j.biomaterials.2006.08.015.
- Lu S., Wang P., Zhang F., Zhou X., Zuo B., You X., Gao Y., Liu H., Tang H. A novel silk fibroin nanofibrous membrane for guided bone regeneration: a study in rat calvarial defects. Am J Transl Res 2015; 7(11): 2244–2253.
- Katoch A., Choi S.W., Sun G.J., Kim H.W., Kim S.S. Mechanism and prominent enhancement of sensing ability to reducing gases in p/n core-shell nanofiber. Nanotechnology 2014; 25(17): 175501, http://dx.doi.org/10.1088/0957-4484/25/17/175501.
- Xu T., Miszuk J.M., Zhao Y., Sun H., Fong H. Electrospun polycaprolactone 3D nanofibrous scaffold with interconnected and hierarchically structured pores for bone tissue engineering. Adv Healthc Mater 2015; 4(15): 2238–2246, http://dx.doi.org/10.1002/adhm.201570089.
- Felsenfeld D.P., Choquet D., Sheetz P. Ligand binding regulates the directed movement of β1 integrins on fibroblasts. Nature 1996; 383(6599): 438–440, http://dx.doi.org/10.1038/383438a0.
- Perez R.A., Mestres G. Role of pore size and morphology in musculo-skeletal tissue regeneration. Mater Sci Eng C Mater Biol Appl 2016; 61: 922–939, http://dx.doi.org/10.1016/j.msec.2015.12.087.
- Abercombie M. Contact inhibition in tissue culture. In Vitro 1970; 6(2): 128–142, http://dx.doi.org/10.1007/bf02616114.
- Мойсенович М.М., Куликов Д.А., Архипова А.Ю., Малюченко Н.В., Котлярова М.С., Гончаренко А.В., Куликов А.В., Машков А.Е., Агапов И.И., Палеев Ф.Н., Свистунов А.А., Кирпичников М.П. Фундаментальные основы использования биорезорбируемых микроносителей на основе фиброина шелка в терапевтической практике на примере регенерации кожи. Терапевтический архив 2015; 87(12): 66–72.
- Vatankhah E., Prabhakaran M.P., Semnani D., Razavi S., Morshed M., Ramakrishna S. Electrospun tecophilic/gelatin nanofibers with potential for small diameter. Biopolymers 2014; 101(12): 1165–1180, http://dx.doi.org/10.1002/bip.22524.
- Hiraoka Y., Kimura Y., Ueda H., Tabata Y. Fabrication and biocompatibility of collagen sponge reinforced with poly(glycolic acid) fiber. Tissue Eng 2003; 9(6): 1101–1112, http://dx.doi.org/10.1089/10763270360728017.
- Li D., Ye Y., Li D., Li X., Mu C. Biological properties of dialdehyde carboxymethyl cellulose crosslinked gelatin–PEG composite hydrogel fibers for wound dressings. Carbohydr Polym 2016; 137: 508–514, http://dx.doi.org/10.1016/j.carbpol.2015.11.024.
- Panas-Perez E., Gatt C.J., Dunn M.G. Development of a silk and collagen fiber scaffold for anterior cruciate ligament reconstruction. J Mater Sci Mater Med 2014; 24(1): 257–265, http://dx.doi.org/10.1007/s10856-012-4781-5.
- Guan L., Tian P., Ge H., Tang X., Zhang H., Du L., Liu P. Chitosan-functionalized silk fibroin 3D scaffold for keratocyte culture. J Mol His 2013; 44(5): 609–618, http://dx.doi.org/10.1007/s10735-013-9508-5.
- Poursamar S.A., Hatami J., Lehner A.N., da Silva C.L., Ferreira F.C., Antunes A.P. Gelatin porous scaffolds fabricated using a modified gas foaming technique: characterisation and cytotoxicity assessment. Mater Sci Eng C Mater Biol Appl 2015; 48: 63–70, http://dx.doi.org/10.1016/j.msec.2014.10.074.
- Moisenovich M.M., Pustovalova O.L., Arhipova A.Y., Vasiljeva T.V., Sokolova O.S., Bogush V.G., Debabov V.G., Sevastianov V.I., Kirpichnikov M.P., Agapov I.I. In vitro and in vivo biocompatibility studies of a recombinant analogue of spidroin 1 scaffolds. J Biomed Mater Res A 2011; 96(1): 125–131, http://dx.doi.org/10.1002/jbm.a.32968
- Moisenovich M.M., Malyuchenko N.V., Arkhipova A.Y., Goncharenko A.V., Kotlyarova M.S., Davydova L.I., Vasil’evaa T.V., Bogush V.G., Agapov I.I., Debabov V.G., Kirpichnikov M.P. Novel 3D-microcarriers from recombinant spidroin for regenerative medicine. Dokl Biochem Biophys 2016; 463(1): 232–235, http://dx.doi.org/10.1134/s1607672915040109.