Применение портативного биопринтера для терапии ишемических ран: пилотное исследование
Цель исследования — разработка нового подхода к восстановлению незаживающих ран с использованием портативного биопринтера «Биоган» с чернилами на основе фибрин-желатинового гидрогеля и сфероидов из мезенхимных стромальных клеток (МСК) жировой ткани на модели ишемической раны свиньи.
Материалы и методы. Для моделирования раны использовали титановые уплотнительные кольца, которые механически сдавливали кожу, создавая локальную ишемическую рану. Через сутки кольца снимали и иссекали эпидермис кожи. Лечение проводили спустя сутки и 2 нед после нанесения раны. Для этого на поверхность раны с использованием портативного биопринтера «Биоган» (прототип разработан авторами) наносили комбинированные чернила. Равномерное смешивание биочернил на основе фибрин-желатинового гидрогеля и сфероидов из МСК жировой ткани человека обеспечивал адаптированный пассивный смеситель. В течение 36 дней оценивали скорость закрывания раны и затем проводили гистологический анализ.
Результаты. Применение чернил на основе фибрин-желатинового гидрогеля и сфероидов из МСК жировой ткани значительно ускоряет заживление, о чем свидетельствует уменьшение площади раны по сравнению с контрольной группой и просто гидрогелем, а также полное восстановление всех слоев кожи к 36-му дню. Терапевтический эффект разработанного подхода обусловлен именно сфероидами, входящими в состав биочернил, а не гидрогелем. Применение разработанного смесителя не снижает жизнеспособность клеток и обеспечивает удобное нанесение чернил на поверхность раны.
Введение
Хронические незаживающие раны являются распространенным осложнением у пациентов с сахарным диабетом и венозной недостаточностью и значительно снижают качество жизни пациентов. Согласно статистике, около 20% пациентов с сахарным диабетом страдают от хронических раневых дефектов нижних конечностей и почти в 20% случаев им требуется ампутация на уровне голени [1]. Экономические затраты на лечение в Европе составляют от 7 до 13 тыс. евро [2]. Таким образом, поиск новых подходов к лечению диабетических язв имеет важное значение с медицинской и экономической точки зрения, поскольку раннее и эффективное лечение может снизить риск образования рубцов и рецидивов.
Аутотрансплантаты широко применяются в хирургической практике и на данный момент остаются основным методом лечения. Однако этот подход является очень травматичным для пациента [3]. Использование современных методов, включая кожные заменители на основе синтетических и биологических каркасов [4] и эпидермальные эквиваленты [5], позволило достигнуть значительных успехов в восстановлении повреждений и уже неоднократно продемонстрировало свою эффективность.
В большинстве исследований применяют биоэквиваленты на основе эпидермальных кератиноцитов и дермальных фибробластов, которые могут быть выделены из здоровой кожи пациента [6] и нанесены на рану с использованием матрицы/носителя либо с помощью клеточного распыления [7]. Фибробласты, обладая высокой пластичностью и гетерогенностью, играют ключевую роль в заживлении диабетических язв за счет стимуляции ангиогенеза, формирования грануляционной ткани и ремоделирования внеклеточного матрикса [8]. Иммортализованные кератиноциты в сочетании со скаффолдами стимулируют реэпителизацию и заживление раны [9]. Клеточные пласты на основе кератиноцитов и фибробластов показали свою эффективность на модели незаживающих ран у крыс с сахарным диабетом 2-го типа [10]. Однако использование аутологичных фибробластов и кератиноцитов значительно замедляет и усложняет лечение, так как сначала необходимо получить биоптат для выделения клеток, а затем культивировать эти клетки в течение длительного времени. В связи с этим поиск универсального и доступного клеточного источника для терапии остается одной из ключевых задач регенеративной медицины.
Мезенхимные стромальные клетки (МСК) хорошо зарекомендовали себя для терапии многих патологий, включая лечение ожогов [11] и диабетических язв [12, 13]. Эффективность МСК в лечении диабетических язв обусловлена тем, что данные клетки выделяют факторы и экзосомы, способствующие ангиогенезу; стимулируют кератиноциты к миграции и формированию эпидермиса [14]; привлекают клетки в область повреждения и снижают воспаление [15]. Среди всех источников МСК жировая ткань (ЖТ) является наиболее доступной и позволяет получить культуру клеток с минимальным хирургическим вмешательством и высоким выходом. Более того, МСК-ЖТ обладают высоким ангиогенным потенциалом [16, 17], что особенно важно при заживлении ишемических ран. В настоящее время все большее предпочтение отдается 3D-культивированию клеток в виде сфероидов, так как это способствует их дифференцировке, повышает стабильность и выживаемость после трансплантации [18]. Более того, для МСК-ЖТ показано увеличение ангиогенного потенциала клеток в сфероидах по сравнению с монослойной культурой [19].
Применение кожных заменителей является эффективным подходом, однако имеет ряд недостатков. Готовые эквиваленты не позволяют точно повторить профиль раневой поверхности. Решением данной проблемы может быть использование клеточного распыления [20, 21] или портативного биопринтера [22]. При клеточном распылении необходимо учитывать множество параметров, таких как давление, размер сопла, скорость распыления и расстояние от раневой поверхности [20]. Однако жизнеспособность клеток даже при оптимальных параметрах снижается во время процедуры [23]. При этом использование портативного биопринтера в сочетании с гидрогелями практически не влияет на жизнеспособность клеток. Более того, гидрогели позволяют создать для клеток благоприятную среду, а также могут применяться для доставки факторов роста и экзосом, стимулирующих регенерацию [24].
Цель исследования — разработка нового подхода к восстановлению незаживающих ран с использованием портативного биопринтера «Биоган» с чернилами на основе фибрин-желатинового гидрогеля и сфероидов из мезенхимных стромальных клеток жировой ткани на модели ишемической раны свиньи.
Материалы и методы
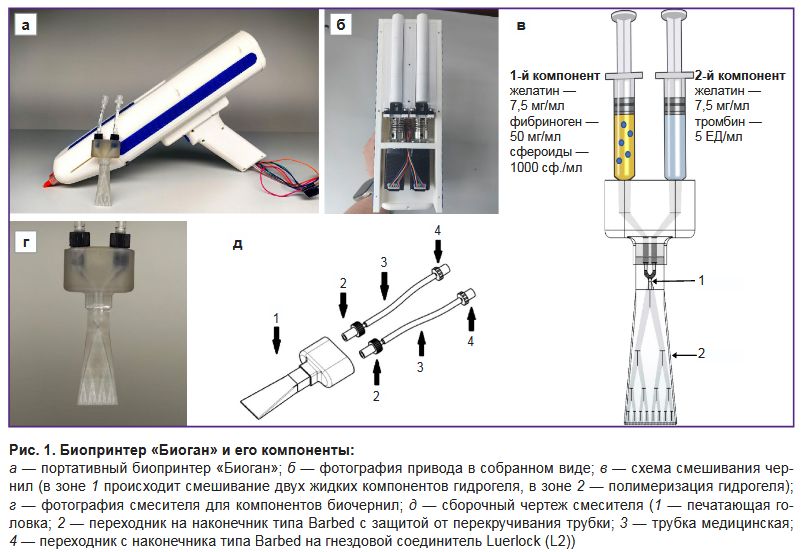
Разработка биопринтера и смесителя для биочернил. Авторами разработан портативный биопринтер «Биоган» (рис. 1, а), позволяющий с высокой точностью позиционирования наносить биочернила на поверхность раны. Прототип биопринтера получен методом трехмерной печати с помощью принтера Raise3D Pro 3 Plus (Raise3D, Китай) с последующей механической обработкой на токарном станке. Для нанесения биочернил разработан привод, основанный на двухшаговых двигателях с передачей винт–гайка (рис. 1, б), что позволило обеспечить высокую точность позиционирования, плавность движения и снизить нагрузку на двигатель. Корпус биопринтера изготовлен из полилактида, обладающего высокой прочностью и характеризующегося легкостью обработки. Для управления биопринтером создана специализированная система, включающая дисплей и программное обеспечение. Для управления аппаратными компонентами разработана прошивка микроконтроллера Arduino Nano. Предлагаемая нами система позволяет оптимизировать давление, скорость и тип (непрерывный или импульсный) печати.
С целью обеспечения равномерного смешивания компонентов биочернил для достижения оптимальных реологических свойств был создан адаптированный пассивный смеситель (рис. 1, г, д) из биосовместимого фотополимера HARZ Labs Dental Clear Pro (Harz Lab, Россия) на LCD-принтере Mighty 8K (Phrozen, Тайвань). Диаметр пор — 0,2–0,4 мм.
Принцип работы смесителя представлен на рис. 1, в. В зоне 1 осуществляется смешивание двух жидких компонентов гидрогеля. По мере прохождения смеси по каналам смесителя (зона 2) происходит полимеризация гидрогеля, который затем равномерно распределяется на поверхность раны. Диаметр пор и количество ветвлений смесителя обеспечивают оптимальную полимеризацию гидрогеля.
Клеточные культуры. В работе использовали культуру МСК-ЖТ человека, предоставленную Биобанком Сеченовского университета (Москва, Россия) и выделенную из донорского материала после подписания информированного согласия. Клетки культивировали в среде, состоящей из DMEM/F12 (1:1; Gibco, США), гентамицина (50 мкг/мл; Sigma-Aldrich, Германия), фетальной бычьей сыворотки (10%; Thermo Fisher Scientific, США), инсулина–трансферрина–селенита (1:100; «БиолоТ», Россия) и основного фактора роста фибробластов (bFGF, 10 нг/мл; ProSpec, Израиль), в стандартных условиях (37ºC и 5% СО2). Для формирования трехмерных культур — сфероидов — суспензию клеток с концентрацией 3,4·106 кл./мл помещали в агарозные планшеты, полученные с использованием силиконовых форм 3D Petri Dish (Microtissues, США), и культивировали в течение 3 сут.
Получение биочернил. Разработанные биочернила состояли из сфероидов (1000 кл./сф.), полученных из МСК-ЖТ человека в концентрации 1000 сф./мл гидрогеля. Гидрогелевый компонент биочернил изготовлен из фибрина и желатина. Разработанные биочернила включают два жидких компонента, при смешивании которых с использованием смесителя (см. рис. 1, г) происходит полимеризация и гидрогель застывает на поверхности раны.
Для получения первого компонента биочернил желатин (75 мг/мл; neoFroxx, Китай) смешивали с фибриногеном (25 мг/мл; Sigma-Aldrich, Германия) в PBS и затем добавляли гетеробифункциональный полиэтиленгликоль (Sigma-Aldrich, Германия). Реакцию конъюгации проводили в течение 2 ч при 37°C в темноте. Далее добавляли сфероиды в концентрации 1000 сф./мл.
Для получения второго компонента биочернил смешивали тромбин (5 ЕД/мл; Sigma-Aldrich, Германия) с желатином (75 мг/мл; neoFroxx, Китай) в соотношении 1:1.
Для проверки печатаемости чернил описанные компоненты загружали в картриджи и с использованием биопринтера наносили на поверхность чашки Петри с температурой 37ºC (рис. 2, а). Затем в течение 12 ч гидрогель держали при 37ºC, чтобы убедиться, что он полностью заполимеризовался (рис. 2, б). При использовании непрерывного режима наилучшая печатаемость достигалась при объемной скорости подачи биочернил, равной 0,2 мл/с. При этом осуществлялось равномерное экструдирование потока материала и смешивание компонентов чернил, что обеспечивало сохранение формы с четкими границами нанесенного слоя. При использовании импульсного режима оптимальными параметрами печати были объемная скорость 0,2–0,5 мл/с при частоте импульсов 15–20 в минуту.

|
Рис. 2. Внешний вид гидрогеля: а — после нанесения с использованием смесителя на поверхность с температурой 37ºС; б — спустя 12 ч в инкубаторе при 37ºС |
Для проведения экспериментов in vivo был выбран протокол с непрерывным режимом подачи чернил и объемной скоростью подачи 0,2 мл/с.
Оценка жизнеспособности сфероидов в составе биочернил. Для подтверждения того, что при использовании смесителя сохраняется жизнеспособность сфероидов, была проведена оценка качества полученного биоэквивалента. Для этого биочернила наносили на поверхность чашки Петри с использованием биопринтера «Биоган», а также вручную (стандартным смешиванием) в качестве контроля. Затем сфероиды культивировали в течение 3 дней в стандартной ростовой среде и проводили окраску Live/Dead с использованием красителя CalceinAM (Sigma-Aldrich, Германия) и пропидий йодида. Ядра клеток окрашивали Hoechst 33258 (Thermo Fisher Scientific, США) и анализировали с помощью флуоресцентного микроскопа Evos (Thermo Fisher Scientific, США).
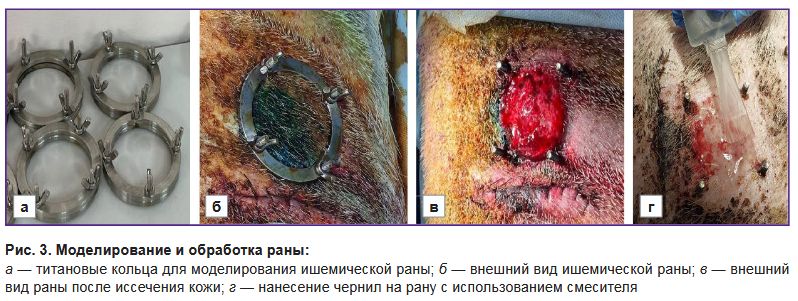
Моделирование раны. Для моделирования ишемической раны применяли метод, основанный на использовании титановых колец для сдавливания кожи, который ранее применялся в аналогичных исследованиях [25]. Для эксперимента был выбран самец вьетнамской вислоухой свиньи породы везинау в возрасте 1 год массой тела 45 кг. Перед операцией свинью седировали 12 мг/кг Золетила и 12 мг/кг Медитина и очищали кожу. Первичная операция заключалась в создании карманов на боковых поверхностях животного посредством рассечения внешнего покрова и отделения дермы от подкожно-жировой клетчатки слева и справа от изначального разреза. Всего было по два иссечения с каждого бока на расстоянии 25 см друг от друга. В получившиеся карманы внедряли нижние уплотнительные кольца из титана с болтами (d=5 см) (рис. 3, а). Устройством для панч-биопсии (Apexmed, Индия) диаметром 8,0 мм проделывали отверстия для болтов, после чего устанавливали верхнее кольцо и фиксировали его винтами (рис. 3, б). Спустя 24 ч свинью снова седировали, проводили предоперационную подготовку, после чего, удалив верхнее кольцо, иссекали кожу по диаметру (рис. 3, в). Затем наносили гидрогель со сфероидами или без в зависимости от группы с использованием смесителя (рис. 3, г), а контрольную рану оставляли без лечения. Раны обрабатывали с интервалом в 3–4 дня. Антибиотикотерапию проводили каждый день с использованием цефтриаксона в дозе 20 мг/кг и 5% энрофлоксацина в дозе 45 мг/кг, анальгетическую терапию — с использованием мелоксикама в дозе 300 мг/кг. На 18-й день после операции вновь наносили биочернила. На 36-й день животное выводили из эксперимента Пропофолом-Липуро (10 мг/кг) и лидокаином (10 мг/кг), после чего образцы тканей передавали на гистологическое исследование.
Анализ заживления ран. На 5, 14, 18, 24, 32 и 36-й дни раны фотографировали для оценки скорости их закрытия и реэпителизации. Размеры раны оценивали по снимкам с помощью программного обеспечения Image J. Расстояние между всеми болтами измеряли на каждой фотографии, брали среднее и выводили соотношение пикселей и сантиметров. Далее измеряли площадь открытой раны и полученные значения переводили в квадратные сантиметры.
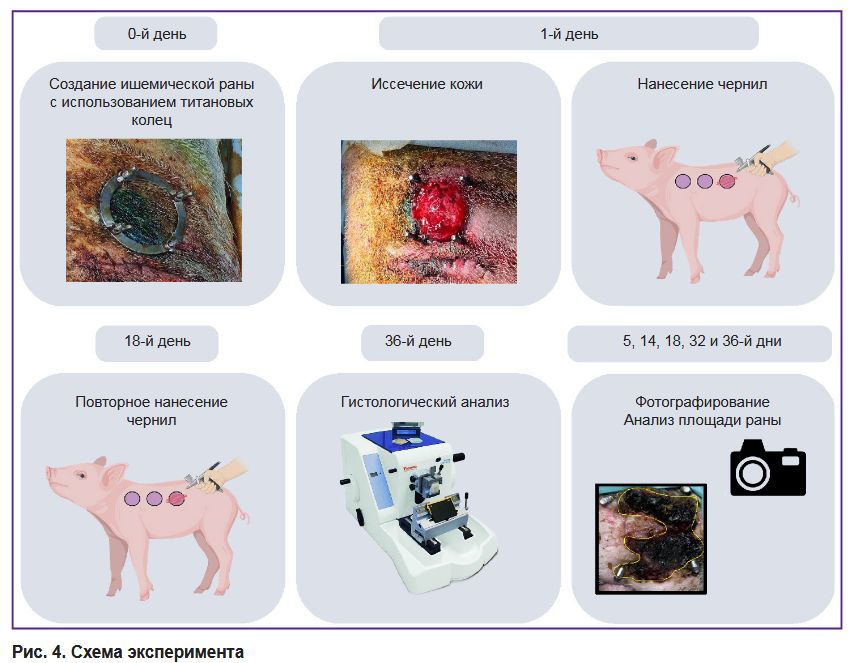
Дизайн эксперимента представлен на рис. 4.
|
Рис. 4. Схема эксперимента |
Результаты и обсуждение
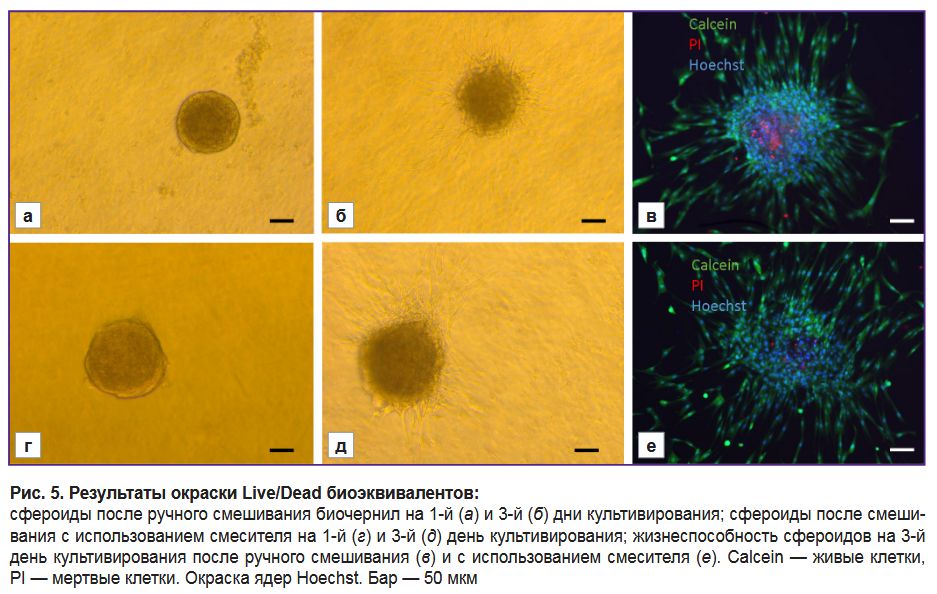
Оценка жизнеспособности сфероидов после биопечати. Нанесение биочернил с использованием прототипа ручного биопринтера «Биоган» не приводит к снижению жизнеспособности сфероидов в составе биоэквивалента. На рис. 5 представлены результаты окраски Live/Dead биоэквивалентов, полученных путем ручного смешивания биочернил (а–в), а также с использованием биопринтера (г–е). В обоих случаях клетки в составе сфероида оставались живыми, о чем свидетельствует положительная окраска на Calcein (см. рис. 5, в, е). Спустя 3 дня культивирования сфероиды формировали отростки в гидрогели, что говорит о созревании конструкта.
Таким образом, применение разработанного смесителя позволяет смешивать два жидких компонента биочернил и получать стабильный гидрогель, который может применяться для in situ биопечати на поверхности кожи и не снижает жизнеспособность клеток.
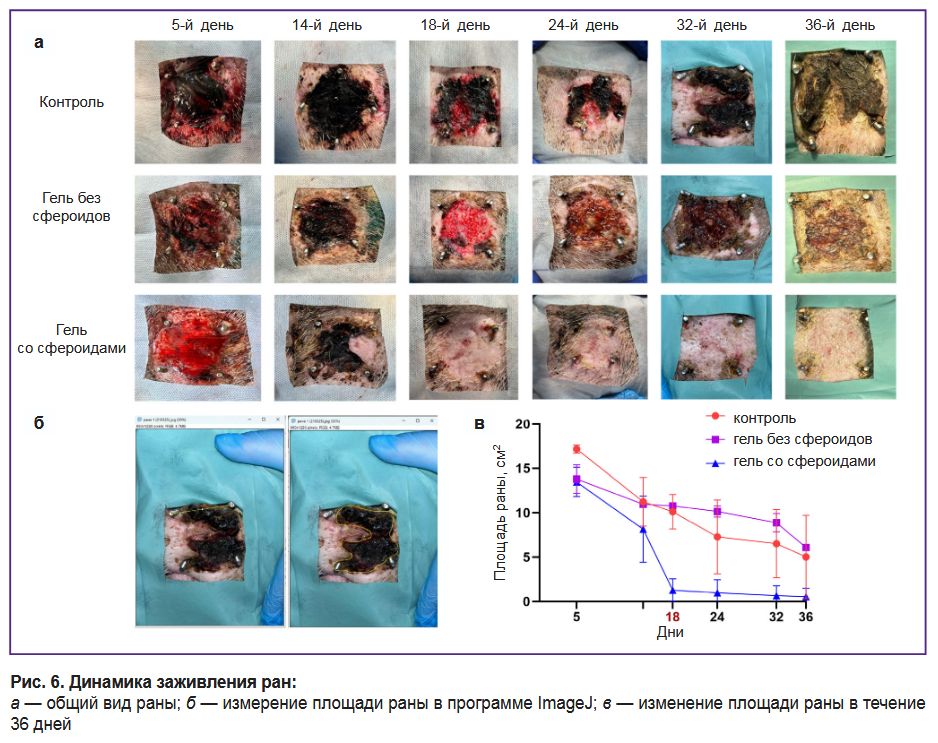
Общая оценка заживления ран. На 5-й день раневые поверхности во всех группах были покрыты толстым слоем рыхлого фибрина (рис. 6, а). К 14-му дню площадь раны снижалась примерно на 35, 30 и 40% в группах «контроль», «гидрогель без сфероидов» и «гидрогель со сфероидами» соответственно. Заметные отличия были выявлены на 18-й день, когда в группе «гидрогель со сфероидами» площадь раны уменьшилась на 90% и составила 1,28±0,70 см2 против 10,8±0,4 см2 для группы «гель без сфероидов» и 10,12±0,28 см2 для контроля (рис. 6, в). На 18-й день также проводилось повторное лечение. К 36-му дню рана в группе «гидрогель со сфероидами» полностью эпителизовалась и зажила, тогда как в группах «контроль» и «гидрогель без сфероидов» рана сохранялась (см. рис. 6, а, в).
|
Рис. 6. Динамика заживления ран:
а — общий вид раны; б — измерение площади раны в программе ImageJ; в — изменение площади раны в течение 36 дней |
Таким образом, разработанные биочернила на основе сфероидов МСК-ЖТ и фибрин-желатинового гидрогеля значительно ускоряют процесс заживления. Это подтверждается уменьшением площади раны по сравнению с контрольной группой, которая не получала лечения. При этом терапевтический эффект обусловлен именно сфероидами, входящими в состав биочернил, а не гидрогелем. В группе, где использовался гидрогель без сфероидов, заживление происходило с такой же скоростью, как и в контрольной.
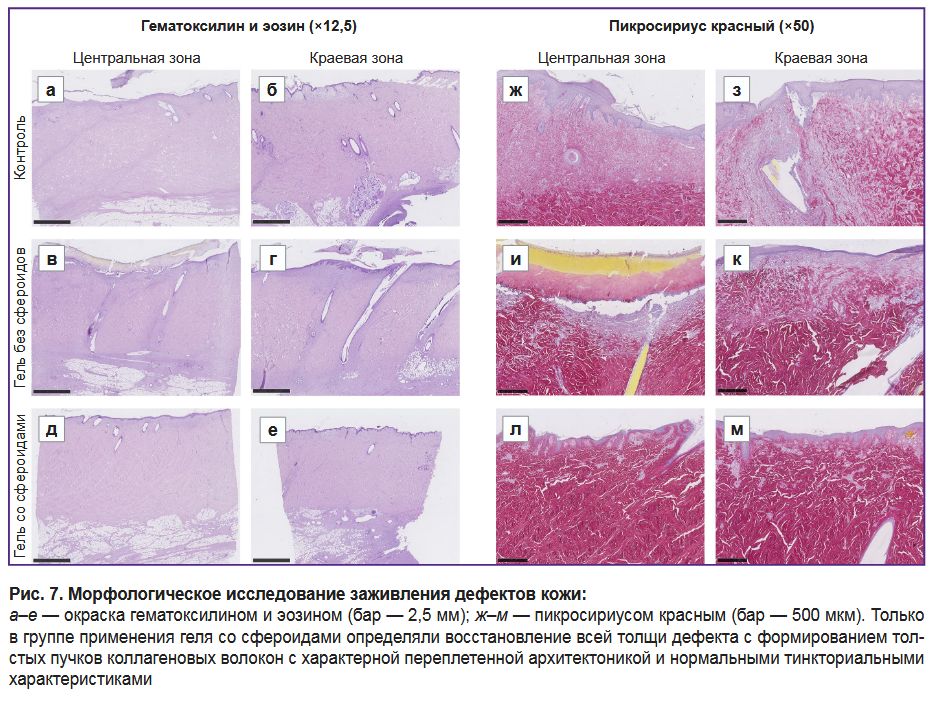
Гистологический анализ. Кожа свиньи была выстлана многослойным ороговевающим эпителием, который содержал редкие, но крупные волосы. Под эпителием определялся глубокий слой дермы, представленной толстыми пучками коллагеновых волокон, переплетенными в характерном паттерне — крест-накрест. Сама дерма была толщиной 5–10 мм и переходила в подкожно-жировую клетчатку. Во всех образцах больший объем дермы был нормальным (интактным или восстановленным после ишемического повреждения), без признаков повышенной клеточности, с зонами прорастания толстой соединительнотканной прослойки — следствие травмы и реакции ткани на болты.
В группе контроля в центральной зоне (рис. 7, а, ж) поверхностная часть дермы толщиной 1–1,5 мм была представлена рыхлой фиброзирующейся грануляционной тканью, с высокой клеточностью и плотной сетью кровеносных сосудов. Значительных признаков инфильтрации иммунными клетками не обнаружено; умеренное количество лимфоцитов и макрофагов определялось периваскулярно, небольшими очагами. Эпителий был непрерывным за исключением мест помещения винтов. В краевой зоне (рис. 7, б, з) наблюдались признаки реорганизации дермы с формированием толстых пучков коллагена, идентичных таковым в интактной дерме. Одновременно с этим в ткани отмечалось очень высокое содержание фибробластов, ориентированных параллельно поверхности раны, и вертикальных петель кровеносных сосудов. В этих зонах определялась умеренно зрелая соединительнотканная капсула, сформированная вокруг винтов. Капсула была плотно инфильтрирована макрофагами и лимфоцитами.
В группе применения геля без сфероидов в центральной зоне дефекта кожи (рис. 7, в, и) зона повреждения также слабо отличалась от группы контроля. В одном случае эпителизация была нарушена, а рана покрыта слоем фибрина, под которым обнаруживалась зона густой инфильтрации лимфоцитами и макрофагами. В другом образце рана была выстлана непрерывным многослойным эпителием с небольшими кистами. Поверхностная зона дермы так же, как и в контроле, была представлена очень рыхлой соединительной тканью с начальными признаками реорганизации. В краевой зоне (рис. 7, г, к) реорганизация поврежденной соединительной ткани происходила несколько быстрее, чем в группе контроля, и активнее, чем в центре дефекта кожи. Тем не менее темпы восстановления значительно не отличались от группы контроля.
В группе применения геля со сфероидами (рис. 7, д, е, л, м) во всех образцах раны были выстланы непрерывным эпителием. Поверхностные дефекты дермы были тонкими, в них активно происходила реорганизация с формированием новых толстых пучков коллагеновых волокон. В отдельных зонах под эпителием ткань была очагово более рыхлой, однако бóльшая ее часть представляла собой фиброзированную грануляционную ткань с высоким содержанием внеклеточного матрикса и без признаков активного воспаления. В краевых зонах (см. рис. 7, е, м) наблюдалось полное восстановление дермы: внеклеточный матрикс был полностью представлен толстыми пучками коллагеновых волокон с нормальными тинкториальными свойствами. Тем не менее можно было установить признаки регенерации: в дерме определялись прослойки рыхлой соединительной ткани с кровеносными сосудами.
Таким образом, в группе без лечения отмечался процесс самостоятельного раневого заживления, который выражался в полном возмещении объема дефекта и реорганизации краев раны. При использовании геля без сфероидов регенеративные и воспалительные изменения значительно не отличались от группы контроля, тогда как в группе геля со сфероидами наблюдались полное восстановление всех слоев дефекта по краю образца и активная регенерация в центре дефекта.
Заключение
Доказана эффективность разработанного нами портативного биопринтера «Биоган» для восстановления незаживающих ран. Применение чернил на основе фибрин-желатинового гидрогеля и сфероидов из МСК-ЖТ значительно ускоряет заживление ишемической раны, о чем свидетельствует уменьшение ее площади по сравнению с контрольной группой и просто гидрогелем, а также способствует полному восстановлению всех слоев кожи к 36-му дню. Терапевтический эффект предлагаемого подхода обусловлен именно сфероидами, входящими в состав биочернил, а не гидрогелем. Разработанный смеситель обеспечивает удобное нанесение чернил на поверхность раны и не снижает жизнеспособность клеток.
Таким образом, портативный биопринтер «Биоган» представляет собой важный инструмент в области регенеративной медицины для персонализированного лечения ишемических ран непосредственно в клинических условиях. Более того, данное устройство и биочернила могут быть оптимизированы для терапии других типов тканей, что значительно расширит спектр их применения.
Благодарности. Исследование проведено на научной базе лаборатории, созданной в рамках Программы академического лидерства «Приоритет 2030».
Финансирование. Работа выполнена при финансовой поддержке гранта Российского научного фонда №22–75–10120 «Восстановление сложноорганизованных комплексов тканей с использованием прототипа портативного биопринтера “Биоган”».
Конфликт интересов отсутствует.
Литература
- Vargas Guerrero M.G., Vonken L., Peters E., Lucchesi J., Arts J.J.C. Material technologies for improved diabetic foot ulcer (DFU) treatment: a questionnaire study of healthcare professionals' needs. Biomedicines 2024; 12(11): 2483, https://doi.org/10.3390/biomedicines12112483.
- Waibel F.W.A., Uçkay I., Soldevila-Boixader L., Sydler C., Gariani K. Current knowledge of morbidities and direct costs related to diabetic foot disorders: a literature review. Front Endocrinol (Lausanne) 2024; 14: 1323315, https://doi.org/10.3389/fendo.2023.1323315.
- Coruh A., Yontar Y. Application of split-thickness dermal grafts in deep partial- and full-thickness burns: a new source of auto-skin grafting. J Burn Care Res 2012; 33(3): e94–e100, https://doi.org/10.1097/BCR.0b013e31823499e9.
- Lesher A.P., Curry R.H., Evans J., Smith V.A., Fitzgerald M.T., Cina R.A., Streck C.J., Hebra A.V. Effectiveness of Biobrane for treatment of partial-thickness burns in children. J Pediatr Surg 2011; 46(9): 1759–1763, https://doi.org/10.1016/j.jpedsurg.2011.03.070.
- Gibbs S., Spiekstra S.W. Epidermal equivalent (EE) potency assay. In: Eskes C., van Vliet E., Maibach H. (editors). Alternatives for dermal toxicity testing. Springer, Cham; 2017, https://doi.org/10.1007/978-3-319-50353-0_20.
- Normand J., Karasek M.A. A method for the isolation and serial propagation of keratinocytes, endothelial cells, and fibroblasts from a single punch biopsy of human skin. In Vitro Cell Dev Biol Anim 1995; 31(6): 447–455, https://doi.org/10.1007/BF02634257.
- Kirsner R.S., Marston W.A., Snyder R.J., Lee T.D., Cargill D.I., Slade H.B. Spray-applied cell therapy with human allogeneic fibroblasts and keratinocytes for the treatment of chronic venous leg ulcers: a phase 2, multicentre, double-blind, randomised, placebo-controlled trial. Lancet 2012; 380(9846): 977–985, https://doi.org/10.1016/S0140-6736(12)60644-8.
- Rai V., Moellmer R., Agrawal D.K. Role of fibroblast plasticity and heterogeneity in modulating angiogenesis and healing in the diabetic foot ulcer. Mol Biol Rep 2023; 50(2): 1913–1929, https://doi.org/10.1007/s11033-022-08107-4.
- Zhong J., Wang H., Yang K., Wang H., Duan C., Ni N., An L., Luo Y., Zhao P., Gou Y., Sheng S., Shi D., Chen C., Wagstaff W., Hendren-Santiago B., Haydon R.C., Luu H.H., Reid R.R., Ho S.H., Ameer G.A., Shen L., He T.C., Fan J. Reversibly immortalized keratinocytes (iKera) facilitate re-epithelization and skin wound healing: potential applications in cell-based skin tissue engineering. Bioact Mater 2021; 9: 523–540, https://doi.org/10.1016/j.bioactmat.2021.07.022.
- Benchaprathanphorn K., Muangman P., Chinaroonchai K., Namviriyachote N., Ampawong S., Angkhasirisap W., Kengkoom K., Viravaidya-Pasuwat K. Translational application of human keratinocyte-fibroblast cell sheets for accelerated wound healing in a clinically relevant type 2 diabetic rat model. Cytotherapy 2024; 26(4): 360–371, https://doi.org/10.1016/j.jcyt.2024.01.003.
- Rodgers K., Jadhav S.S. The application of mesenchymal stem cells to treat thermal and radiation burns. Adv Drug Deliv Rev 2018; 123: 75–81, https://doi.org/10.1016/j.addr.2017.10.003.
- Wu Q., Chen B., Liang Z. Mesenchymal stem cells as a prospective therapy for the diabetic foot. Stem Cells Int 2016; 2016: 4612167, https://doi.org/10.1155/2016/4612167.
- Berlanga-Acosta J.A., Guillén-Nieto G.E., Rodríguez-Rodríguez N., Mendoza-Mari Y., Bringas-Vega M.L., Berlanga-Saez J.O., García Del Barco Herrera D., Martinez-Jimenez I., Hernandez-Gutierrez S., Valdés-Sosa P.A. Cellular senescence as the pathogenic hub of diabetes-related wound chronicity. Front Endocrinol (Lausanne) 2020; 11: 573032, https://doi.org/10.3389/fendo.2020.573032.
- Dos Santos J.F., Borçari N.R., da Silva Araújo M., Nunes V.A. Mesenchymal stem cells differentiate into keratinocytes and express epidermal kallikreins: towards an in vitro model of human epidermis. J Cell Biochem 2019; 120(8): 13141–13155, https://doi.org/10.1002/jcb.28589.
- Guillamat-Prats R. The role of MSC in wound healing, scarring and regeneration. Cells 2021; 10(7): 1729, https://doi.org/10.3390/cells10071729.
- Cao Y., Yan J., Dong Z., Wang J., Jiang X., Cui T., Huang Y., Liu H. Adipose-derived mesenchymal stem cells are ideal for the cell-based treatment of refractory wounds: strong potential for angiogenesis. Stem Cell Rev Rep 2024; 20(1): 313–328, https://doi.org/10.1007/s12015-023-10641-y.
- Almalki S.G. Adipose-derived mesenchymal stem cells and wound healing: potential clinical applications in wound repair. Saudi Med J 2022; 43(10): 1075–1086, https://doi.org/10.15537/smj.2022.43.10.20220522.
- Ravi M., Paramesh V., Kaviya S.R., Anuradha E., Solomon F.D. 3D cell culture systems: advantages and applications. J Cell Physiol 2015; 230(1): 16–26, https://doi.org/10.1002/jcp.24683.
- Gorkun A.A., Revokatova D.P., Zurina I.M., Nikishin D.A., Bikmulina P.Y., Timashev P.S., Shpichka A.I., Kosheleva N.V., Kolokoltsova T.D., Saburina I.N. The duo of osteogenic and angiogenic differentiation in ADSC-derived spheroids. Front Cell Dev Biol 2021; 9: 572727, https://doi.org/10.3389/fcell.2021.572727.
- Pleguezuelos-Beltrán P., Gálvez-Martín P., Nieto-García D., Marchal J.A., López-Ruiz E. Advances in spray products for skin regeneration. Bioact Mater 2022; 16: 187–203, https://doi.org/10.1016/j.bioactmat.2022.02.023.
- Nuutila K., Katayama S., Laitinen A., Siltanen A., Patrikoski M., Valtonen J., Kankainen M., Kerkelä E., Kaartinen T., Juteau S., Korhonen M., Vuola J., Kankuri E. ATMP-classified, scalable, autologous cell spray for the treatment of skin wounds and assessment of its effects on wound healing clinically and on a molecular level. Burns 2023; 49(5): 1144–1156, https://doi.org/10.1016/j.burns.2022.09.006.
- Albanna M., Binder K.W., Murphy S.V., Kim J., Qasem S.A., Zhao W., Tan J., El-Amin I.B., Dice D.D., Marco J., Green J., Xu T., Skardal A., Holmes J.H., Jackson J.D., Atala A., Yoo J.J. In situ bioprinting of autologous skin cells accelerates wound healing of extensive excisional full-thickness wounds. Sci Rep 2019; 9(1): 1856, https://doi.org/10.1038/s41598-018-38366-w.
- Harkin D.G., Dawson R.A., Upton Z. Optimized delivery of skin keratinocytes by aerosolization and suspension in fibrin tissue adhesive. Wound Repair Regen 2006; 14(3): 354–363, https://doi.org/10.1111/j.1743-6109.2006.00132.x.
- Pazhouhnia Z., Beheshtizadeh N., Namini M.S., Lotfibakhshaiesh N. Portable hand-held bioprinters promote in situ tissue regeneration. Bioeng Transl Med 2022; 7(3): e10307, https://doi.org/10.1002/btm2.10307.
- Singer A.J., Toussaint J., Chung W.T., McClain S.A., Clark R.A.F., Asculai E., Geblinger D., Rosenberg L. Development of a contaminated ischemic porcine wound model and the evaluation of bromelain based enzymatic debridement. Burns 2018; 44(4): 896–904, https://doi.org/10.1016/j.burns.2017.07.022.