Иммуногистохимическое выявление микроглии с использованием маркера Iba-1 в норме и при патологии
Цель исследования — оценить возможности и ограничения использования метода иммуногистохимического выявления белка Iba-1 для морфофункционального анализа микроглии в разных условиях.
Материалы и методы. Материалом для исследования служили образцы головного мозга крыс линии Wistar разных возрастных групп: 7-е сутки постнатального онтогенеза (n=18), 14-е сутки постнатального онтогенеза (n=18), половозрелые животные в возрасте 4–6 мес (n=22); а также образцы головного мозга крыс-самцов линии SHR (spontaneously hypertensive rats) в возрасте 3–6 мес (n=4); образцы коры больших полушарий головного мозга человека (n=10). Для иммуногистохимического выявления микроглии использовали кроличьи поликлональные антитела против кальций-связывающего белка Iba-1 (Biocare Medical, США) с последующей идентификацией методами световой и конфокальной лазерной микроскопии. Для одновременного выявления клеток микроглии и амилоидных бляшек применяли оригинальную методику, разработанную ранее.
Результаты. В рамках проведенных исследований показано, что белок Iba-1 присутствует в клетках микроглии в сером и белом веществе во всех изученных областях головного мозга. Отмечено, что в разных областях для клеток микроглии характерны выраженные структурно-функциональные особенности при реакции на Iba-1. Помимо клеток микроглии в головном мозге крысы обнаружены другие Iba-1-иммунопозитивные клетки, которые являются тканевыми макрофагами мозга и отличаются от клеток микроглии по морфологии и локализации. Продемонстрировано, что белок Iba-1 присутствует в микроглиоцитах на всех изученных стадиях постнатального онтогенеза, что делает его удобным маркером для сравнительно-онтогенетических исследований этих клеток. Локализация Iba-1 в телах и отростках микроглиоцитов позволяет наиболее полно выявлять сложную отростчатую морфологию клеток и строить трехмерные реконструкции. Показано, что в головном мозге у спонтанно гипертензивных крыс линии SHR микроглия имеет ряд структурно-функциональных особенностей при реакции на Iba-1, указывающих на умеренную активацию микроглии. В головном мозге у крыс через 48 ч после ишемического воздействия в сером веществе стриатума ипсилатерального полушария рядом с областью повреждения выявлено аномально большое число крупных Iba-1-иммунопозитивных клеток с амебоидной морфологией. Отмечено, что в коре головного мозга человека клетки микроглии присутствуют в составе большинства выявленных амилоидных бляшек и имеют амебоидную морфологию, что указывает на их сильную активацию.
Заключение. Представленные результаты свидетельствуют о том, что белок Iba-1 является надежным и универсальным маркером микроглии. Иммуногистохимическое выявление этого белка позволяет идентифицировать, а также качественно и количественно анализировать микроглию в разных отделах головного мозга у человека и лабораторных животных в норме и при патологии. К ограничениям использования Iba-1 в качестве маркера микроглии можно отнести невозможность определения вектора активации микроглии и сложность различения микроглии и инфильтрирующих макрофагов мозга при патологии. В этих случаях необходимо совершенствовать технологию выявления микроглии, что может быть основано на использовании многомаркерного анализа.
Введение
В современной нейробиологии особый интерес исследователей сосредоточен на изучении микроглии, что связано с полифункциональностью этих клеток и пониманием их ведущей роли в развитии нейровоспаления—ключевого фактора нейродегенерации [1, 2]. Активное изучение микроглии делает особенно актуальным наличие в арсенале исследователей надежной технологии для идентификации этих клеток в физиологических и патологических условиях. Сложность в данном случае состоит в том, что микроглия является высокогетерогенной популяцией [3–6]. Отмечена межвидовая гетерогенность микроглии [7, 8], а также половая и региональная неоднородность этой клеточной популяции [5, 8, 9]. Кроме того, микроглия высокодинамична и легко изменяет профиль экспрессии генов в течение онтогенеза и в условиях развития патологии [7, 8, 10, 11]. Показано, что клетки микроглии экспрессируют более 1000 рецепторных систем, что делает их исключительно чувствительными к факторам локального микроокружения [3, 7, 12]. Вследствие столь высокой чувствительности клетки микроглии способны быстро менять свое структурно-функциональное состояние [13].
Среди современных технологий выявления микроглии наиболее широко используется методика иммуногистохимической идентификации этих клеток с помощью антител против кальций-связывающего белка Iba-1 (ionized calcium-binding adapter molecule 1) [5, 14, 15]. Однако, учитывая выраженную гетерогенность и динамичность микроглии, актуальным остается вопрос о границах применения Iba-1 в качестве маркера.
Цель исследования — оценить возможности и ограничения использования метода иммуногистохимического выявления белка Iba-1 для морфофункционального анализа микроглии в разных условиях.
Материалы и методы
Все исследования проведены в соответствии с положениями Хельсинкcкой декларации (2024) и одобрены локальным этическим комитетом Института экспериментальной медицины (протокол №3/17 от 30.11.2017 г., протокол №3/18 от 22.11.2018 г., протокол №1/22 от 18.02.2022 г.).
Материалом для исследования служили образцы головного мозга крыс линии Wistar разных возрастных групп: 7-е сутки постнатального онтогенеза (n=18), 14-е сутки постнатального онтогенеза (n=18), половозрелые животные возрастом 4–6 мес (n=22); а также образцы головного мозга крыс-самцов линии SHR (spontaneously hypertensive rats) в возрасте 3–6 мес (n=4); образцы коры больших полушарий головного мозга человека (n=10).
Крысят с датированным сроком рождения получали согласно рекомендациям А.П. Дыбана «Объекты биологии развития» [16]. Моделирование транзиторной фокальной ишемии проводили по методике, описанной ранее [17]. В случае изучения образцов головного мозга человека использовали архивный материал, полученный ранее в результате аутопсии [18], —10 образцов коры больших полушарий головного мозга людей (мужчин, n=2 и женщин, n=8) в возрасте от 65 до 94 лет с наличием амилоидных бляшек. Сохранность материала и его пригодность для иммуногистохимического исследования определяли с использованием стандартной тестовой иммуногистохимической реакции на глиальный фибриллярный кислый белок.
Образцы головного мозга человека были фиксированы в 10% забуференном формалине, образцы головного мозга крыс — в цинк-этанол-формальдегиде [19]. После фиксации материал обезвоживали и заливали в парафин, изготавливали срезы толщиной 5 мкм и монтировали на предметные стекла с адгезивным покрытием (Menzel, Германия).
Для иммуногистохимической идентификации микроглии использовали кроличьи поликлональные антитела против Iba-1 в разведении 1:1000 (Biocare Medical, США). В качестве вторичных реагентов применяли компоненты из набора Reveal Rabbit Specific HRP-DAB Detection System (Spring Bioscience, США). Для визуализации продукта реакции применяли хромоген 3,3'-диаминобензидин из набора DAB+ (Agilent, США). После проведения реакции часть срезов подкрашивали квасцовым гематоксилином.
Для одновременного выявления амилоидных бляшек и клеток микроглии на срезах коры больших полушарий головного мозга человека применяли оригинальную методику, основанную на иммуногистохимическом выявлении микроглии с использованием антител против Iba-1 и на гистохимическом окрашивании амилоидных бляшек красителем альциановым синим [20].
Полученные препараты анализировали на световом микроскопе Leica DM750 (Leica Microsystems, Германия) и фотографировали с помощью фотокамеры ICC50 (Leica Microsystems, Германия); применяли компьютерную программу LAS EZ (Leica Microsystems, Германия).
Для иммунофлуоресценого анализа микроглии использовали кроличьи поликлональные антитела против Iba-1 в разведении 1:500 (Biocare Medical, США). Выявление первичных антител осуществляли с применением моновалетного Fab-фрагмента антикроличьего иммуноглобулина осла, конъюгированного с флуорохромом Rhodamine Red™-X (RRX) (Jackson ImmunoResearch, США). Ядра подкрашивали флуоресцентным ядерным красителем Sytox Green (Invitrogen, США). Полученные препараты анализировали на конфокальном лазерном микроскопе Zeiss LSM 800 (Zeiss, Германия). Для возбуждения флуоресценции RRX использовали лазер с длиной волны 561 нм, для Sytox Green — 488 нм. Применяли объективы Plan-Apochromat 20×/0.8 M27 и Plan-Apochromat 63×/1.40 Oil DICM27 (масляная иммерсия). Анализ полученных изображений проводили при помощи компьютерной программы ZEN 2.6 blue edition (Zeiss, Германия).
Результаты
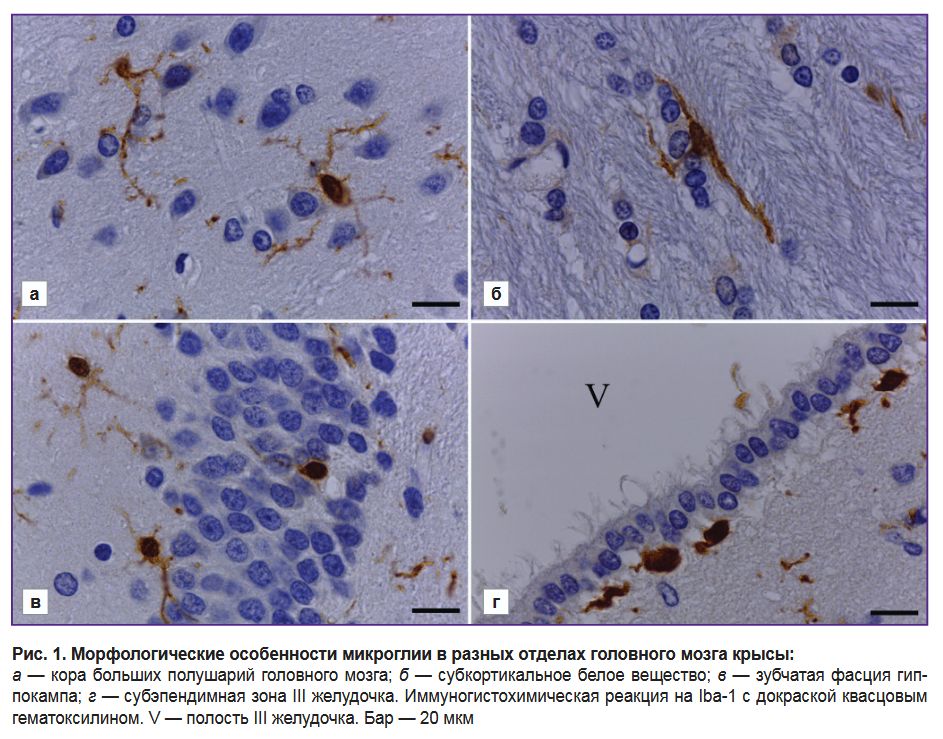
Использование маркера Iba-1 для изучения структурно-функционального состояния и региональных особенностей микроглии. При анализе препаратов головного мозга половозрелых крыс отмечено, что во всех проанализированных случаях Iba-1-иммунопозитивные клетки присутствуют во всех отделах головного мозга, попавших в плоскость среза. Иммуногистохимическая реакция характеризуется высокой интенсивностью и отсутствием фонового окрашивания. В коре больших полушарий, субкортикальном белом веществе, стриатуме, гиппокампе и других подкорковых структурах конечного мозга Iba-1-иммунопозитивные клетки имеют преимущественно отростчатую форму, свойственную микроглии без признаков активации (рис. 1). Iba-1 присутствует в теле и отростках микроглиоцитов.
Было отмечено морфологическое разнообразие Iba-1-иммунопозитивных клеток в зависимости от их локализации в разных отделах головного мозга. В коре больших полушарий наблюдаются микроглиоциты некрупной сомы (круглой или овальной формы) с длинными тонкими отростками, сильно ветвящимися в разных направлениях (рис. 1, а).
В субкортикальном белом веществе клетки микроглии имеют веретеновидную форму (рис. 1, б). Они характеризуются наличием одного или двух (редко трех) длинных неветвящихся или слабоветвящихся отростков, которые отходят от разных полюсов тела клетки в противоположных направлениях. Тела и отростки клеток микроглии ориентированы вдоль нервных волокон (см. рис. 1, б).
В гиппокампе клетки микроглии имеют морфологию, сходную с микроглией в коре больших полушарий, и характеризуются наличием небольшой сомы с малым объемом перинуклеарной цитоплазмы и многочисленных тонких ветвящихся отростков (рис. 1, в). Отростки микроглии пронизывают весь нейропиль гиппокампа и проникают в слои нейронов гиппокампа. Тела микроглиоцитов, как правило, выявляются за пределами слоев нейронов, часто — непосредственно примыкают к ним. Изредка тела микроглиоцитов обнаруживаются непосредственно в составе пирамидного слоя или зернистого слоя зубчатой извилины, они локализованы между телами нейронов (см. рис. 1 в).
В субэпендимной зоне желудочков головного мозга (боковых, III) микроглиоциты имеют амебоидную морфологию — это клетки с округлой/вытянутой сомой и короткими неветвящимися отростками либо без отростков (рис. 1, г). Некоторые клетки веретеновидной формы образуют небольшое число отростков, которые направлены в подлежащую нервную ткань или в пласт эпендимных клеток.
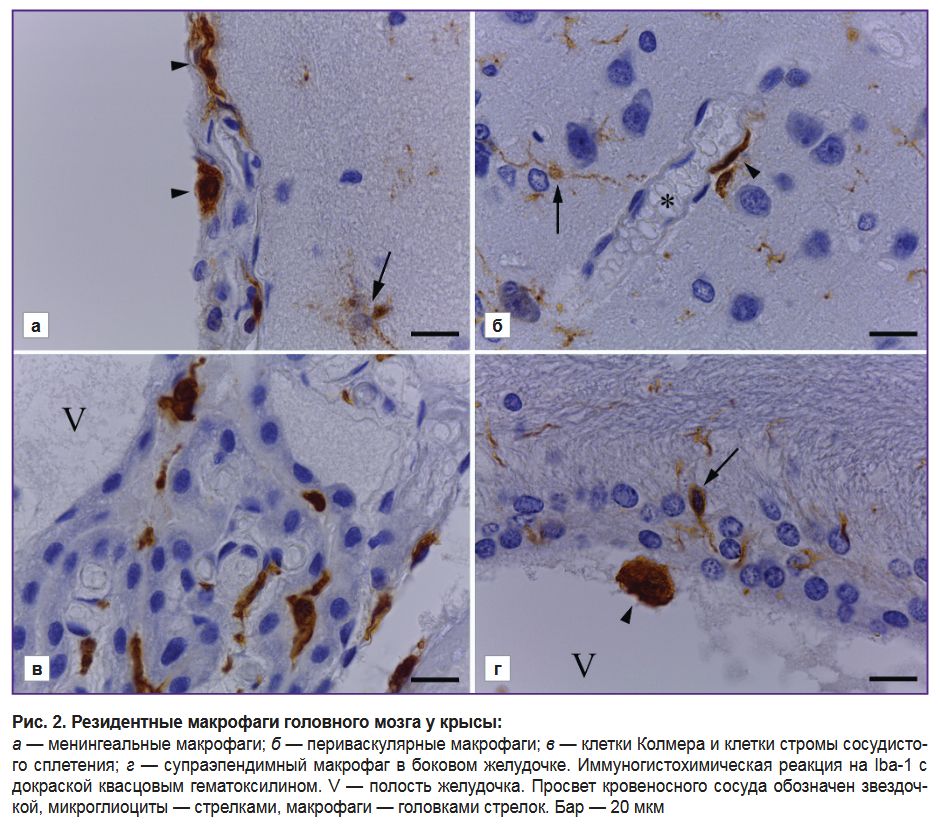
Помимо клеток микроглии в головном мозге крысы отмечено наличие других Iba-1-иммунопозитивных клеток, которые являются тканевыми макрофагами мозга (рис. 2). В оболочках головного мозга выявлены менингеальные макрофаги — безотростчатые клетки круглой и овальной, реже — веретеновидной формы с интенсивно окрашенной цитоплазмой (рис. 2, а). Вблизи кровеносных сосудов в разных отделах головного мозга обнаружены периваскулярные Iba-1-иммунопозитивные малоотростчатые клетки, распластанные вдоль оси капилляра, которые являются периваскулярными макрофагами (рис. 2, б). В сосудистом сплетении головного мозга присутствуют клетки Колмера, которые имеют овальную форму сомы и либо не формируют отростков, либо имеют короткие неразветвленные отростки. В соединительнотканной строме сосудистого сплетения вокруг кровеносных сосудов располагаются вытянутые Iba-1-иммунопозитивные клетки (рис. 2, в). На поверхности эпендимы желудочков наблюдаются отдельные супраэпендимные макрофаги — безотростчатые, овальной формы, с интенсивной реакцией цитоплазмы на антиген Iba-1 (рис. 2, г).
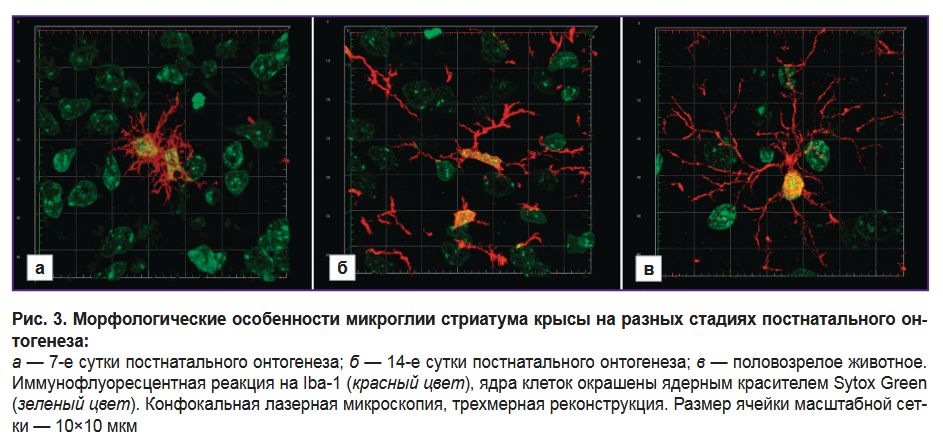
Использование маркера Iba-1 для сравнительно-онтогенетических исследований микроглии. С помощью метода конфокальной лазерной микроскопии изучены микроглиоциты стриатума крысы на разных стадиях постнатального онтогенеза (Р7, Р14, половозрелые животные). Белок Iba-1 присутствовал в телах и отростках микроглиоцитов на всех изученных стадиях онтогенеза.
На 7-е сутки постнатального развития микроглия характеризовалась разнообразием морфотипов: одни микроглиоциты имели широкие лопастные цитоплазматические выросты, другие — 2–3 крупных неветвящихся отростка; присутствовали также микроглиоциты с большим числом коротких тонких ветвящихся отростков (рис. 3, а). Все выявленные микроглиоциты на этой стадии постнатального развития характеризовались небольшим размером.
На 14-е сутки постнатального развития большинство выявленных Iba-1-иммунопозитивных клеток имели небольшое, часто вытянутое тело и несколько длинных относительно тонких умеренно ветвящихся отростков (рис. 3, б).
У половозрелых животных микроглия в стриатуме отличается морфологическим единообразием: все выявленные микроглиоциты имели небольшое тело и многочисленные тонкие сильно ветвящиеся отростки, отходящие от тела клетки в разных направлениях (рис. 3, в).
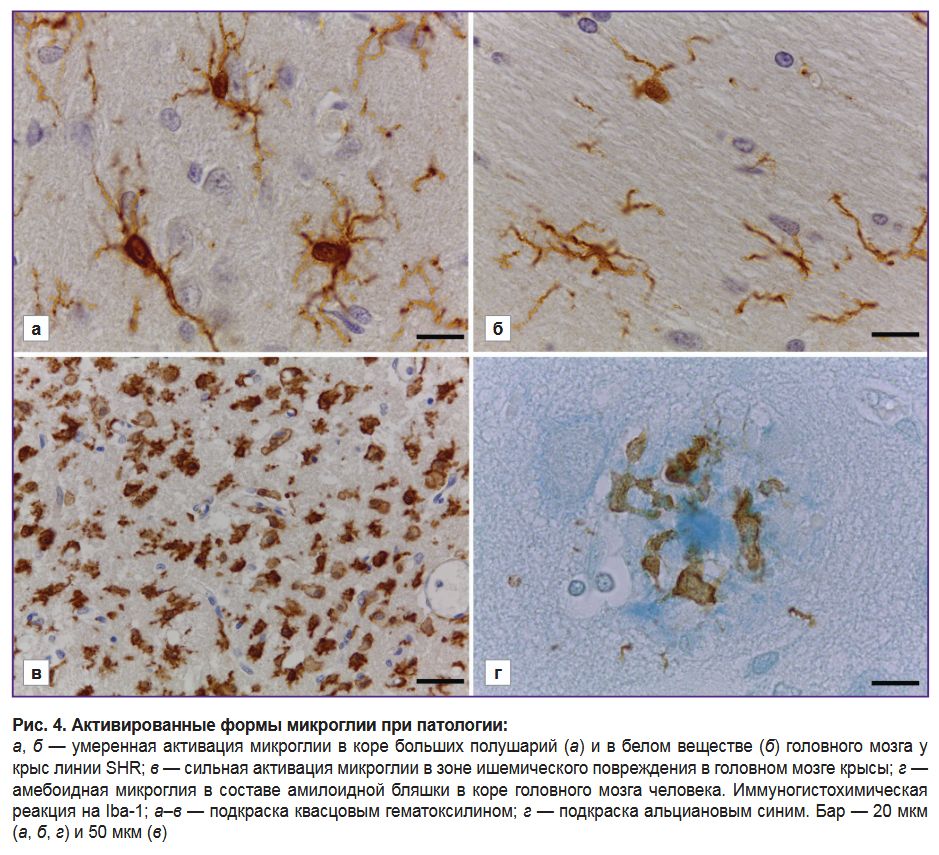
Использование маркера Iba-1 для изучения микроглии при патологии нервной системы. В головном мозге у спонтанно гипертензивных крыс линии SHR (рис. 4, а, б) микроглия имеет ряд структурно-функциональных особенностей при реакции на белок Iba-1: наблюдается увеличение размеров тел микроглиальных клеток, а также утолщение их отростков, которые обладают интенсивным ветвлением как в сером (см. рис. 4, а), так и в белом веществе (см. рис. 4, б).
В головном мозге у крыс через 48 ч после ишемического воздействия в сером веществе стриатума ипсилатерального полушария рядом с областью повреждения присутствует аномально большое число крупных Iba-1-иммунопозитивных клеток (см. рис. 4, в). Они характеризуются округлой или амебоидной формой, отсутствием отростков. Некоторые клетки имеют лишь небольшие цитоплазматические выросты (см. рис. 4, в). Однозначно определить принадлежность этих клеток к микроглии или к макрофагам не представляется возможным. Микроглия с нормальной разветвленной морфологией в области ишемического повреждения отсутствует.
В коре головного мозга человека клетки микроглии присутствуют в составе большинства амилоидных бляшек, выявленных с использованием альцианового синего (рис. 4, г). Микроглиальные клетки имеют амебоидную морфологию: тела их крупные, неправильной формы, иногда наблюдаются короткие цитоплазматические выросты с бульбообразными утолщениями. Микроглия локализована в пределах волокнистого ореола бляшки. Отростки микроглии могут тянуться и плотно примыкать к центральному кору, при этом внутри центральной части Iba-1-иммунопозитивные структуры отсутствуют (см. рис. 4, г). Интенсивность иммуноокрашивания микроглии в данном случае значительно ниже по сравнению с интенсивностью иммуногистохимической реакции на Iba-1 у крысы.
Обсуждение
В рамках представленного исследования мы оценили возможности и границы применения метода иммуногистохимического выявления белка Iba-1 для морфофункционального анализа микроглии в разных условиях. Продемонстрировано, что в головном мозге у половозрелых крыс линии Wistar белок Iba-1 присутствует в клетках микроглии во всех изученных областях головного мозга, в сером и в белом веществе. При этом в разных областях для клеток микроглии характерны морфологические особенности, что хорошо согласуется с имеющимися представлениями о высокой региональной гетерогенности этой клеточной популяции [9]. Нами не отмечено различий в интенсивности иммуногистохимической реакции на Iba-1 в разных отделах головного мозга. С этой точки зрения Iba-1 может рассматриваться в качестве универсального маркера для изучения микроглии разных областей мозга, независимо от высокой региональной специфичности, характерной для этих клеток. Достоинством Iba-1 как маркера микроглии является также высокая консервативность этого белка, что позволяет использовать антитела против Iba-1 для выявления микроглии у разных видов лабораторных животных и человека [21].
Iba-1 — это цитоплазматический белок, который присутствует как в теле, так и в отростках микроглиоцитов [7, 15]. Благодаря цитоплазматической локализации и равномерному распределению Iba-1 внутри клетки иммуногистохимическое определение данного белка позволяет наиболее полно выявлять сложную структуру отростков микроглиоцитов, а также строить пространственные реконструкции этих клеток, что позволяет применять иммуногистохимическую реакцию на Iba-1 в качестве инструмента для наиболее полного изучения морфологии микроглии. Другие широко используемые белки-маркеры микроглии (CD68, P2Y12R, TMEM119) [5, 7, 22, 23] менее пригодны для этой цели, так как являются трансмембранными молекулами и часто имеют «пунктирный» характер распределения. Их применение в качестве иммуногистохимических маркеров не позволяет в полной мере оценить особенности сложной морфологии микроглиальных клеток.
При исследовании микроглии в стриатуме крысы на разных стадиях постнатального онтогенеза нами было показано, что Iba-1 является удобным маркером для изучения динамики изменения морфологии клеток микроглии. Из данных литературы известно, что Iba-1 начинает экспрессироваться в клетках-предшественниках микроглии на ранних этапах эмбриогенеза [24] и сохраняется на протяжении всего последующего онтогенеза, что делает возможным проведение сравнительно-онтогенетических исследований микроглии с использованием Iba-1 в качестве маркера. Это отличает Iba-1 от многих других маркерных белков микроглии. Так, например, TMEM119 отсутствует в незрелой микроглии в пренатальном и раннем (до Р14) постнатальном периоде [15].
Полученные нами результаты вместе с многочисленными данными литературы [23] свидетельствуют о том, что белок Iba-1 присутствует в клетках микроглии разной степени активации. Микроглию обычно подразделяют на два основных морфофункциональных типа: разветвленную (отростчатую) и амебоидную. Отростчатая микроглия является «покоящейся» формой микроглии (по старой терминологии), которую в настоящее время чаще называют «наблюдающей». Эти клетки характеризуются небольшим телом и наличием тонких длинных ветвящихся отростков, которые находятся в постоянном движении: они способны быстро удлиняться, укорачиваться, формировать небольшие временные выросты (филоподии). Считается, что отростчатая микроглия не способна к фагоцитозу, а основной функцией этих клеток является непрерывное сканирование локального микроокружения на наличие патологических стимулов и взаимодействие с другими клетками и внеклеточными компонентами нервной ткани [5]. В ответ на повреждение микроглия быстро меняет молекулярные и структурные свойства, что отражается на ее морфологии — размер тела клеток увеличивается, отростки укорачиваются и утолщаются [5, 23]. Терминальной стадией активации микроглии является амебоидная форма — высокомобильные фагоцитирующие клетки, участвующие в презентации антигена [5, 15]. Данные, полученные нами при изучении разных видов патологии, свидетельствуют о том, что Iba-1 присутствует как в разветвленной, так и в амебоидной микроглии, а также во всех промежуточных формах. Это делает данный белок удобным инструментом для изучения микроглии в норме и при патологии, а также позволяет оценить и дифференцировать различные патологические состояния. Так, при проведении Iba-1-иммуноокрашивания на препаратах головного мозга крыс линии Wistar после транзиторной окклюзии средней мозговой артерии нами была получена характерная картина изменений микроглии при ишемическом повреждении, описанная ранее [25–27]: интенсивность окрашивания и плотность Iba-1-иммунопозитивных элементов была значительно увеличена в ядре ишемии и зоне «ишемической полутени» по сравнению с неповрежденным полушарием, а для Iba-1-позитивных клеток была характерна амебоидная или округлая форма. Данные литературы также свидетельствуют об увеличении экспрессии белка Iba-1 в ишемическом ядре и прилежащей зоне [28].
Типичную морфологическую картину мы наблюдали при изучении препаратов коры головного мозга человека с амилоидными бляшками. Выявлено, что в данном случае активированные клетки микроглии плотно окружают амилоидные скопления. Активация микроглии и ее кластеризация вокруг амилоидных бляшек — хорошо известный феномен, однако точная роль микроглии в данном случае остается неясной. С одной стороны, показано, что микроглия сдерживает токсическое действие бета-амилоида, образуя отграничивающий барьер вокруг амилоидных скоплений [29]. Кроме того, микроглия способна фагоцитировать амилоидные фибриллы [30]. С другой стороны, длительная активация микроглии вызывает хроническое нейровоспаление, приводящее к повреждению нейронов [31]. Исследования, выполненные S. Bubnova и соавт. [32] на посмертных образцах головного мозга людей с болезнью Альцгеймера, продемонстрировали увеличение экспрессии белка Iba-1, выраженное в разной степени в зависимости от стадии заболевания. Интересно, что нами была отмечена пониженная интенсивность Iba-1-иммуноокрашивания микроглии, ассоциированной с амилоидными бляшками в коре головного мозга человека. Это может быть результатом изменения фенотипа микроглии на амебоидный. Однако нельзя исключать и того, что у микроглии, ассоциированной с амилоидными скоплениями, уровень экспрессии Iba-1 уменьшается на определенных стадиях развития заболевания, что приводит к снижению содержания белка Iba-1 в этих клетках.
Помимо многочисленных преимуществ иммуногистохимического выявления Iba-1 для изучения микроглии, этот метод имеет ряд ограничений, которые следует учитывать при планировании исследований. Так, в мировой научной литературе имеются данные об утрате экспрессии Iba-1 клетками микроглии в некоторых отделах головного мозга при развитии таких заболеваний, как шизофрения, болезнь Гентингтона, ожирение [9, 23, 33]. В указанных случаях использование только Iba-1 в качестве маркера не позволяет полностью выявлять популяцию микроглии.
Кроме того, применение Iba-1 не позволяет определить вектор активации микроглии (М1/провоспалительный или М2/противовоспалительный), что делает невозможным точное определение функционального вклада микроглии в конкретную патологию.
Еще одним существенным ограничением использования Iba-1 является присутствие этого белка не только в клетках микроглии, но также в тканевых макрофагах мозга и в периферических макрофагах [5, 23, 34]. Проведенные нами исследования продемонстрировали, что в норме отличить микроглию от тканевых макрофагов при реакции на Iba-1 возможно по особенностям локализации и морфологии. Однако в условиях патологии отличить активированную амебоидную микроглию от рекрутируемых макрофагов (потомков моноцитов крови) может быть затруднительно. Так, нами отмечено, что после временной окклюзии средней мозговой артерии у крыс плотность и интенсивность окрашивания Iba-1 были значительно увеличены в ишемическом ядре и ишемической пограничной зоне по сравнению с непораженным полушарием. В зоне ишемического повреждения присутствовало большое количество Iba-1-иммунопозитивных клеток амебоидной формы. В данном случае определить, являются эти клетки активированной микроглией или рекрутированными макрофагами, не представляется возможным. Очевидно, что в подобных случаях использования только Iba-1 в качестве маркера для анализа микроглии недостаточно. Возможностью совершенствования технологии является одновременное применение нескольких маркерных белков. Наиболее перспективными для этих целей в настоящее время представляются описанные сравнительно недавно белки TMEM119 и P2RY12. TMEM119 — это трансмембранный белок, состоящий из 283 аминокислот, который присутствует исключительно на поверхности микроглиальных клеток и не экспрессируется в других клетках моноцитарно-макрофагального ряда [22]. Связанный с G-белком пуринергический рецептор P2RY12 также высокоспецифичен для микроглии [6, 11, 35, 36]. Оба белка были охарактеризованы как гомеостатические маркеры микроглии, демонстрирующие снижение экспрессии при активации микроглиальных клеток [11, 22, 37, 38]. С такой точки зрения использование комбинаций этих маркеров с Iba-1, экспрессия которого, наоборот, увеличивается при активации [5, 23], должно позволить наиболее полно и высокоспецифично выявлять популяцию микроглии в норме и при патологии. Разработка соответствующих протоколов двойного и/или тройного маркирования представляется важной методической задачей современной нейробиологии.
Заключение
Iba-1 может считаться надежным и универсальным маркером микроглии. Его иммуногистохимическое выявление позволяет идентифицировать и анализировать (качественно и количественно) микроглию в разных отделах головного мозга у человека и лабораторных животных в норме и при патологии. Ограничения использования Iba-1 в качестве маркера микроглии связаны прежде всего с невозможностью определить вектор активации микроглии, а также со сложностью различения микроглии и инфильтрирующих макрофагов мозга при патологии. В этих случаях необходимо совершенствовать технологию выявления микроглии, что может быть основано на применении многомаркерного анализа.
Финансирование. Работа выполнена при поддержке Российского научного фонда, проект №24-15-00032, https://rscf.ru/project/24-15-00032/.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Литература
- Adamu A., Li S., Gao F., Xue G. The role of neuroinflammation in neurodegenerative diseases: current understanding and future therapeutic targets. Front Aging Neurosci 2024; 16: 1347987, https://doi.org/10.3389/fnagi.2024.1347987.
- Muzio L., Viotti A., Martino G. Microglia in neuroinflammation and neurodegeneration: from understanding to therapy. Front Neurosci 2021; 15: 742065, https://doi.org/10.3389/fnins.2021.742065.
- Healy L.M., Zia S., Plemel J.R. Towards a definition of microglia heterogeneity. Commun Biol 2022; 5(1): 1114, https://doi.org/10.1038/s42003-022-04081-6.
- Malinovskaya N.A., Frolova O.V., Shishelova K.O., Panina Yu.A. Current methods for the isolation and cultivation of microglia (review). Sovremennye tehnologii v medicine 2021; 13(6): 89, https://doi.org/10.17691/stm2021.13.6.10.
- Jurga A.M., Paleczna M., Kuter K.Z. Overview of general and discriminating markers of differential microglia phenotypes. Front Cell Neurosci 2020; 14: 198, https://doi.org/10.3389/fncel.2020.00198.
- Cserép C., Pósfai B., Dénes Á. Shaping neuronal fate: functional heterogeneity of direct microglia-neuron interactions. Neuron 2021; 109(2): 222–240, https://doi.org/10.1016/j.neuron.2020.11.007.
- Masuda T., Sankowski R., Staszewski O., Prinz M. Microglia heterogeneity in the single-cell era. Cell Rep 2020; 30(5): 1271–1281, https://doi.org/10.1016/j.celrep.2020.01.010.
- Galatro T.F., Holtman I.R., Lerario A.M., Vainchtein I.D., Brouwer N., Sola P.R., Veras M.M., Pereira T.F., Leite R.E.P., Möller T., Wes P.D., Sogayar M.C., Laman J.D., den Dunnen W., Pasqualucci C.A., Oba-Shinjo S.M., Boddeke E.W.G.M., Marie S.K.N., Eggen B.J.L. Transcriptomic analysis of purified human cortical microglia reveals age-associated changes. Nat Neurosci 2017; 20(8): 1162–1171, https://doi.org/10.1038/nn.4597.
- Tan Y.L., Yuan Y., Tian L. Microglial regional heterogeneity and its role in the brain. Mol Psychiatry 2020; 25(2): 351–367, https://doi.org/10.1038/s41380-019-0609-8.
- Hickman S.E., Kingery N.D., Ohsumi T.K., Borowsky M.L., Wang L.C., Means T.K., El Khoury J. The microglial sensome revealed by direct RNA sequencing. Nat Neurosci 2013; 16(12): 1896–1905, https://doi.org/10.1038/nn.3554.
- Mildner A., Huang H., Radke J., Stenzel W., Priller J. P2Y12 receptor is expressed on human microglia under physiological conditions throughout development and is sensitive to neuroinflammatory diseases. Glia 2017; 65(2): 375–387, https://doi.org/10.1002/glia.23097.
- Zia S., Rawji K.S., Michaels N.J., Burr M., Kerr B.J., Healy L.M., Plemel J.R. Microglia diversity in health and multiple sclerosis. Front Immunol 2020; 11: 588021, https://doi.org/10.3389/fimmu.2020.588021.
- Fumagalli L., Nazlie Mohebiany A., Premereur J., Polanco Miquel P., Bijnens B., Van de Walle P., Fattorelli N., Mancuso R. Microglia heterogeneity, modeling and cell-state annotation in development and neurodegeneration. Nat Neurosci 2025; 28(7): 1381–1392, https://doi.org/10.1038/s41593-025-01931-4.
- Kanazawa H., Ohsawa K., Sasaki Y., Kohsaka S., Imai Y. Macrophage/microglia-specific protein Iba1 enhances membrane ruffling and Rac activation via phospholipase C-gamma-dependent pathway. J Biol Chem 2002; 277(22): 20026–20032, https://doi.org/10.1074/jbc.M109218200.
- Kolos E.A., Korzhevskii D.E. Spinal cord microglia in health and disease. Acta Naturae 2020; 12(1): 4–17, https://doi.org/10.32607/actanaturae.10934.
- Дыбан А.П., Пучков В.Ф., Баранов В.С., Самошкина Н.А., Чеботарь Н.А. Лабораторные млекопитающие: мышь Mus musculus, крыса Rattus norvegicus, кролик Oryctolagus cuniculus, хомячок Cricetus griseous. В кн.: Объекты биологии развития. М: Наука; 1975; с. 505–566.
- Коржевский Д.Э., Кирик О.В., Власов Т.Д. Появление звездчатых гладких миоцитов в головном мозгу крысы после транзиторной фокальной ишемии. Морфология 2013; 143(1): 073–075.
- Гусельникова В.В., Антипова М.В., Федорова Е.А., Сафрай А.Е., Рукавишникова А.А., Михайлова Е.В., Коржевский Д.Э. Особенности применения методов гистохимии и иммуногистохимии для выявления амилоидных бляшек в коре головного мозга человека. Журнал анатомии и гистопатологии 2019; 8(2): 91–99, https://doi.org/10.18499/2225-7357-2019-8-2-91-99.
- Коржевский Д.Э., Сухорукова Е.Г., Гилерович Е.Г., Петрова Е.С., Кирик О.В., Григорьев И.П. Преимущества и недостатки цинк-этанол-формальдегида как фиксатора для иммуноцитохимических исследований и конфокальной лазерной микроскопии. Morphology 2013; 143(2): 081–085.
- Носова О.И., Гусельникова В.В., Коржевский Д.Э. Метод одновременного выявления глиальных клеток и скоплений амилоида на светооптическом уровне. Цитология 2021; 63(6): 557–567, https://doi.org/10.31857/S0041377121060092.
- Korzhevskii D.E., Kirik O., Sukhorukova E. Immunocytochemistry of microglial cells. In: Merigh A., Lossi L. (editors). Immunocytochemistry and related techniques. Neuromethods. Vol. 101. Humana Press, New York; 2015, https://doi.org/10.1007/978-1-4939-2313-7_12.
- Bennett M.L., Bennett F.C., Liddelow S.A., Ajami B., Zamanian J.L., Fernhoff N.B., Mulinyawe S.B., Bohlen C.J., Adil A., Tucker A., Weissman I.L., Chang E.F., Li G., Grant G.A., Hayden Gephart M.G., Barres B.A. New tools for studying microglia in the mouse and human CNS. Proc Natl Acad Sci U S A 2016; 113(12): E1738–E1746, https://doi.org/10.1073/pnas.1525528113.
- Lier J., Streit W.J., Bechmann I. Beyond activation: characterizing microglial functional phenotypes. Cells 2021; 10(9): 2236, https://doi.org/10.3390/cells10092236.
- Hirasawa T., Ohsawa K., Imai Y., Ondo Y., Akazawa C., Uchino S., Kohsaka S. Visualization of microglia in living tissues using Iba1-EGFP transgenic mice. J Neurosci Res 2005; 81(3): 357–362, https://doi.org/10.1002/jnr.20480.
- Shui X., Chen J., Fu Z., Zhu H., Tao H., Li Z. Microglia in ischemic stroke: pathogenesis insights and therapeutic challenges. J Inflamm Res 2024; 17: 3335–3352, https://doi.org/10.2147/JIR.S461795.
- Taylor R.A., Sansing L.H. Microglial responses after ischemic stroke and intracerebral hemorrhage. Clin Dev Immunol 2013; 2013: 746068, https://doi.org/10.1155/2013/746068.
- Коржевский Д.Э., Кирик О.В., Сухорукова Е.Г., Власов Т.Д. Cтруктурная организация микроглиоцитов стриатума после транзиторной фокальной ишемии. Морфология 2012; 141(2): 28–32.
- Murata Y., Sugimoto K., Yang C., Harada K., Gono R., Harada T., Miyashita Y., Higashisaka K., Katada R., Tanaka J., Matsumoto H. Activated microglia-derived macrophage-like cells exacerbate brain edema after ischemic stroke correlate with astrocytic expression of aquaporin-4 and interleukin-1 alpha release. Neurochem Int 2020; 140: 104848, https://doi.org/10.1016/j.neuint.2020.104848.
- Hansen D.V., Hanson J.E., Sheng M. Microglia in Alzheimer's disease. J Cell Biol 2018; 217(2): 459–472, https://doi.org/10.1083/jcb.201709069.
- Grubman A., Choo X.Y., Chew G., Ouyang J.F., Sun G., Croft N.P., Rossello F.J., Simmons R., Buckberry S., Landin D.V., Pflueger J., Vandekolk T.H., Abay Z., Zhou Y., Liu X., Chen J., Larcombe M., Haynes J.M., McLean C., Williams S., Chai S.Y., Wilson T., Lister R., Pouton C.W., Purcell A.W., Rackham O.J.L., Petretto E., Polo J.M. Transcriptional signature in microglia associated with Aβ plaque phagocytosis. Nat Commun 2021; 12(1): 3015, https://doi.org/10.1038/s41467-021-23111-1.
- Miao J., Ma H., Yang Y., Liao Y., Lin C., Zheng J., Yu M., Lan J. Microglia in Alzheimer's disease: pathogenesis, mechanisms, and therapeutic potentials. Front Aging Neurosci 2023; 15: 1201982, https://doi.org/10.3389/fnagi.2023.1201982.
- Bubnova S., Guryanov A., Konkina D., Karapetian V., Kaldybaev l., Pavlova D., Shorina V., Sigalov M., Сhen C. Evaluation of the levels of inflammatory proteins, such as Iba1 and GFAP, in brain tissues of patients with Alzheimer’s disease by western blot analysis. Arzneimitteltherapie 2025; 1385–1397. URL: https://arzneimitteltherapie.com/archives/1520.
- Lier J., Winter K., Bleher J., Grammig J., Mueller W.C., Streit W., Bechmann I. Loss of Iba1-expression in brains from individuals with obesity and hepatic dysfunction. Brain Res 2019; 1710: 220–229, https://doi.org/10.1016/j.brainres.2019.01.006.
- Imai Y., Ibata I., Ito D., Ohsawa K., Kohsaka S. A novel gene Iba1 in the major histocompatibility complex class III region encoding an EF hand protein expressed in a monocytic lineage. Biochem Biophys Res Commun 1996; 224(3): 855–862, https://doi.org/10.1006/bbrc.1996.1112.
- Hollopeter G., Jantzen H.M., Vincent D., Li G., England L., Ramakrishnan V., Yang R.B., Nurden P., Nurden A., Julius D., Conley P.B. Identification of the platelet ADP receptor targeted by antithrombotic drugs. Nature 2001; 409(6817): 202–207, https://doi.org/10.1038/35051599.
- Butovsky O., Jedrychowski M.P., Moore C.S., Cialic R., Lanser A.J., Gabriely G., Koeglsperger T., Dake B., Wu P.M., Doykan C.E., Fanek Z., Liu L., Chen Z., Rothstein J.D., Ransohoff R.M., Gygi S.P., Antel J.P., Weiner H.L. Identification of a unique TGF-β-dependent molecular and functional signature in microglia. Nat Neurosci 2014; 17(1): 131–143, https://doi.org/10.1038/nn.3599.
- Maeda J., Minamihisamatsu T., Shimojo M., Zhou X., Ono M., Matsuba Y., Ji B., Ishii H., Ogawa M., Akatsu H., Kaneda D., Hashizume Y., Robinson J.L., Lee V.M., Saito T., Saido T.C., Trojanowski J.Q., Zhang M.R., Suhara T., Higuchi M., Sahara N. Distinct microglial response against Alzheimer's amyloid and tau pathologies characterized by P2Y12 receptor. Brain Commun 2021; 3(1): fcab011, https://doi.org/10.1093/braincomms/fcab011.
- Amadio S., Parisi C., Montilli C., Carrubba A.S., Apolloni S., Volonté C. P2Y(12) receptor on the verge of a neuroinflammatory breakdown. Mediators Inflamm 2014; 2014: 975849, https://doi.org/10.1155/2014/975849.