Церебральная нейродегенерация и когнитивные нарушения у пациентов, получающих программный гемодиализ: роль нейроглии и ассоциированных факторов (обзор)
Хроническая болезнь почек (ХБП), в исходе которой зачастую необходимо проведение программного гемодиализа (ПГД), представляет собой «модель ускоренного старения». В связи с этим понимание механизмов развития церебральной нейродегенерации (ЦНД) и когнитивных нарушений (КН) у пациентов, получающих ПГД, представляется особенно значимым. Повреждение головного мозга у пациентов с терминальной стадией ХБП рассматривают как многокомпонентный процесс, связанный с воздействием цереброваскулярных, нейродегенеративных и многочисленных дисметаболических факторов. Отдельное внимание уделяется механизмам ЦНД, опосредованным активацией клеток микроглии и астроцитов. Высокая распространенность КН в общей популяции и в особенности у пациентов с терминальной стадией ХБП, получающих ПГД, определяет необходимость уточнения факторов риска и биомаркеров ЦНД. Кроме того, важен поиск терапевтических мишеней, а также управляемых современных стратегий и технологий, направленных на снижение темпов развития ЦНД.
В настоящем обзоре обобщены данные о роли нейроглии и ассоциированных факторов в развитии ЦНД и КН у пациентов, получающих ПГД. Представлены механизмы, воздействующие на нейроглию и участвующие в патогенезе ЦНД и КН. Отдельное внимание уделяется хроническому системному воспалению, воздействию уремических токсинов и активации церебральной ренин-ангиотензин-альдостероновой системы. Рассматриваются такие факторы хронического системного воспаления, ассоциированные с нейроглией, как белок S100B, ИЛ-1β, ИЛ-6, ФНО-α и фибриноген. Проанализированы экспериментальные и клинические данные, посвященные изучению воздействия на микроглию и астроциты уремических токсинов (индоксил сульфата, p-крезол сульфата и имидазолпропионата), а также активации церебральной ренин-ангиотензин-альдостероновой системы. Рассмотрены возможные направления дальнейших клинических исследований, нацеленных на замедление темпов развития ЦНД и КН у данной категории больных.
Введение
Церебральная нейродегенерация (ЦНД) — состояние, характеризующееся прогрессирующим нарушением функции, структурным повреждением и гибелью нейронов головного мозга. ЦНД лежит в основе последующего развития различных нейродегенеративных и психиатрических заболеваний. ЦНД и темпы ее прогрессирования могут оказывать влияние на наличие и выраженность у пациента различных когнитивных и некогнитивных нервно-психических (эмоционально-аффективных, поведенческих и психотических) расстройств [1, 2].
По данным метаанализа и систематического обзора, проведенного в 2022 г. [3], глобальная распространенность умеренных когнитивных нарушений (КН) среди взрослого населения в возрасте 50 лет и старше составляет более 15%. Считается, что у 60% из них в течение последующих лет жизни разовьется клинически значимая деменция. К 2050 г. прогнозируется кратное увеличение количества лиц, страдающих деменцией (до 152 млн человек) [2, 4–6].
Развитие ЦНД и КН особенно характерно для лиц с хронической болезнью почек (ХБП), в том числе для пациентов с терминальной стадией ХБП, получающих программный гемодиализ (ПГД). Необходимо отметить, что с современных позиций ХБП рассматривается как «модель преждевременного/ускоренного старения» [7], поэтому понимание механизмов развития ЦНД и КН у данной категории пациентов представляется значимым для популяции в целом.
В Российской Федерации распространенность ХБП составляет 11,35% [8], при этом более 47 тыс. пациентов находятся на ПГД [9, 10]. КН различной степени выраженности наблюдаются у подавляющего большинства (до 81% случаев) пациентов, получающих ПГД [11–20]. Повреждение головного мозга у пациентов с терминальной стадией ХБП рассматривается как многокомпонентный процесс, связанный с воздействием цереброваскулярных, нейродегенеративных и многочисленных дисметаболических факторов [11, 12, 14, 21]. К настоящему времени более изученной считается проблема развития сосудистых КН у пациентов данной категории; значительно менее исследованными остаются нейродегенеративные механизмы развития высших психических нарушений [12, 22, 23]. Отдельное внимание ученых в настоящее время уделяется ЦНД, опосредованной активацией клеток микроглии и астроцитов [24–30].
Цель данного обзора — анализ и обобщение актуальной информации, относящейся к ассоциированным с нейроглией механизмам развития и усугубления ЦНД и КН у пациентов, получающих терапию методом ПГД.
Стратегия поиска литературы
Поиск литературы производили по реферативным электронным базам данных Scopus, Web of Science, РИНЦ; в поисковой системе PubMed по базам MEDLINE и PubMed Central; на платформах Springer Link, BioMed Central, Free Medical Journals, SSRN, Google Scholar за период с 2014 по 2025 г. по ключевым словам: нейродегенерация/neurodegeneration, гемодиализ/hemodialysis, когнитивные нарушения/cognitive impairment, нейроглия/neuroglia, хроническое системное воспаление/chronic systemic inflammation, уремические токсины/uremic toxins, церебральная ренин-ангиотензин-альдостероновая система (РААС)/brain (cerebral) RAAS.
Патогенез ассоциированных с нейроглией механизмов развития церебральной нейродегенерации и когнитивных нарушений у пациентов, получающих программный гемодиализ
Нарушения в сложном взаимодействии нейронов и нейроглии все чаще признаются важным патофизиологическим механизмом развития ЦНД и КН у пациентов, получающих ПГД. В целом можно выделить 2 основных пути развития:
1) ЦНД, преимущественно опосредованная изменениями нейроглии;
2) ЦНД вследствие прямого влияния факторов на нейроны головного мозга.
В данной статье будут рассмотрены возможные механизмы ЦНД и КН, относящиеся к 1-му пути (опосредованные влиянием на нейроглию).
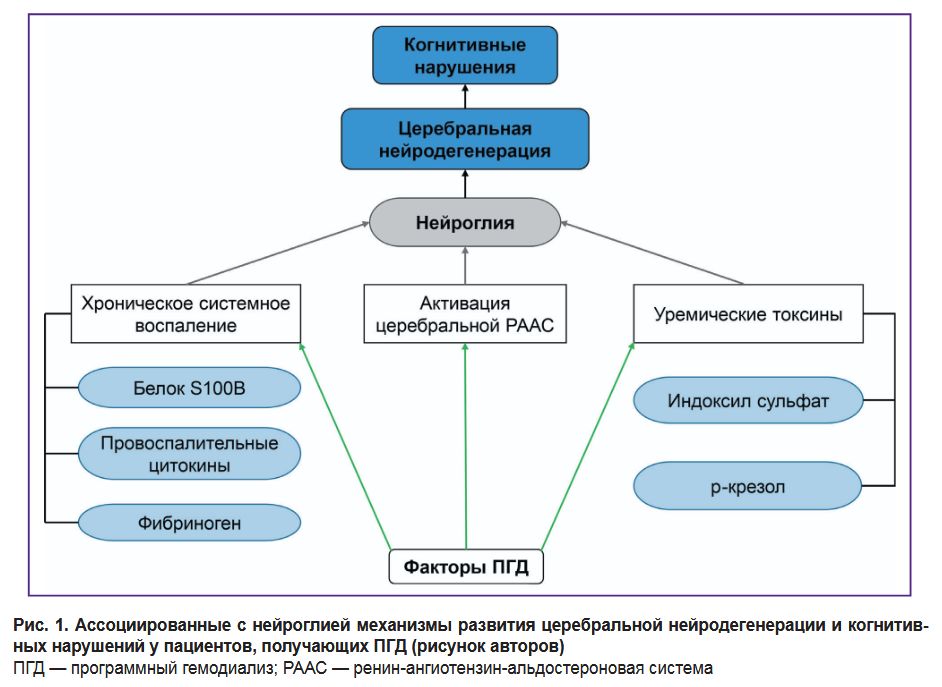
Известно, что нейроглия головного мозга состоит из макроглии (астроцитов, олигодендроцитов, эпендимоцитов) и микроглии (преимущественно мононуклеарных фагоцитов) [24, 31, 32]. Клетки нейроглии играют ключевую роль в поддержании гомеостаза и регуляции иммунных реакций мозга [33, 34]. Необходимо отметить, что на сегодняшний день среди всех нейроглиальных структур именно астроцитам и микроглии отводится основная роль в патогенезе ЦНД [25, 26, 28]. Результаты проведенного анализа ассоциированных с нейроглией механизмов развития ЦНД и КН у пациентов, получающих ПГД, представлены на рис. 1.
При обнаружении сигнала, связанного с физиологическими или патологическими процессами, клетки нейроглии активируются и трансформируются, запуская различные ответные реакции (фагоцитоз, секрецию воспалительных и трофических факторов) [33, 34]. Вследствие этого происходят пролиферация и дифференцировка нейронов, оказывается влияние на синаптические связи и, следовательно, на когнитивные и поведенческие функции [33, 34].
Считается, что в здоровом мозге микроглия, представленная резидентными иммунными клетками мозга, находится в состоянии покоя (М0) [35, 36]. При появлении определенных стрессоров и триггеров, например DAMPs (damage-associated molecular patterns; молекулярные паттерны, ассоциированные с повреждением ткани) или PAMPs (patogen-associated molecular patterns; молекулярные паттерны, ассоциированные с патогенами), в головном мозге происходит микроглиоз. Данный процесс реализуется через PRRs-рецепторы (pattern recognition receptors; рецепторы распознавания паттернов), играющие центральную роль в регуляции врожденного иммунитета [37–39]. При этом клетки микроглии из состояния покоя (М0) могут поляризоваться либо в провоспалительный (М1), либо в противовоспалительный (М2) фенотипы [26, 30, 32, 35, 36, 39, 40]. Полагают, что специфичность микроглиальной активации и направление поляризации определяются видом повреждающего агента, особенностями воздействия и локализацией патологического процесса [36].
У пациентов на ПГД количество специфических для ХБП и диализ-ассоциированных факторов, способных взаимодействовать с PRRs-рецепторами и запускать микроглиоз, увеличивается. Микроглиальная активация М1, индуцируя воспалительные реакции через продукцию провоспалительных цитокинов, способствует повреждению нейронов и тем самым — развитию нейродегенеративных процессов [36, 39, 41]. Наряду с поляризацией микроглии в сторону М1-фенотипа и активацией нейровоспаления при микроглиозе происходит нарушение регуляции аутофагии и усугубление ЦНД.
Кроме провоспалительного фенотипа микроглии (М1) выделяют противовоспалительный фенотип (М2). Поляризация микроглии в М2-фенотип оказывает нейропротективное действие, подавляя нейровоспаление путем выработки противовоспалительных факторов, что приводит к восстановлению ряда гомеостатических процессов в мозге [35, 39, 41].
Подобно микроглии, дифференцировку самой многочисленной разновидности глиальных клеток макроглии — астроцитов — также принято подразделять на провоспалительную (А1) и противовоспалительную (А2) [25, 27]. Считается, что в ответ на острый или хронический клеточный дистресс преобладающей становится дифференцировка астроцитов в провоспалительный (А1) фенотип (реактивный астроглиоз). Напротив, поляризация астроцитов (астроглиоз) в противовоспалительный (А2) фенотип приводит к нейропротективному и нейротрофическому эффектам и поддержанию гомеостаза гематоэнцефалического барьера (ГЭБ) [25, 27].
На фоне ПГД в головном мозге создаются условия для избыточной поляризации астроцитов в А1-фенотип, что может усугублять ЦНД путем дополнительной экспрессии нейротоксичных и провоспалительных цитокинов [25, 27, 42]. Кроме того, в связи с реактивным астроглиозом поляризованные А1-астроциты утрачивают ряд защитных физиологических функций, поддерживающих нормальный гомеостаз нейрона. Как следствие, усугубляются процессы, связанные с обратным захватом глутамата, метаболизмом глюкозы и жирных кислот, ухудшается синаптическая передача импульсов [25, 27, 42].
Необходимо отметить, что в основе гемодиализа лежат процессы переноса веществ из крови в диализат через полупроницаемую мембрану. Современные методы и режимы ПГД позволяют добиться более эффективного удаления из крови низкомолекулярных компонентов, токсических веществ и продуктов метаболизма [43–47]. Однако полностью воссоздать естественный почечный обмен аппаратом «искусственная почка» не удается. Часть оставшихся в крови продуктов обмена может проникать через ГЭБ и изменять активность нейроглии. Кроме того, во время гемодиализа не удается очистить кровь пациентов от веществ с молекулярной массой свыше 30 000 Да, так как через современные диализные мембраны эти молекулы не проходят [44, 45]. По-видимому, темпы ЦНД и степень провоспалительной поляризации нейроглии зависят в том числе от технологий, применяемых во время процедуры гемодиализа (гемодиализ, гемофильтрация или гемодиафильтрация), и свойств диализной мембраны [43–46].
В целом остаются неясными представления о роли микроглии и астроцитов в развитии ЦНД у пациентов с ХБП, находящихся на ПГД. Молекулярный путь, определяющий направление фенотипической дифференцировки микроглии/астроцитов из М0/А0 в М1/А1 или М2/А2, в настоящий момент до конца не изучен. Окончательная роль морфологической и функциональной клеточной поляризации в развитии ЦНД в общей популяции и у пациентов, получающих ПГД, также требует уточнения. Возможные механизмы активации нейроглии, опосредованные взаимодействием специфических для ХБП и диализ-ассоциированных факторов с цитокиновыми рецепторами, будут представлены ниже. Данные о влиянии гемодиализа на другие рецептор-зависимые механизмы регуляции нейроглии в настоящее время отсутствуют.
Таким образом, нейроглия пациентов, получающих ПГД, находится в неблагоприятных условиях, способствующих микроглиальной активации, реактивному астроглиозу и ЦНД [44–46, 48]. На основе имеющихся экспериментальных и клинических данных к ассоциированным с нейроглией механизмам развития и усугубления ЦНД и КН у пациентов, получающих ПГД, отнесены хроническое системное воспаление, персистирующее воздействие уремических токсинов и активация церебральной РААС. Более подробно они рассмотрены ниже.
Хроническое системное воспаление как фактор развития церебральной нейродегенерации у пациентов, получающих программный гемодиализ
По данным ряда клинических исследований, пациенты с терминальной стадией ХБП и в особенности получающие ПГД имеют признаки хронического системного воспаления [16, 49–52]. Считается, что исходами данного состояния являются повышение риска развития сердечно-сосудистых событий, синдрома MICS (malnutrition-inflammation complex syndrome; синдром истощения, ассоциированный с системным воспалением), анемии, минерально-костных нарушений, а также ЦНД и КН [21, 50, 53]. В исследованиях приводятся данные о таких факторах хронического системного воспаления, ассоциированных с воздействием на нейроглию у пациентов, получающих ПГД, как белок S100B, некоторые провоспалительные цитокины и фибриноген [21, 50, 53, 54].
Белок S100B
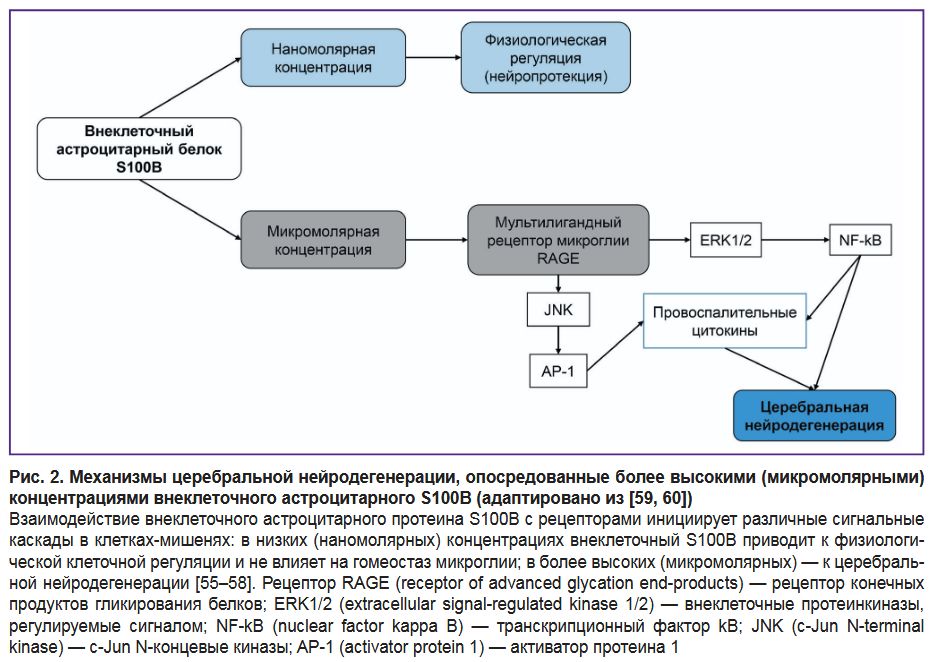
Белок S100B (молекулярная масса 21 кДа) — кальций-связывающий протеин семейства S100, сконцентрированный в центральной нервной системе преимущественно в астроцитах [21, 55–57]. Ряд авторов [55, 57, 58] относят S100B к одному из маркеров повреждения головного мозга. В то же время F. Michetti и соавт. [57] предполагают, что сам внеклеточный белок S100B может являться не только биомаркером повреждения, но и самостоятельным патогенетическим фактором, провоцирующим нейровоспаление и ЦНД. Развитие ЦНД на фоне патологически повышенных (микромолярных) концентраций внеклеточного белка S100B происходит посредством активации внутриклеточных путей (внутриклеточной перегрузки кальцием, накопления активных форм кислорода), высвобождения микроглией провоспалительных цитокинов и активации апоптоза нейронов (рис. 2) [55–60].
Н.В. Фомина и соавт. [59] изучали взаимосвязь когнитивных функций с уровнем S100B у лиц молодого и среднего возраста с ХБП I–III стадии (n=108). КН определяли с помощью Краткой шкалы оценки психического статуса (Mini Mental State Examination; MMSE). Повышенные концентрации S100B регистрировались уже на ранних стадиях ХБП и нарастали по мере снижения скорости клубочковой фильтрации (rs=–0,37; p=0,001). Повышенные концентрации были ассоциированы с КН нейродинамического характера: в частности, с минимальной и средней экспозицией сложной зрительно-моторной реакции (rs=0,29, p=0,001; rs=0,39, p=0,001 соответственно), а также с суммарным временем опережения и количеством точных движений в тестах, оценивающих реакцию на движущийся объект (rs=–0,39, p=0,001; rs=–0,31, p=0,001).
B.S. Park и соавт.[15] приводят данные о взаимосвязи наличия КН с повышением концентрации S100B у пациентов с терминальной стадией ХБП. В исследовании принимали участие 30 пациентов, получавших ПГД 3 раза в неделю (продолжительность сеансов не указывается), средний стаж диализа составлял 21 мес. Оценку когнитивных функций участников исследования проводили на основании шкалы MMSE. Пациенты были разделены на две группы: без КН (n=17) и с КН (n=13). Множественный логистический регрессионный анализ показал, что концентрация S100B в сыворотке крови пациентов с КН оказалась значительно выше и являлась независимым предиктором развития у них КН (S100B≥36, 1 пг/мл). Авторы связывают полученные результаты с изменениями нейроглии головного мозга у пациентов на ПГД и высоким содержанием у них внеклеточного астроцитарного S100B. Необходимо отметить, что проведенное исследование имело некоторые недостатки: относительно небольшая выборка участников и скрининговый характер выбранного метода нейропсихического исследования с использованием шкалы MMSE, которые могли повлиять на достоверность результатов.
Данные, полученные B.S. Park и соавт. [15], согласуются с результатами более поздних исследований. Так, H.K. Al-Hakeim и соавт. [54] изучали связь ряда воспалительных биомаркеров крови, в том числе S100B, с развитием нейропсихиатрических симптомов у пациентов, получающих ПГД (n=70). Повышенная концентрация S100B была связана с развитием и тяжестью одного или нескольких нейропсихиатрических синдромов. M. Bossola и соавт. [60] в своей работе, помимо уровня S100B до или после сеанса гемодиализа, исследовали связь «постдиализной усталости» с концентрацией данного белка в сыворотке крови. Всего в исследовании приняло участие 30 пациентов, находившихся на ПГД. У 22 из них (73,4%) был выявлен синдром «постдиализной усталости». Концентрация S100B в сыворотке крови после диализа (Me [межквартильный размах] = 17,4 мкг [7,1–30,9]) была значительно выше аналогичного показателя до диализа (Me [межквартильный размах] = 5 мкг [1,4–22,1]; p=0,0001) [60].
В целом необходимо отметить, что публикаций, посвященных уровню внеклеточного S100B и его роли в развитии ЦНД и КН у пациентов, получающих ПГД, в современной литературе недостаточно [15, 54, 60]. Окончательная роль S100B в развитии ЦНД до конца не ясна, необходимо проведение дальнейших клинических исследований в этом направлении. Данный показатель хронического системного воспаления, по-видимому, может быть предложен в качестве потенциального биомаркера тяжести ЦНД. Кроме того, в будущем применение ингибиторов S100B, способных преодолевать ГЭБ, может оказаться перспективным направлением терапии КН у данной категории пациентов [56, 61].
Провоспалительные цитокины интерлейкин-1β, интерлейкин-6, фактор некроза опухоли альфа
К факторам хронического системного воспаления, ассоциированным с воздействием на нейроглию через ее цитокиновые рецепторы, относят множество различных провоспалительных цитокинов [33, 62]. Необходимо отметить, что астроциты и микроглия экспрессируют широкий спектр цитокиновых рецепторов на поверхность своих клеток, а также способны к самостоятельной продукции достаточно широкого ряда цитокинов. Ниже представлены только те провоспалительные цитокины, которые в экспериментальных или клинических исследованиях изучались в аспекте влияния гемодиализа на нейроглию. Считается, что активация нейроглии зависит от уровней и соотношений провоспалительных цитокинов, проникших через ГЭБ, и потенцирует развитие ЦНД и КН [33, 62, 63]. Приводятся данные о высоких концентрациях ряда провоспалительных цитокинов у пациентов додиализных и диализных стадий ХБП [64, 65]. Это может быть связано с воздействием факторов, специфических для ХБП, и влиянием факторов, ассоциированных с самой процедурой диализа (взаимодействие крови с диализной мембраной, хроническая циркуляция уремических токсинов, персистенция хронических очагов инфекции, транслокация кишечной флоры в кровеносное русло) [53, 64–67]. Особый интерес исследователей вызывает возможная роль интерлейкинов (ИЛ-1β, ИЛ-6) и фактора некроза опухоли альфа (ФНО-α) в развитии ЦНД у пациентов додиализного и диализного периодов ХБП. Отмечается, что повышенная внеклеточная концентрация данных цитокинов ассоциирована с воспалительной активацией нейроглии головного мозга [21, 39, 64, 65].
ИЛ-1β (молекулярная масса 18 кДа) в норме играет важную роль в головном мозге: активизирует процессы обучения и памяти, участвует в нейрональной сигнализации, синаптической пластичности, регуляции сна, индукции нейротрофических факторов и нейрогенезе у взрослых. Необходимо отметить, что в физиологических условиях уровень лигандов ИЛ-1 низкий, микроглия при этом является ключевым источником продукции ИЛ-1 в головном мозге [68]. При развитии инфекционного процесса и/или асептическом воспалении в мозге быстро повышается экспрессия ИЛ-1β, начинают преобладать процессы когнитивной дисфункции и ЦНД, связанные с активацией нейроглии и стимуляцией микроглиальных и астроцитарных провоспалительных реакций [69–71]. Кроме того, считается, что ИЛ-1β опосредованно может приводить к накоплению глутамата, глутаматной эксайтотоксичности и к гибели нейронов [69, 72].
В настоящее время ИЛ-1β считается основным медиатором врожденного нейровоспаления, уровень которого можно фармакологически корректировать. Наибольшее количество исследований с использованием антител к ИЛ-1β [68, 73, 74] было проведено в эксперименте при черепно-мозговой травме. Целью этих исследований являлось уменьшение прогрессирования нейровоспаления и замедление ЦНД. В большинстве из них регистрировались улучшения со стороны когнитивных и двигательных функций у обследуемых.
Антицитокиновая терапия с применением антагонистов рецепторов ИЛ-1 в аспекте замедления темпов ЦНД и КН может оказаться патогенетически обоснованным направлением дальнейших клинических исследований, в том числе для пациентов, получающих ПГД [75]. Так, в многоцентровом рандомизированном плацебо-контролируемом исследовании L.M. Dember и соавт. [75] оценивали безопасность, переносимость и эффективность применения антагониста рецепторов ИЛ-1 у 80 пациентов, находившихся на ПГД. Из них 38 пациентов получали лечение антагонистом рецепторов ИЛ-1 (анакинра, 100 мг 3 раза в неделю) в течение 24 нед; 42 участника вошли в группу плацебо. ПГД проводили 3 раза в неделю (продолжительность сеансов авторами не указана), средний стаж диализа составил 4,4 года. Применение антагонистов рецепторов ИЛ-1 позволило снизить концентрацию С-реактивного белка (СРБ) (в 41% случаев против 6% в группе плацебо) и ИЛ-6 (в 25% случаев против 0% в группе контроля) в плазме крови пациентов, получавших ПГД. Частота серьезных нежелательных явлений и летальных исходов была сопоставимой в группах антицитокиновой терапии и плацебо. Частота клинически значимых нежелательных явлений (включая инфекции и цитопении) была значительно ниже в группе с применением антагониста рецепторов ИЛ-1 в отличие от группы сравнения (0,48 против 1,40 событий/пациента в год).
В целом участие цитокинов семейства ИЛ-1 в патогенезе ЦНД и КН у пациентов, находящихся на ПГД, мало изучено [73]. Применение антогонистов рецепторов ИЛ-1, по-видимому, может сокращать темпы развития ЦНД и КН посредством снижения уровней факторов хронического системного воспаления и прямого блокирования рецепторов ИЛ-1. Многообещающие данные по безопасности и возможной эффективности в отношении концентраций СРБ и ИЛ-6 подтверждают необходимость дальнейших клинических исследований в отношении значимости применения блокаторов ИЛ-1 у этой категории пациентов.
ИЛ-6 (молекулярная масса 21–28 кДа) — плейотропный цитокин, описанный при широком спектре патологических состояний как мощный индуктор и модулятор активации микроглии. В физиологических условиях здорового мозга ИЛ-6 продуцируется в низких концентрациях, выполняет функцию регулятора воспалительных и иммунологических реакций и оказывает нейропротективное действие [76]. При нарушении гомеостаза центральной нервной системы (в условиях острой ишемии, черепно-мозговой травмы, нейродегенеративных заболеваний) возникает хроническая повышенная продукция ИЛ-6, что «переводит» нейроглию в провоспалительный фенотип и усугубляет течение ЦНД [76, 77].
В проспективном контролируемом одноцентровом исследовании B. Zhu и соавт. [65] изучали уровень экспрессии ряда биомаркеров сыворотки крови у пациентов с умеренными КН, находившихся на ПГД [65]. В этом исследовании 58 пациентов получали заместительную почечную терапию методом ПГД 2 раза в неделю и сеанс гемодиафильтрации 1 раз в неделю. Продолжительность одного сеанса составляла 240 мин, средний стаж диализа — 6 лет. В группу контроля вошли 20 человек. Когнитивные функции оценивали на основании шкалы MMSE и Монреальской шкалы оценки когнитивных функций (Montreal Cognitive Assessment, MoCA). У пациентов с КН, получавших ПГД, были значительно повышены концентрации ИЛ-6 и ФНО-α, при этом высокая концентрация ИЛ-6 была связана с более низкими результатами скрининговой оценки нейропсихологического статуса по шкале MoCA (r=0,02; p<0,0001) [65].
Применение моноклональных антител к ИЛ-6 является одним из развивающихся направлений, ориентированных на управление сердечно-сосудистым риском и снижение уровня «сосудистого» воспаления у пациентов, находящихся на ПГД [78, 79]. Так, в 2024 г. завершилось рандомизированное исследование фазы 2b [79]. Было изучено воздействие клазакизумаба, представляющего собой высокоаффинное гуманизированное моноклональное антитело, на лиганд ИЛ-6 и ингибирующее последующее каскадное влияние данного цитокина. Терапия клазакизумабом (первичная конечная точка исследования) привела к значительному снижению концентраций высокочувствительного СРБ в сыворотке крови на 12-й неделе на 86, 90 и 92% в рандомизированных группах клазакизумаба (2,5; 5 и 10 мг соответственно) по сравнению с группой плацебо (p<0,0001). Вторичной конечной точкой данной терапии явилось снижение концентрации сывороточного фибриногена, амилоида А, секреторной фосфолипазы А2 и липопротеина (а), а также увеличение средней концентрации сывороточного альбумина на 12-й неделе лечения по сравнению с группой плацебо. Пациенты в группах клазакизумаба (2,5; 5 и 10 мг) с исходно повышенной концентрацией высокочувствительного СРБ достигли целевого уровня данного показателя (<2,0 мг/л) в 79, 82 и 79% случаев соответственно по сравнению с пациентами, получавшими плацебо (0%). Результаты исследования свидетельствуют о том, что у пациентов, находившихся на ПГД, клазакизумаб снижал уровень ряда воспалительных биомаркеров, связанных с риском сердечно-сосудистых событий. Когнитивные функции пациентов и состояние нейроглии в данном исследовании не изучались.
ФНО-α (молекулярная масса 17 кДа) представляет собой полифункциональную молекулу, также участвующую в нейровоспалении [80, 81]. Большинство исследователей акцентируют внимание на роли данного цитокина в развитии ЦНД и КН, опосредованных активацией нейроглии и усилением процессов нейротоксичности [39, 80, 81]. Предполагается, что высвобождение ФНО-α усиливает активность M1, но снижает активность маркеров M2 в микроглии; инициирует аутокринную активацию и процессы глутаматной эксайтотоксичности, оксидативного стресса; нарушает процессы инсулинорезистентности и аутофагии в клетках головного мозга [39, 81]. Приводятся данные о том, что нейротоксичность, вызванная ФНО-α, ослабевала при предварительной обработке микроглии рапамицином (активатором аутофагии) [39].
В нескольких клинических исследованиях продемонстрированы повышенные концентрации ФНО-α в плазме крови пациентов, получавших ПГД [51, 82]. Указывается на наличие связи между повышенной концентрацией ФНО-α в плазме крови и развитием КН у диализных пациентов [65]. Кроме того, в упоминавшейся выше работе B. Zhu и соавт. [65] помимо ИЛ-6 изучали зависимость между концентрацией ФНО-α в плазме крови пациентов, получавших ПГД, и наличием у них КН. Установлено, что у пациентов с умеренными КН высокое содержание ФНО-α было связано с более низкими результатами скрининговой оценки нейропсихологического статуса по шкале MoCA (r=0,27; p<0,0001).
Применение пероральных биоактивных добавок может оказаться еще одним перспективным направлением клинических исследований, направленных на коррекцию уровней провоспалительных цитокинов у пациентов, получающих ПГД, и замедление у них темпов ЦНД и КН [51, 67]. G. Vafadar-Afshar и соавт. [67] показали, что концентрации ИЛ-6 и ФНО-α в сыворотке крови 54 пациентов, получавших ПГД, снизились через 12 нед лечения нанокуркумином по сравнению с плацебо (p=0,024 для ИЛ-6 и p=0,02 для ФНО-α). Экспрессия генов ИЛ-6 и ФНО-α в мононуклеарных клетках периферической крови через 12 нед терапии также находилась на более низких уровнях по сравнению с исходными значениями в группе, получавшей нанокуркумин, а изменения уровней экспрессии указанных генов коррелировали с изменениями концентраций ИЛ-6 и ФНО-α в сыворотке крови. R. Supriyadi и соавт. [51] изучали эффект применения супероксиддисмутазы (СОД) на уровень ФНО-α у пациентов, находившихся на ПГД [51]. В исследование было включено 28 пациентов (средний возраст составил 42±11 лет), получавших ПГД 2 раза в неделю (продолжительность сеансов не указывается), средний стаж диализа составил 24 (5–72) мес. Все участники получали СОД-глиадин по 250 МЕ 2 раза в день в течение 4 нед. Концентрации ФНО-α в сыворотке крови оценивали до и после лечения. Экзогенное добавление СОД-глиадина привело к снижению концентрации ФНО-α в плазме крови с 0,109 (0,087–0,223) до 0,099 (0,083–0,149) пг/мл (p=0,036). Результаты были получены на относительно небольшой выборке исследуемых пациентов, что указывает на необходимость дальнейших контролируемых клинических исследований в данном направлении.
Фибриноген
Фибриноген (молекулярная масса 340 кДа) представляет собой гликопротеин системы свертывания крови, который является предшественником фибринового сгустка, синтезируется в печени и циркулирует в плазме крови [48, 83, 84]. Поскольку высокие концентрации фибриногена связаны с повышенным риском развития деменции, исследователи отводят ему значимую роль в развитии ЦНД [83–86]. Дисфункция ГЭБ позволяет фибриногену просачиваться из крови в мозг, где он под действием периваскулярного тканевого фактора и тромбина превращается в нерастворимый фибрин и откладывается в паренхиме и сосудах головного мозга. Расщепление фибриногена тромбином обнажает эпитоп P2, который может взаимодействовать с молекулами CD11b и CD11c клеток нейроглии. Таким образом, в ответ на появление фибрина в тканях мозга происходит нейротоксическая поляризация микроглии и астроцитов, развиваются процессы ЦНД [83–88]. К настоящему времени доказано, что концентрация плазменного фибриногена коррелирует с плазменными концентрациями бета-амилоида Aβ40, Aβ42 и фосфорилированным тау-181 (p-tau) спинномозговой жидкости, а также с индикаторами отложения Aβ в мозге (такими как p-tau/Aβ42) и стенках кровеносных сосудов коры головного мозга [88].
J.M. Pyun и соавт. [89] изучали когнитивный статус пациентов во взаимосвязи с уровнем фибриногена плазмы крови [89]. В ретроспективное исследование было включено 643 участника с умеренными КН. У 323 из них регистрировались высокие концентрации фибриногена; у 320 — низкие. Когнитивные функции оценивали с помощью шкалы MMSE, Шкалы оценки клинической деменции по сумме ячеек (Clinical Dementia Rating Scale Sum of Boxes, CDR-SOB), Шкалы общего ухудшения когнитивных функций (Global Deterioration Scale, GDS). Пациенты с умеренными КН и более высоким уровнем фибриногена плазмы демонстрировали более низкие результаты по показателям внимания и управляющих функций, вне зависимости от генотипа аполипопротеина E или других факторов сосудистого риска. Авторы исследования подчеркивают, что одним из механизмов развития КН у пациентов с высокими концентрациями фибриногена является ЦНД, опосредованная активацией нейроглии. Полученные J.M. Pyun и соавт. [89] данные согласуются с рядом других клинических исследований, в которых также была продемонстрирована связь высокой концентрации фибриногена с низкими показателями в различных когнитивных доменах (память, внимание, скорость обработки информации и управляющие функции) [90–92].
Считается, что у пациентов, находящихся на ПГД, концентрация фибриногена крови повышена [48, 83]. Так, K. Pénzes и соавт. [48] изучали концентрацию фибриногена сыворотки крови у пациентов, получавших ПГД, до и после 4-часового сеанса гемодиализа. В исследование вошли 30 пациентов; сеансы ПГД продолжительностью 240 мин каждый проводили 3 раза в неделю; средний стаж диализа составил 4,5 года. Более чем у 50% пациентов, получавших ПГД, отмечались повышенные концентрации фибриногена — выше референсного интервала (1,5–4,0 г/л); у остальных значения находились преимущественно в верхней половине референсного интервала. Средняя концентрация фибриногена у пациентов, получавших лечение методом гемодиафильтрации, составила 4,21±0,82 г/л; в группе гемодиализа — 4,23±0,87 г/л [48]. После 4-часового сеанса гемодиализа концентрация фибриногена плазмы крови увеличивалась. Авторы связывают выявленные высокие уровни фибриногена у данной категории пациентов с наличием у них хронических нарушений в системе гемостаза, а также с повышенными уровнями СРБ на фоне хронического системного воспаления. Уровень СРБ, характеризующий воспалительный статус обследованных лиц, авторы считают ключевым фактором, определившим концентрацию фибриногена.
Необходимо отметить, что исследования, посвященные ЦНД и КН у пациентов, получающих ПГД, во взаимосвязи с уровнями фибриногена и состоянием у них ГЭБ в настоящее время отсутствуют.
Роль уремических токсинов в развитии церебральной нейродегенерации и когнитивных нарушений у пациентов, находящихся на программном гемодиализе
Кроме факторов, относящихся к хроническому системному воспалению, в современной литературе приводятся данные о значительной роли уремических токсинов в развитии ЦНД и КН у пациентов, получающих ПГД [16, 17, 93, 94]. Аминокислоты, присутствующие в пищевом белке, являются субстратом ферментации для бактерий толстого кишечника (особенно при их чрезмерном потреблении) [95]. Уремические токсины являются остатками органических соединений кишечного происхождения, бактериальными аминокислотными метаболитами, которые не могут быть выведены из организма вследствие нарушения функции почек и поэтому накапливаются в крови и головном мозге [16, 96, 97]. Избыточное и длительное воздействие уремических токсинов рассматривается как причина активации нейроглии, а также их негативного влияния на нейроны головного мозга и процессы ЦНД [16, 28, 93, 98]. Исследователи полагают, что к общим патофизиологическим аспектам данных процессов относятся снижение скорости синаптогенеза и активности натрий-калиевой АТФ-азы, нарушение баланса нейротрансмиттеров и повышение проницаемости ГЭБ [16, 93, 99–102]. Известно, что проникновение уремических токсинов в головной мозг опосредовано специфическими переносчиками (транспортерами органических анионов) [16, 93, 100]. Показана потенциальная роль индоксил сульфата (IS), p-крезола и его производного — p-крезол сульфата (PCS), а также имидазолпропионата в активации нейроглии пациентов, получающих ПГД. Необходимо отметить, что в связи с высокой способностью связываться с белками плазмы крови эти молекулы плохо элиминируются из организма с помощью применяемых в настоящее время диализных технологий [93, 95].
Индоксил сульфат (indoxyl sulfate, IS; молекулярная масса 213 Да) является продуктом метаболизма триптофана [103–105]. Данный уремический токсин начинает накапливаться у пациентов уже на додиализных стадиях ХБП и с трудом выводится в процессе процедуры гемодиализа [93, 104, 106]. IS может запускать процессы ЦНД, негативно влияя на функцию микроглии и астроцитов, индуцируя в клетках нейроглии окислительный стресс, образование провоспалительных цитокинов и апоптоз [23, 28, 38, 107].
В контролируемом исследовании Y.T. Lin и соавт. [93] была выявлена зависимость между повышением уровня свободной формы IS в крови и КН у 260 пациентов (средний возраст — 58,1±11,3 года), получавших ПГД. Гемодиализ проводили 3 раза в неделю, продолжительность одного сеанса составляла 240 мин, средний стаж диализа — 7 лет. Поток диализата поддерживался на уровне 500 мл/мин, скорость кровотока — на уровне 250 и 300 мл/мин, а показатель адекватности проводимого диализа Kt/V составлял более 1,2. Циркулирующие свободные формы IS и PCS количественно определяли с помощью тандемной масс-спектрометрии. Оценку когнитивных функций пациентов проводили с помощью MMSE и Шкалы оценки когнитивных способностей (Cognitive Abilities Screening Instrument, CASI). Способность IS и PCS проникать через ГЭБ прогнозировали с помощью компьютерного моделирования in silico. Согласно оценке, оба соединения имели статус ГЭБ «+» и высокую вероятность проникновения через ГЭБ (0,8727 — для IS и 0,9405 — для PCS). У пациентов, получавших ПГД, чаще наблюдались КН и более высокие уровни циркулирующих IS и PCS в отличие от группы сравнения. Выявлена взаимосвязь между высокой концентрацией IS плазмы крови (>1,45 мкг/мл) и низкими показателями когнитивных тестов (долговременной памяти, мышления, речевых и зрительно-пространственных функций). Авторы делают вывод о том, что высокий уровень свободной циркулирующей формы IS, но не PCS, был связан с наличием КН, что, по-видимому, обусловлено большей способностью IS связываться с белками сыворотки крови и более плохой элиминацией IS во время диализа по сравнению с PCS [93].
Необходимо проведение дальнейших клинических исследований в аспекте влияния элиминации и уменьшения продукции IS на замедление темпов ЦНД и КН у пациентов, получающих ПГД.
Продукт метаболизма тирозина р-крезол (молекулярная масса 108 Да) представляет собой еще один кишечный нейротоксин, индуцирующий апоптоз, окислительный стресс и нейровоспаление. PCS и р-крезол накапливаются в крови пациентов, получающих ПГД, и в высоких концентрациях негативно влияют на нейроглию [95, 96, 99, 105, 106, 108]. Учитывая тот факт, что кишечная микробиота является основным источником эндогенного p-крезола, баланс между штаммами кишечной микробиоты (особенно видами Clostridium) может напрямую влиять на нейропластичность и процессы ЦНД [49, 109].
В экспериментах выявлена связь между высокой концентрацией р-крезола и поведенческими нарушениями у животных. Так, в исследовании C.Y. Sun и соавт. [99] мышам с односторонней нефрэктомией (n=68) и интактным животным группы контроля (n=20) внутрибрюшинно вводили PCS в дозе 100 мг/кг в течение 7 нед. Введение PCS увеличило его концентрацию в тканях префронтальной коры, в то время как введение абсорбента уремического токсина уменьшало ее. Для оценки изменений в поведении были проведены следующие тесты: открытое поле (open field test), Водный лабиринт Морриса (Morris Water Maze), тест на принудительное плавание (forced swim test), тест на подвешивание хвоста (tail suspension test) и тест светлого/темного ящика (light/dark box test). После воздействия PCS у мышей с односторонней нефрэктомией по сравнению с группой контроля отмечалось накопление PCS в головном мозге и развивалось депрессивно-подобное и/или тревожно-подобное поведение. Выявлено также, что повышенные концентрации р-крезола увеличивали экспрессию и активность в тканях префронтальной коры целого ряда молекул (ИЛ-1β, JNK, р38, NF-kB, AP-1). Кроме этого, введение PCS приводило к снижению концентрации BDNF и серотонина. Авторы выявили связь между высокими и низкими концентрациями вышеуказанных молекул уремических токсинов, выживаемостью нейронов префронтальной коры, нейрогенезом и результатами нейропсихологического обследования.
Таким образом, в литературе приводятся данные о том, что именно клетки нейроглии головного мозга являются мишенями для негативного действия уремических токсинов [93, 99]. Вместе с тем публикаций, посвященных роли IS и PCS в развитии ЦНД и КН у пациентов, получающих ПГД, недостаточно. IS и PCS в будущем могут оказаться терапевтическими мишенями при нейродегенеративных заболеваниях у пациентов с ХБП. В связи с этим разработка и применение абсорбентов уремических токсинов могут оказаться перспективным научно-практическим направлением в аспекте сдерживания темпов ЦНД и КН у данной категории пациентов [97, 105, 110, 111], однако проверка этой научной гипотезы требует дальнейшего уточнения в клинических исследованиях.
Активация церебральной ренин-ангиотензин-альдостероновой системы как фактор развития церебральной нейродегенерации и когнитивных нарушений у пациентов, получающих программный гемодиализ
РААС представляет собой эндокринную систему, широко известную своей физиологической ролью в электролитном гомеостазе, регуляции системного сосудистого сопротивления и артериального давления [62, 112, 113]. Известно, что РААС функционирует не только в тканях почек, но и в других органах (в сердце, легких, печени, сетчатке и др.) [32, 112, 114]. Головной мозг также обладает собственной локальной тканевой РААС (церебральная РААС), которая через аутокринные, паракринные и другие внутримозговые механизмы может оказывать влияние на различные физиологические и патологические церебральные процессы независимо от системной РААС [115]. Составные компоненты церебральной РААС синтезируются локально в головном мозге [114]. Так, предшественник ангиотензина I в основном вырабатывается в астроцитах; ренин экспрессируется в нейронах и астроцитах; ангиотензинпревращающий фермент — в нейронах, астроцитах, олигодендроцитах и микроглии различных отделов головного мозга [112, 116].
Предполагается, что тканевой ангиотензин, вырабатываемый за пределами головного мозга, может взаимодействовать с рецепторами церебральной РААС после его проникновения в головной мозг в местах отсутствия ГЭБ (субфорникальном органе, медиальных отделах мозолистого тела, гиппокампе, миндалевидном теле) или при нарушении его целостности [62, 112, 114, 117]. Отдельные авторы отмечают, что чрезмерная активность церебральной РААС оказывает непосредственное влияние на нейроглию. Это воздействие осуществляется через ангиотензин II и активацию различных внутриклеточных и внеклеточных путей, что в свою очередь приводит к повышенной активации окислительного стресса, нейровоспалению, апоптозу и развитию ЦНД [112, 117]. В ряде клинических исследований [62, 112, 118] приводятся данные о наличии прямой связи между избыточной активацией рецепторов ангиотензина в головном мозге и КН. В доказательство этому сообщается о положительном влиянии на когнитивные функции антигипертензивной терапии антагонистами рецепторов ангиотензина II [62, 112, 119].
S.H. Kang и соавт. [120] оценивали 5-летнюю выживаемость пациентов из Южной Кореи (n=54 903), получавших ПГД и антигипертезивную терапию (при необходимости). Самые высокие показатели выживаемости отмечались у пациентов, которые не использовали антигипертензивные препараты. Среди лиц, нуждавшихся в назначении лекарственных средств, показатели выживаемости были выше у пациентов, получавших блокаторы РААС. Когнитивный статус пациентов в данном исследовании не изучался.
Следует отметить, что убедительные данные о влиянии церебральной РААС на развитие ЦНД и КН у пациентов, получающих ПГД, в настоящее время отсутствуют. Применение блокаторов церебральной РААС, например с помощью соответствующих антагонистов рецепторов ангиотензина II, можно считать еще одним перспективным направлением дальнейших клинических исследований с целью нейропротекции и снижения темпов ЦНД и КН у данной категории пациентов с сопутствующей артериальной гипертензией.
Заключение
Известно, что ХБП, в исходе которой зачастую необходимо проведение ПГД, представляет собой модель ускоренного старения, поэтому понимание механизмов развития ЦНД и КН у пациентов, получающих ПГД, представляется особенно значимым. Отдельное внимание в патогенезе ЦНД и КН на фоне проводимого ПГД уделяется механизмам и факторам, ассоциированным с активацией нейроглии, а именно: хроническому системному воспалению, персистирующему воздействию уремических токсинов и активации церебральной РААС.
Возможными научно-обоснованными направлениями дальнейших клинических исследований по данной проблеме можно считать разработку стратегий, уменьшающих системное воспаление и улучшающих цитокиновый профиль «диализного» пациента, применение ингибиторов белка S100B, способных преодолевать ГЭБ, а также использование абсорбентов уремических токсинов и ингибиторов церебральной РААС. Необходим дальнейший поиск терапевтических мишеней, управляемых современных стратегий и технологий, направленных на снижение темпов ЦНД и КН у пациентов, получающих ПГД. Научно-обоснованная разработка таких подходов возможна по мере накопления результатов клинических исследований, посвященных изучаемой проблеме и установлению клинической эффективности и безопасности предложенных терапевтических направлений.
Вклад авторов. А.Е. Хрулев — формулировка темы научной статьи, разработка концепции и дизайна статьи, обзор и критический анализ литературы, написание и редактирование текста статьи, супервизия, внесение окончательной правки; О.М. Чернова — разработка концепции, сбор материала, обзор и критический анализ литературы, написание текста статьи; В.Н. Григорьева — формулировка темы и редактирование текста научной статьи; Н.А. Шиянова — разработка концепции, сбор материала, обзор и критический анализ литературы, написание текста статьи; Н.С. Хрулева — формулировка темы и редактирование текста научной статьи; И.В. Мухина — формулировка темы и редактирование текста научной статьи.
Финансирование. Исследование не финансировалось какими-либо источниками.
Конфликт интересов отсутствует.
Литература
- Battaglia S., Avenanti A., Vécsei L., Tanaka M. Neurodegeneration in cognitive impairment and mood disorders for experimental, clinical and translational neuropsychiatry. Biomedicines 2024; 12(3): 574, https://doi.org/10.3390/biomedicines12030574.
- Клинические рекомендации «Когнитивные расстройства у лиц пожилого и старческого возраста». 2024. URL: https://cr.minzdrav.gov.ru/preview-cr/617_5.
- Bai W., Chen P., Cai H., Zhang Q., Su Z., Cheung T., Jackson T., Sha S., Xiang Y.T. Worldwide prevalence of mild cognitive impairment among community dwellers aged 50 years and older: a meta-analysis and systematic review of epidemiology studies. Age Ageing 2022; 51(8): afac173, https://doi.org/10.1093/ageing/afac173.
- Sakurai T., Sugimoto T., Akatsu H., Doi T., Fujiwara Y., Hirakawa A., Kinoshita F., Kuzuya M., Lee S., Matsumoto N., Matsuo K., Michikawa M., Nakamura A., Ogawa S., Otsuka R., Sato K., Shimada H., Suzuki H., Suzuki H., Takechi H., Takeda S., Uchida K., Umegaki H., Wakayama S., Arai H; J-MINT study group. Japan-multimodal intervention trial for the prevention of dementia: a randomized controlled trial. Alzheimers Dement 2024; 20(6): 3918–3930, https://doi.org/10.1002/alz.13838.
- Bushell D., Jones C., Moro C. The effectiveness of educational interventions in the community that aim to improve informal carers knowledge of dementia anatomy, physiology, progression, and impact on behavior: a systematic review. Front Dement 2023; 2: 1156863, https://doi.org/10.3389/frdem.2023.1156863.
- Старчина Ю.А. Недементные когнитивные нарушения: современный взгляд на проблему. Неврология, нейропсихиатрия, психосоматика 2017; 9(2): 71–76, https://doi.org/10.14412/2074-2711-2017-2-71–76.
- Ткачева О.Н., Котовская Ю.В., Бобкова И.Н., Шутов А.М., Виллевальде С.В., Ефремова Е.В., Рунихина Н.К., Ерусланова К.А., Арутюнов Г.П., Батюшин М.М., Фролова Е.В. Хроническая болезнь почек у пациентов пожилого и старческого возраста. Согласованное мнение экспертов Российской ассоциации геронтологов и гериатров, Научного общества нефрологов России и Евразийской ассоциации терапевтов. Российский журнал гериатрической медицины 2024; 1: 6–20, https://doi.org/10.37586/2686-8636-1-2024-6-20.
- International Society of Nephrology (ISN). ISN Global Kidney Health Atlas. 2023. URL: https://www.theisn.org/initiatives/global-kidney-health-atlas/.
- Клинические рекомендации «Хроническая болезнь почек (ХБП)». 2024. URL: https://cr.minzdrav.gov.ru/preview-cr/469_3.
- Андрусев А.М., Перегудова Н.Г., Шинкарев М.Б., Томилина Н.А. Заместительная почечная терапия хронической болезни почек 5 стадии в Российской Федерации 2016–2020 гг. Краткий отчет по данным Общероссийского Регистра заместительной почечной терапии Российского диализного общества. Нефрология и диализ 2022; 24(4): 555–565, https://doi.org/10.28996/2618-9801-2022-4-555-565.
- Arnold R., Issar T., Krishnan A.V., Pussell B.A. Neurological complications in chronic kidney disease. JRSM Cardiovasc Dis 2016; 5: 2048004016677687, https://doi.org/10.1177/2048004016677687.
- Хрулев А.Е., Толбузова Д.Д., Плохенко Е.А., Егорова П.А., Сорокоумова С.Н., Суворова О.В., Янкевич Д.С. Когнитивный статус и факторы риска когнитивных нарушений у диализных пациентов. Общая реаниматология 2020; 16(4): 21–31, https://doi.org/10.15360/1813-9779-2020-4-21-31.
- Смакотина С.А., Боханов Ю.А., Фомина Н.В. Показатели нейродинамики и внимания у пациентов с терминальной стадией хронической болезни почек. Влияние процедуры гемодиализа. Нефрология 2020; 24(4): 67–72, https://doi.org/10.36485/1561-6274-2020-24-4-67-72.
- Karakizlis H., Bohl K., Ziemek J., Dodel R., Hoyer J. Assessment of cognitive impairment and related risk factors in hemodialysis patients. J Nephrol 2022; 35(3): 931–942, https://doi.org/10.1007/s40620-021-01170-3.
- Park B.S., Lee H.W., Lee Y.J., Park S., Kim Y.W., Kim S.E., Kim I.H., Park J.H., Park K.M. Serum S100B represents a biomarker for cognitive impairment in patients with end-stage renal disease. Clin Neurol Neurosurg 2020; 195: 105902, https://doi.org/10.1016/j.clineuro.2020.105902.
- Natale G., Calabrese V., Marino G., Campanelli F., Urciuolo F., de Iure A., Ghiglieri V., Calabresi P., Bossola M., Picconi B. Effects of uremic toxins on hippocampal synaptic transmission: implication for neurodegeneration in chronic kidney disease. Cell Death Discov 2021; 7(1): 295, https://doi.org/10.1038/s41420-021-00685-9.
- Hamed S.A. Neurologic conditions and disorders of uremic syndrome of chronic kidney disease: presentations, causes, and treatment strategies. Expert Rev Clin Pharmacol 2019; 12(1): 61–90, https://doi.org/10.1080/17512433.2019.1555468.
- Michna M., Kovarova L., Valerianova A., Malikova H., Weichet J., Malik J. Review of the structural and functional brain changes associated with chronic kidney disease. Physiol Res 2020; 69(6): 1013–1028, https://doi.org/10.33549/physiolres.934420.
- Pei X., Bakerally N.B., Wang Z., Bo Y., Ma Y., Yong Z., Zhu S., Gao F., Bei Z., Zhao W. Kidney function and cognitive impairment: a systematic review and meta-analysis. Ren Fail 2025; 47(1): 2463565, https://doi.org/10.1080/0886022X.2025.2463565.
- Хрулев А.Е., Студяникова С.Ф., Лангран С.В., Садырин Р.В., Григорьева В.Н. Когнитивные нарушения у пациентов, находящихся на программном гемодиализе. Неврологический вестник 2019; 51(2): 36–40.
- Olczyk P., Kusztal M., Gołębiowski T., Letachowicz K., Krajewska M. Cognitive impairment in end stage renal disease patients undergoing hemodialysis: markers and risk factors. Int J Environ Res Public Health 2022; 19(4): 2389, https://doi.org/10.3390/ijerph19042389.
- Юсупов Ф.А., Юлдашев А.А., Юсупов А.Ф., Ормонова Г.М., Абдыкадыров М.Ш. Неврологические расстройства при хронической болезни почек. The Scientific Heritage 2022; 84(2): 51–61.
- Adesso S., Magnus T., Cuzzocrea S., Campolo M., Rissiek B., Paciello O., Autore G., Pinto A., Marzocco S. Indoxyl sulfate affects glial function increasing oxidative stress and neuroinflammation in chronic kidney disease: interaction between astrocytes and microglia. Front Pharmacol 2017; 8: 370, https://doi.org/10.3389/fphar.2017.00370.
- Хачатрян А.А., Ерофеева Л.М., Кутвицкая С.А. Роль нейроглии в функционировании нервной системы. Успехи современного естествознания 2014; 6: 66–70.
- Huang J., Li C., Shang H. Astrocytes in neurodegeneration: inspiration from genetics. Front Neurosci 2022; 16: 882316, https://doi.org/10.3389/fnins.2022.882316.
- Hickman S., Izzy S., Sen P., Morsett L., El Khoury J. Microglia in neurodegeneration. Nat Neurosci 2018; 21(10): 1359–1369, https://doi.org/10.1038/s41593-018-0242-x.
- Augusto-Oliveira M., Arrifano G.P., Lopes-Araújo A., Santos-Sacramento L., Takeda P.Y., Anthony D.C., Malva J.O., Crespo-Lopez M.E. What do microglia really do in healthy adult brain? Cells 2019; 8(10): 1293, https://doi.org/10.3390/cells8101293.
- Gotoh M., Miyamoto Y., Ikeshima-Kataoka H. Astrocytic neuroimmunological roles interacting with microglial cells in neurodegenerative diseases. Int J Mol Sci 2023; 24(2): 1599, https://doi.org/10.3390/ijms24021599.
- Mendiola A.S., Yan Z., Dixit K., Johnson J.R., Bouhaddou M., Meyer-Franke A., Shin M.G., Yong Y., Agrawal A., MacDonald E., Muthukumar G., Pearce C., Arun N., Cabriga B., Meza-Acevedo R., Alzamora M.D.P.S., Zamvil S.S., Pico A.R., Ryu J.K., Krogan N.J., Akassoglou K. Defining blood-induced microglia functions in neurodegeneration through multiomic profiling. Nat Immunol 2023; 24(7): 1173–1187, https://doi.org/10.1038/s41590-023-01522-0.
- Mohamed W., Kumar J., Alghamdi B.S., Soliman A.H., Toshihide Y. Neurodegeneration and inflammation crosstalk: therapeutic targets and perspectives. IBRO Neurosci Rep 2022; 14: 95–110, https://doi.org/10.1016/j.ibneur.2022.12.003.
- Verkhratsky A., Ho M.S., Zorec R., Parpura V. The concept of neuroglia. Adv Exp Med Biol 2019; 1175: 1–13, https://doi.org/10.1007/978-981-13-9913-8_1.
- Бонь Е.И., Максимович Н.Е., Малыхина А.В. Нейроглия и ее роль в патогенезе ишемического повреждения головного мозга. Иммуногистохимические маркеры нейроглии. Вестник Смоленской государственной медицинской академии 2021; 20(3): 18–24, https://doi.org/10.37903/vsgma.2021.3.3.
- Al-Onaizi M., Al-Khalifah A., Qasem D., ElAli A. Role of microglia in modulating adult neurogenesis in health and neurodegeneration. Int J Mol Sci 2020; 21(18): 6875, https://doi.org/10.3390/ijms21186875.
- Reyes-Haro D., López-Juárez A., Rodríguez-Contreras A. Editorial: Physiology and pathology of neuroglia. Front Cell Neurosci 2023; 17: 1246885, https://doi.org/10.3389/fncel.2023.1246885.
- Патлай Н.И., Сотников Е.Б., Тучина О.П. Роль микроглиальных цитокинов в модуляции нейрогенеза во взрослом мозге. Международный журнал прикладных и фундаментальных исследований 2020; 5: 15–23, https://doi.org/10.17513/mjpfi.13062.
- Malinovskaya N.A., Frolova O.V., Shishelova K.O., Panina Yu.A. Current methods for the isolation and cultivation of microglia (review). Sovremennye tehnologii v medicine 2021; 13(6): 89, https://doi.org/10.17691/stm2021.13.6.10.
- Li D., Wu M. Pattern recognition receptors in health and diseases. Signal Transduct Target Ther 2021; 6(1): 291, https://doi.org/10.1038/s41392-021-00687-0.
- Amarante-Mendes G.P., Adjemian S., Branco L.M., Zanetti L.C., Weinlich R., Bortoluci K.R. Pattern recognition receptors and the host cell death molecular machinery. Front Immunol 2018; 9: 2379, https://doi.org/10.3389/fimmu.2018.02379.
- Jin M.M., Wang F., Qi D., Liu W.W., Gu C., Mao C.J., Yang Y.P., Zhao Z., Hu L.F., Liu C.F. A critical role of autophagy in regulating microglia polarization in neurodegeneration. Front Aging Neurosci 2018; 10: 378, https://doi.org/10.3389/fnagi.2018.00378.
- Mata-Martínez E., Díaz-Muñoz M., Vázquez-Cuevas F.G. Glial cells and brain diseases: inflammasomes as relevant pathological entities. Front Cell Neurosci 2022; 16: 929529, https://doi.org/10.3389/fncel.2022.929529.
- Lee J.W., Chun W., Lee H.J., Kim S.M., Min J.H., Kim D.Y., Kim M.O., Ryu H.W., Lee S.U. The role of microglia in the development of neurodegenerative diseases. Biomedicines 2021; 9(10): 1449, https://doi.org/10.3390/biomedicines9101449.
- Stoklund Dittlau K., Freude K. Astrocytes: the stars in neurodegeneration? Biomolecules 2024; 14(3): 289, https://doi.org/10.3390/biom14030289.
- Tienda-Vazquez M.A., Arredondo P., Mejía-Delgadillo X., Rodríguez-González J.A., Soto-Cajiga J.A., Sabath E., Lozano O., Almanza-Arjona Y.C. Biological testing unification for hemodialysis membranes evaluation: a step towards standardization. Biomater Adv 2025; 169: 214165, https://doi.org/10.1016/j.bioadv.2024.214165.
- Строков А.Г., Гуревич К.Я., Ильин А.П., Денисов А.Ю., Земченков А.Ю., Андрусев А.М., Шутов Е.В., Котенко О.Н., Злоказов В.Б. Лечение пациентов с хронической болезнью почек 5 стадии (ХБП 5) методами гемодиализа и гемодиафильтрации. клинические рекомендации. Нефрология 2017; 21(3): 92–111, https://doi.org/10.24884/1561-6274-2017-3-92-111.
- Chen Y.A., Ou S.M., Lin C.C. Influence of dialysis membranes on clinical outcomes: from history to innovation. Membranes (Basel) 2022; 12(2): 152, https://doi.org/10.3390/membranes12020152.
- Строков А.Г., Поз Я.Л. Высокая проницаемость мембран для гемодиализа: плюсы и минусы. Вестник трансплантологии и искусственных органов 2018; 20(4): 100–106, https://doi.org/10.15825/1995-1191-2018-4-100-106.
- Abdelrasoul A., Westphalen H., Saadati S., Shoker A. Hemodialysis biocompatibility mathematical models to predict the inflammatory biomarkers released in dialysis patients based on hemodialysis membrane characteristics and clinical practices. Sci Rep 2021; 11(1): 23080, https://doi.org/10.1038/s41598-021-01660-1.
- Pénzes K., Hurják B., Katona É., Becs G., Balla J., Muszbek L. Terminal phase components of the clotting cascade in patients with end-stage renal disease undergoing hemodiafiltration or hemodialysis treatment. Int J Mol Sci 2020; 21(22): 8426, https://doi.org/10.3390/ijms21228426.
- Belova I.V., Khrulev A.E., Tochilina A.G., Khruleva N.S., Lobanova N.A., Zhirnov V.A., Molodtsova S.B., Lobanov V.N., Solovieva I.V. Colon microbiocenosis and its correction in patients receiving programmed hemodialysis. Sovremennye tehnologii v medicine 2021; 12(5): 62–68, https://doi.org/10.17691/stm2020.12.5.07.
- Rapa S.F., Di Iorio B.R., Campiglia P., Heidland A., Marzocco S. Inflammation and oxidative stress in chronic kidney disease-potential therapeutic role of minerals, vitamins and plant-derived metabolites. Int J Mol Sci 2019; 21(1): 263, https://doi.org/10.3390/ijms21010263.
- Supriyadi R., Rakhmawati Kurniaatmaja E., Huang I., Sukesi L., Makmun A. The effect of superoxide dismutase supplementation on TNF-α and TGF-β levels in patients undergoing hemodialysis. Eur Rev Med Pharmacol Sci 2023; 27(3): 893–898, https://doi.org/10.26355/eurrev_202302_31182.
- Kunz M., Ceresér K.M., Goi P.D., Fries G.R., Teixeira A.L., Fernandes B.S., Belmonte-de-Abreu P.S., Kauer-Sant'Anna M., Kapczinski F., Gama C.S. Serum levels of IL-6, IL-10 and TNF-α in patients with bipolar disorder and schizophrenia: differences in pro- and anti-inflammatory balance. Braz J Psychiatry 2011; 33(3): 268–274, https://doi.org/10.1590/s1516-44462011000300010.
- Айтбаев К.А., Муркамилов И.Т., Фомин В.В., Муркамилова Ж.А., Райимжанов З.Р., Юсупов Ф.А., Айдаров З.А. Воспаление при хронической болезни почек: источники, последствия и противовоспалительная терапия. Клиническая медицина 2018; 96(4): 314–320, https://doi.org/10.18821/0023-2149-2018-96-4-314-320.
- Al-Hakeim H.K., Twaij B.A.A., Al-Naqeeb T.H., Moustafa S.R., Maes M. Neuronal damage and inflammatory biomarkers are associated with the affective and chronic fatigue-like symptoms due to end-stage renal disease. J Affect Disord 2024; 347: 220–229, https://doi.org/10.1016/j.jad.2023.11.078.
- Angelopoulou E., Paudel Y.N., Piperi C. Emerging role of S100B protein implication in Parkinson's disease pathogenesis. Cell Mol Life Sci 2021; 78(4): 1445–1453, https://doi.org/10.1007/s00018-020-03673-x.
- Hernández-Ortega K., Canul-Euan A.A., Solis-Paredes J.M., Borboa-Olivares H., Reyes-Muñoz E., Estrada-Gutierrez G., Camacho-Arroyo I. S100B actions on glial and neuronal cells in the developing brain: an overview. Front Neurosci 2024; 18: 1425525, https://doi.org/10.3389/fnins.2024.1425525.
- Michetti F., Clementi M.E., Di Liddo R., Valeriani F., Ria F., Rende M., Di Sante G., Romano Spica V. The S100B protein: a multifaceted pathogenic factor more than a biomarker. Int J Mol Sci 2023; 24(11): 9605, https://doi.org/10.3390/ijms24119605.
- Маркелова Е.В., Зенина А.А., Кадыров Р.В. Нейропептиды как маркеры повреждения головного мозга. Современные проблемы науки и образования 2018; 5: 206.
- Фомина Н.В., Егорова М.В., Смакотина С.А., Квиткова Л.В. Белок S100B, нейронспецифичная енолаза и когнитивная дисфункция у пациентов с хронической болезнью почек. Нефрология 2019; 23(4): 73–79, https://doi.org/10.24884/1561-6274-2019-23-4-73-79.
- Bossola M., Picca A., Marzetti E., Pepe G., Antocicco M., Di Stasio E. Post-dialysis fatigue and serum S100B protein in patients on chronic hemodialysis. A pilot study. Ther Apher Dial 2023; 27(3): 471–479, https://doi.org/10.1111/1744-9987.13944.
- Barros C., Barateiro A., Neto A., Soromenho B., Basto A.P., Mateus J.M., Xapelli S., Sebastião A.M., Brites D., Graça L., Fernandes A. S100B inhibition protects from chronic experimental autoimmune encephalomyelitis. Brain Commun 2022; 4(3): fcac076, https://doi.org/10.1093/braincomms/fcac076.
- Stanciu G.D., Ababei D.C., Bild V., Bild W., Paduraru L., Gutu M.M., Tamba B.I. Renal contributions in the pathophysiology and neuropathological substrates shared by chronic kidney disease and Alzheimer's disease. Brain Sci 2020; 10(8): 563, https://doi.org/10.3390/brainsci10080563.
- Gryka-Marton M., Grabowska A.D., Szukiewicz D. Breaking the barrier: the role of proinflammatory cytokines in BBB dysfunction. Int J Mol Sci 2025; 26(8): 3532, https://doi.org/10.3390/ijms26083532.
- Perna A.F., Russo L., D'Esposito V., Formisano P., Bruzzese D., Vigorito C., Coppola A., Lombari P., Russo D., Ingrosso D. Lanthionine, a novel uremic toxin, in the vascular calcification of chronic kidney disease: the role of proinflammatory cytokines. Int J Mol Sci 2021; 22(13): 6875, https://doi.org/10.3390/ijms22136875.
- Zhu B., Jin L.N., Shen J.Q., Liu J.F., Jiang R.Y., Yang L., Zhang J., Luo A.L., Miao L.Y., Yang C. Differential expression of serum biomarkers in hemodialysis patients with mild cognitive decline: a prospective single-center cohort study. Sci Rep 2018; 8(1): 12250, https://doi.org/10.1038/s41598-018-29760-5.
- Hernandez L., Ward L.J., Arefin S., Ebert T., Laucyte-Cibulskiene A; GOING-FWD Collaborators; Heimbürger O., Barany P., Wennberg L., Stenvinkel P., Kublickiene K. Blood-brain barrier and gut barrier dysfunction in chronic kidney disease with a focus on circulating biomarkers and tight junction proteins. Sci Rep 2022; 12(1): 4414, https://doi.org/10.1038/s41598-022-08387-7.
- Vafadar-Afshar G., Rasmi Y., Yaghmaei P., Khadem-Ansari M.H., Makhdoomi K., Rasouli J. The effects of nanocurcumin supplementation on inflammation in hemodialysis patients: a randomized controlled trial. Hemodial Int 2021; 25(2): 232–239, https://doi.org/10.1111/hdi.12911.
- Lindblad C., Rostami E., Helmy A. Interleukin-1 receptor antagonist as therapy for traumatic brain injury. Neurotherapeutics 2023; 20(6): 1508–1528, https://doi.org/10.1007/s13311-023-01421-0.
- Mendiola A.S., Cardona A.E. The IL-1β phenomena in neuroinflammatory diseases. J Neural Transm (Vienna) 2018; 125(5): 781–795, https://doi.org/10.1007/s00702-017-1732-9.
- Liu X., Quan N. Microglia and CNS interleukin-1: beyond immunological concepts. Front Neurol 2018; 9: 8, https://doi.org/10.3389/fneur.2018.00008.
- Skelly D.T., Griffin É.W., Murray C.L., Harney S., O'Boyle C., Hennessy E., Dansereau M.A., Nazmi A., Tortorelli L., Rawlins J.N., Bannerman D.M., Cunningham C. Acute transient cognitive dysfunction and acute brain injury induced by systemic inflammation occur by dissociable IL-1-dependent mechanisms. Mol Psychiatry 2019; 24(10): 1533–1548, https://doi.org/10.1038/s41380-018-0075-8.
- Armada-Moreira A., Gomes J.I., Pina C.C., Savchak O.K., Gonçalves-Ribeiro J., Rei N., Pinto S., Morais T.P., Martins R.S., Ribeiro F.F., Sebastião A.M., Crunelli V., Vaz S.H. Going the extra (synaptic) mile: excitotoxicity as the road toward neurodegenerative diseases. Front Cell Neurosci 2020; 14: 90, https://doi.org/10.3389/fncel.2020.00090.
- Boraschi D., Italiani P., Migliorini P., Bossù P. Cause or consequence? The role of IL-1 family cytokines and receptors in neuroinflammatory and neurodegenerative diseases. Front Immunol 2023; 14: 1128190, https://doi.org/10.3389/fimmu.2023.1128190.
- Retinasamy T., Shaikh M.F. Interleukin 1 receptor antagonist and neurodegenerative diseases: the future treatment strategy. Neurosci Res Notes 2023; 6(1): 164, https://doi.org/10.31117/neuroscirn.v6i1.164.
- Dember L.M., Hung A., Mehrotra R., Hsu J.Y., Raj D.S., Charytan D.M., Mc Causland F.R., Regunathan-Shenk R., Landis J.R., Kimmel P.L., Kliger A.S., Himmelfarb J., Ikizler T.A.; Hemodialysis Novel Therapies Consortium. A randomized controlled pilot trial of anakinra for hemodialysis inflammation. Kidney Int 2022; 102(5): 1178–1187, https://doi.org/10.1016/j.kint.2022.06.022.
- Recasens M., Almolda B., Pérez-Clausell J., Campbell I.L., González B., Castellano B. Chronic exposure to IL-6 induces a desensitized phenotype of the microglia. J Neuroinflammation 2021; 18(1): 31, https://doi.org/10.1186/s12974-020-02063-1.
- Kerkis I., da Silva Á.P., Araldi R.P. The impact of interleukin-6 (IL-6) and mesenchymal stem cell-derived IL-6 on neurological conditions. Front Immunol 2024; 15: 1400533, https://doi.org/10.3389/fimmu.2024.1400533.
- Rose-John S., Jenkins B.J., Garbers C., Moll J.M., Scheller J. Targeting IL-6 trans-signalling: past, present and future prospects. Nat Rev Immunol 2023; 23(10): 666–681, https://doi.org/10.1038/s41577-023-00856-y.
- Chertow G.M., Chang A.M., Felker G.M., Heise M., Velkoska E., Fellström B., Charytan D.M., Clementi R., Gibson C.M., Goodman S.G., Jardine M., Levin A., Lokhnygina Y., Mears J., Mehran R., Stenvinkel P., Wang A.Y., Wheeler D.C., Zoccali C., Ridker P.M., Mahaffey K.W., Tricoci P., Wolf M. IL-6 inhibition with clazakizumab in patients receiving maintenance dialysis: a randomized phase 2b trial. Nat Med 2024; 30(8): 2328–2336, https://doi.org/10.1038/s41591-024-03043-1.
- Воронина Е.В., Лобанова Н.В., Яхин И.Р., Романова Н.А., Серегин Ю.А. Роль фактора некроза опухолей-альфа в иммунопатогенезе заболеваний различной этиологии и его значимость в развитии антицитокиновой терапии моноклональными антителами. Медицинская иммунология 2018; 20(6): 797–806, https://doi.org/10.15789/1563-0625-2018-6-797-806.
- Sasidharakurup H., Diwakar S. Computational modelling of TNFα related pathways regulated by neuroinflammation, oxidative stress and insulin resistance in neurodegeneration. Appl Netw Sci 2020; 5(1): 72, https://doi.org/10.1007/s41109-020-00307-w.
- Samy A.E., Elrahman A.A.M., El Shafei M., Adel A.O., Ahmed S.I. The relation between the level of serum tumor necrosis factor-alpha and hemodialysis adequacy in diabetic and non diabetic patients on maintenance hemodialysis. Urol Nephrol Open Access J 2016; 3(2): 60–65.
- Kantor A.B., Akassoglou K., Stavenhagen J.B. Fibrin-targeting immunotherapy for dementia. J Prev Alzheimers Dis 2023; 10(4): 647–660, https://doi.org/10.14283/jpad.2023.105.
- Pluvinage J.V., Wyss-Coray T. Systemic factors as mediators of brain homeostasis, ageing and neurodegeneration. Nat Rev Neurosci 2020; 21(2): 93–102, https://doi.org/10.1038/s41583-019-0255-9.
- Petersen M.A., Ryu J.K., Akassoglou K. Fibrinogen in neurological diseases: mechanisms, imaging and therapeutics. Nat Rev Neurosci 2018; 19(5): 283–301, https://doi.org/10.1038/nrn.2018.13.
- Wen T., Zhang Z. Cellular mechanisms of fibrin (ogen): insight from neurodegenerative diseases. Front Neurosci 2023; 17: 1197094, https://doi.org/10.3389/fnins.2023.1197094.
- Sulimai N., Brown J., Lominadze D. The role of fibrinogen in neurodegeneration during a neuroinflammatory disease. Alzheimer's Dement 2023; 19(S17): e075879, https://doi.org/10.1002/alz.075879.
- Fan D.Y., Sun H.L., Sun P.Y., Jian J.M., Li W.W., Shen Y.Y., Zeng F., Wang Y.J., Bu X.L. The correlations between plasma fibrinogen with amyloid-beta and tau levels in patients with Alzheimer's disease. Front Neurosci 2021; 14: 625844, https://doi.org/10.3389/fnins.2020.625844.
- Pyun J.M., Ryoo N., Park Y.H., Kim S. Fibrinogen levels and cognitive profile differences in patients with mild cognitive impairment. Dement Geriatr Cogn Disord 2020; 49(5): 489–496, https://doi.org/10.1159/000510420.
- Seidel U.K., Gronewold J., Volsek M., Todica O., Kribben A., Bruck H., Hermann D.M. The prevalence, severity, and association with HbA1c and fibrinogen of cognitive impairment in chronic kidney disease. Kidney Int 2014; 85(3): 693–702, https://doi.org/10.1038/ki.2013.366.
- Tampubolon G. Repeated systemic inflammation was associated with cognitive deficits in older Britons. Alzheimers Dement (Amst) 2015; 3: 1–6, https://doi.org/10.1016/j.dadm.2015.11.009.
- Pedersen A., Stanne T.M., Redfors P., Viken J., Samuelsson H., Nilsson S., Jood K., Jern C. Fibrinogen concentrations predict long-term cognitive outcome in young ischemic stroke patients. Res Pract Thromb Haemost 2018; 2(2): 339–346, https://doi.org/10.1002/rth2.12078.
- Lin Y.T., Wu P.H., Liang S.S., Mubanga M., Yang Y.H., Hsu Y.L., Kuo M.C., Hwang S.J., Kuo P.L. Protein-bound uremic toxins are associated with cognitive function among patients undergoing maintenance hemodialysis. Sci Rep 2019; 9(1): 20388, https://doi.org/10.1038/s41598-019-57004-7.
- Liabeuf S., Pepin M., Franssen C.F.M., Viggiano D., Carriazo S., Gansevoort R.T., Gesualdo L., Hafez G., Malyszko J., Mayer C., Nitsch D., Ortiz A., Pešić V., Wiecek A., Massy Z.A.; CONNECT Action (Cognitive Decline in Nephro-Neurology European Cooperative Target). Chronic kidney disease and neurological disorders: are uraemic toxins the missing piece of the puzzle? Nephrol Dial Transplant 2021; 37(Suppl 2): ii33–ii44, https://doi.org/10.1093/ndt/gfab223.
- Connell E., Le Gall G., Pontifex M.G., Sami S., Cryan J.F., Clarke G., Müller M., Vauzour D. Microbial-derived metabolites as a risk factor of age-related cognitive decline and dementia. Mol Neurodegener 2022; 17(1): 43, https://doi.org/10.1186/s13024-022-00548-6.
- Falconi C.A., Junho C.V.D.C., Fogaça-Ruiz F., Vernier I.C.S., da Cunha R.S., Stinghen A.E.M., Carneiro-Ramos M.S. Uremic toxins: an alarming danger concerning the cardiovascular system. Front Physiol 2021; 12: 686249, https://doi.org/10.3389/fphys.2021.686249.
- Xu Y., Bi W.D., Shi Y.X., Liang X.R., Wang H.Y., Lai X.L., Bian X.L., Guo Z.Y. Derivation and elimination of uremic toxins from kidney-gut axis. Front Physiol 2023; 14: 1123182, https://doi.org/10.3389/fphys.2023.1123182.
- Swer N.M., Venkidesh B.S., Murali T.S., Mumbrekar K.D. Gut microbiota-derived metabolites and their importance in neurological disorders. Mol Biol Rep 2023; 50(2): 1663–1675, https://doi.org/10.1007/s11033-022-08038-0.
- Sun C.Y., Li J.R., Wang Y.Y., Lin S.Y., Ou Y.C., Lin C.J., Wang J.D., Liao S.L., Chen C.J. p-Cresol sulfate caused behavior disorders and neurodegeneration in mice with unilateral nephrectomy involving oxidative stress and neuroinflammation. Int J Mol Sci 2020; 21(18): 6687, https://doi.org/10.3390/ijms21186687.
- Bobot M. Cognitive impairment and the blood-brain barrier in chronic kidney disease: role of the uremic toxins. Nephrol Ther 2023; 19(7): 607–615, https://doi.org/10.1684/ndt.2023.51.
- Bobot M., Thomas L., Moyon A., Fernandez S., McKay N., Balasse L., Garrigue P., Brige P., Chopinet S., Poitevin S., Cérini C., Brunet P., Dignat-George F., Burtey S., Guillet B., Hache G. Uremic toxic blood-brain barrier disruption mediated by AhR activation leads to cognitive impairment during experimental renal dysfunction. J Am Soc Nephrol 2020; 31(7): 1509–1521, https://doi.org/10.1681/ASN.2019070728.
- Faucher Q., van der Made T.K., De Lange E., Masereeuw R. Blood-brain barrier perturbations by uremic toxins: key contributors in chronic kidney disease-induced neurological disorders? Eur J Pharm Sci 2023; 187: 106462, https://doi.org/10.1016/j.ejps.2023.106462.
- Sankowski B., Księżarczyk K., Raćkowska E., Szlufik S., Koziorowski D., Giebułtowicz J. Higher cerebrospinal fluid to plasma ratio of p-cresol sulfate and indoxyl sulfate in patients with Parkinson's disease. Clin Chim Acta 2020; 501: 165–173, https://doi.org/10.1016/j.cca.2019.10.038.
- Brito J.S., Borges N.A., Anjos J.S.D., Nakao L.S., Stockler-Pinto M.B., Paiva B.R., Cardoso-Weide L.C., Cardozo L.F.M.F., Mafra D. Aryl hydrocarbon receptor and uremic toxins from the gut microbiota in chronic kidney disease patients: is there a relationship between them? Biochemistry 2019; 58(15): 2054–2060, https://doi.org/10.1021/acs.biochem.8b01305.
- Laville S.M., Massy Z.A., Kamel S., Chillon J.M., Choukroun G., Liabeuf S. Intestinal chelators, sorbants, and gut-derived uremic toxins. Toxins (Basel) 2021; 13(2): 91, https://doi.org/10.3390/toxins13020091.
- Deltombe O., Van Biesen W., Glorieux G., Massy Z., Dhondt A., Eloot S. Exploring protein binding of uremic toxins in patients with different stages of chronic kidney disease and during hemodialysis. Toxins (Basel) 2015; 7(10): 3933–3946, https://doi.org/10.3390/toxins7103933.
- Lin Y.T., Wu P.H., Tsai Y.C., Hsu Y.L., Wang H.Y., Kuo M.C., Kuo P.L., Hwang S.J. Indoxyl sulfate induces apoptosis through oxidative stress and mitogen-activated protein kinase signaling pathway inhibition in human astrocytes. J Clin Med 2019; 8(2): 191, https://doi.org/10.3390/jcm8020191.
- Davoli-Ferreira M., Thomson C.A., McCoy K.D. Microbiota and microglia interactions in ASD. Front Immunol 2021; 12: 676255, https://doi.org/10.3389/fimmu.2021.676255.
- Tevzadze G., Barbakadze T., Kvergelidze E., Zhuravliova E., Shanshiashvili L., Mikeladze D. Gut neurotoxin p-cresol induces brain-derived neurotrophic factor secretion and increases the expression of neurofilament subunits in PC-12 cells. AIMS Neurosci 2021; 9(1): 12–23, https://doi.org/10.3934/Neuroscience.2022002.
- Лукичев Б.Г., Стрелко В.В., Мосикян А.А., Трихлеб В.А. Современное состояние вопроса об использовании энтеросорбции при хронической болезни почек. Нефрология 2014; 18(6): 43–50.
- Айтбаев К.А., Муркамилов И.Т., Калиев Р.Р. Хроническая болезнь почек: патофизиологическая роль дисбиоза кишечника и ренопротективная эффективность вмешательств по его модуляции. Российский медицинский журнал 2016; 22(3): 157–162, https://doi.org/10.18821/0869-2106-2016-22-4-157-162.
- Abiodun O.A., Ola M.S. Role of brain renin angiotensin system in neurodegeneration: an update. Saudi J Biol Sci 2020; 27(3): 905–912, https://doi.org/10.1016/j.sjbs.2020.01.026.
- Карлович Н.В., Мохорт Т.В., Волчек Ю.А. Ренин-ангиотензин-альдостероновая система: традиционная функция и плейотропные эффекты регуляции фосфорно-кальциевого метаболизма. Медицинские новости 2021; 10: 22–26.
- Cruz-López E.O., Uijl E., Danser A.H.J. Fifty years of research on the brain renin-angiotensin system: what have we learned? Clin Sci (Lond) 2021; 135(14): 1727–1731, https://doi.org/10.1042/CS20210579.
- Villapol S., Janatpour Z.C., Affram K.O., Symes A.J. The renin angiotensin system as a therapeutic target in traumatic brain injury. Neurotherapeutics 2023; 20(6): 1565–1591, https://doi.org/10.1007/s13311-023-01435-8.
- Labandeira-Garcia J.L., Rodríguez-Perez A.I., Garrido-Gil P., Rodriguez-Pallares J., Lanciego J.L., Guerra M.J. Brain renin-angiotensin system and microglial polarization: implications for aging and neurodegeneration. Front Aging Neurosci 2017; 9: 129, https://doi.org/10.3389/fnagi.2017.00129.
- Gouveia F., Camins A., Ettcheto M., Bicker J., Falcão A., Cruz M.T., Fortuna A. Targeting brain renin-angiotensin system for the prevention and treatment of Alzheimer's disease: past, present and future. Ageing Res Rev 2022; 77: 101612, https://doi.org/10.1016/j.arr.2022.101612.
- Singh K.D., Karnik S.S. Angiotensin receptors: structure, function, signaling and clinical applications. J Cell Signal (Los Angel) 2016; 1(2): 111, https://doi.org/10.4172/2576-1471.1000111.
- Мусина Н.С., Семенова Р.И., Сейдуманов М.Т., Куразов Б.Р. Эффективность применения антигипертензивной терапии у пациентов, находящихся на гемодиализе. Вестник Казахского Национального медицинского университета 2015; 1: 255–256.
- Kang S.H., Kim B.Y., Son E.J., Kim G.O., Do J.Y. Association of renin-angiotensin system blockers with survival in patients on maintenance hemodialysis. J Clin Med 2023; 12(9): 3301, https://doi.org/10.3390/jcm12093301.