Оценка функциональной пригодности радиоиммуноконъюгатов наноантител против PD-L1 и HER2/neu для тераностики опухолей
Цель исследования — оценить возможность использования радиоиммуноконъюгатов (РИК) наноантител против PD-L1 и HER2/neu для диагностики и терапии злокачественных опухолей.
Материалы и методы. Наноантитела к биомаркерам человека PD-L1 и HER2/neu конъюгировали с радионуклидами 68Ga и 177Lu с использованием хелатирующего агента DOTA. Биораспределение РИК исследовали в экспериментальных моделях на мышах F1(DBA/2xBALB/c), которым прививали генно-модифицированные клетки мышиной карциномы CT26, экспрессирующие PD-L1 или HER2/neu человека. РИК, содержащие изотоп 68Ga и предназначенные для выявления опухолей, вводили животным внутривенно в дозе 1,0–1,2 МБк. Накопление радиоактивности в специфических опухолях, несущих биомаркеры человека, оценивали методом прямой дозиметрии через 0,5, 1,5 и 4 ч в сравнении с контрольными опухолями. Для терапии использовали РИК, содержащие 177Lu, которые вводили в дозе 0,8–1,6 МБк и исследовали аналогично в течение 96 ч после введения.
Результаты. После введения мышам РИК, содержащих 68Ga, наибольшую разницу между специфическими и контрольными опухолями наблюдали на сроке 1,5 ч. В это же время отмечалось многократное превышение радиоактивности специфической опухоли над радиоактивностью крови и мышечной ткани, что должно обеспечивать высокую контрастность визуализации. После введения мышам РИК, содержащих 177Lu, радиоактивность в специфических опухолях сохранялась в течение 48 ч, что создавало длительное воздействие радиоизотопа на опухоль. При введении всех РИК происходила быстрая элиминация радиоактивности из крови через мочу, что было связано с использованием наноантител, имеющих молекулярную массу 13 кДа и не содержащих участков взаимодействия с Fc-рецепторами. Отмечено значительное накопление и длительное сохранение радиоактивности в почках. В работе была выявлена зависимость биораспределения радиоактивности от использованного изотопа: нормализованная по времени радиоактивность ряда органов и тканей, включая опухоли, после введения РИК, содержащих 68Ga, была выше, чем после введения РИК той же специфичности, но содержащих радиоизотопы 177Lu.
Заключение. Результаты исследования указывают на функциональную пригодность пар РИК наноантител с радиоизотопами 68Ga и 177Lu для тераностики злокачественных опухолей, экспрессирующих биомаркеры PD-L1 и HER2/neu.
Введение
Использование селективных радиоконъюгатов, специфичных к биомаркерам, открыло новые возможности для диагностики и терапии онкологических заболеваний. Радионуклид в таких радиофармпрепаратах присоединен к направленному на мишень вектору: целому моноклональному антителу, его фрагменту, каркасному белку, пептидному лиганду или другой небольшой молекуле. Тераностикой в радионуклидной терапии называют использование связывающейся с одной молекулярной мишенью пары радиофармацевтических препаратов, один из которых применяется для диагностики, а другой — для терапии опухолей. Тераностика открывает большие возможности для персонализированной терапии опухолей, позволяя заранее оценить эффективность того или иного подхода при лечении пациента [1]. В последнее десятилетие в тераностике опухолевых заболеваний достигнут большой прогресс. Он прежде всего связан с использованием лигандов соматостатинового рецептора (SSTR), а также лигандов простатспецифического мембранного антигена (PSMA), меченных радионуклидами 68Gaи 177Lu [2–4].
Белки PD-L1 и HER2/neu представляют собой хорошо изученные биомаркеры опухолевых заболеваний. PD-L1 является лигандом рецептора программируемой клеточной гибели PD1. Он конститутивно экспрессируется в ряде клеток иммунной системы, в некоторых эпителиальных клетках и клетках многих опухолей. Этот белок является одной из ключевых контрольных точек иммунитета, которую опухолевые клетки используют для уклонения от иммунного ответа. Связывание PD-L1 на поверхности антиген-презентирующих клеток с рецептором PD1, экспрессируемым T-лимфоцитами, приводит к подавлению пролиферации и цитотоксичности T-лимфоцитов, а также к продукции ими цитокинов [5, 6]. При этом экспрессия PD-L1 на поверхности опухолевых клеток может блокировать иммунный ответ, способствуя росту опухоли [7–9]. Тирозинкиназа HER2/neu (рецептор эпидермального фактора роста человека 2-го типа) является белком семейства рецепторов эпидермального фактора роста. Гетеродимеризация этого белка с другими членами семейства, а также его гомодимеризация приводят к активации сигнальных каскадов и пролиферации клеток [10–12]. При раке молочной железы, желудка, яичников, легких и матки часто наблюдается повышенная экспрессия HER2/neu, ведущая к его димеризации и, как следствие, к постоянной активации сигнальных путей [10]. Для терапии опухолей с повышенной экспрессией PD-L1 и HER2/neu применяют блокировку этих биомаркеров моноклональными антителами, а также используют конъюгаты антитело–лекарство [8, 13].
Гиперэкспрессия PD-L1 и HER2/neu связана с агрессивным развитием заболевания, при этом возможно использование для терапии конъюгатов, специфически связывающихся с этими биомаркерами. Отсутствие выраженной экспрессии PD-L1 и HER2/neu на поверхности опухолевых клеток делает нецелесообразным селективное воздействие на эти белки. Таким образом, определение уровня экспрессии PD-L1 и HER2/neu имеет большую прогностическую ценность и необходимо при выборе терапии. Для оценки уровня экспрессии применяется инвазивная биопсия с последующим иммуногистохимическим анализом, что является стандартной практикой при лечении пациентов. Однако этот метод не учитывает пространственную гетерогенность и временную динамику экспрессии PD-L1 и HER2/neu. Соответственно, неинвазивное определение статуса этих биомаркеров с использованием методов визуализации, прежде всего позитронно-эмиссионной томографии, является важным дополнением для исследования с применением иммуногистохимии.
Создание тераностических пар радиофармпрепаратов для диагностики и лечения опухолей, специфически связывающихся с PD-L1 или с HER2/neu, является актуальной задачей. В настоящей работе мы исследовали радиоиммуноконъюгаты (РИК), изготовленные на основе наноантител против PD-L1 и HER2/neu. Наноантитела, имеющие массу 12–15 кДа, представляют собой антигенсвязывающие VHH-фрагменты, образованные только тяжелыми цепями антител IgG, которые обнаружены в семействе парнокопытных млекопитающих Camelidae. Эти наноантитела также называются VHH-антителами. Наноантитела, имеющие массу 12–15 КДа, обладают меньшей иммуногенностью и значительно большей стабильностью, чем целые моноклональные антитела с массой 150 кДа [14]. Поскольку наноантитела не гликозилированы, их можно получать, в отличие от моноклональных антител, в прокариотах, снижая этим стоимость производства. Петля домена CDR3 у наноантител длиннее, чем у обычных IgG, что вместе с малым размером позволяет наноантителам связываться со скрытыми эпитопами [15]. В последние годы опубликованы работы по изучению радиофармпрепаратов на основе наноантител, включая публикации обисследованиях РИК наноантител против PD-L1 и HER2/neu [16–23].
При использовании тераностической пары радиофармацевтических препаратов желательно, чтобы они различались только радионуклидами, а векторные молекулы были бы одинаковыми. Этот подход облегчает стандартизацию и упрощает логистику изготовления радиоконъюгатов, что повышает качество лечения и снижает его стоимость. Нами были синтезированы две тераностические пары РИК, каждая на основе одного наноантитела: 68Ga-VHH PD-L1 и 177Lu-VHH PD-L1, 68Ga-VHH HER2/neu и 177Lu-VHH HER2/neu. При их изготовлении был использован один хелатирующий агент DOТА и радионуклиды 68Ga и 177Lu. Галлий-68 — изотоп с периодом полураспада 68 мин, излучающий позитроны и применяемый для диагностики при помощи позитронно-эмиссионной томографии [24]. Лютеций-177 — изотоп с периодом полураспада 6,65 сут, являющийся источником β-излучения и используемый для терапии опухолей [25].
Цель исследования — изучение функциональной пригодности (возможности применения) РИК наноантител против PD-L1 и HER2/neu для диагностики и терапии опухолей. Для этого были определены специфичность связывания РИК с целевым антигеном опухоли и динамика биораспределения РИК в организме мышей.
Материалы и методы
Аффинные к PD-L1 человека и к HER2/neu антитела. Объектами исследования служили конъюгированные с радиоизотопами рекомбинантные однодоменные тяжело-цепные антитела (наноантитела, VHH), распознающие эпитоп PD-L1 (VHH-PD-L1) и HER2/neu (VHH-HER2/neu) человека (предоставлены ООО «Иннова плюс», Россия).
Синтез РИК. Для получения хелатирующих предшественников использовали наноантитела, специфичные к биомаркерам PD-L1 и HER2/neu, и коммерчески доступный бифункциональный хелатирующий агент p-SCN-Bn_DOTA (Macrocyclics, США). Для синтеза РИК, содержащих 68Ga, применяли элюат генератора галлия-68 (АО «Циклотрон», Россия) в виде раствора хлорида галлия в 0,1 М хлористоводородной кислоты. К 100 мкг хелатирующего предшественника, растворенного в 20 мкл 50 мМ аммоний-ацетатного буфера (рН=7,5), добавляли 100 мкл 50 мМ аммоний-ацетатного буфера (рН=7,5) и 100 мкл элюата генератора, содержавшего 30–50 МБк 68Ga. Реакционную смесь инкубировали в течение 15 мин с использованием термошейкера TS-100C (SIA Biosan, Латвия) при 1000 об./мин и 70°C в защитном ламинарном боксе. Специфическая активность РИК составляла 0,3–0,5 МБк/мкг.
Для получения РИК, содержащих 177Lu, использовали раствор хлорида лютеция (177Lu) без носителя в 0,1 М HCl (ГНЦ НИИАР ГК Росатом, Россия). 100 мкг хелатирующего предшественника разбавляли 100 мкл 50 мМ раствора ацетата аммония. Полученную смесь подкисляли 22,5 мкл 0,1 М соляной кислоты до значения pH, равного ~5,5–5,8, и добавляли [177Lu]LuCl3 (15–45 МБк, 2,5 мкл). Радиомечение 177Lu проводили в закрытой пробирке при 37°C в течение 60 мин в присутствии кислорода воздуха, перемешивали в термошейкере (1000 об./мин) в защитном ламинарном боксе.
Полученные РИК анализировали методами радио-тонкослойной хроматографии с использованием пластинок ITLC SG (Agilent, США) и радио-высокоэффективной жидкостной хроматографии, которую выполняли с помощью хроматографа Ultimate 3000 (Dionex, США) и колонки Superdex 75 Increase (Cytiva, США). Специфическая активность РИК составляла 0,15–0,45 МБк/мкг. Радиохимическая чистота всех РИК была не менее 95%.
Оценка специфического связывания РИК с антигенами с помощью магнитных частиц. Специфическую активность РИК определяли, как описано ранее [26], используя коммерчески доступные магнитные частицы, покрытые протеином А (SureBeads, кат. №161–4013; Bio-Rad, США; MagBeads, кат. №L00273; MagBio Genomics, США или SileksMag, кат. №K0181; SileksMag, Россия). Для этого специфический антиген, конъюгированный с Fc-фрагментом (PD-L1-Fc или HER2/neu-Fc), иммобилизовывали на магнитных частицах. Затем частицы инкубировали с раствором РИК (0,5–4,0 мкг/мл). После отмывания частиц от несвязавшегося РИК измеряли их радиоактивность с помощью радиометра активности радионуклидов Triathler и программного обеспечения Triathler Becquerel Finder (Hidex, Финляндия). Для контроля РИК инкубировали с частицами, не покрытыми антигеном. Показателем специфического связывания РИК служила доля радиоактивности, связавшейся с покрытыми антигеном частицами, от радиоактивности, исходно добавленной в инкубационную пробу. Тестированию in vivo подвергали РИК, у которых доля радиоактивности, специфически связавшейся с белками-мишенями на магнитных частицах, составляла 70–90% от радиоактивности, добавленной в пробу.
Биологические модели для тестирования РИК in vivo. Исследование динамики биораспределения РИК проводили с помощью разработанных нами биологических моделей. Для тестирования РИК на основе VHH-PD-L1 использовали клетки штамма CT26-PD-L1, представляющие собой генно-модифицированные клетки CT26 карциномы кишечника мышей BALB/c, экспрессирующие на мембране PD-L1 человека. Создание и характеристики биологической модели, основанной на этих клетках, описаны ранее [27]. Для оценки динамики биораспределения РИК, созданных на основе наноантител VHH-HER2/neu, использовали клетки штамма CT26-HER2/neu, которые были созданы также методом генной инженерии. Их получение и основные свойства описаны ниже.
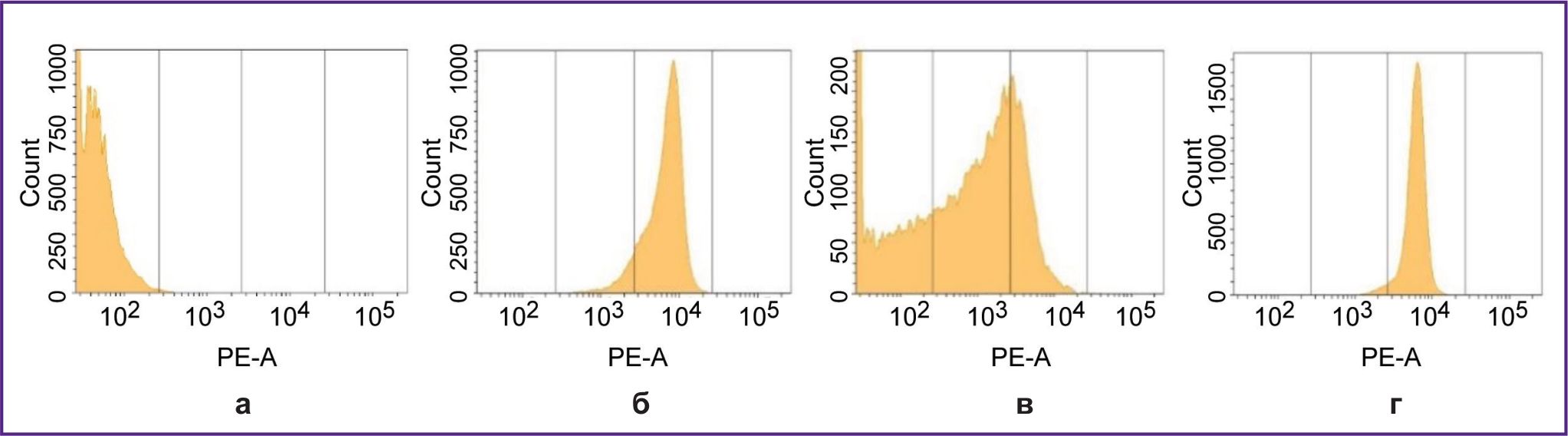
Биологическая модель для тестирования РИК на основе VHH-HER2/neu. Штамм CT26-HER2/neu был получен методом ретровирусной трансдукции клеток мышиной карциномы CT26 плазмидой pQCXIP-HER2/neu. Донором кДНК HER2/neu для создания вектора служили клетки меланомы человека линии MeWo. Клетки штамма CT26-HER2/neu, в отличие от родительских мышиных клеток CT26, имели высокую экспрессию гена и белка HER2/neu человека, что было подтверждено с помощью полимеразной цепной реакции в режиме реального времени и проточной иммуноцитофлоуриметрии (рис. 1). Штамм обладал высокой стабильностью и сохранял исходный уровень экспрессии биомаркера в процессе культивирования на протяжении 15 пассажей (срок наблюдения) как в присутствии селективного антибиотика, так и при его отсутствии. При подкожном введении 5 млн клеток CT26-HER2/neu сублетально облученным мышам F1(DBA/2xBALB/c) на 9–11-й дни у животных формировались солидные опухоли объемом 100–500 мм3. Содержание клеток, имеющих на мембране HER2/neu человека, на 15–17-е сутки роста опухолей составляло 30–40% (рис. 1, б). После эксплантации и культивирования in vitro клеток из этих опухолей в течение 11 сут содержание HER2/neu-позитивных клеток возрастало до 99%, что свидетельствовало о высокой стабильности экспрессии биомаркера клетками штамма CT26-HER2/neu (рис. 1, в). Количество молекул HER2/neu, определенное путем связывания с РИК, составило 1,6 млн на клетку.
Эксперименты на животных. Эксперименты проводили на мышах F1(DBA/2хBALB/c) обоего пола. Мышей содержали в стандартных условиях в соответствии с Директивой 2010/63/EU Европейского парламента и совета Европейского Союза от 22 сентября 2010 г. по охране животных, используемых в научных целях. Исследование одобрено этическим комитетом Российского научного центра радиологии и хирургических технологий им. академика А.М. Гранова (Санкт-Петербург, Россия). В день начала эксперимента мышей облучали на терапевтическом рентгеновском аппарате (доза 5 Гр). Эта доза облучения была подобрана в серии предварительных экспериментов с целью снизить иммунореактивность животных в отношении антигенов человека. Облучение мышей в дозе 5 Гр не вызывало гибели животных в течение 6 мес. В контрольных опытах использовали необлученных интактных мышей. Клетки СТ26-PD-L1 или CT26-HER2/neu, стабильно экспрессирующие на мембране биомаркеры человека, трансплантировали подкожно в количестве 5·106 клеток на мышь в правый бок животного. Под кожу левого бока вводили 1 млн контрольных клеток CT26, не экспрессирующих биомаркеры человека.
Исследование динамики биораспределения РИК методом прямой радиометрии. В исследование брали мышей на 9–13-е сутки после трансплантации опухолевых клеток. Животных наркотизировали (Золетил 100, 30 мг/кг, и ксилавет, 8 мг/кг, внутримышечно), после чего в ретроорбитальный венозный синус вводили по 100 мкл растворов РИК. Объемная активность РИК, содержащих 68Ga, составляла 10–12 МБк/мл, 177Lu — 8–16 МБк/мл.
Через 0,5 1,5, 4, 24, 48 и 96 ч после введения антител, конъюгированных с радиоизотопом 177Lu (время полураспада 6,65 сут), или через 0,5, 1,5 и 4 ч после введения антител, меченных радиоизотопом 68Ga (время полураспада 68 мин), проводили исследование биораспределения в организме экспериментальных животных. Для этого мышей умерщвляли введением избыточной дозы Золетила 100, после чего производили вскрытие и отбирали образцы тканей и биологических жидкостей. Количественное определение активности радионуклидов в образцах проводили с помощью радиометра активности радионуклидов Triathler (Hidex, Финляндия), используя для 68Ga энергетическое окно 150–350 каналов, для 177Lu — 0–150 каналов. Значения радиоактивности изъятых органов и тканей пересчитывали для времени вскрытия (нулевой временнóй точки) по формуле: А0=АТ1·е^(Ln(2)·(T1–T0)/T1/2), где А0 — активность образца на момент вскрытия, Бк; АТ1 — активность образца на момент измерения активности, Бк; T1 — время измерения активности, ч; T0 — время вскрытия, ч; T1/2 — период полураспада, ч. Затем вычисляли показатель радиоактивности ткани в процентах от введенной активности в пересчете на 1 г ткани.
Статистическая обработка данных. При статистической обработке экспериментальных данных использовали программу GraphPad Prizm 10. Данные представлены в виде гистограмм с обозначением стандартного отклонения для каждого среднего значения (m±σ). Для оценки различий между двумя независимыми выборками использовали U-критерий Манна–Уитни. Результаты считали статистически значимыми при p≤0,05. Все результаты получены не менее чем в трех повторах.
Результаты
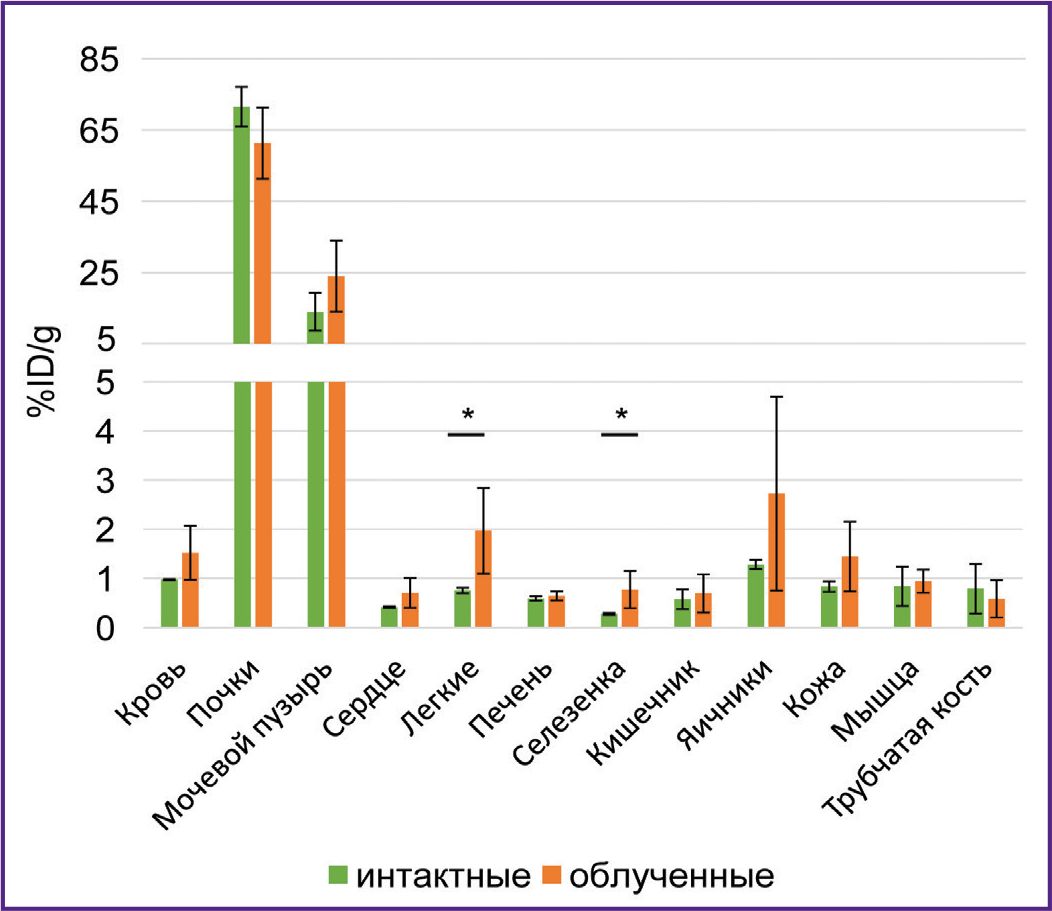
Чтобы исследовать биораспределение РИК, были созданы модели опухолей человека. Для их создания мышам F1(DBA/2xBALB/c) вводили мышиные генно-модифицированные клетки СT26-PD-L1 или СT26-HER/neu, экспрессирующие человеческие биомаркеры опухолей PD-L1 или HER2/neu. Этим же животным прививали контрольную опухоль введением мышиных клеток СТ26. Для образования опухолей иммунореактивность мышей была предварительно снижена сублетальной дозой рентгеновского облучения (5 Гр). Влияние рентгеновского облучения на биораспределение РИК не обнаружено: после введения 68Ga-VHH HER2/neu накопление радиоактивности в органах и тканях мышей, облученных за 8 сут до вскрытия, не отличалась от такого накопления у необлученных (рис. 2). Аналогичные результаты получены после введения 177Lu-VHH PD-L1 (данные не показаны).
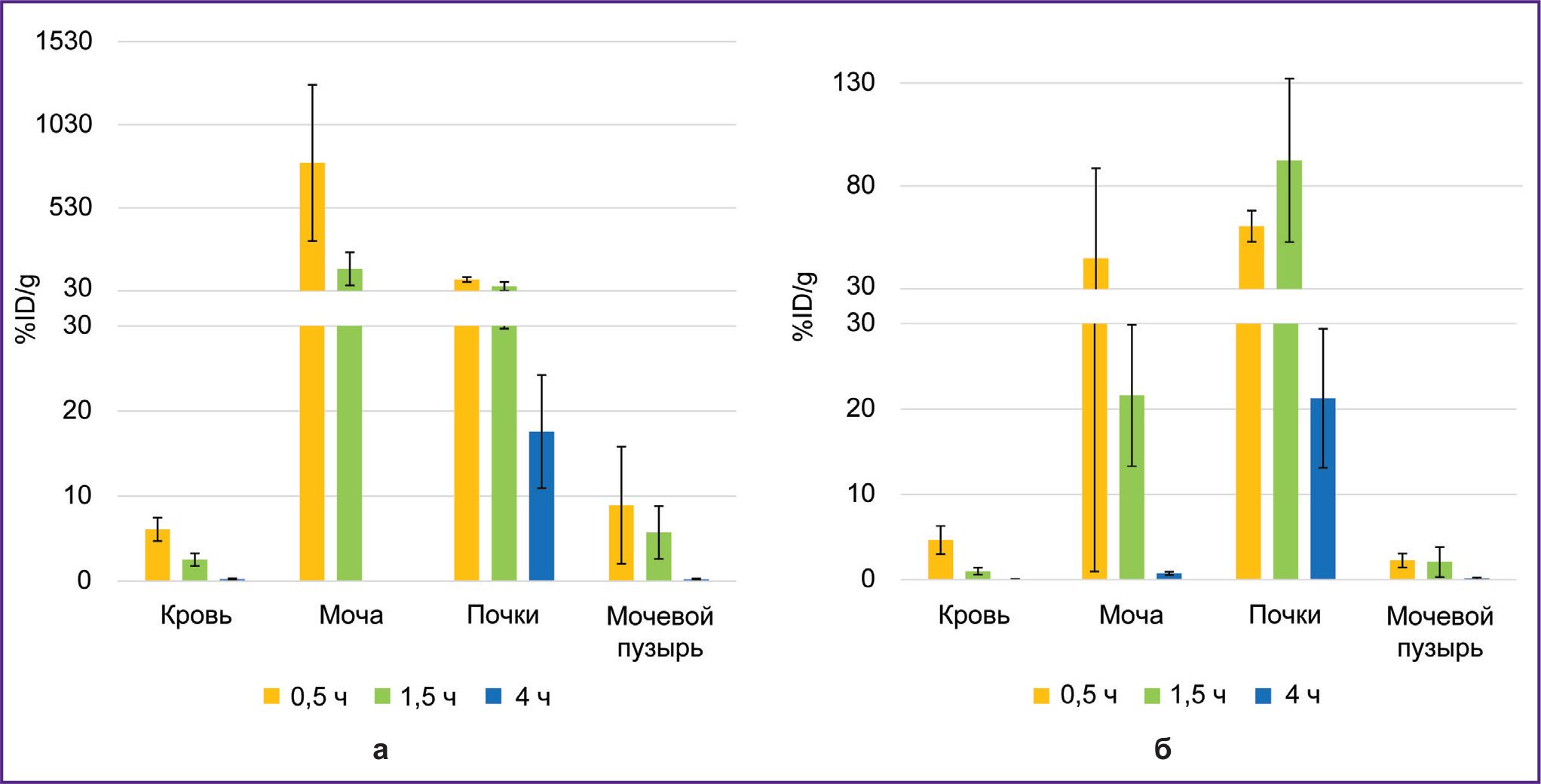
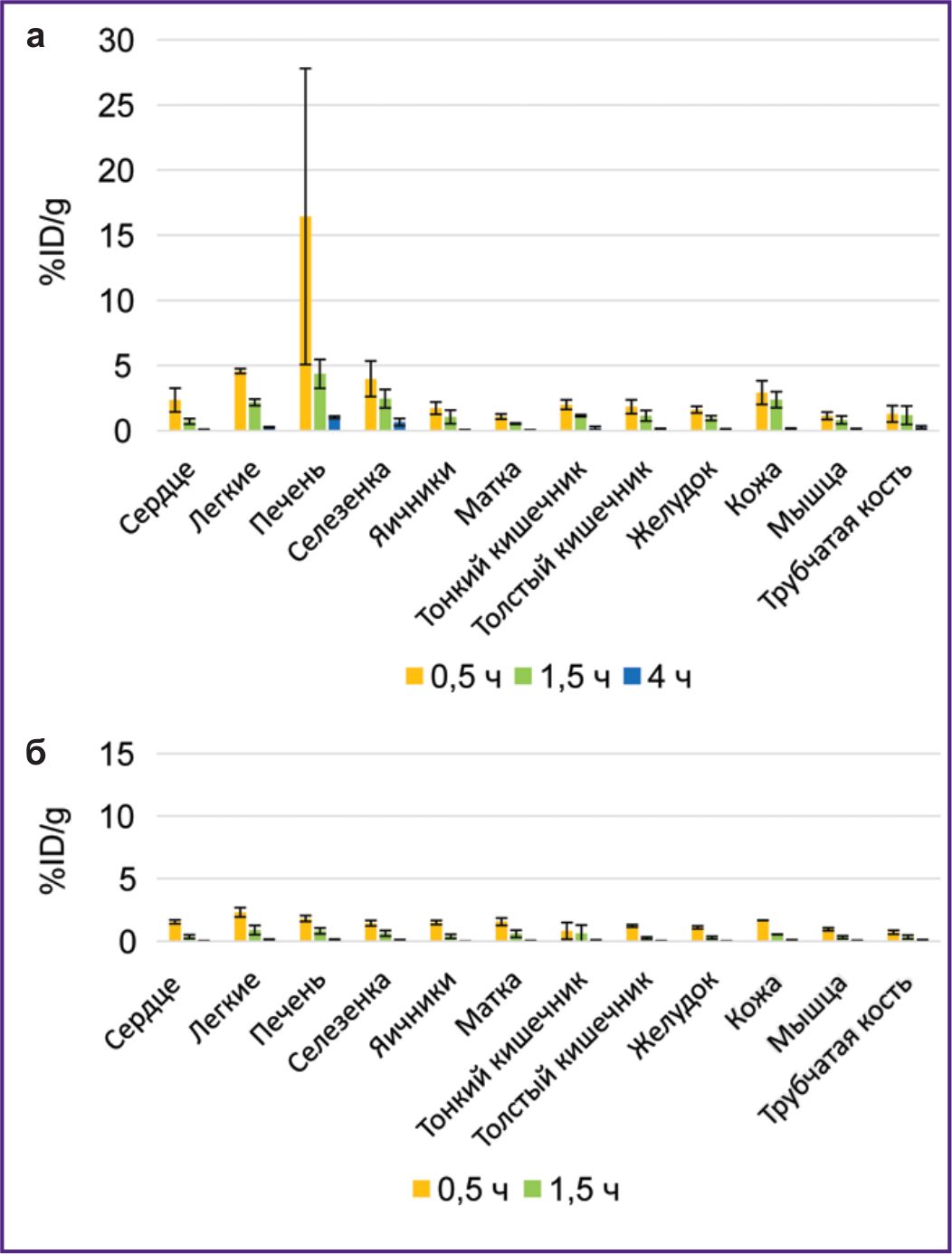
Биораспределение 68Ga-VHH PD-L1 или 68Ga-VHH HER2/neu исследовали через 0,5, 1,5 и 4 ч после введения в кровь мышей. Установлено, что происходило быстрое удаление радионуклида 68Gaиз кровотока мышей через мочевыделительную систему (рис. 3). Через 1,5 ч радиоактивность крови не превышала в среднем 2,5%. (Здесь и далее радиоактивность будет представлена в процентах от введенной дозы на 1 г веса ткани.) При этом обнаружено значительное накопление радиоактивности в почках, причем оно было максимальным через 30 мин после введения 68Ga-VHH PD-L1 и через 1,5 ч после введения 68Ga-VHH HER2/neu. Вероятно, это связано с более интенсивным выведением 68Ga-VHH PD-L1 с мочой.
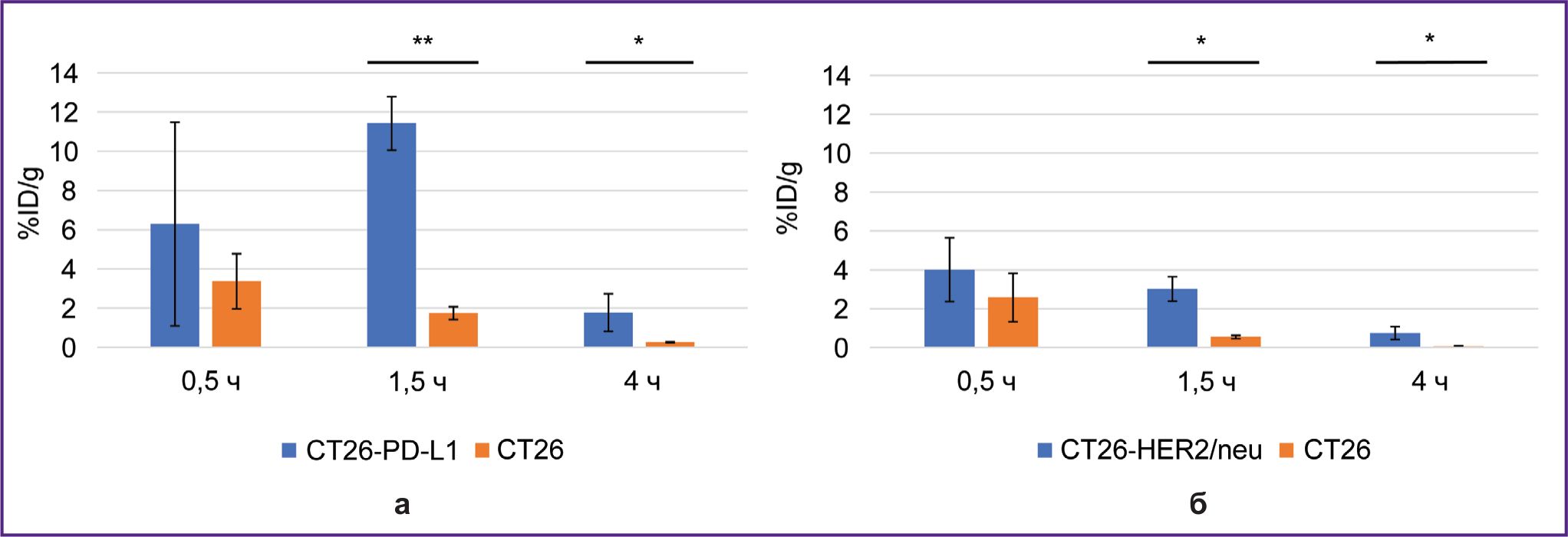
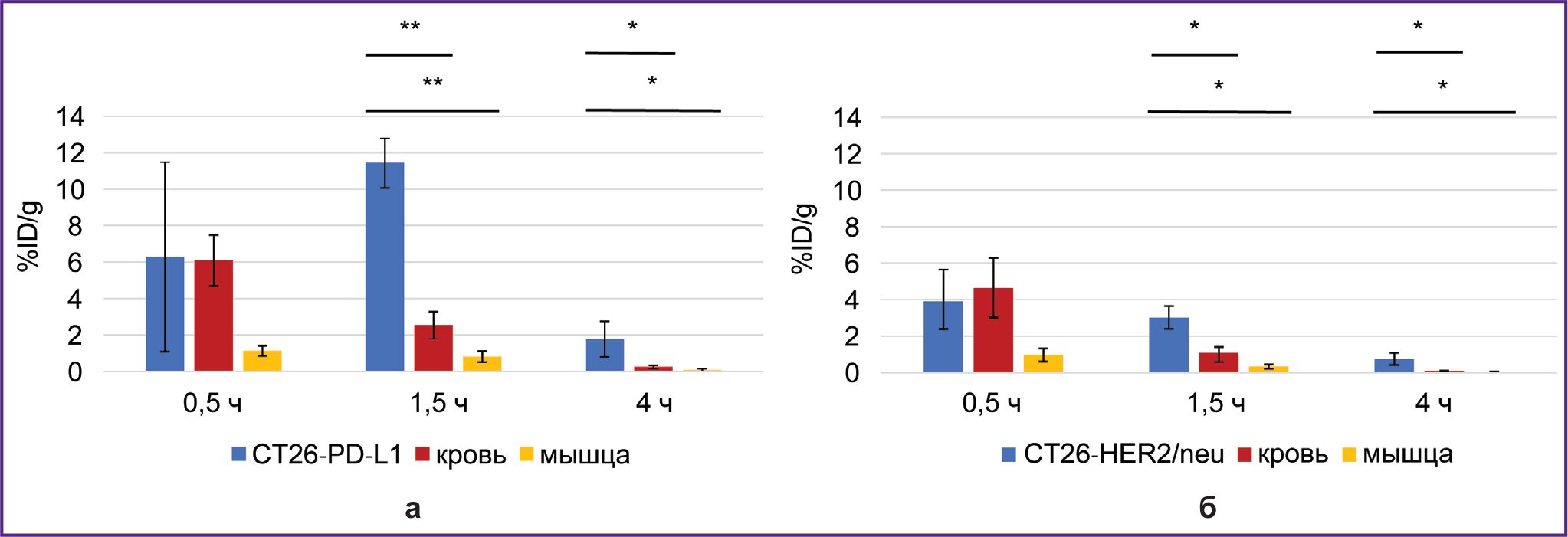
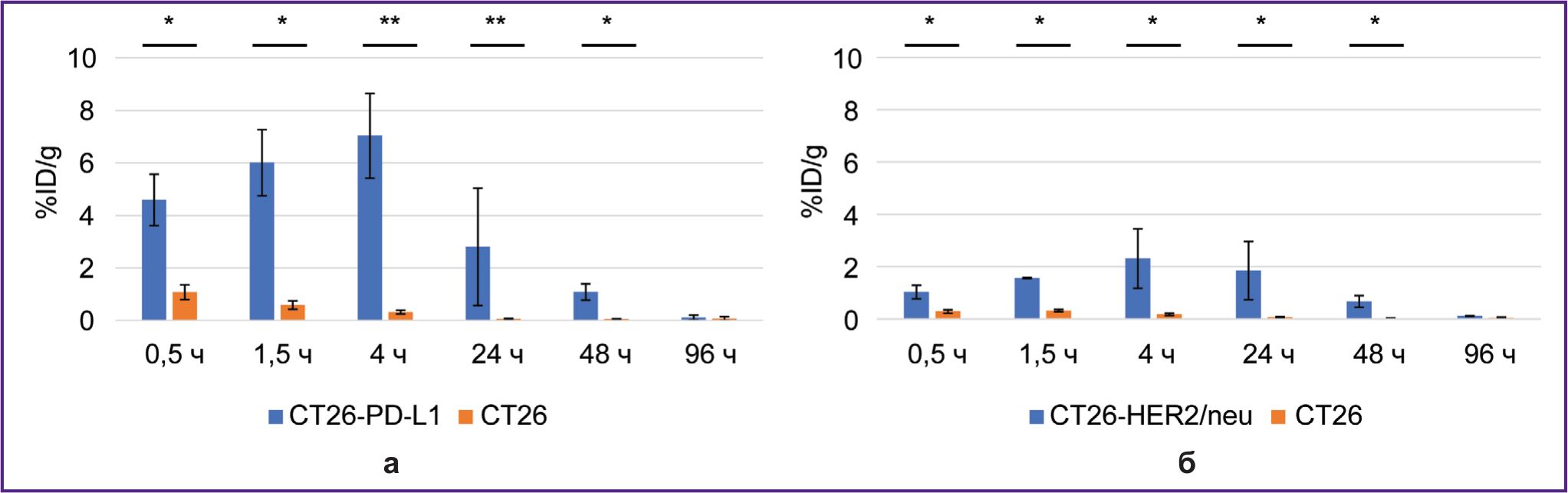
Через 1,5 и 4 ч после введения 68Ga-VHH PD-L1 или 68Ga-VHH HER2/neu радиоактивность специфической опухоли была выше, чем контрольной (рис. 4). Это показывает наличие селективного связывания РИК с целевыми биомаркерами PD-L1 и HER2/neu, экспрессируемыми клетками специфической опухоли. Общей закономерностью после введения этих РИК было быстрое снижение радиоактивности контрольной опухоли, в результате чего наибольшее превышение радиоактивности специфической опухоли над радиоактивностью контрольной достигалось через 1,5 ч. Максимальное значение радиоактивности в специфической опухоли 68Ga-VHH PD-L1 составило в среднем 11,4% после введения 68Ga-VHH PD-L1 и 4,0% после введения 68Ga-VHH HER2/neu (см. рис. 4). Благодаря селективному связыванию 68Ga-VHH PD-L1 и 68Ga-VHH HER2/neu радиоактивность в специфической опухоли была больше, чем радиоактивность в других органах и тканях, за исключением почек (рис. 5). Данная разница была статистически значимой для крови и мышечной ткани через 1,5 и 4 ч (рис. 6), причем через 1,5 ч она была наибольшей. Это должно обеспечивать контрастность визуализации при диагностике опухолей с использованием позитронно-эмиссионной томографии. Так, через 1,5 ч после введения 68Ga-VHH PD-L1 радиоактивность специфической опухоли превышала радиоактивность в крови в 4,5 раза, в мышечной ткани — в 14,1 раза. Для 68Ga-VHH HER2/neu это превышение составило соответственно 3,1 и 9,4 раза.
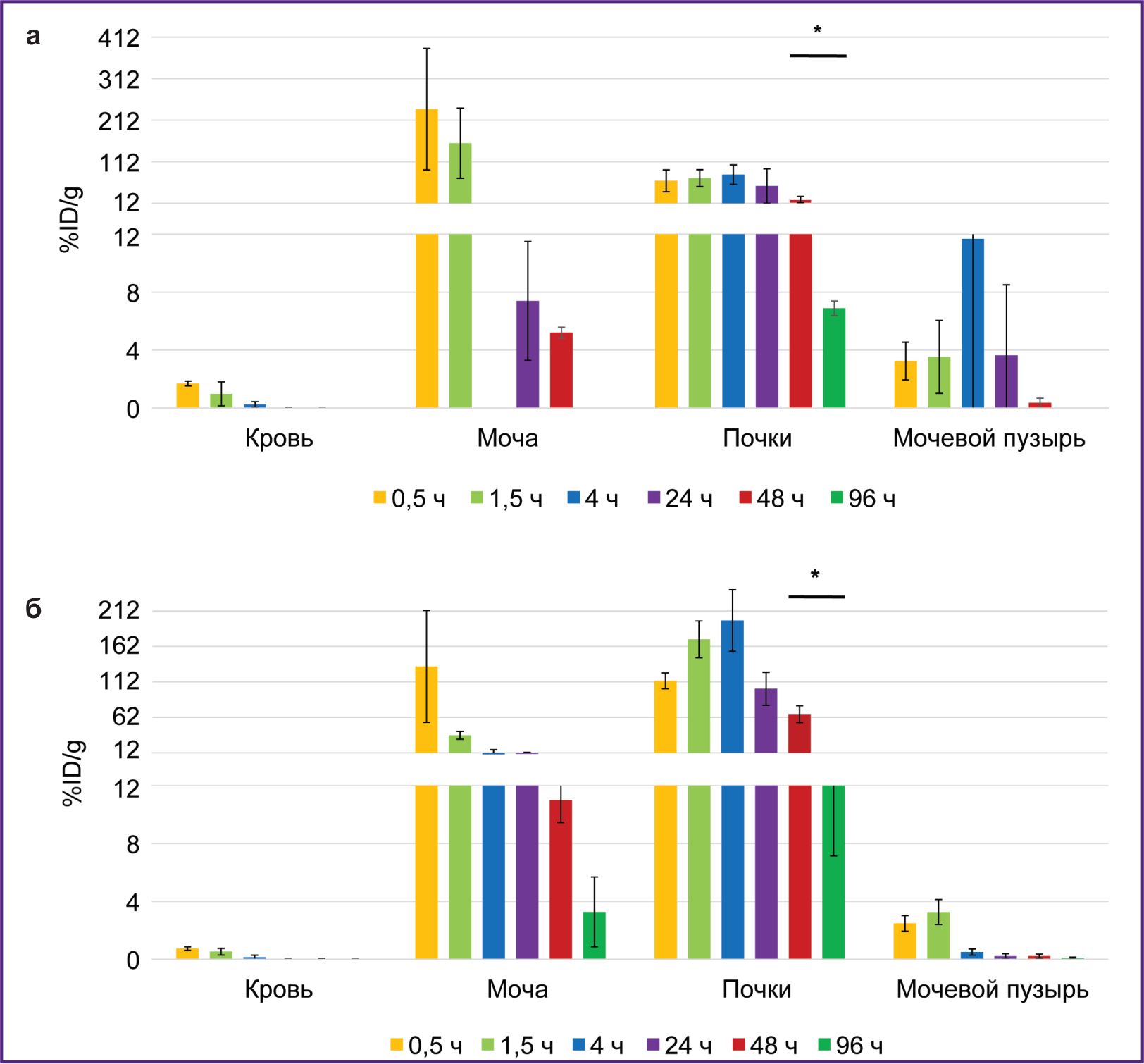
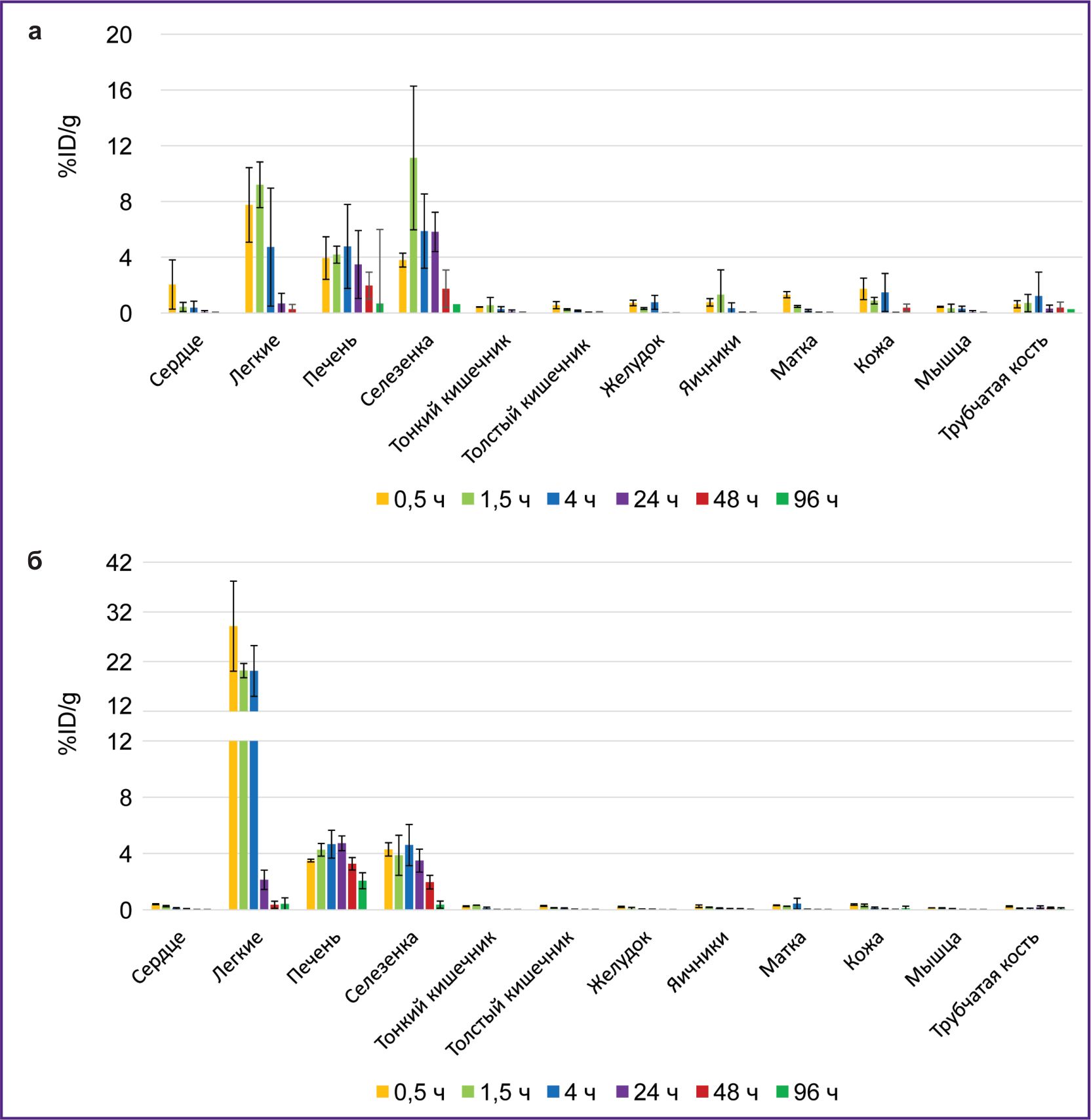
Исследование биораспределения в организме мышей РИК, содержащих 177Lu, проводили в течение 96 ч после введения, что обусловлено временем полураспада этого изотопа. После введения 177Lu-VHH PD-L1 или 177Lu-VHH HER2/neu также происходило быстрое снижение радиоактивности крови: через 4 ч ее значение не превышало 0,25% (см. рис. 6). Это было следствием того, что после введения данных РИК радионуклиды также интенсивно выводились с мочой, при этом значительная их часть задерживалась в почках, где накопление радиоактивности было наибольшим по сравнению с другими органами и тканями (рис. 7 и 8). Радиоактивность специфической опухоли была сопоставима (для 177Lu-VHH HER2/neu) или меньше (177Lu-VHH HER2/neu), чем радиоактивность легких, печени и селезенки, но больше, чем остальных органов и тканей, исключая почки (см. рис. 8; рис. 9).
В течение 48 ч после введения 177Lu-VHH PD-L1 или 177Lu-VHH HER2/neu радиоактивность специфической опухоли превышала радиоактивность контрольной опухоли (см. рис. 9). Эти данные демонстрируют, что 177Lu-VHH PD-L1 и 177Lu-VHH HER2/neu также специфично связываются in vivo с опухолью, экспрессирующей целевой биомаркер. Накопление радиоактивности в специфической опухоли достигало максимума через 4 ч: в среднем 6,6% для 177Lu-VHH PD-L1 и 2,3% для 177Lu-VHH HER2/neu. Далее радиоактивность специфической опухоли медленно снижалась, что может обеспечить длительное терапевтическое воздействие.
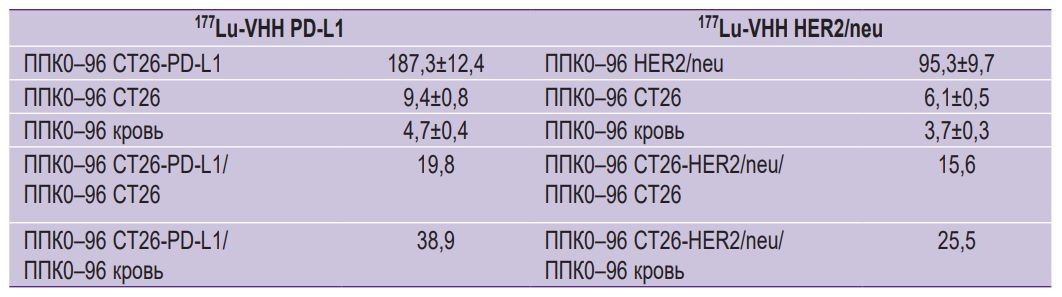
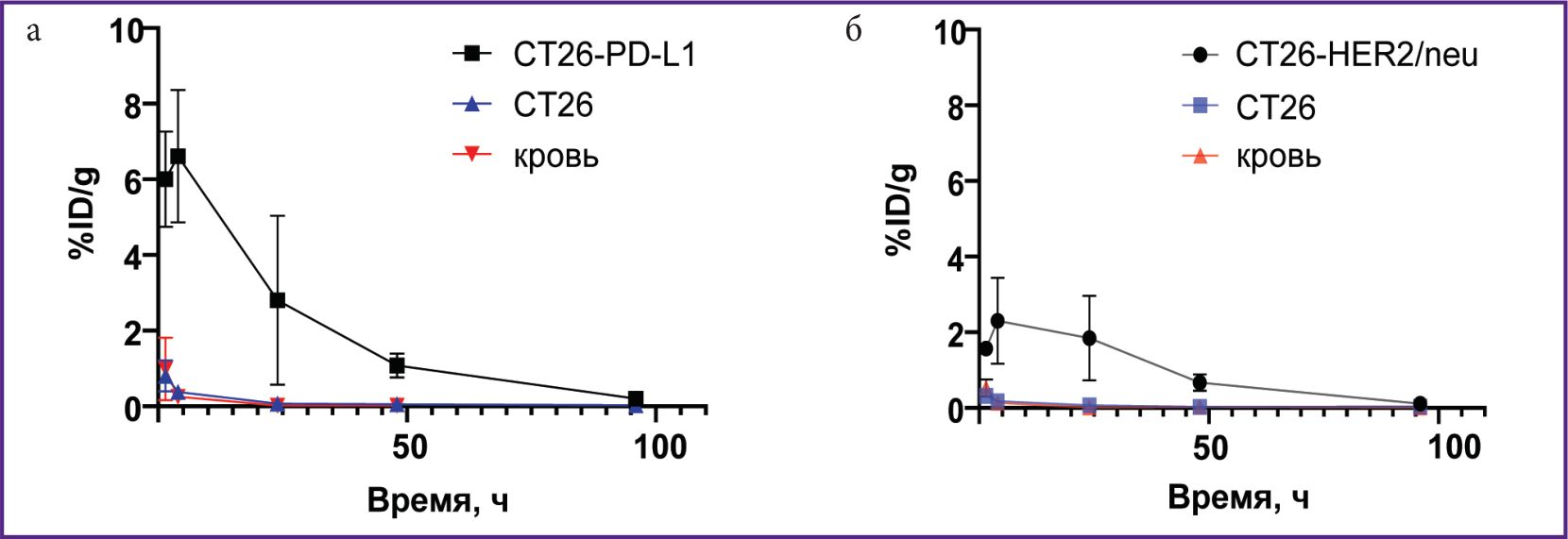
На рис. 10 показано соотношение площадей под кривой для графиков радиоактивности специфической и контрольной опухолей, а также крови в течение 96 ч после введения 177Lu-VHH PD-L1 и 177Lu-VHH HER2/neu. Отношения этих площадей для специфической и контрольной опухоли составили 19,8 после введения 177Lu-VHH PD-L1 и 15,6 после введения 177Lu-VHH HER2/neu (см. таблицу). Такие высокие значения подтверждают селективность связывания РИК со специфической опухолью. Отношения таких площадей для специфической опухоли и крови были соответственно 38,9 и 25,5. Это значит, что применение РИК для терапии не должно приводить к значительному радиационному воздействию на организм.
|
Рис. 10. Графики зависимости радиоактивности специфической и контрольной опухолей и крови от времени после введения радиоиммуноконъюгатов: а — 177Lu-VHH PD-L1; б — 177Lu-VHH HER2/neu |
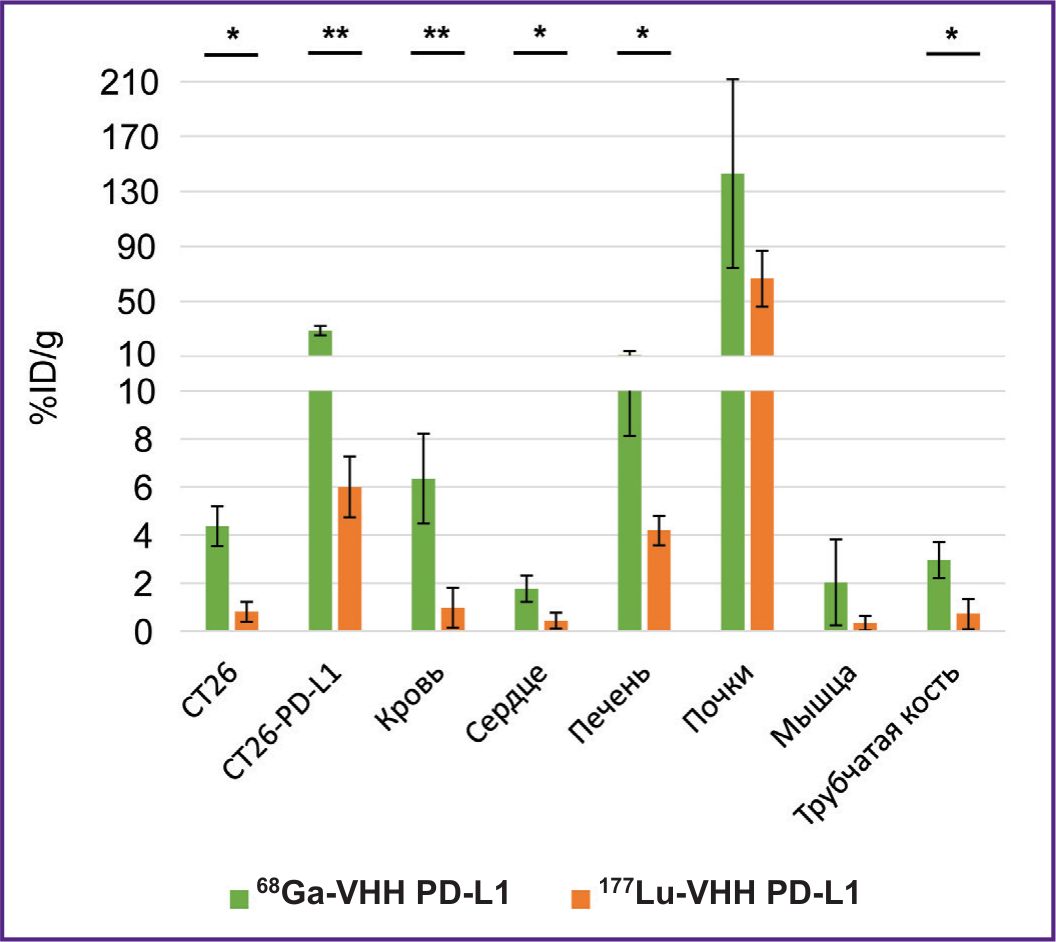
В настоящей работе исследована зависимость биораспределения РИК не только от входящих в их состав наноантител, но и от радионуклидов, так как в литературе мы не нашли данные по сравнению биораспределения РИК, содержащих одни и те же наноантитела, с этими радионуклидами. Проведено сравнение радиоактивности органов и тканей мышей через 1,5 ч после введения 68Ga-VHH PD-L1 и 177Lu-VHH PD-L1. Для того чтобы провести такое сравнение, был учтен быстрый распад 68Ga путем нормализации радиоактивности на время введения. Показано, что в специфической и неспецифической опухолях, крови, сердце и печени накопление наноантител, меченных 68Ga, кратно превышает накопление наноантител, меченных 177Lu (рис. 11). Важно: эти препараты были изготовлены на основе одного наноантитела и имели один хелатирующий агент DOTA, что уменьшает варианты интерпретаций полученных результатов.
Обсуждение
Основная цель работы заключалась в том, чтобы продемонстрировать возможность использования пар РИК наноантител с радиоизотопами для тераностики опухолей, экспрессирующих биомаркеры PD-L1 и HER2/neu. Наноантитела были конъюгированы с 68Ga, используемым в диагностических целях, и с 177Lu, применяемым для терапии опухолей. Результаты показали наличие специфического связывания всех РИК с опухолями, экспрессирующими PD-L1 или HER2/neu соответственно. Показано также, что после введения этих РИК в кровоток происходит интенсивное выведение радионуклидов 68Ga и 177Lu через мочевыделительную систему. Это обусловлено тем, что молекулярная масса белковых молекул в РИК меньше пороговой массы, равной 65 кДа. Благодаря этому данные молекулы могут проходить через почечный барьер и выводиться с мочой [28, 29]. В результате наблюдается быстрое падение радиоактивности органов и тканей. Известно, что фрагменты антител, включая VHH, удаляются из крови гораздо быстрее, чем целые моноклональные антитела, период полувыведения которых составляет несколько суток из-за большой молекулярной массы (150 кДа) и обусловленной этим невозможности пройти через почечный фильтр из крови в первичную мочу [30–32]. Еще одним преимуществом РИК на основе наноантител и других низкомолекулярных векторных молекул является отсутствие Fc-фрагмента. Этот фрагмент целых моноклональных антител связывается в организме с неонатальным рецептором Fc-фрагмента (FcRn), экспрессируемым клетками организма, включая эндотелиальные клетки кровеносных сосудов, что препятствует деградации моноклональных антител в лизосомах после эндоцитоза, приводит к их рециркуляции обратно к клеточной поверхности и, соответственно, к задержке в крови [33, 34]. Кроме того, у таких РИК нет обусловленных данным фрагментом эффекторных функций, которые необходимы для функционирования иммунной системы, но в ряде случаев могут быть нежелательны для радиофармпрепаратов [35, 36].
Более низкий молекулярный вес наноантител и других векторных молекул обусловливает еще одну особенность их фармакокинетики по сравнению с целыми антителами. Помимо интенсивного выведения из организма с мочой VHHи другие фрагменты быстрее и равномернее проникают в ткань специфической опухоли [37]. Благодаря сочетанию этих свойств происходит быстрое и значительное превышение радиоактивности опухоли, экспрессирующей целевые биомаркеры, над радиоактивностью крови и мышечной ткани. Это делает возможным использование РИК с короткоживущими изотопами, такими как 68Ga, для контрастной визуализации опухолей. Быстрое выведение радионуклидов из кровотока также приводит к снижению радиационной нагрузки при терапии опухолевых заболеваний. Исследованные ранее радиоконъюгаты, созданные на основе небольших каркасных белков и фрагментов антител, быстрее выводились из крови и больше накапливались в почках по сравнению с целыми антителами [18–22].
Одной из проблем при использовании РИК на основе наноантител является относительно высокая скорость выведения радионуклидов из специфической опухоли: через 96 ч после введения таких РИК, содержащих 177Lu, радиоактивность опухоли была крайне мала (см. рис. 9). Это является следствием быстрого выведения РИК из крови, в результате чего только небольшая часть меченых наноантител достигает цели. Для достижения высокой целевой радиационной нагрузки РИК можно вводить несколько раз [38]. Другой проблемой является накопление радиоактивности в почках. Выведение РИК на основе наноантител через мочевыделительную систему приводит к значительной радиоактивности этих органов, вероятно из-за того, что металл-хелатные комплексы задерживаются в лизосомах эпителиальных клеток почечных канальцев при реабсорбции из первичной мочи [28]. Это в первую очередь актуально для РИК, содержащих радионуклиды, используемые в терапевтических целях, чье излучение скорее способно повредить ткани организма, чем излучение радионуклидов, применяемых для диагностики. В настоящее время в клинике для снижения радиоактивности в почках вместе с некоторыми радиофармпрепаратами вводят аргинин и лизин в качестве сопутствующих веществ. Конкурируя с радиофармпрепаратом за сайты связывания, используемые при реабсорбции, эти вещества уменьшают накопление радиоактивности в почках. Исследуют и другие подходы для решения этой проблемы, в том числе предварительное нацеливание, присоединение альбуминсвязывающего домена, использование расщепляющихся линкеров [39–41].
Представленные результаты показывают возможность применения пар РИК 68Ga-VHH PD-L1 и 177Lu-VHH PD-L1, 68Ga-VHH HER2/neu и 177Lu-VHH HER2/neu для тераностики опухолей, экспрессирующих PD-L1 и HER2/neu. В каждой паре РИК различались только радионуклидами, но не векторными молекулами и хелатирующими агентами. Использование таких пар облегчит, как уже было отмечено, стандартизацию изготовления РИК, упростит логистику лечебного процесса и снизит его стоимость. Ранее проведенные исследования [23, 42–45] конъюгатов радионуклидов с иммунными векторными молекулами, специфичными к PD-L1 или HER2/neu, не предусматривали подобного подхода.
В отличие от уже широко используемых для тераностики радиоконъюгатов на основе пептидов и других низкомолекулярных лигандов наноантитела могут иметь селективность к любым эпитопам. Соответственно, можно ожидать получения на основе наноантител новых тераностических пар РИК, специфичных к другим биомаркерам. Кроме того, РИК могут содержать другие изотопы, предназначенные для диагностики или терапии. Радионуклиды различаются по излучению, периоду полураспада и токсичности, что дает возможность подобрать нужный изотоп при разработке радиофармпрепарата, предназначенного для решения конкретной задачи. Таким образом, возникает необходимость исследовать и сравнивать большое количество РИК, различающихся векторными молекулами и/или радионуклидами. Это делает актуальным использование в доклинических исследованиях стандартизированных, охарактеризованных, воспроизводимых и желательно недорогих экспериментальных моделей. Такими моделями являются генно-инженерные клетки, созданные на основе опухолевых клеток мышей и несущие биомаркеры опухолей человека, которые могут быть привиты мышам с минимально модифицированной или интактной иммунной системой [27, 46, 47]. Как было отмечено, в данной работе для образования опухолей мышам прививали гуманизированные клетки СT26-PD-L1 и СT26-HER2/neu, созданные на основе мышиных клеток СT26 и экспрессирующие соответственно PD-L1 и HER2/neuчеловека.
Интересным и неожиданным наблюдением является зависимость биораспределения исследованных РИК в органах и тканях не только от входящих в их состав наноантител, но и от радионуклидов. Показано, что в ряде органов и тканей, включая опухоли, накопление наноантител, меченных 68Ga, кратно превышает накопление таких же наноантител, меченных 177Lu. Известно, что биораспределение радиофармпрепаратов, содержащих радиоактивные изотопы металлов и галогенов, различно, поскольку галогены меньше задерживаются в почках [28]. Нами была получена существенная разница в биораспределении РИК, содержавших изотопы разных металлов.
Заключение
Показана функциональная пригодность пар РИК наноантител с радиоизотопами 68Ga и 177Lu для диагностики и терапии опухолей, экспрессирующих биомаркеры PD-L1 и HER2/neu. Каждая пара РИК с одинаковой специфичностью была синтезирована с использованием одной и той же векторной молекулы и одного и того же хелатирующего агента. Это дает возможность повысить надежность лечения и снизить его стоимость. Создание подобных тераностических пар радиофармпрепаратов на основе фрагментов моноклональных антител может открыть большие возможности для эффективного персонализированного лечения онкологических заболеваний.
Финансирование. Работа выполнена в рамках государственного задания Министерства здравоохранения РФ, рег. №122040800129-5.
Конфликт интересов отсутствует.
Литература
- Duan H., Iagaru A., Aparici C.M. Radiotheranostics — precision medicine in nuclear medicine and molecular imaging. Nanotheranostics 2022; 6(1): 103–117, https://doi.org/10.7150/ntno.64141.
- Burkett B.J., Bartlett D.J., McGarrah P.W., Lewis A.R., Johnson D.R., Berberoğlu K., Pandey M.K., Packard A.T., Halfdanarson T.R., Hruska C.B., Johnson G.B., Kendi A.T. A review of theranostics: perspectives on emerging approaches and clinical advancements. Radiol Imaging Cancer 2023; 5(4): e220157, https://doi.org/10.1148/rycan.220157.
- Strosberg J., El-Haddad G., Wolin E., Hendifar A., Yao J., Chasen B., Mittra E., Kunz P.L., Kulke M.H., Jacene H., Bushnell D., O'Dorisio T.M., Baum R.P., Kulkarni H.R., Caplin M., Lebtahi R., Hobday T., Delpassand E., Van Cutsem E., Benson A., Srirajaskanthan R., Pavel M., Mora J., Berlin J., Grande E., Reed N., Seregni E., Öberg K., Lopera Sierra M., Santoro P., Thevenet T., Erion J.L., Ruszniewski P., Kwekkeboom D., Krenning E; NETTER-1 Trial Investigators. Phase 3 trial of 177Lu-Dotatate for midgut neuroendocrine tumors. N Engl J Med 2017; 376(2): 125–135, https://doi.org/10.1056/NEJMoa1607427.
- Chi K.N., Yip S.M., Bauman G., Probst S., Emmenegger U., Kollmannsberger C.K., Martineau P., Niazi T., Pouliot F., Rendon R., Hotte S.J., Laidley D.T., Saad F. 177Lu-PSMA-617 in metastatic castration-resistant prostate cancer: a review of the evidence and implications for Canadian clinical practice. Curr Oncol 2024; 31(3): 1400–1415, https://doi.org/10.3390/curroncol31030106.
- Guleria I., Khosroshahi A., Ansari M.J., Habicht A., Azuma M., Yagita H., Noelle R.J., Coyle A., Mellor A.L., Khoury S.J., Sayegh M.H. A critical role for the programmed death ligand 1 in fetomaternal tolerance. J Exp Med 2005; 202(2): 231–237, https://doi.org/10.1084/jem.20050019.
- Brown J.A., Dorfman D.M., Ma F.R., Sullivan E.L., Munoz O., Wood C.R., Greenfield E.A., Freeman G.J. Blockade of programmed death-1 ligands on dendritic cells enhances T cell activation and cytokine production. J Immunol 2003; 170(3): 1257–1266, https://doi.org/10.4049/jimmunol.170.3.1257.
- Iwai Y., Ishida M., Tanaka Y., Okazaki T., Honjo T., Minato N. Involvement of PD-L1 on tumor cells in the escape from host immune system and tumor immunotherapy by PD-L1 blockade. Proc Natl Acad Sci U S A 2002; 99(19): 12293–12297, https://doi.org/10.1073/pnas.192461099.
- Lin X., Kang K., Chen P., Zeng Z., Li G., Xiong W., Yi M., Xiang B. Regulatory mechanisms of PD-1/PD-L1 in cancers. Mol Cancer 2024; 23(1): 108, https://doi.org/10.1186/s12943-024-02023-w.
- Dong H., Strome S.E., Salomao D.R., Tamura H., Hirano F., Flies D.B., Roche P.C., Lu J., Zhu G., Tamada K., Lennon V.A., Celis E., Chen L. Tumor-associated B7-H1 promotes T-cell apoptosis: a potential mechanism of immune evasion. Nat Med 2002; 8(8): 793–800, https://doi.org/10.1038/nm730.
- Cheng X. A comprehensive review of HER2 in cancer biology and therapeutics. Genes (Basel) 2024; 15(7): 903, https://doi.org/10.3390/genes15070903.
- Trenker R., Diwanji D., Bingham T., Verba K.A., Jura N. Structural dynamics of the active HER4 and HER2/HER4 complexes is finely tuned by different growth factors and glycosylation. Elife 2024; 12: RP92873, https://doi.org/10.7554/eLife.92873.
- Dvir K., Giordano S., Leone J.P. Immunotherapy in breast cancer. Int J Mol Sci 2024; 25(14): 7517, https://doi.org/10.3390/ijms25147517.
- Pruszynski M., Leszczuk E., Radchenko V., John K., Bruchertseifer F., Morgenstern A., D’huyvetter M., Lahoutte T. Anti-HER2 nanobody labeled with 225Ac as a potential radiopharmaceutical for TRT. Eur J Nucl Med Mol Imaging 2016; 43(Suppl 1): S177.
- Jin B.K., Odongo S., Radwanska M., Magez S. NANOBODIES®: a review of diagnostic and therapeutic applications. Int J Mol Sci 2023; 24(6): 5994, https://doi.org/10.3390/ijms24065994.
- Manning D., Santana L.F. Regulating voltage-gated ion channels with nanobodies. Nat Commun 2022; 13(1): 7557, https://doi.org/10.1038/s41467-022-35027-5.
- Bridoux J., Broos K., Lecocq Q., Debie P., Martin C., Ballet S., Raes G., Neyt S., Vanhove C., Breckpot K., Devoogdt N., Caveliers V., Keyaerts M., Xavier C. Anti-human PD-L1 nanobody for immuno-PET imaging: validation of a conjugation strategy for clinical translation. Biomolecules 2020; 10(10): 1388, https://doi.org/10.3390/biom10101388.
- Zhao L., Gong J., Liao S., Huang W., Zhao J., Xing Y. Preclinical evaluation and preliminary clinical study of 68Ga-NODAGA-NM-01 for PET imaging of PD-L1 expression. Cancer Imaging 2025; 25(1): 6, https://doi.org/10.1186/s40644-025-00826-8.
- Vosjan M.J., Perk L.R., Roovers R.C., Visser G.W., Stigter-van Walsum M., van Bergen En Henegouwen P.M., van Dongen G.A. Facile labelling of an anti-epidermal growth factor receptor Nanobody with 68Ga via a novel bifunctional desferal chelate for immuno-PET. Eur J Nucl Med Mol Imaging 2011; 38(4): 753–763, https://doi.org/10.1007/s00259-010-1700-1.
- Gao H., Wu Y., Shi J., Zhang X., Liu T., Hu B., Jia B., Wan Y., Liu Z., Wang F. Nuclear imaging-guided PD-L1 blockade therapy increases effectiveness of cancer immunotherapy. J Immunother Cancer 2020; 8(2): e001156, https://doi.org/10.1136/jitc-2020-001156.
- D'Huyvetter M, Vincke C., Xavier C., Aerts A., Impens N., Baatout S., De Raeve H., Muyldermans S., Caveliers V., Devoogdt N., Lahoutte T. Targeted radionuclide therapy with a 177Lu-labeled anti-HER2 nanobody. Theranostics 2014; 4(7): 708–720, https://doi.org/10.7150/thno.8156.
- Keyaerts M., Xavier C., Heemskerk J., Devoogdt N., Everaert H., Ackaert C., Vanhoeij M., Duhoux F.P., Gevaert T., Simon P., Schallier D., Fontaine C., Vaneycken I., Vanhove C., De Greve J., Lamote J., Caveliers V., Lahoutte T. Phase I study of 68Ga-HER2-nanobody for PET/CT assessment of HER2 expression in breast carcinoma. J Nucl Med 2016; 57(1): 27–33, https://doi.org/10.2967/jnumed.115.162024.
- Gondry O., Caveliers V., Xavier C., Raes L., Vanhoeij M., Verfaillie G., Fontaine C., Glorieus K., De Grève J., Joris S., Luyten I., Zwaenepoel K., Vandenbroucke F., Waelput W., Thyparambil S., Vaneycken I., Cousaert J., Bourgeois S., Devoogdt N., Goethals L., Everaert H., De Geeter F., Lahoutte T., Keyaerts M. Phase II trial assessing the repeatability and tumor uptake of [68Ga]Ga-HER2 single-domain antibody PET/CT in patients with breast carcinoma. J Nucl Med 2024; 65(2): 178–184, https://doi.org/10.2967/jnumed.123.266254.
- D'Huyvetter M., Vos J., Caveliers V., Vaneycken I., Heemskerk J., Duhoux F.P., Fontaine C., Vanhoeij M., Windhorst A.D., Aa F.V., Hendrikse N.H., Eersels J.L.E., Everaert H., Gykiere P., Devoogdt N., Raes G., Lahoutte T., Keyaerts M. Phase I trial of 131I-GMIB-anti-HER2-VHH1, a new promising candidate for HER2-targeted radionuclide therapy in breast cancer patients. J Nucl Med 2021; 62(8): 1097–1105, https://doi.org/10.2967/jnumed.120.255679.
- Shetty D., Lee Y.S., Jeong J.M. (68)Ga-labeled radiopharmaceuticals for positron emission tomography. Nucl Med Mol Imaging 2010; 44(4): 233–240, https://doi.org/10.1007/s13139-010-0056-6.
- Niu T., Fan M., Lin B., Gao F., Tan B., Du X. Current clinical application of lutetium‑177 in solid tumors (review). Exp Ther Med 2024; 27(5): 225, https://doi.org/10.3892/etm.2024.12514.
- Avrov K.O., Shatik S.V., Zaitsev V.V., Al-Shehadat R.I., Shashkova O.A., Terekhina L.A., Malakhov I.S., Samoylovich M.P. Application of magnetic particles for fast determination of immunoreactive fraction of 68Ga-labelled VHH antibodies to PD-L1. Sovremennye tehnologii v medicine 2023; 15(3): 26–33, https://doi.org/10.17691/stm2023.15.3.03.
- Shashkova O.A., Terekhina L.A., Malakhov I.S., Pinevich A.A., Vartanyan N.L., Avrov K.O., Krutetskaya I.Yu., Gryazeva I.V., Berlina M.A., Stolbovaya A.Yu., Smirnov I.V., Fedorenko S.V., Krylova A.A., Nadporojskii M.A., Shatik S.V., Stanzhevskii A.A., Samoilovich M.P. Cell model for testing pharmaceuticals targeting human PD-L1. Sovremennye tehnologii v medicine 2024; 16(5): 5, https://doi.org/10.17691/stm2024.16.5.01.
- Chigoho D.M., Bridoux J., Hernot S. Reducing the renal retention of low- to moderate-molecular-weight radiopharmaceuticals. Curr Opin Chem Biol 2021; 63: 219–228, https://doi.org/10.1016/j.cbpa.2021.06.008.
- Vegt E., de Jong M., Wetzels J.F., Masereeuw R., Melis M., Oyen W.J., Gotthardt M., Boerman O.C. Renal toxicity of radiolabeled peptides and antibody fragments: mechanisms, impact on radionuclide therapy, and strategies for prevention. J Nucl Med 2010; 51(7): 1049–1058, https://doi.org/10.2967/jnumed.110.075101.
- Allen K.J.H., Jiao R., Malo M.E., Frank C., Dadachova E. Biodistribution of a radiolabeled antibody in mice as an approach to evaluating antibody pharmacokinetics. Pharmaceutics 2018; 10(4): 262, https://doi.org/10.3390/pharmaceutics10040262.
- Rasaneh S., Rajabi H., Babaei M.H., Johari Daha F. Synthesis and biodistribution studies of 177Lu-trastuzumab as a therapeutic agent in the breast cancer mice model. J Label Compd Radiopharm 2010; 53(9): 575–579, https://doi.org/10.1002/jlcr.1780.
- Glatt D.M., Beckford Vera D.R., Parrott M.C., Luft J.C., Benhabbour S.R., Mumper R.J. The interplay of antigen affinity, internalization, and pharmacokinetics on CD44-positive tumor targeting of monoclonal antibodies. Mol Pharm 2016; 13(6): 1894–1903, https://doi.org/10.1021/acs.molpharmaceut.6b00063.
- Vivier D., Sharma S.K., Zeglis B.M. Understanding the in vivo fate of radioimmunoconjugates for nuclear imaging. J Labelled Comp Radiopharm 2018; 61(9): 672–692, https://doi.org/10.1002/jlcr.3628.
- Roopenian D.C., Akilesh S. FcRn: the neonatal Fc receptor comes of age. Nat Rev Immunol 2007; 7(9): 715–725, https://doi.org/10.1038/nri2155.
- Bournazos S., Gupta A., Ravetch J.V. The role of IgG Fc receptors in antibody-dependent enhancement. Nat Rev Immunol 2020; 20(10): 633–643, https://doi.org/10.1038/s41577-020-00410-0.
- Rodriguez C., Sarrett S.M., Sebastiano J., Delaney S., McGlone S.A., Hosny M.M., Thau S., Bournazos S., Zeglis B.M. Exploring the interplay between radioimmunoconjugates and Fcγ receptors in genetically engineered mouse models of cancer. ACS Pharmacol Transl Sci 2024; 7(11): 3452–3461, https://doi.org/10.1021/acsptsci.4c00275.
- Fu R., Carroll L., Yahioglu G., Aboagye E.O., Miller P.W. Antibody fragment and affibody immunoPET imaging agents: radiolabelling strategies and applications. ChemMedChem 2018; 13(23): 2466–2478, https://doi.org/10.1002/cmdc.201800624.
- Altunay B., Morgenroth A., Beheshti M., Vogg A., Wong N.C.L., Ting H.H., Biersack H.J., Stickeler E., Mottaghy F.M. HER2-directed antibodies, affibodies and nanobodies as drug-delivery vehicles in breast cancer with a specific focus on radioimmunotherapy and radioimmunoimaging. Eur J Nucl Med Mol Imaging 2021; 48(5): 1371–1389, https://doi.org/10.1007/s00259-020-05094-1.
- Long X., Cheng S., Lan X., Wei W., Jiang D. Trends in nanobody radiotheranostics. Eur J Nucl Med Mol Imaging 2025; 52(6): 2225–2238, https://doi.org/10.1007/s00259-025-07077-6.
- Molitoris B.A., Sandoval R.M., Yadav S.P.S., Wagner M.C. Albumin uptake and processing by the proximal tubule: physiological, pathological, and therapeutic implications. Physiol Rev 2022; 102(4): 1625–1667, https://doi.org/10.1152/physrev.00014.2021.
- Bendre S., Zhang Z., Kuo H.T., Rousseau J., Zhang C., Merkens H., Roxin Á., Bénard F., Lin K.S. Evaluation of Met-Val-Lys as a renal brush border enzyme-cleavable linker to reduce kidney uptake of 68Ga-labeled DOTA-conjugated peptides and peptidomimetics. Molecules 2020; 25(17): 3854, https://doi.org/10.3390/molecules25173854.
- Wang X., Teng F., Kong L., Yu J. PD-L1 expression in human cancers and its association with clinical outcomes. Onco Targets Ther 2016; 9: 5023–5039, https://doi.org/10.2147/OTT.S105862.
- Zanello A., Bortolotti M., Maiello S., Bolognesi A., Polito L. Anti-PD-L1 immunoconjugates for cancer therapy: are available antibodies good carriers for toxic payload delivering? Front Pharmacol 2022; 13: 972046, https://doi.org/10.3389/fphar.2022.972046.
- Luna-Gutiérrez M., Azorín-Vega E., Oros-Pantoja R., Ocampo-García B., Cruz-Nova P., Jiménez-Mancilla N., Bravo-Villegas G., Santos-Cuevas C., Meléndez-Alafort L., Ferro-Flores G. Lutetium-177 labeled iPD-L1 as a novel immunomodulator for cancer-targeted radiotherapy. EJNMMI Radiopharm Chem 2025; 10(1): 5, https://doi.org/10.1186/s41181-025-00328-9.
- Elster N., Collins D.M., Toomey S., Crown J., Eustace A.J., Hennessy B.T. HER2-family signalling mechanisms, clinical implications and targeting in breast cancer. Breast Cancer Res Treat 2015; 149(1): 5–15, https://doi.org/10.1007/s10549-014-3250-x.
- Ertveldt T., De Beck L., De Ridder K., Locy H., de Mey W., Goyvaerts C., Lecocq Q., Ceuppens H., De Vlaeminck Y., Awad R.M., Keyaerts M., Devoogdt N., D'Huyvetter M., Breckpot K., Krasniqi A. Targeted radionuclide therapy with low and high-dose lutetium-177-labeled single domain antibodies induces distinct immune signatures in a mouse melanoma model. Mol Cancer Ther 2022; 21(7): 1136–1148, https://doi.org/10.1158/1535-7163.MCT-21-0791.
- Nilofar Danishmalik S., Lee S.H., Sin J.I. Tumor regression is mediated via the induction of HER263-71-specific CD8+ CTL activity in a 4T1.2/HER2 tumor model: no involvement of CD80 in tumor control. Oncotarget 2017; 8(16): 26771–26788, https://doi.org/10.18632/oncotarget.15816.