Диагностический потенциал новых маркеров системного воспаления (MLR, SIRI, CAR, dNLR, ALB/dNLR) в прогнозировании тяжести патогенетических признаков ревматоидного артрита
Цель исследования — гистологически обосновать диагностический потенциал новых биомаркеров системного воспаления (MLR, SIRI, CAR, dNLR, ALB/dNLR) в оценке выраженности ревматоидного артрита (РА), сформированного у теплокровных животных с генетически обусловленной резистентностью к гипоксии.
Материалы и методы. Модель аутоиммунного РА (опытные группы) формировали подкожным введением полного адъюванта Фрейнда в правую заднюю конечность самцам 8-месячных крыс линий, имеющих высокую (ВУ/SmY) и низкую (НУ/SmY) резистентность к гипоксии. Крысам контрольных групп вводили растворители. Через 35 дней у всех крыс из сердца отбирали кровь. Для расчета новых биомаркеров воспаления — CAR, ALB/dNLR, SIRI, dNLR, NC/LС, MLR — использовали следующие лабораторные показатели: ALB (альбумин), СРБ (C-реактивный белок), MC (моноциты), LC (лимфоциты) и NC (нейтрофилы). Эффективность оценки тяжести заболевания с помощью биомаркеров определяли по результатам гистологического исследования плантарных срезов заплюсневых и плюснефаланговых суставов контрольных и опытных крыс.
Результаты. Генетически обусловленная резистентность к гипоксии является важным фактором в манифестации патогенетических механизмов РА. В случае низкой устойчивости организма к гипоксии наблюдается развитие более тяжелых форм патологии соединительной ткани, чем при высокой устойчивости: НУ/ВУ — 164 балла/113 баллов, p≤0,05. Тяжесть патоморфологических изменений при РА (с учетом устойчивости организма к гипоксии), выявленную гистологически (степень дегенерации хряща НУ/ВУ — 29 баллов/18 баллов, p≤0,01; общее воспаление сустава НУ/ВУ — 37 баллов/26 баллов, p≤0,01; остеолизис НУ/ВУ — 6 баллов/0 баллов, p≤0,01), наиболее эффективно отображали следующие интегральные индексы воспаления: CAR (НУ/ВУ — 11,55·10–6 ед./12,73·10–6 ед.), ALB/dNLR (НУ/ВУ — 86,93 ед./78,51 ед.) и SIRI (НУ/ВУ — 0,14 ед./0,19 ед.).
Заключение. Выраженность патоморфологических признаков РА зависит от генетически обусловленной резистентности к гипоксии. Для эффективного прогнозирования заболевания, риска осложнений и результативности назначенного лечения целесообразно использовать новые биомаркеры системного воспаления CAR, ALB/dNLR и SIRI.
Введение
Ревматоидный артрит (РА) занимает 42-е место в мире по степени инвалидизации населения, вызывая стойкую потерю трудоспособности у половины пациентов при стаже заболевания 3–5 лет. Являясь системным иммуновоспалительным заболеванием соединительной ткани, РА демонстрирует многочисленные генетические полиморфизмы, связанные сВ- и Т-клетками, а также сопровождается прогрессирующей деструкцией суставов и поражением внутренних органов. Высокий риск снижения продолжительности жизни больных (в среднем на 10 лет) прогнозируется за счет развития коморбидных заболеваний [1].
Патогенетические механизмы заболевания связаны с изменением врожденной иммунной реактивности организма, наличием аберрантной взаиморегуляции Т- и В-клеток, нарушением баланса между синтезом провоспалительных и антивоспалительных цитокинов, поляризацией иммунного ответа по типам Тh1 иTh17. Образование аутоантител, идентифицирующих посттрансляционно модифицированные цитруллинированные белки, а также индукция специфичных к карбамилированным и ацетилированным пептидам аутоантител опосредуют развитие синовита. Хемокины, вырабатывающиеся в макрофагах, лимфоцитах, клетках соединительной ткани и эпителия, способствуют миграции иммунных клеток (Т-лимфоцитов, В-лимфоцитов, плазматических клеток, макрофагов, тучных клеток, активированных стромальных клеток и синовиальных фибробластов) вместа воспаления, где активированные стромальные клетки синовиальных фибробластов стимулируют развитие гиперплазии синовиальной оболочки и образование паннуса. В разрушенном внеклеточном матриксе воспаленной ткани отмечается присутствие инфильтрирующих Т-, В-лимфоцитов, плазматических и тучных клеток, макрофагов. Гиперпродукция провоспалительных цитокинов (IL-1, IL-6 и IL-17, ФНО-α) способствует активации хондроцитов, экспрессии матриксных металлопротеиназ, деградации компонентов белкового внеклеточного матрикса и аггреканаз, что стимулирует процессы деструкции хряща и увеличения костно-резорбтивной активности остеокластов [2, 3].
Поскольку этиология РА неизвестна, проведение эффективной этиотропной терапии заболевания на данный момент затруднено и представляется одной из сложных проблем современной клинической медицины и фармакологии, требующих решения. Сегодня частота ответа на применение терапевтических схем лечения РА редко превышает порог в 60%. В исследованиях А.А. Абрамкина и соавт. [4] сообщается, что за пятилетний период терапии устойчивой ремиссии достигли всего 26,5% больных, удовлетворительный ответ показали 44,6% пациентов, не ответили на лечение 28,9%.
Несмотря на гетерогенность этиологических аспектов РА и механизмов его развития, а также наличие широкого спектра фенотипов и эндотипов, объединяющим объективным критерием патогенетической родственности симптомов заболевания является наличие синовиальной гипоксии [5]. По данным J. Falconerс соавт. [6], напряжение кислорода в суставе больного РА более чем в 8 раз (<1%) ниже, чем у здорового человека. Согласно L. Wangс соавт. [5], содержание кислорода в образцах синовиальной жидкости коленных суставов больных РА значительно ниже (в некоторых случаях — 0 мм рт. ст.) по сравнению с пробами пациентов с остеоартрозом и пациентов с травматическими экссудатами. Являясь постоянным признаком РА, синовиальная гипоксия способствует прогрессированию болезни. Индуцируемые гипоксией факторы оказывают прямое или косвенное воздействие на реализацию каждого из патогенетических звеньев заболевания, включая окислительное повреждение клеток, иммуновоспалительные процессы, ангиогенез, деструкцию хряща, резорбцию костной ткани и развитие коморбидных состояний [7].
В последнее время исследуется возможность новых высокотехнологичных подходов с использованием методов лучевой диагностики в области оценки активности РА с учетом динамики значений оксигенации пораженной синовиальной ткани. Обнадеживающие результаты исследований опубликованы в 2023–2024 гг. двумя независимыми научными группами. Используя методы фотоакустической визуализации гипоксии [8] и мультимодальной магнитно-резонансной томографии/ультразвуковой визуализации пораженных суставов [9], исследователи выявили наличие корреляции между снижением содержания кислорода в синовиальной жидкости, стандартными клиническими показателями и более высокой активностью заболевания у пациентов с РА.
Необходимо учитывать, что резистентность к гипоксии является генетически обусловленной индивидуальной характеристикой организма, детерминирующей действие его физиологических механизмов, а также риски развития и тяжесть манифестации воспалительных, сердечно-сосудистых и нейродегенеративных заболеваний, в том числе в зависимости от условий окружающей среды [10]. По данным И.В. Зарубиной [11], 80–95% линейных крыс линии Wistarобладают низкой толерантностью к гипоксии, асреди крыс линии Август преобладающее большинство — высокорезистентные животные.
В человеческой популяции резистентность к гипоксии неоднородна и генетически предопределена [12–15]. Достоверных маркеров на устойчивость к гипоксии, применяемых в клинической практике, на данный момент не существует. В доклинических исследованиях предпринимаются попытки оценить толерантность организма к недостаточной оксигенации по индексам, вычисленным на основе стандартных гематологических показателей. Опираясь на эти показатели, М.В. Кондашевская с соавт. [16] выявили в популяции крыс линии Wistar 30% животных, высокоустойчивых к гипоксии (ВУ), 40% — низкоустойчивых (НУ) и 30% — среднеустойчивых. Следовательно, разработка новых эффективных подходов кдиагностике и терапии РА требует обязательного учета комплексной роли гипоксии и резистентности к ней в патогенезе заболевания.
Американская коллегия ревматологов (ACR), Европейский альянс ассоциаций ревматологов (EULAR) и Ассоциация ревматологов России рекомендуют проводить оценку активности РА с использованием одной из доступных шкал: DAS28, CDAI, SDAI, RAPID3, PAS-II. Поскольку основным классификационным критерием тяжести РА является визуально подтвержденное воспаление синовиальных суставов (синовит), ключевым показателем эффективности лечения служит оценка динамики активности воспаления. В число классификационных критериев РА, позволяющих определить индекс активности заболевания, входят показатели скорости оседания эритроцитов (СОЭ) и концентрации С-реактивного белка (СРБ) (DAS28 — СОЭ, СРБ; SDAI — СРБ), отражающие локальный и системный воспалительный процесс при РА [3].
Представленные выше высокотехнологичные методы визуализации позволяют точно определить тяжесть патологических процессов при РА, однако требуют больших временных и материальных ресурсов, а существующие неточности и ограничения стандартных лабораторных маркеров заболевания зачастую недостаточно отражают активность РА [17–19]. Все это обусловливает необходимость поиска надежных и легко вычисляемых биомаркеров. В настоящее время в научной литературе появились публикации [20–29], указывающие на возможность более эффективной диагностики воспалительной активности с использованием индексов общего системного воспаления по сравнению с общепринятыми лабораторными показателями. Индексы общего системного воспаления (MLR, AISI SIRI, CAR, dNLR, ALB/dNLR) рассчитываются на основе результатов общего анализа крови.
В отличие от широко представленных исследований о роли новых биомаркеров системного воспаления в прогнозировании характера течения кардиоваскулярных заболеваний [20–23], исследований в области терапии аутоиммунных патологий, включая РА, недостаточно [24–28]. В российском сегменте доступной нам литературы клинические исследования ограничиваются данными, представленными в работе Ю.В. Муравьева и соавт. [29]. При этом доклинических исследований, гистологически подтверждающих или опровергающих соответствие степени выраженности воспаления в синовиальных суставах новым биомаркерам системного воспаления, нами не зафиксировано.
Поскольку персонализированный подход в здравоохранении предполагает оптимизацию диагностики, терапии и профилактики заболеваний с учетом индивидуальных особенностей пациента, интерес представляет оценка роли генетически обусловленной резистентности к гипоксии.
Цель исследования — гистологически обосновать диагностический потенциал новых биомаркеров системного воспаления (MLR, SIRI, CAR, dNLR, ALB/dNLR) в оценке выраженности ревматоидного артрита, сформированного у теплокровных животных с генетически обусловленной резистентностью к гипоксии.
Материалы и методы
Исследования проводили на базе Института биомедицинских исследований ВНЦ РАН. Работа согласована с локальным этическим комитетом и соответствует сводам правил и этических норм, касающихся содержания лабораторных животных и ухода за ними, сформулированных в руководстве National Research Council (2011) и ГОСТ 33044-2014 «Принципы надлежащей лабораторной практики».
Животных содержали в стандартных условиях вивария с 12-часовой сменой светового режима исвободным доступом к воде и пище.
Дизайн эксперимента: модель аутоиммунного РА воспроизводили на 8-месячных самцах крыс линий ВУ/SmY (высокоустойчивые к гипоксии) и НУ/SmY (низкоустойчивые к гипоксии), произведенных в филиале «Андреевка» ФГБУН НЦБМТ ФМБА России. Перед началом исследований крысы прошли акклиматизацию в течение 30 дней. Сформированы 4 экспериментальные группы из животных весом 400–450 г (по 12 крыс в каждой): контрольная группа 1 — линия НУ/SmY; контрольная группа 2 — линия ВУ/SmY; опытная группа 3 — линия НУ/SmY; опытная группа 4 — линия ВУ/SmY. Крысам опытных групп индуцировали развитие аутоиммунного РА. Для этого подкожно в правую заднюю конечность вводили полный адъювант Фрейнда (Difco Laboratories, США) из расчета 0,1 мл на 200 г массы тела. Крысам контрольных групп аналогично вводили в качестве растворителя вазелиновое масло (жидкий парафин) из расчета 0,1 мл на 200 г массы тела [30]. Длительность исследований составляла 35 дней.
По окончании эксперимента у животных под общим наркозом из сердца отбирали кровь, после чего осуществляли эвтаназию в СО2-затравочной камере. Пробы крови анализировали на гематологическом анализаторе Abacus Vet 5 (Diatron, Австрия) и биохимическом анализаторе ChemWell-T (Awareness Technology Inc., США) для определения концентрации СРБ и альбумина, применяя биохимические наборы реагентов фирмы «Ольвекс Диагностикум» (Россия). Использование сертифицированного оборудования и регулярные проверки калибровки гарантировали точность выполненных измерений. Для расчета индексов системного воспаления измеряли следующие лабораторные показатели: ALB — уровень сывороточного альбумина, г/л; CRP — уровень СРБ, г/л; MC — количество моноцитов, %; LC — количество лимфоцитов, %; NC — количество нейтрофилов, %.
Формулы для расчета индексов воспаления [31–33]:
MLR = MC : LC;
SIRI = NC · MC : LC;
CAR = CRP : ALB;
NC/LC = NC : LC;
dNLR = NC : (LC–NC);
ALB/dNLR = ALB : dNLR.
Для гистологического исследования заплюсневых и плюснефаланговых суставов крыс (плантарные срезы) ампутировали части тазовых конечностей на уровне 1/3 голени и помещали их в 10% нейтральный раствор формалина. Декальцинацию проводили в течение двух недель в электролитном растворе на основе муравьиной и соляной кислот. Препараты готовили стандартным методом, окрашивали гематоксилином и эозином и анализировали в поле зрения светового микроскопа Primo Star (ZEISS, Германия) с цифровой камерой (видеоокуляр) ToupCam 9.0 MP (ToupCam, Китай) при увеличении 40, 100, 400, 1000. Изображения обрабатывали с использованием программного обеспечения ToupView.
Степень манифестации патогенетических признаков РА определяли по модифицированной шкале M. Hegen и соавт. [34], представленной в работе А.А. Мужикяна с соавт. [35]. Деструктивные изменения фиброзной и синовиальной капсулы оценивали в баллах (от 0 до 5) по следующим параметрам: наличие инфильтрата и выпота, характеризующее общее воспаление сустава; степень сужения суставной щели; степень резорбции костного матрикса остеокластами (остеолизис); увеличение числа клеточных элементов синовиальной оболочки (гиперплазия). Степень разрушения хряща оценивали по наличию структурных изменений поверхности хряща (неровности, трещины, расслоение), снижению степени его окрашивания и уровню пролиферативной активности хондроцитов (соотношение изогенных хондроцитов к группам из 2–3 и более клеток).
Статистическая обработка данных. Полученные результаты сравнивали, обработав в программе Statistica (StatSoft, США). Нормальность распределения признака определяли с помощью критерия Шапиро–Уилка (n<50). Поскольку распределение отличалось от нормального, для сравнения статистических гипотез использовали непараметрический U-критерий Манна–Уитни. Медиану частоты параметра определяли с интерквартильным размахом — Me [25; 75]. Статистическую значимость различий показателей оценивали между контрольной и опытной группами (1/3; 2/4); между контрольными группами (1/2); между опытными группами (3/4). Статистически значимой считали разницу между выборками при p≤0,05. Для оценки связи между показателями использовали коэффициент корреляции Пирсона (rxy). Исходя из полученного значения rxy определяли тесноту связи по шкале Чеддока и ее направление (прямая или обратная).
Результаты
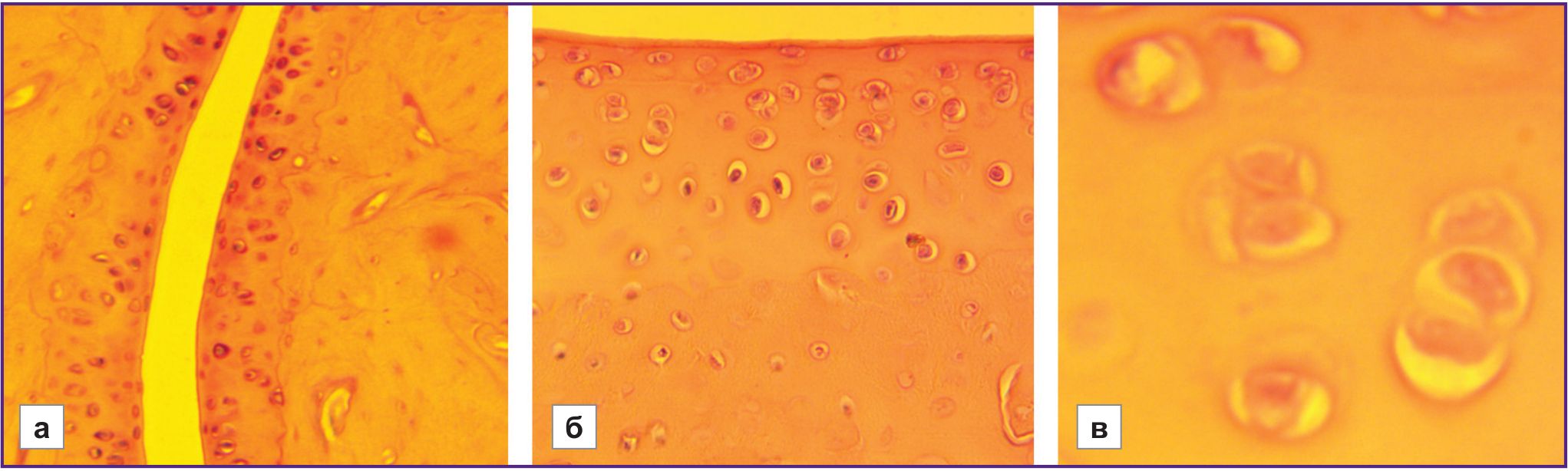
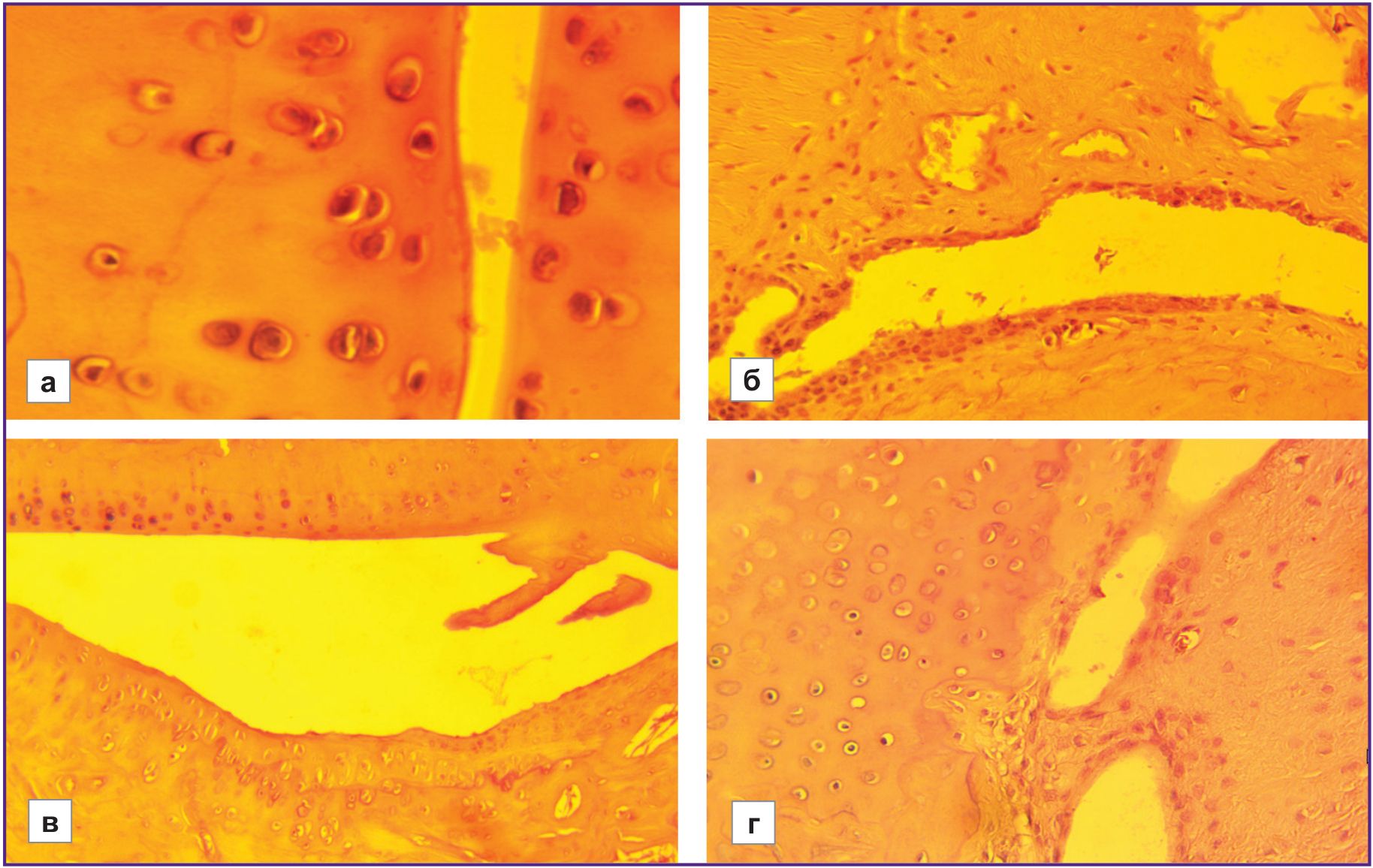
В контрольных группах крыс с разной резистентностью к гипоксии была исследована гистоархитектоника тканей суставного аппарата задних конечностей крыс, образованных плюсневыми костями, проксимальными, средними и дистальными фалангами. Образцы не имели патологических изменений (рис. 1).
В каждой из опытных групп отмечено наличие воспалительного процесса в суставах — НУ/ВУ=1,4 (р≤0,01) (табл. 1).
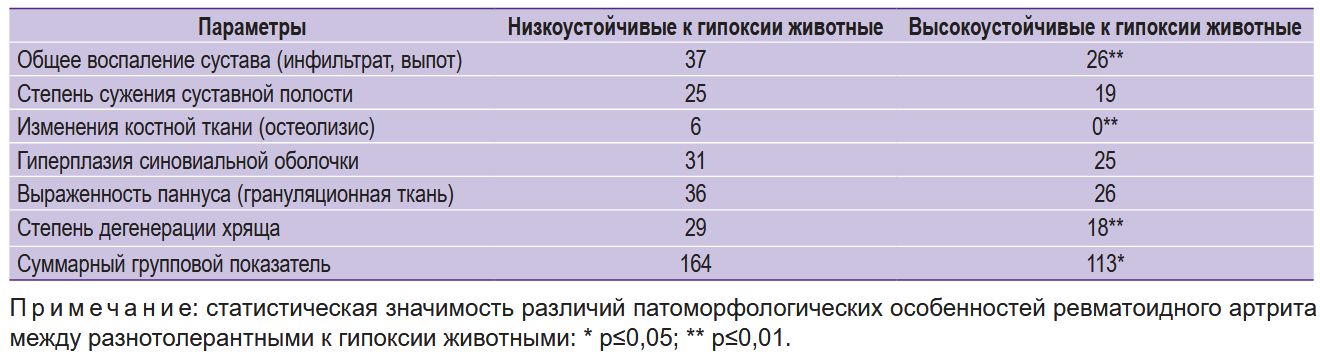 |
Таблица 1. Патоморфологические характеристики адъювантного ревматоидного артрита, индуцированного у крыс с разной толерантностью к гипоксии, баллов |
Периваскулярный инфильтрат представлен лимфоцитами и плазматическими клетками. Степень пролиферации и гиперплазии синовиальной оболочки варьировала от умеренной до выраженной (НУ/ВУ=1,2). Формирование паннуса осуществлялось за счет пролиферации рыхлой грануляционной ткани, в которой на фоне усиленного ангиогенеза отмечалось присутствие макрофагов, нейтрофилов и эозинофилов. При более тяжелых формах патологии отмечено врастание паннуса в субинтимальную оболочку фиброваскулярного синовиального слоя разной степени выраженности (НУ/ВУ=1,4). Суставные щели имели патологическое сужение (уровень от минимального до умеренного), признаки деформаций и фиброзных анкилозов (НУ/ВУ=1,3).
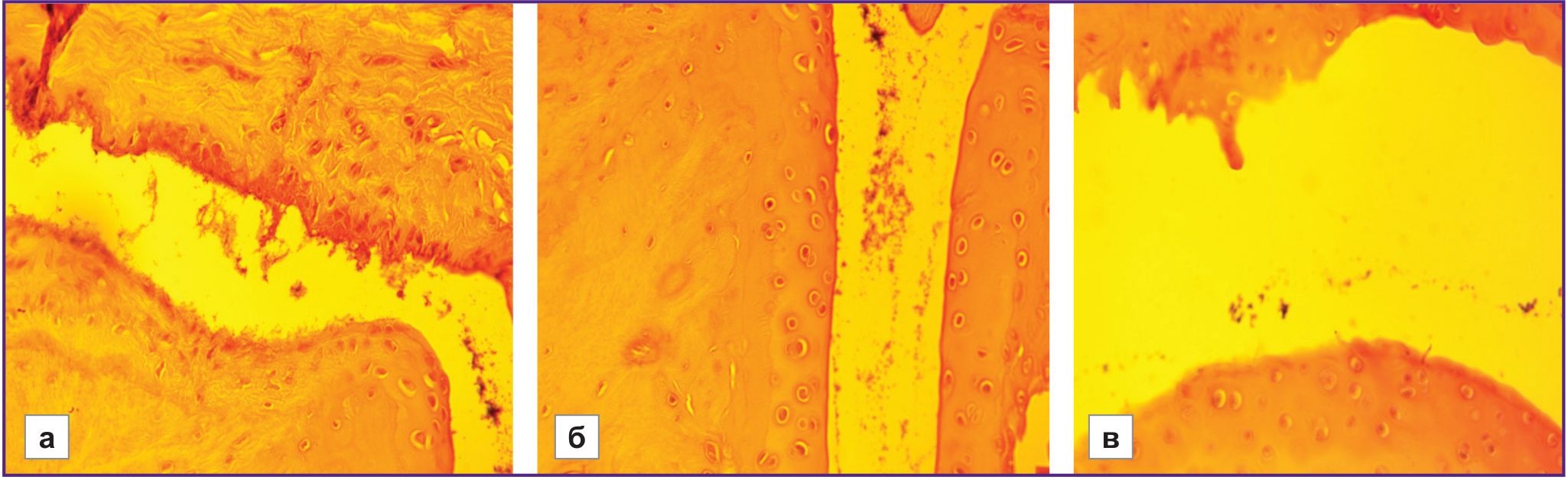
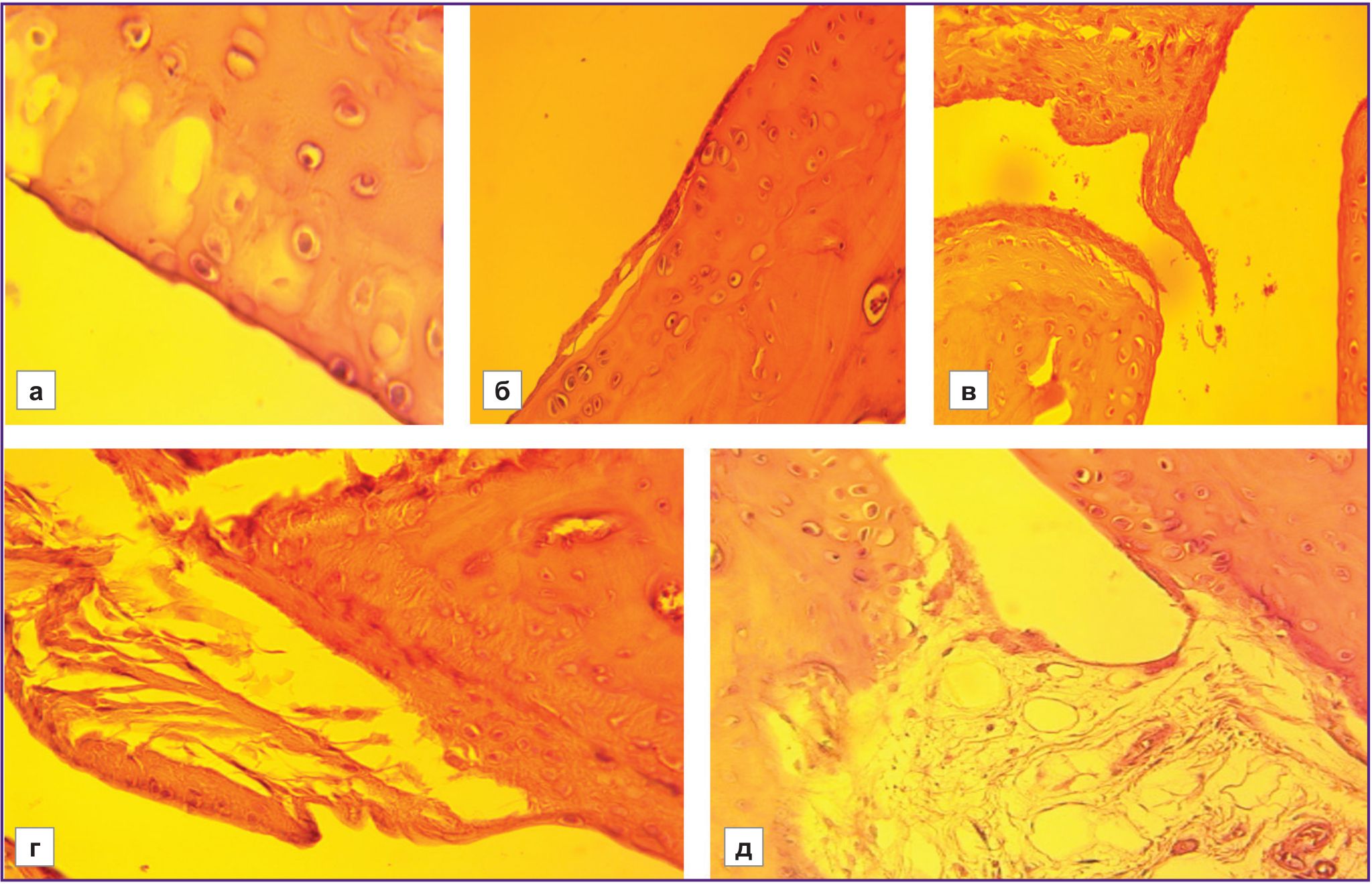
Степень дегенеративных изменений хряща в группе животных с низкой устойчивостью к гипоксии статистически значимо превосходит таковую у высокоустойчивых (НУ/ВУ=1,61, р≤0,01). Изменения имеют градацию от начальных этапов замещения грануляционной ткани на зрелую фиброзную, а также от поверхностных эрозий и очаговой вакуолизации матрикса до признаков разволокнения соединительной ткани, разуплотнения межклеточного вещества вокруг изогенных групп хондроцитов, образования узур и трещин, а также формирования анкилоза (рис. 2–4).
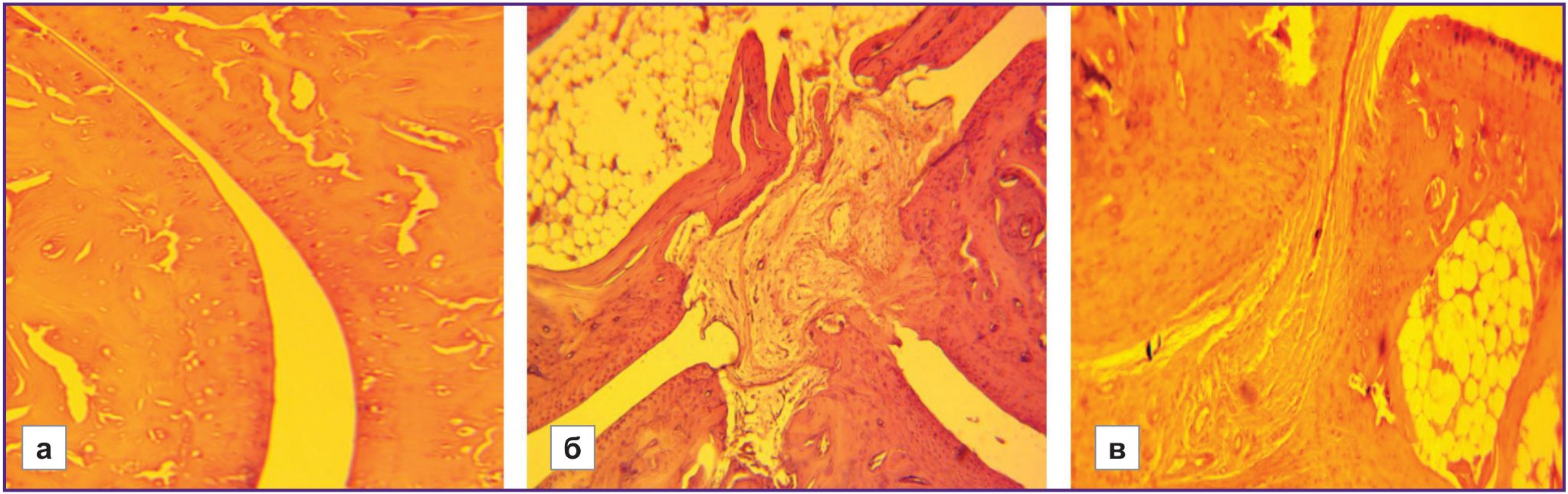
У животных с низкой устойчивостью к гипоксии на фоне более тяжелых дегенеративных изменений хряща отмечались очаги с остеопорозом, не встречающиеся у высокоустойчивых крыс (НУ/ВУ— 6 баллов/0 баллов). Гистоархитектоника соединительной ткани высокорезистентных к гипоксии животных сохранена в большей степени, чем у низкорезистентных (рис. 5). Поверхности суставов в большей степени ровные, у отдельных животных наблюдаются незначительное разволокнение хряща и признаки сужения суставных полостей. Границы между слоями сохранены. Хондроциты в зоне зрелого хряща расположены в виде правильных изогенных групп. Незначительный фиброзный анкилоз отмечен у 2 животных из 12.
Суммарный групповой показатель тяжести патоморфологических признаков РА по группе НУ крыс превышает таковой у ВУ животных в 1,5 раза (р≤0,05). Внутригрупповая гистологическая выраженность патоморфологических изменений при РА сформирована на основе индивидуальных показателей по каждому животному и представлена в табл. 2.

|
Таблица 2. Внутригрупповая градация индивидуальных показателей гистологической выраженности патоморфологических признаков ревматоидного артрита у крыс с разной толерантностью к гипоксии |
Максимально возможный уровень тяжести заболевания (критический) для одного животного по шкале Hegen–Мужикян составляет 30 баллов. В нашем исследовании максимальная выраженность патогенетических признаков РА соответствовала уровню «значительный» и была характерна для половины НУ особей (6 из 12). В группе ВУ особей, являющейся лидером по количеству животных с незначительной выраженностью патологии (7 из 12), такие признаки полностью отсутствовали.
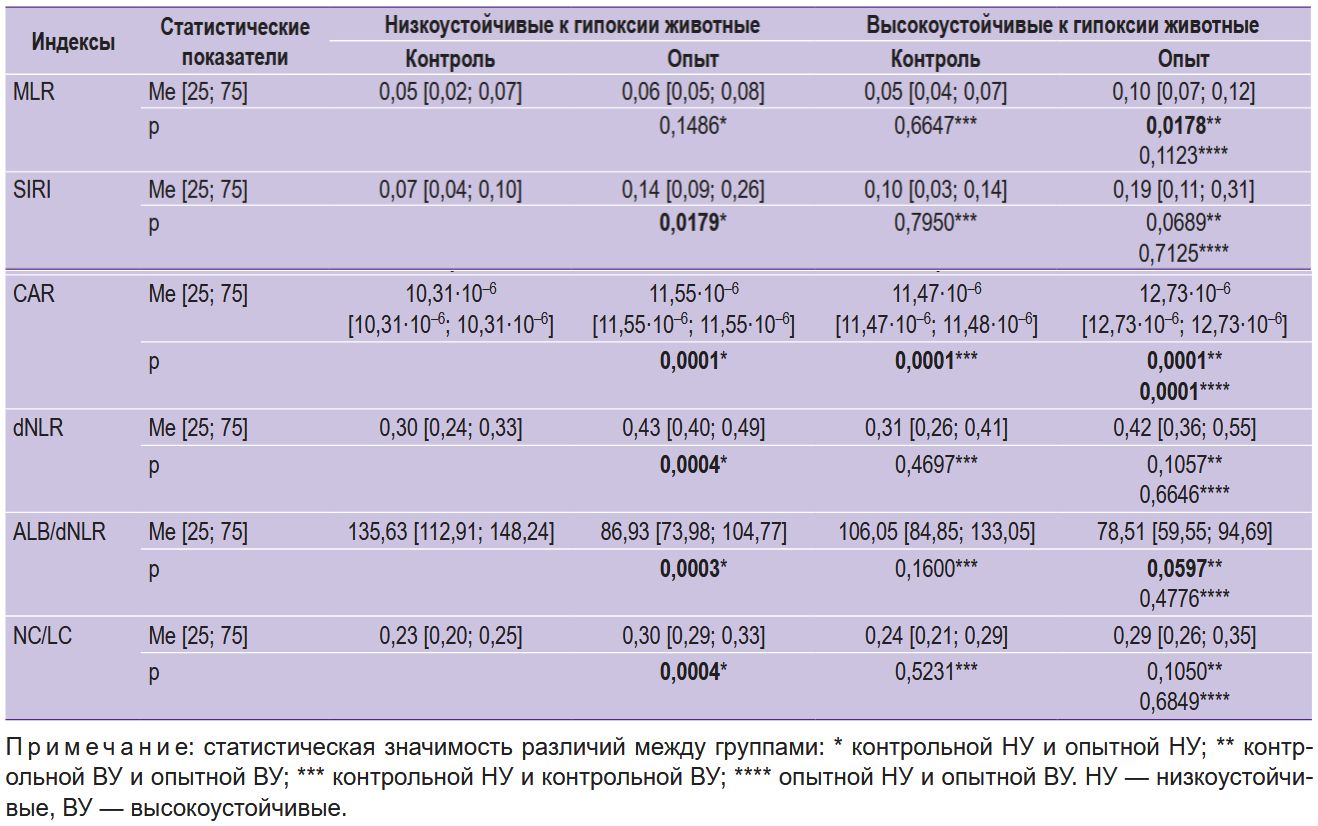
Диагностический потенциал новых маркеров системного воспаления (табл. 3) оценивали согласно результатам гистологического исследования, представленным в табл. 1, 2.
|
Таблица 3. Динамика лабораторных индексов у крыс с высокой и низкой резистентностью к гипоксии в контроле и в группах с модельным ревматоидным артритом |
Обсуждение
Синовиальная гипоксия, являясь постоянным признаком РА, активирует механизмы, позволяющие организму адаптироваться в условиях дисбаланса между потребностью тканей в кислороде и его поступлением в тканевую среду. Субъединица индуцируемого гипоксией транскрипционного комплекса HIF, — фактор HIF-2α, экспрессируясь в фибробластоподобных синовиоцитах больных РА, играет фундаментальную роль в патогенезе заболевания. Участвуя в регуляции воспалительного процесса, HIF-2α потенцирует возрастание экспрессии лиганда рецептора ядерного фактора NF-κB, который контролирует экспрессию генов, связанных с регуляцией иммунного ответа, апоптозом и клеточным циклом, а также индукцию нескольких катаболических факторов и активацию пролиферационного и остеокластогенного потенциала клеток паннуса [36].
Вместе с тем низкорезистентные крысы, обладающие генетически предопределенным высоким уровнем HIF-1α, формирующимся в ответ на гипоксические условия среды, имеют более высокую напряженность на клеточное звено иммунитета. Этому способствует опосредованная HIF-1α более высокая экспрессия генов NF-κB, что обусловливает усиление продукции молекул адгезии, хемокинов, а также миграцию и снижение количества нейтрофилов, вступающих в апоптоз [37, 38]. Экспериментальное подтверждение участия HIFв патогенезе РА получено Y.H. Huhс соавт. [39] в модели мышиного артрита: индукция хондроцитов HIF-2α вследствие инициации выработки хемокинов, стимулирующих миграцию и инвазию синовиальных фибробластов, способствовала эрозии хрящевой ткани.
В нашем исследовании получено гистологическое подтверждение аддитивному и синергетическому взаимодействию NF-kBи HIF, которое выразилось в большей амплитуде воспалительных процессов у НУ животных в сравнении с ВУ. Значительный уровень выраженности патоморфологических изменений соединительной ткани наблюдался у 6 из 12 НУ особей, тогда как в группе ВУ такие изменения не зафиксированы. Вместе с тем 7 из 12 ВУ крыс характеризовались незначительным проявлением патологии, которое в группе НУ было в 2,3 раза ниже (3 из 12).
Суммарный показатель патоморфологических изменений тканей сустава у НУ крыс — в 1,5 раза выше, чем у ВУ (164 балла/113 баллов, р≤0,05); показатели общего воспаления, включающие наличие инфильтрата в суставной полости, — в 1,4 раза (37 баллов/26 баллов, р≤0,01). Подобная тенденция отмечалась и в значениях других показателей (соответственно степень сужения суставной полости — 25баллов/19 баллов; гиперплазия синовиальной оболочки — 31 балл/25 баллов; наличие паннуса — 36 баллов/26 баллов).
Разрушение хряща при РА связано с повышением экспрессии матриксных металлопротеиназ (MMPs), активность которых регулируется эндогенными тканевыми ингибиторами (TIMPs). В условиях гипоксической среды экспрессия MMP-1 и MMP-3 в ревматоидных синовиальных фибробластах повышается, в то время как TIMP-1 — снижается и на уровне белка, и на уровне мРНК [40]. Исследователи указывают на значимую роль HIF-1α в индуцируемой гипоксией экспрессии IL-8, MMP-1 и MMP-3 в фибробластоподобных синовиоцитах при РА [41]. Следовательно, увеличение соотношения производства MMP-1, MMP-3 к TIMP-1 может способствовать более активному разрушению суставов при нарастании тканевой гипоксии в условиях системного воспаления при РА. Нами получено косвенное подтверждение представленных литературных данных: гистологическое исследование заплюсневых и плюснефаланговых суставов крыс выявило наличие более глубоких признаков деструкции хряща у низкорезистентных животных по сравнению с высокорезистентными. Степень дегенерации хряща у НУ крыс в 1,6 раза превышает таковую у ВУ (29 баллов/18 баллов, р≤0,01).
P.E. Poubelleс соавт. [42] выяснили, что присутствующие в синовиальной жидкости нейтрофилы экспрессируют лиганд рецептора активатора ядерного фактора κB, являющегося фактором дифференцировки остеокластов и запускающего процессы резорбции кости. Поэтому более высокая амплитуда воспалительных процессов с участием нейтрофильных гранулоцитов может быть причиной интенсификации остеолизиса у НУ особей. Проведенный нами гистологический анализ подтвердил данное предположение: изменения костной ткани были зафиксированы только у НУ животных с РА (остеолизис — 6 баллов, р≤0,01).
Исходя из патогенетических механизмов РА, формулы для расчета биомаркеров воспаления обязательно должны учитывать роль клеточного звена иммунитета в патогенезе РА. Индекс MLR, представляющий отношение моноцитов (воспалительное звено) к показателям регуляторных механизмов иммунной системы (Т-, В- лимфоциты, естественные киллеры суммарно), оказался менее информативным, чем индекс системного воспаления SIRI (в формулу входит еще и показатель количества нейтрофилов). Нам удалось показать примерные границы показателя SIRI в норме с учетом устойчивости животных к гипоксии (от 0,07 до 0,10 ед.) и на 35-й день развития патологии — от 0,14 ед. (НУ) (р≤0,01) до 0,19 ед. (ВУ) (p>0,05) (см. табл. 3).При этом значения показателей соотносятся с гистологической выраженностью параметров заболевания в группах животных с высокой и низкой резистентностью к гипоксии.
По литературным данным, индекс воспалительного показателя MLR способен эффективно прогнозировать динамику сердечно-сосудистых заболеваний [33]. В нашем эксперименте MLR не был показательным в оценке различий между НУ и ВУ животными в контроле (0,05 ед.), а значения индексов опытных групп (НУ/ВУ — 0,06 ед./0,10 ед.) при наличии тенденции не отражали достоверно референсную зону данных по интенсивности воспаления и не соответствовали выявленной гистологически градации патоморфологических особенностей РА.
В работе Ю.В. Муравьева с соавт. [29] коэффициент воспаления, вычисленный у больных с РА как отношение нейтрофилов к лимфоцитам, коррелировал с DAS28, уровнем СРБ, СОЭ, в отличие от показателя «тромбоциты/лимфоциты». В нашем исследовании прогностическая ценность индекса NC/LС оказалась минимальной, поскольку не отражала динамику заболевания у животных с разной устойчивостью к гипоксии.
В то же время, поскольку клеточное звено иммунитета (нейтрофилы, лимфоциты) играет важную роль в формировании патогенетических механизмов РА, нами было вычислено производное соотношение нейтрофилов к лимфоцитам — dNLR. Имеются данные о том, что dNLR является негативным прогностическим маркером при различных системных заболеваниях: злокачественных опухолях, рассеянном склерозе, сепсисе [43, 44]. Мониторинг пациентов с РА независимыми группами исследователей показал, что уровень dNLR больных повышен по сравнению с показателями здоровых людей и коррелирует с реактантами острой фазы, DAS28, клиническими показателями и данными ультразвуковых исследований [28, 45–47]. В рамках нашего эксперимента показатели dNLR не имели достоверных различий между группами разнотолерантных к гипоксии здоровых животных (НУ/ВУ — 0,30 ед./0,31 ед.), но указывали на наличие воспалительных процессов при РА в каждой из опытных групп (НУ/ВУ — 0,43 ед./0,42 ед.). Поскольку тяжесть патоморфологических изменений не нашла подтверждения в значении коэффициента для опытных групп животных НУ и ВУ, нами был учтен еще один важный в патогенезе РА биохимический параметр — сывороточный альбумин.
Альбумин участвует в воспалении и является модулятором иммунной системы. Он оказывает влияние на транспорт антител, формирование иммунных комплексов и общую эффективность иммунного ответа; играет важную роль в транспортировке гормонов, метаболитов, лекарственных соединений; поддерживает нормальное онкотическое давление и способствует антиоксидантной защите организма [48]. При обострении РА уровень альбумина снижается в силу его повышенного потребления в очагах воспаления; при достижении ремиссии — имеет тенденцию к повышению. Альбумин играет важную роль в регуляции гуморального звена иммунитета [49]. В условиях воспаления окисленный альбумин служит активатором моноцитов и нейтрофилов [50], способствует запуску ингибитора продукции провоспалительных цитокинов р38 МАРК через сигнальные пути TLR3 и TLR4. Важно отметить, что TLR3 и TLR4 являются активаторами ядерного фактора транскрипции NF-κB, нарушение регуляции которого потенцирует развитие воспаления, индукцию провоспалительных цитокинов (интерфероны I типа), инициацию аутоиммунных процессов, а также способствует развитию онкологических заболеваний [51–53]. Известна роль альбумина в гистоархитектонике соединительной ткани, главными компонентами которой являются фибробласты и межклеточное вещество, представленное белками (в основном коллагеном, альбумином, глобулинами) и углеводами (в основном гликозаминогликанами). Межклеточное вещество образуется за счет продукции коллагенов и гликозаминогликанов фибробластами, а также за счет веществ, поступающих из плазмы крови, таких как альбумины и глобулины [54]. Следовательно, в оценке патоморфологических изменений в суставных тканях при РА целесообразно использовать показатели сывороточного альбумина.
В нашем эксперименте показатель ALB/dNLR имел референсные границы от 106,05 ед. (ВУ) до 135,63 ед. (НУ). В опытных группах значения были ниже контрольных (НУ/ВУ — 86,93 ед./78,51 ед., р≤0,01) и соответствовали гистологическим показателям патологии соединительной ткани. Следовательно, интегральный показатель воспаления ALB/dNLR можно рекомендовать к использованию для прогнозирования РА. Необходимо отметить, что в исследовании S. Ganeb с соавт. [49] в ходе мониторинга пациентов с РА на фоне лечения значения данного показателя у больных были выше, чем у здоровых людей. Противоречивость результатов нашего эксперимента с данными группы S. Ganeb, вероятно, связана с высокой чувствительностью концентрации альбумина к лекарственной терапии, на фоне которой проводилось исследование, поскольку альбумин принимает активное участие в транспорте лекарственных веществ. Понижение индекса в условиях нашего исследования соответствует как физиологической, так и математической логике, поскольку, согласно формуле расчета показателя ALB/dNLR, концентрация сывороточного альбумина, понижающаяся в условиях воспаления при РА, находится в числителе, а возрастающие значения воспалительного индекса dNLR — в знаменателе.
Одним из основных стандартных диагностических лабораторных критериев РА служит уровень СРБ, являющийся ключевым медиатором острой фазы воспаления, который значительно (до 1000 раз) повышается в местах инфекции, травмы, ишемии, воспаления, что позволяет отслеживать активность процесса в динамике. Длительное повышение концентрации СРБ может быть признаком скрытых аутоиммунных заболеваний, воспалительных процессов в кишечнике и суставах, атеросклероза [55]. СРБ не является специфическим маркером РА, но играет важную роль в мониторинге заболевания, поскольку отражает наличие и степень воспалительных реакций в соединительной ткани. Высокий уровень СРБ в начале лечения и во время лечения РА считается неблагоприятным прогностическим признаком и варьируется в зависимости от возраста и тяжести заболевания [56].
Белки как отрицательной (альбумин), так и положительной острой (СРБ) фазы воспаления синтезируются в печени, где бóльшая часть аминокислот используется для синтеза белков положительной фазы, а не альбумина [57].
С учетом сказанного выше можно утверждать, что соотношение показателей СРБ и ALB в индексе системного воспаления CAR может иметь большую прогностическую ценность при РА. Данное предположение подтверждается результатами нашего исследования: CAR имел статистически значимые референсные зоны как у здоровых животных (НУ/ВУ — 10,31·10–6 ед./11,47·10–6 ед.; р≤0,0001), так и у крыс с РА, характеризующихся генетически обусловленной высокой и низкой резистентностью к гипоксии (НУ/ВУ — 11,5510–6 ед./12,73 10–6 ед.; р≤0,0001; rxy — 0,57 ед.); показатель также статистически значим внутри каждой из групп «контроль–опыт» (р≤0,0001) и обратно коррелирует с тяжестью патоморфологических признаков РА, выявленных гистологически.
Таким образом, результаты исследования показали, что тяжесть патоморфологических изменений при РА, выражающуюся в степени дегенерации хряща (НУ/ВУ — 29 баллов/18 баллов, p≤0,01), а также в наличии общего воспаления в суставах (НУ/ВУ— 37 баллов/26 баллов, p≤0,01) и остеолизиса (НУ/ВУ — 6 баллов/0 баллов, p≤0,01), наиболее эффективно отображали следующие интегральные индексы воспаления: CAR (НУ/ВУ — 11,55·10–6 ед./12,73·10–6ед.; обратная корреляция: rxy — 0,57 ед.); ALB/dNLR (НУ/ВУ — 86,93 ед./78,51 ед.); SIRI (НУ/ВУ — 0,14 ед./0,19 ед.).
Заключение
Оценка диагностического потенциала новых биомаркеров системного воспаления MLR, SIRI, CAR, dNLR, ALB/dNLR показала, что наиболее точным для прогнозирования тяжести патогенетических признаков РА является биомаркер CAR, который с учетом резистентности организма к гипоксии значимо отражает тяжесть патоморфологических изменений в суставах при индуцированном РА. Интегральные показатели воспаления ALB/dNLR и SIRI целесообразно рекомендовать к применению с целью индивидуального мониторинга патологии соединительной ткани при РА. Прогностическая ценность индексов MLR и NC/LС не высока. Результаты исследования могут быть использованы для оптимизации диагностики, терапии и профилактики РА с учетом индивидуальных особенностей пациента.
Финансирование. Статья подготовлена в рамках фундаментальной научной темы государственного задания на 2025–2027 гг. «Роль митохондриальной дисфункции в патогенезе аутоиммунного ревматоидного артрита и разработка мер профилактики патологий соединительной ткани».
Конфликт интересов отсутствует.
Литература
- Квливидзе Т.З., Бедина С.А. Коморбидная патология у больных ревматоидным артритом. Кардиоваскулярная терапия и профилактика 2023; 22(S6): 54–55.
- McGonagle D., Watad A., Savic S. Mechanistic immunological based classification of rheumatoid arthritis. Autoimmun Rev 2018; 17(11): 1115–1123, https://doi.org/10.1016/j.autrev.2018.06.001.
- Клинические рекомендации «Ревматоидный артрит». 2024.
- Абрамкин А.А., Лисицына Т.А., Вельтищев Д.Ю., Серавина О.Ф., Ковалевская О.Б., Глухова С.И., Насонов Е.Л. Факторы, влияющие на эффективность терапии у больных ревматоидным артритом: роль коморбидной психической и соматической патологии. Научно-практическая ревматология 2018; 56(4): 439–448, https://doi.org/10.14412/1995-4484-2018-439-448.
- Wang L., Nakamura A. Where are we in targeting hypoxia-induced pathways in inflammatory arthritis? Current understanding, insights, and future directions. Int Immunopharmacol 2025; 146: 113883, https://doi.org/10.1016/j.intimp.2024.113883.
- Falconer J., Murphy A.N., Young S.P., Clark A.R., Tiziani S., Guma M., Buckley C.D. Review: synovial cell metabolism and chronic inflammation in rheumatoid arthritis. Arthritis Rheumatol 2018; 70(7): 984–999, https://doi.org/10.1002/art.40504.
- Quiñonez-Flores C.M., González-Chávez S.A., Pacheco-Tena C. Hypoxia and its implications in rheumatoid arthritis. J Biomed Sci 2016; 23(1): 62, https://doi.org/10.1186/s12929-016-0281-0.
- Yang M., Zhao C., Wang M., Wang Q., Zhang R., Bai W., Liu J., Zhang S., Xu D., Liu S., Li X., Qi Z., Yang F., Zhu L., He X., Tian X., Zeng X., Li J., Jiang Y. Synovial oxygenation at photoacoustic imaging to assess rheumatoid arthritis disease activity. Radiology 2023; 306(1): 220–228, https://doi.org/10.1148/radiol.212257.
- Huang Z., Liu D., Mo S., Hong X., Xie J., Chen Y., Liu L., Song D., Tang S., Wu H., Xu J., Dong F. Multimodal PA/US imaging in rheumatoid arthritis: enhanced correlation with clinical scores. Photoacoustics 2024; 38: 100615, https://doi.org/10.1016/j.pacs.2024.100615.
- Венерин А.А., Запара М.А., Михалищина А.С., Пупо Мачарашвили Д., Глазачев О.С. Индивидуальная толерантность к гипоксии: индикаторы, прикладное значение и методы определения. Вестник Российского университета дружбы народов. Серия: Медицина 2025; 29(1): 57–72, https://doi.org/10.22363/2313-0245-2025-29-1-57-72.
- Зарубина И.В. Молекулярные механизмы индивидуальной устойчивости к гипоксии. Обзоры по клинической фармакологии и лекарственной терапии 2005; 4(1): 49–51.
- Hochachka P.W. Mechanism and evolution of hypoxia-tolerance in humans. J Exp Biol 1998; 201(Pt 8): 1243–1254, https://doi.org/10.1242/jeb.201.8.1243.
- Arima H., Koirala S., Nema K., Nakano M., Ito H., Poudel K.M., Pandey K., Pandey B.D., Yamamoto T. High prevalence of rheumatoid arthritis and its risk factors among Tibetan highlanders living in Tsarang, Mustang district of Nepal. J Physiol Anthropol 2022; 41(1): 12, https://doi.org/10.1186/s40101-022-00283-3.
- Song D., Li L.S., Arsenault P.R., Tan Q., Bigham A.W., Heaton-Johnson K.J., Master S.R., Lee F.S. Defective Tibetan PHD2 binding to p23 links high altitude adaption to altered oxygen sensing. J Biol Chem 2014; 289(21): 14656–14665, https://doi.org/10.1074/jbc.M113.541227.
- Greer S.N., Metcalf J.L., Wang Y., Ohh M. The updated biology of hypoxia-inducible factor. EMBO J 2012; 31(11): 2448–2460, https://doi.org/10.1038/emboj.2012.125.
- Кондашевская М.В., Артемьева К.А., Алексанкина В.В., Тихонова Н.Б., Болтовская М.Н. Индикаторы устойчивости к гипоксии, определяемые по клеточным элементам крови крыс. Журнал эволюционной биохимии и физиологии 2021; 57(6): 475–483, https://doi.org/10.31857/S0044452921060061.
- Orr C.K., Najm A., Young F., McGarry T., Biniecka M., Fearon U., Veale D.J. The utility and limitations of CRP, ESR and DAS28-CRP in appraising disease activity in rheumatoid arthritis. Front Med (Lausanne) 2018; 5: 185, https://doi.org/10.3389/fmed.2018.00185.
- Farheen K., Agarwal S.K. Assessment of disease activity and treatment outcomes in rheumatoid arthritis. J Manag Care Pharm 2011; 17(9 Suppl B): S09–S13, https://doi.org/10.18553/jmcp.2011.17.s9-b.s09.
- Keenan R.T., Swearingen C.J., Yazici Y. Erythrocyte sedimentation rate and C-reactive protein levels are poorly correlated with clinical measures of disease activity in rheumatoid arthritis, systemic lupus erythematosus and osteoarthritis patients. Clin Exp Rheumatol 2008; 26(5): 814–819.
- Талибова С.М., Басиева М.А., Шварц В.А. Роль «новых» биомаркеров системного воспаления в прогнозировании характера течения ишемической болезни сердца и результатов реваскуляризации миокарда. Клиническая физиология кровообращения 2023; 20(3): 221–230, https://doi.org/10.24022/1814-6910-2023-20-3-221-230.
- Ыгиева Д.Г., Пивина Л.М., Батенова Г.Б., Токбулатова М.О. Прогностическое значение показателя отношения нейтрофилов к лимфоцитам у пациентов пожилого возраста с острым коронарным синдромом без подъема ST. Наука и здравоохранение 2020; 22(2): 79–85.
- Шварц В.А., Талибова С.М., Сокольская М.А., Испирян А.Ю., Шварц Е.Н., Петросян А.Д., Мерзляков В.Ю., Скопин А.И., Донаканян С.А. Ассоциация новых биомаркеров системного воспаления с развитием атеросклероза и его выраженностью. Российский кардиологический журнал 2024; 29(8): 6025, https://doi.org/10.15829/1560-4071-2024-6025.
- Петрова Е.Б., Огурцова С.Э., Бельская М.И., Колядко М.Г., Русских И.И., Статкевич Т.В., Кожемяко М.В., Митьковская Н.П. Индексы системного воспаления, взаимосвязь с биологическими маркерами раннего сосудистого старения и масштабами атеросклеротического поражения коронарного и прецеребрального бассейнов у бессимптомных пациентов трудоспособного возраста с субклиническим гипотиреозом. Кардиология в Беларуси 2024; 16(6): 640–657, https://doi.org/10.34883/PI.2024.16.6.005.
- Yang Z., Zhang Z., Lin F., Ren Y., Liu D., Zhong R., Liang Y. Comparisons of neutrophil-, monocyte-, eosinophil-, and basophil-lymphocyte ratios among various systemic autoimmune rheumatic diseases. APMIS 2017; 125(10): 863–871, https://doi.org/10.1111/apm.12722.
- Hao X., Li D., Wu D., Zhang N. The relationship between hematological indices and autoimmune rheumatic diseases (ARDs), a meta-analysis. Sci Rep 2017; 7(1): 10833, https://doi.org/10.1038/s41598-017-11398-4.
- Uslu A.U., Küçük A., Şahin A., Ugan Y., Yılmaz R., Güngör T., Bağcacı S., Küçükşen S. Two new inflammatory markers associated with Disease Activity Score-28 in patients with rheumatoid arthritis: neutrophil-lymphocyte ratio and platelet-lymphocyte ratio. Int J Rheum Dis 2015; 18(7): 731–735, https://doi.org/10.1111/1756-185X.12582.
- Gasparyan A.Y., Ayvazyan L., Mukanova U., Yessirkepov M., Kitas G.D. The platelet-to-lymphocyte ratio as an inflammatory marker in rheumatic diseases. Ann Lab Med 2019; 39(4): 345–357, https://doi.org/10.3343/alm.2019.39.4.345.
- Erre G.L., Paliogiannis P., Castagna F., Mangoni A.A., Carru C., Passiu G., Zinellu A. Meta-analysis of neutrophil-to-lymphocyte and platelet-to-lymphocyte ratio in rheumatoid arthritis. Eur J Clin Invest 2019; 49(1): e13037, https://doi.org/10.1111/eci.13037.
- Муравьев Ю.В., Лебедева В.В., Глухова С.И. Изучение показателей периферической крови для диагностики воспалительной активности при ревматоидном артрите. Научно-практическая ревматология 2022; 60(1): 52–56, https://doi.org/10.47360/1995-4484-2022-52-56.
- Громыко М.В., Грицук А.И. Экспериментальные модели ревматоидного артрита. Проблемы здоровья и экологии 2012; 2: 115–118, https://doi.org/10.51523/2708-6011.2012-9-2-22.
- Masoumi M., Bozorgi M., Nourmohammadi Z., Mousavi M.J., Shariati A., Karami J. Evaluation of hematological markers as prognostic tools in rheumatoid arthritis. BMC Rheumatol 2024; 8(1): 75, https://doi.org/10.1186/s41927-024-00444-0.
- Kong F., Huang J., Xu C., Huang T., Wen G., Cheng W. System inflammation response index: a novel inflammatory indicator to predict all-cause and cardiovascular disease mortality in the obese population. Diabetol Metab Syndr 2023; 15(1): 195, https://doi.org/10.1186/s13098-023-01178-8.
- Li X., Zhang L., Du Y., Shen Y., Gong Y., Wang J., Zhou J., Wang S. Association between monocyte-to-lymphocyte ratio and cardiovascular diseases: insights from NHANES data. Diabetol Metab Syndr 2025; 17(1): 98, https://doi.org/10.1186/s13098-025-01640-9.
- Hegen M., Keith J.C. Jr, Collins M., Nickerson-Nutter C.L. Utility of animal models for identification of potential therapeutics for rheumatoid arthritis. Ann Rheum Dis 2008; 67(11): 1505–1515, https://doi.org/10.1136/ard.2007.076430.
- Мужикян А.А., Шекунова Е.В., Кашкин В.А., Макарова М.Н., Макаров В.Г. Гистологическая оценка патологических изменений суставов при различных способах индукции хронического артрита у крыс. Лабораторные животные для научных исследований 2018; 1: 32–45, https://doi.org/10.29296/2618723X-2018-01-04.
- Ryu J.H., Chae C.S., Kwak J.S., Oh H., Shin Y., Huh Y.H., Lee C.G., Park Y.W., Chun C.H., Kim Y.M., Im S.H., Chun J.S. Hypoxia-inducible factor-2α is an essential catabolic regulator of inflammatory rheumatoid arthritis. PLoS Biol 2014; 12(6):e1001881, https://doi.org/10.1371/journal.pbio.1001881.
- Xiu Q., Kong C., Gao Y., Gao Y., Sha J., Cui N., Zhu D. Hypoxia regulates IL-17A secretion from nasal polyp epithelial cells. Oncotarget 2017; 8(60): 102097–102109, https://doi.org/10.18632/oncotarget.22189.
- Hirota K. Involvement of hypoxia-inducible factors in the dysregulation of oxygen homeostasis in sepsis. Cardiovasc Hematol Disord Drug Targets 2015; 15(1): 29–40, https://doi.org/10.2174/1871529x15666150108115553.
- Huh Y.H., Lee G., Lee K.B., Koh J.T., Chun J.S., Ryu J.H. HIF-2α-induced chemokines stimulate motility of fibroblast-like synoviocytes and chondrocytes into the cartilage-pannus interface in experimental rheumatoid arthritis mouse models. Arthritis Res Ther 2015; 17: 302, https://doi.org/10.1186/s13075-015-0816-x.
- Ahn J.K., Koh E.M., Cha H.S., Lee Y.S., Kim J., Bae E.K., Ahn K.S. Role of hypoxia-inducible factor-1alpha in hypoxia-induced expressions of IL-8, MMP-1 and MMP-3 in rheumatoid fibroblast-like synoviocytes. Rheumatology (Oxford) 2008; 47(6): 834–839, https://doi.org/10.1093/rheumatology/ken086.
- Cha H.-S., Ahn K.-S., Jeon C.H., Kim J., Song Y.W., Koh E.-M. Influence of hypoxia on the expression of matrix metalloproteinase-1, -3 and tissue inhibitor of metalloproteinase-1 in rheumatoid synovial fibroblasts. Clin Exp Rheumatol 2003; 21(5): 593–598.
- Poubelle P.E., Chakravarti A., Fernandes M.J., Doiron K., Marceau A.A. Differential expression of RANK, RANK-L, and osteoprotegerin by synovial fluid neutrophils from patients with rheumatoid arthritis and by healthy human blood neutrophils. Arthritis Res Ther 2007; 9(2): R25, https://doi.org/10.1186/ar2137.
- Alessi J.V., Ricciuti B., Alden S.L., Bertram A.A., Lin J.J., Sakhi M., Nishino M., Vaz V.R., Lindsay J., Turner M.M., Pfaff K., Sharma B., Felt K.D., Rodig S.J., Gainor J.F., Awad M.M. Low peripheral blood derived neutrophil-to-lymphocyte ratio (dNLR) is associated with increased tumor T-cell infiltration and favorable outcomes to first-line pembrolizumab in non-small cell lung cancer. J Immunother Cancer 2021; 9(11): e003536, https://doi.org/10.1136/jitc-2021-003536.
- Li L., Ai L., Jia L., Zhang L., Lei B., Zhang Q. High score of LDH plus dNLR predicts poor survival in patients with HER2-positive advanced breast cancer treated with trastuzumab emtansine. BMC Cancer 2022; 22(1): 29, https://doi.org/10.1186/s12885-021-09131-6.
- Fawzy R.M., Said E.A., Mansour A.I. Association of neutrophil to lymphocyte ratio with disease activity indices and musculoskeletal ultrasound findings in recent onset rheumatoid arthritis patients. Egypt Rheumatol 2017; 39(4): 203–206, https://doi.org/10.1016/j.ejr.2017.05.001.
- Chandrashekara S., Mukhtar Ahmad M., Renuka P., Anupama K.R., Renuka K. Characterization of neutrophil-to-lymphocyte ratio as a measure of inflammation in rheumatoid arthritis. Int J Rheum Dis 2017; 20(10): 1457–1467, https://doi.org/10.1111/1756-185X.13157.
- Ghang B., Kwon O., Hong S., Lee C.K., Yoo B., Kim Y.G. Neutrophil-to-lymphocyte ratio is a reliable marker of treatment response in rheumatoid arthritis patients during tocilizumab therapy. Mod Rheumatol 2017; 27(3): 405–410, https://doi.org/10.1080/14397595.2016.1214340.
- Ward E.S., Gelinas D., Dreesen E., Van Santbergen J., Andersen J.T., Silvestri N.J., Kiss J.E., Sleep D., Rader D.J., Kastelein J.J.P., Louagie E., Vidarsson G., Spriet I. Clinical significance of serum albumin and implications of FcRn inhibitor treatment in IgG-mediated autoimmune disorders. Front Immunol 2022; 13: 892534, https://doi.org/10.3389/fimmu.2022.892534.
- Ganeb S., Egaila S., Hamed A., Hassan W. Significance of serum albumin and derived neutrophil-to-lymphocyte ratio score in assessment of disease activity in rheumatoid arthritis patients. Egypt Rheumatol Rehabil 2020; 47(5), https://doi.org/10.1186/s43166-020-00010-9.
- Gioannini T.L., Zhang D., Teghanemt A., Weiss J.P. An essential role for albumin in the interaction of endotoxin with lipopolysaccharide-binding protein and sCD14 and resultant cell activation. J Biol Chem 2002; 277(49): 47818–47825, https://doi.org/10.1074/jbc.M206404200.
- Kimura H., Yoshizumi M., Ishii H., Oishi K., Ryo A. Cytokine production and signaling pathways in respiratory virus infection. Front Microbiol 2013; 4: 276, https://doi.org/10.3389/fmicb.2013.00276.
- Soeters P.B., Wolfe R.R., Shenkin A. Hypoalbuminemia: pathogenesis and clinical significance. JPEN J Parenter Enteral Nutr 2019; 43(2): 181–193, https://doi.org/10.1002/jpen.1451.
- Chien S.C., Chen C.Y., Lin C.F., Yeh H.I. Critical appraisal of the role of serum albumin in cardiovascular disease. Biomark Res 2017; 5: 31, https://doi.org/10.1186/s40364-017-0111-x.
- Потехина Ю.П. Роль соединительной ткани в организме. Российский остеопатический журнал 2015; 3–4: 92–104, https://doi.org/10.32885/2220-0975-2015-3-4-92-104.
- Gülcher S.S., Bruins N.A., Kingma W.P., Boerma E.C. Elevated C-reactive protein levels at ICU discharge as a predictor of ICU outcome: a retrospective cohort study. Ann Intensive Care 2016; 6(1): 5, https://doi.org/10.1186/s13613-016-0105-0.
- Уткина Е.А., Афанасьева О.И., Покровский С.Н. С-реактивный белок: патогенетические свойства и возможная терапевтическая мишень. Российский кардиологический журнал 2021; 26(6): 4138, https://doi.org/10.15829/1560-4071-2021-4138.
- Gremese E., Bruno D., Varriano V., Perniola S., Petricca L., Ferraccioli G. Serum albumin levels: a biomarker to be repurposed in different disease settings in clinical practice. J Clin Med 2023; 12(18): 6017, https://doi.org/10.3390/jcm12186017.