Новый количественный метод оценки ультраструктуры митохондрий кардиомиоцитов ушка правого предсердия
Цель исследования — разработать количественный метод оценки ультраструктуры митохондрий кардиомиоцитов ушка правого предсердия у больных с хронической сердечной недостаточностью (ХСН).
Материалы и методы. В одноцентровое проспективное исследование были включены 39 пациентов в возрасте 67 [58; 71] лет, перенесших коронарное шунтирование. Критериями включения стали наличие сердечной недостаточности с фракцией выброса левого желудочка <50%; атеросклеротические бляшки — 70% и более в двух или трех крупных коронарных артериях; решение кардиокоманды о проведении коронарного шунтирования. Во время операции осуществляли забор биоптата миокарда ушка правого предсердия для электронной микроскопии. Для анализа использовали два расчетных показателя: «общая площадь межфибриллярных митохондрий» и «отношение длины внешней мембраны к длине внутренней мембраны», на основе которых рассчитывали суммарный показатель по формуле «общая площадь межфибриллярных митохондрий» / «отношение длины внешней мембраны к длине внутренней мембраны».
Результаты. Медианные значения расчетных показателей, характеризующих ультраструктуру митохондрий кардиомиоцитов ушка правого предсердия, составили 43,7 [35,9; 54,3]% для показателя «общая площадь межфибриллярных митохондрий»; 31 [25; 37]% — для показателя «отношение длины внешней мембраны к длине внутренней мембраны» и 1,4 [0,95; 2,00] — для суммарного показателя, учитывающего обе ультраструктурные характеристики митохондрий: «общая площадь межфибриллярных митохондрий» / «отношение длины внешней мембраны к длине внутренней мембраны».
Для оценки клинической значимости предложенного интегрального показателя изучены ассоциации полученных значений с наличием фибрилляции предсердий (ФП). Ультраструктурные изменения митохондрий были более выраженными у пациентов с сочетанием ФП и ХСН, однако статистическая значимость различий отдельных показателей не достигалась: общая площадь межфибриллярных митохондрий была ниже в группе с ФП (42% против 49%; p=0,224), отношение длины внешней мембраны к внутренней было выше при ФП (35% против 31%; p=0,125). Величина суммарного показателя оказалась статистически значимо ниже у пациентов с ФП (0,96 против 1,75; p=0,021). Был проведен ROC-анализ для выявления связи между расчетным показателем «общая площадь межфибриллярных митохондрий» / «отношение длины внешней мембраны к длине внутренней мембраны» и наличием ФП; площадь под ROC-кривой (AUC) составила 0,773 (р=0,021).
Заключение. Предложенный суммарный показатель для анализа микрофотографий кардиомиоцитов, рассчитанный как «общая площадь межфибриллярных митохондрий» / «отношение длины внешней мембраны к длине внутренней мембраны», позволяет получить комплексную характеристику митохондрий, учитывающую не только их количество и размеры, но и внутреннюю структуру.
Введение
Хроническая сердечная недостаточность (ХСН), являясь заключительным этапом сердечно-сосудистого континуума, представляет собой актуальную и сложную проблему современной медицины [1]. На сегодняшний день накоплено значительное количество экспериментальных и клинических данных, свидетельствующих о наличии тесной ассоциации между развитием ХСН и патологическими изменениями структуры и функций митохондрий кардиомиоцитов, а разработка лекарственных молекул, влияющих на митохондриальные мишени, рассматривается как перспективное направление в оптимизации медикаментозной терапии сердечной недостаточности [2].
Согласно современным представлениям, функции митохондрий тесно ассоциированы с их структурным состоянием [3]. Вместе с тем оценка ультраструктуры митохондрий кардиомиоцитов является крайне затруднительной ввиду необходимости забора биоптатов ткани сердца, что ассоциировано с развитием осложнений и не оправдано с позиции этических норм научных исследований. Выходом из ситуации может быть забор биоптатов миокарда из ушка правого предсердия во время операции на сердце с искусственным кровообращением, при этом забор ткани осуществляется на этапе канюляции правого предсердия, что защищает сердечную мышцу от дополнительной травмы.
Отдельную сложность для изучения данной проблемы представляет интерпретация микрофотографий митохондрий кардиомиоцитов, поскольку на сегодняшний день не существует общепринятого валидизированного метода количественного описания ультраструктуры митохондрий в кардиомиоцитах. Оптимальный метод описания ультраструктуры митохондрий при ХСН должен быть не только воспроизводимым и обоснованным с точки зрения патоморфологии, но и способным обеспечивать корреляцию результатов оценки микрофотографий кардиомиоцитов с клиническими данными, характеризующими тяжесть проявлений сердечной недостаточности: с параметрами систолической и/или диастолической функции сердца, толерантностью к физическим нагрузкам, функциональным классом сердечной недостаточности.
В отдельных публикациях предложены методы количественного описания ультраструктуры митохондрий. В частности, для кардиомиоцитов левого желудочка описаны количественные параметры, характеризующие плотность расположения митохондрий и представляющие собой соотношение их площади к площади кардиомиоцита или площади миофибрилл [4]. Однако, во-первых, представленный метод был разработан для оценки митохондрий лабораторных животных, а не человека. Во-вторых, для описания митохондрий кардиомиоцитов, локализованных в ушке правого предсердия, эти показатели практически не применимы из-за слабоструктурированного расположения клеток в ткани. Ранее нами был предложен расчетный параметр «общая площадь межфибриллярных митохондрий» в кардиомиоцитах ушка правого предсердия, рассчитанный как отношение общей площади межфибриллярных митохондрий к площади межфибриллярного пространства [5]. Полученный расчетный показатель продемонстрировал в том числе и клиническую значимость — полученные расчетные данные коррелировали с толерантностью пациентов с ХСН к физической нагрузке по данным теста шестиминутной ходьбы и с пиковым потреблением кислорода при нагрузке по данным спировелоэргометрии [5]. Вместе с тем предложенный ранее метод не описывает полной морфологической картины митохондрий кардиомиоцитов, поскольку не учитывает их внутреннюю структуру.
Для описания внутренней структуры митохондрий Ч.М. Эльдаровым и соавт. [6] был предложен метод расчета соотношения площади поверхности внутренней мембраны на единицу объема митохондрии. Данный метод также был разработан и применен для описания ультраструктурных изменений митохондрий кардиомиоцитов некоторых линий лабораторных крыс, a не человека. Он очень сложен для применения, поскольку предусматривает необходимость предварительного расчета площадей и объемов и вместе с тем не учитывает количество митохондрий и плотность их расположения между миофибриллами.
Таким образом, на сегодняшний день не существует комплексного метода, позволяющего количественно оценивать ультраструктуру митохондрий кардиомиоцитов ушка правого предсердия у человека.
Цель настоящего исследования — разработка количественного метода оценки ультраструктуры митохондрий кардиомиоцитов ушка правого предсердия у больных с хронической сердечной недостаточностью.
Материалы и методы
В одноцентровое проспективное исследование были включены 39 пациентов в возрасте 67 [58; 71] лет, перенесших коронарное шунтирование (протокол зарегистрирован на ClinicalTrials.gov: NCT05770349). Протокол исследования соответствовал принципам Хельсинкской декларации (2024) и был одобрен локальным этическим комитетом Научно-исследовательского института кардиологии Томского национального исследовательского медицинского центра Российской академии наук (№241 от 9 марта 2023 г.).
Дизайн исследования подробно описан в наших предыдущих публикациях [5, 7]. Критериями включения в исследование явились наличие сердечной недостаточности с фракцией выброса левого желудочка <50%; атеросклеротические бляшки — 70% и более в двух или трех крупных коронарных артериях; решение кардиокоманды о проведении коронарного шунтирования; подписанное пациентом информированное согласие на участие в исследовании. Пациенты не включались в исследование в случае отказа от реваскуляризации, необходимости дополнительных кардиохирургических вмешательств помимо коронарного шунтирования, наличия онкологического заболевания в активной стадии, наличия имплантированных устройств, тяжелой почечной дисфункции (расчетная скорость клубочковой фильтрации CKD-EPI <30 мл/мин/1,73 м2), инфильтративных заболеваний сердца, острых инфекций и обострения хронических соматических заболеваний, тяжелой хронической обструктивной болезни легких, бронхиальной астмы, сахарного диабета любого типа, анемии.
Проведены сбор жалоб, анамнеза, а также стандартное лабораторно-инструментальное обследование всех пациентов, включающее эхокардиографию, определение концентрации N-терминального пропептида натрийуретического гормона. Биоптаты из ушка правого предсердия забирали во время коронарного шунтирования. Электронную микроскопию осуществляли с помощью просвечивающего электронного микроскопа JEM-1400 (JEOL Ltd., Япония). Для обработки изображений использовали программное обеспечение ImageJ [5].
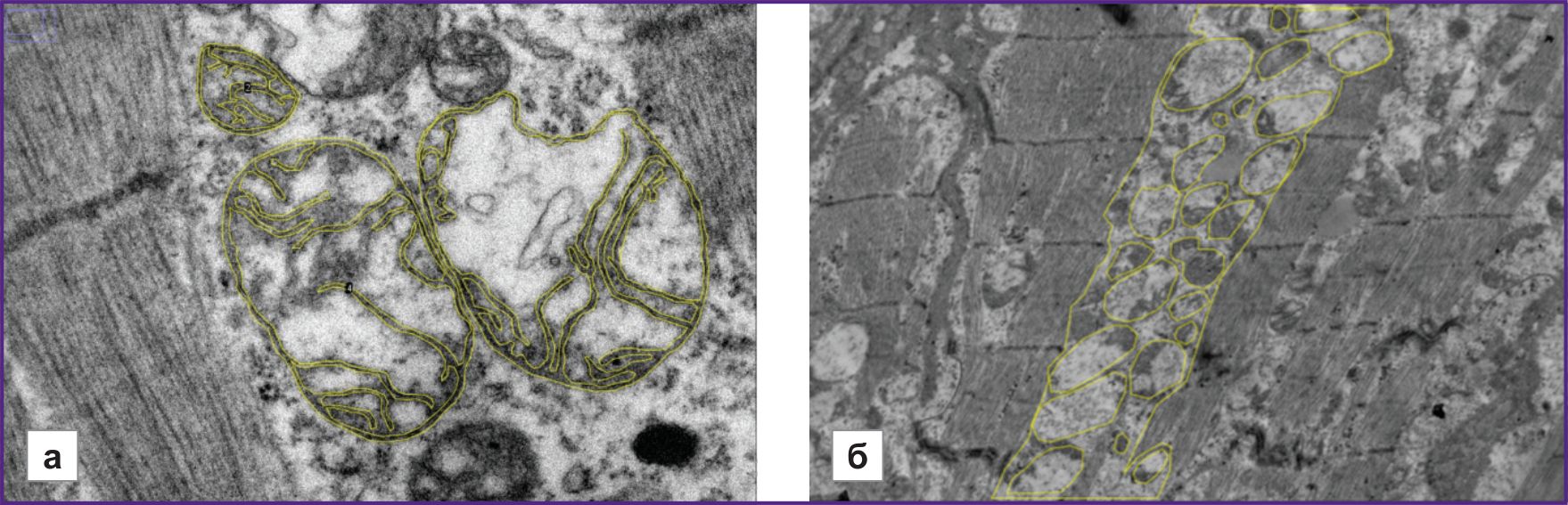
На микрофотографиях при увеличении в 15 000 раз (рис. 1, а) производили расчет соотношения длины внешней мембраны митохондрий к длине внутренней мембраны. Для каждого пациента проанализировано по 3 микрофотографии. На каждой микрофотографии производили расчет данного показателя для трех митохондрий. Результат рассчитывали в виде среднего арифметического; полученное значение выражали в процентах.
На микрофотографиях при увеличении в 5000 раз (рис. 1, б) рассчитывали общую площадь межфибриллярных митохондрий, равную отношению суммарной площади митохондрий, расположенных между сократительными волокнами кардиомиоцита, к общей площади межфибриллярного пространства; полученное значение выражали в процентах [5].
Далее был проведен расчет суммарного показателя, учитывающего обе ультраструктурные характеристики митохондрий (с учетом их разнонаправленного значения) по формуле «общая площадь межфибриллярных митохондрий» / «отношение длины внешней мембраны к длине внутренней мембраны».
Статистическую обработку результатов осуществляли с использованием программы IBM SPSS 21.0. Количественные непрерывные переменные представлены в виде медианы и интерквартильного размаха — Me [Q1; Q3]. Категориальные данные представлены в абсолютных и относительных величинах — n (%). Непрерывные переменные в независимых выборках анализировали с использованием критерия Манна–Уитни. Для определения взаимосвязи между наличием фибрилляции предсердий (ФП) и величиной количественных показателей ультраструктуры митохондрий применяли ROC-анализ. Различия считали статистически значимыми при p≤0,05.
Результаты
Медианные значения расчетных показателей, характеризующих ультраструктуру митохондрий кардиомиоцитов ушка правого предсердия, составили 43,7 [35,9; 54,3]% для показателя «общая площадь межфибриллярных митохондрий»; 31 [25; 37]% — для показателя «отношение длины внешней мембраны к длине внутренней мембраны» и 1,4 [0,95; 2,00] — для суммарного показателя, учитывающего обе ультраструктурные характеристики митохондрий: «общая площадь межфибриллярных митохондрий» / «отношение длины внешней мембраны к длине внутренней мембраны».
Для оценки клинической значимости предложенного интегрального показателя изучены ассоциации полученных значений с наличием ФП.
У 12 пациентов (30,8%) исследуемой когорты диагностирована ФП. В зависимости от ее наличия пациенты были разделены на 2 группы: 1-я — пациенты без ФП (n=27), 2-я — пациенты с ФП (n=12).
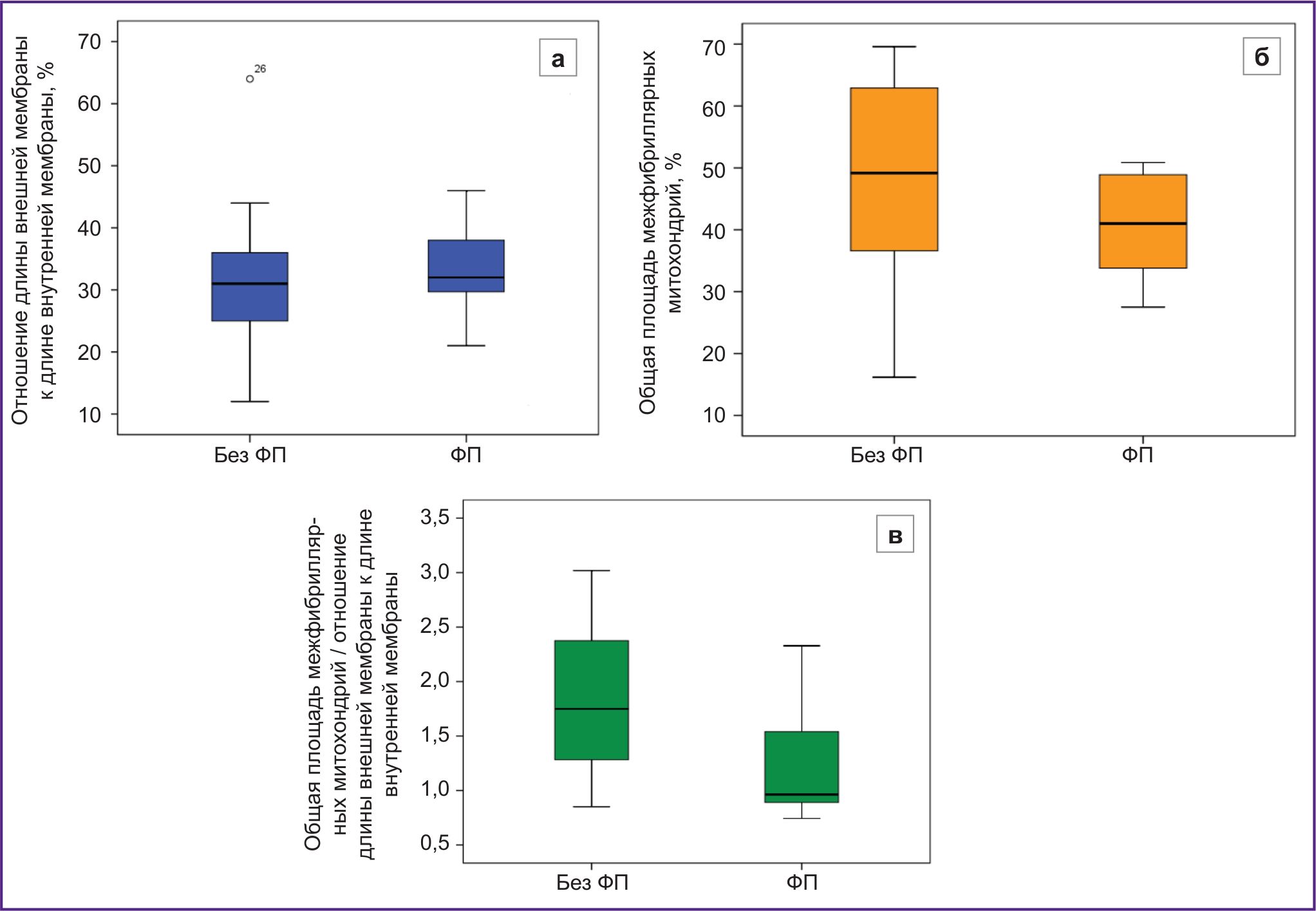
Отдельно взятые показатели, характеризующие плотность расположения митохондрий и их внутреннюю структуру, статистически значимо не различались в группах пациентов. Так, показатель «общая площадь межфибриллярных митохондрий» был несколько меньше в группе пациентов с ФП и составил 42 [33; 49]%, тогда как у пациентов без ФП — 49 [36; 64]% (р=0,224) (рис. 2, б). В свою очередь показатель «отношение длины внешней мембраны к длине внутренней мембраны» был несколько меньше в группе пациентов без ФП, что позволяет предположить более сохранную внутреннюю структуру митохондрий в данной группе по сравнению с пациентами, имеющими ФП (31 [25; 36]% и 35 [30; 45]% соответственно; р=0,125) (рис. 2, а).
Далее был произведен расчет суммарного показателя, учитывающего обе ультраструктурные характеристики митохондрий. Полученный результат был статистически значим (р=0,021) и составил 1,75 [1,28; 2,39] в группе пациентов без ФП и 0,96 [0,89; 1,54] — при наличии данного нарушения ритма (рис. 2, в).
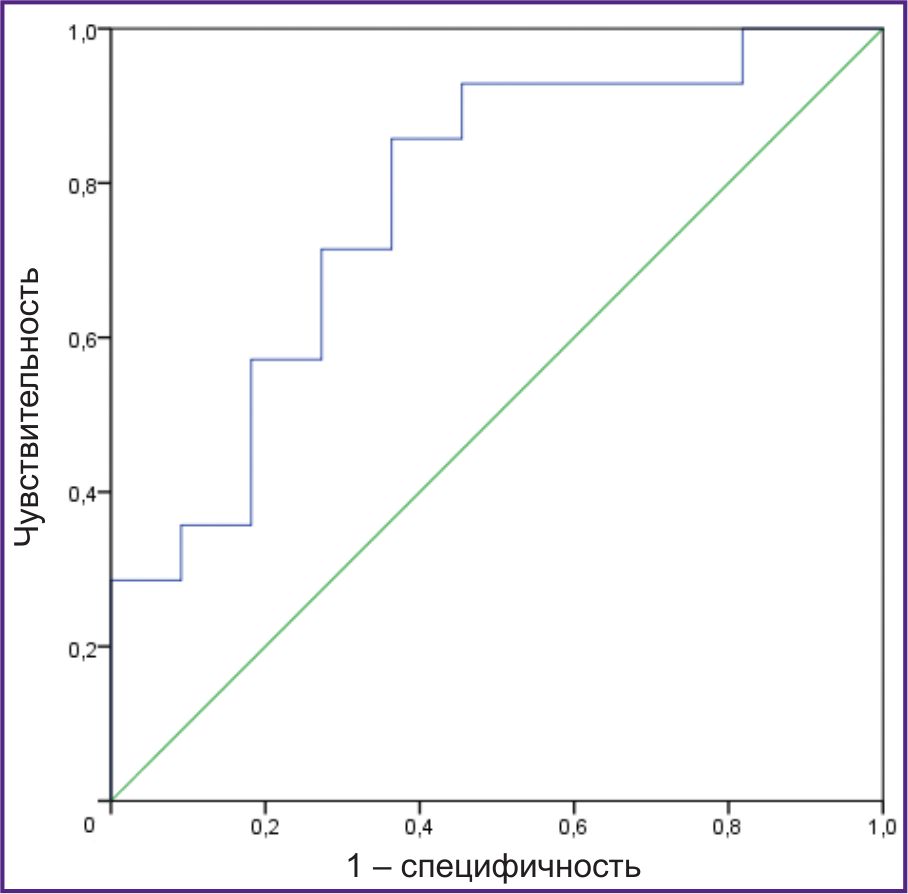
Проведен также ROC-анализ для выявления связи между суммарным показателем «общая площадь межфибриллярных митохондрий» / «отношение длины внешней мембраны к длине внутренней мембраны» и наличием ФП (рис. 3). Площадь под ROC-кривой (AUC) составила 0,773 (р=0,021).
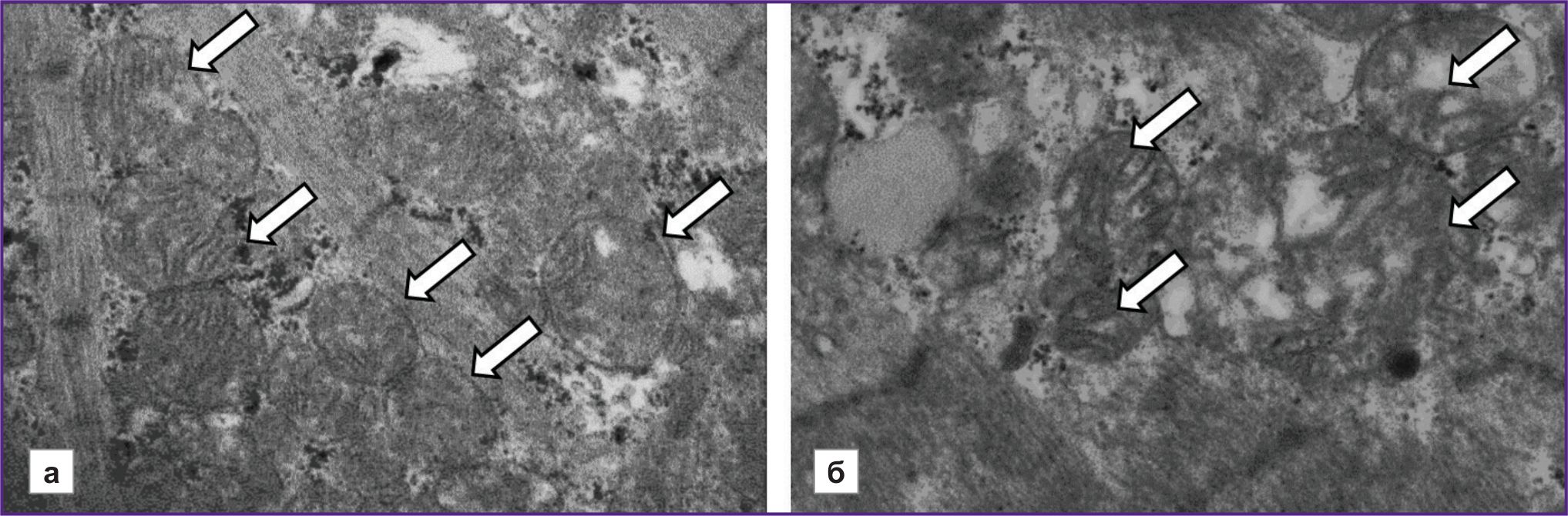
На рис. 4 представлены микрофотографии, иллюстрирующие различия ультраструктуры митохондрий кардиомиоцитов у пациентов с ХСН в зависимости от наличия ФП. Необходимо отметить, что у пациента без ФП митохондрии плотно прилегают друг к другу, их внутренняя структура визуализируется более отчетливо. В свою очередь у пациента с ФП митохондрии разной формы и размеров, удалены друг от друга; в части митохондрий кристы разрушены.
Обсуждение
Количественная оценка ультраструктуры митохондрий кардиомиоцитов при ХСН является крайне важным и перспективным направлением медицинских исследований. В настоящее время получает широкое развитие концепция наднозологической терапии — лечения, направленного на коррекцию фундаментальных патофизиологических процессов, что приводит к множественным благоприятным эффектам при различных заболеваниях. В частности, это касается одной из основных групп лекарственных препаратов, применяемых при ХСН, — ингибиторов натрий-глюкозного ко-транспортера 2-го типа (иНГЛТ2). Данная группа препаратов разрабатывалась исходно для терапии сахарного диабета, но продемонстрировала благоприятное влияние на клиническое течение и исходы ХСН независимо от величины фракции выброса левого желудочка [1, 8]. На сегодняшний день активно обсуждается влияние иНГЛТ2 на митохондриальную структуру и функцию как один из механизмов их кардиопротективного действия [2, 9, 10]. Вместе с тем без эффективного метода количественного описания ультраструктуры митохондрий кардиомиоцитов невозможно объективно охарактеризовать состояние данных органелл и, соответственно, оценить эффективность отдельных классов препаратов по улучшению структурно-функциональных параметров митохондрий.
Предложенные в нашей работе расчетные показатели, такие как «общая площадь межфибриллярных митохондрий» [5] и «отношение длины внешней мембраны к длине внутренней мембраны митохондрий», позволяют описать различные аспекты ультраструктурной организации митохондрий кардиомиоцитов: плотность расположения данных органелл между миофибриллами и сохранность крист, что является необходимым условием для их нормального функционирования.
Похожие методы количественного описания ультраструктуры митохондрий были предложены ранее. В частности, для оценки плотности расположения и количества митохондрий в кардиомиоцитах лабораторных животных применяли расчет соотношения площади митохондрий к площади кардиомиоцита или площади миофибрилл [4]. А для описания внутренней структуры митохондрий кардиомиоцитов лабораторных животных предложен расчетный показатель, вычисляемый как соотношение площади поверхности внутренней мембраны к единице объема митохондрии [6].
Для количественного описания ультраструктуры митохондрий D. Hayashi с соавт. [11] был предложен метод расчета индекса повреждения митохондрий, основанный на определении доли дегенерированных крист в митохондриях с очень сложным расчетом и высокой субъективностью полученных результатов, поскольку авторы были вынуждены в каждом поле зрения производить расчет 6 раз и усреднять полученные значения.
Однако ни один из предложенных ранее способов [4, 6, 11] количественного описания митохондрий не учитывал сразу несколько характеристик: плотность расположения и сохранность внутренней структуры митохондрий. Таким образом, предлагаемое нами объединение полученных значений в один суммарный показатель, рассчитанный как «общая площадь межфибриллярных митохондрий» / «отношение длины внешней мембраны к длине внутренней мембраны», позволяет получить комплексную характеристику митохондрий, учитывающую не только их количество и размеры, но и внутреннюю структуру.
Для подтверждения клинической значимости полученные значения расчетных показателей сравнивали в группах пациентов с наличием и отсутствием ФП.
Как известно, ФП и ХСН имеют взаимное негативное влияние как на патогенез друг друга, так и на прогноз пациентов [12–14]. Ранее проведенные исследования неоспоримо доказали наличие признаков структурного ремоделирования миокарда предсердий при ФП в виде фиброза, липоматоза, изолированного амилоидоза предсердий, гипертрофии кардиомиоцитов с явлениями частичной утраты миофибрилл [15]. В экспериментальных исследованиях также показано изменение структуры митохондрий кардиомиоцитов предсердий при ФП [16, 17].
Таким образом, важно было подтвердить клиническое значение впервые предложенного суммарного показателя, рассчитанного как «общая площадь межфибриллярных митохондрий» / «отношение длины внешней мембраны к длине внутренней мембраны». Полученные результаты полностью согласуются с данными литературы: ФП действительно оказывает дополнительное негативное влияние на ультраструктурное состояние митохондрий у пациентов с выраженной ХСН ишемической этиологии. Это выражается в наличии статистически значимых различий суммарного показателя у пациентов с наличием и отсутствием ФП. Полученные результаты ранее не были описаны в литературе и позволяют достичь более глубокого уровня понимания негативных ассоциаций данных состояний в клиническом и прогностическом отношении.
Необходимо отметить, что исходно исследуемая когорта пациентов характеризовалась наличием тяжелой сердечной недостаточности со снижением фракции выброса левого желудочка на фоне многососудистого стенозирующего атеросклероза коронарных артерий, что само по себе на ультрамикроскопическом уровне проявляется структурными изменениями митохондрий кардиомиоцитов [18]. Вместе с тем наличие у пациентов ФП приводило к снижению количества митохондрий, расположенных между миофибриллами кардиомиоцитов ушка правого предсердия, а также к уменьшению количества крист внутренней мембраны митохондрий, что, безусловно, отражается на эффективности работы данных органелл.
Ограничения исследования. Основным ограничением является небольшой объем выборки, который составил 39 пациентов. Однако для работ с подобным дизайном, включающим электронную микроскопию миокарда человека, представленный объем выборки является внушительным, особенно с учетом того факта, что при обработке результатов электронной микроскопии нами было проанализировано более 250 микрофотографий.
Заключение
Предложенный суммарный показатель для анализа микрофотографий кардиомиоцитов, рассчитанный как «общая площадь межфибриллярных митохондрий» / «отношение длины внешней мембраны к длине внутренней мембраны», позволяет получить комплексную характеристику митохондрий, учитывающую не только их количество и размеры, но и внутреннюю структуру.
Благодарность. Просвечивающая электронная микроскопия проведена на оборудовании, предоставленном ЦКП «Субдиффракционная микроскопия» и Программой развития МГУ им. М.В. Ломоносова (PNR 5.13).
Финансирование. Исследование выполнено за счет гранта Российского научного фонда №23-75-00009, https://rscf.ru/project/23-75-00009/.
Конфликт интересов. Все авторы заявляют об отсутствии конфликта интересов.
Литература
- Галявич А.С., Терещенко С.Н., Ускач Т.М., Агеев Ф.Т., Аронов Д.М., Арутюнов Г.П., Беграмбекова Ю.Л., Беленков Ю.Н., Бойцов С.А., Бубнова М.Г., Васюк Ю.А., Виллевальде С.В., Виноградова Н.Г., Гарганеева A.А., Гендлин Г.Е., Гиляревский С.Р., Глезер М.Г., Готье С.В., Гринштейн Ю.И., Довженко Т.В., Драпкина О.М., Дупляков Д.В., Жиров И.В., Затейщиков Д.А., Звартау Н.Э., Иртюга О.Б., Кобалава Ж.Д., Козиолова Н.А., Коротеев А.В., Либис Р.А., Лопатин Ю.М., Мареев В.Ю., Мареев Ю.В., Мацкеплишвили С.Т., Михайлов Е.Н., Насонова С.Н., Нарусов О.Ю., Недогода С.В., Недошивин А.О., Овчинников А.Г., Орлова Я.А., Перепеч Н.Б., Погосова Н.В., Римская Е.М., Самко А.Н., Саидова М.А., Сапельников О.В., Сафиуллина А.А., Ситникова М.Ю., Скворцов А.А., Скибицкий В.В., Стукалова О.В., Тарловская Е.И., Терещенко А.С., Чесникова А.И., Федотов П.А., Фомин И.В., Хасанов Н.Р., Шевченко А.О., Шапошник И.И., Шария М.А., Шляхто Е.В., Явелов И.С., Якушин С.С. Хроническая сердечная недостаточность. Клинические рекомендации 2024. Российский кардиологический журнал 2024; 29(11): 6162, https://doi.org/10.15829/1560-4071-2024-6162.
- Paillard M., Abdellatif M., Andreadou I., Bär C., Bertrand L., Brundel B.J.J.M., Chiva-Blanch G., Davidson S.M., Dawson D., Di Lisa F., Evans P., Giricz Z., Hausenloy D.J., Kleinbongard P., Lezoualc'h F., Liehn E., Maack C., Maguy A., Murphy E., Perrino C., Pesce M., Rainer P.P., Streckfuss-Bömeke K., Thielmann M., Tian R., Tocchetti C.G., Van Der Velden J., Van Linthout S., Zacchigna S., Krieg T. Mitochondrial targets in ischaemic heart disease and heart failure, and their potential for a more efficient clinical translation. A scientific statement of the ESC Working Group on Cellular Biology of the Heart and the ESC Working Group on Myocardial Function. Eur J Heart Fail 2025; 27(9): 1720–1736, https://doi.org/10.1002/ejhf.3674.
- Гарганеева А.А., Тукиш О.В., Кужелева Е.А., Муслимова Э.Ф., Гуля М.О., Жаргасова В.А., Попов С.В. Сердечная недостаточность и митохондриальная дисфункция: методы исследования в эксперименте и клинической практике. Acta Biomedica Scientifica 2025; 10(1): 103–114, https://doi.org/10.29413/ABS.2025-10.1.11.
- Stepanov A.V., Baidyuk E.V., Sakuta G.A. The features of mitochondria of cardiomyocytes from rats with chronic heart failure. Cell and Tissue Biology 2017; 11(6): 458–465, https://doi.org/10.1134/s1990519x17060086.
- Кужелева Е.А., Гарганеева А.А., Тукиш О.В., Витт К.Н., Андреев С.Л., Сыромятникова Е.Е., Владимирова Е.А. Общая площадь межфибриллярных митохондрий в кардиомиоцитах ушка правого предсердия как показатель функционального состояния сердечно-сосудистой системы при хронической сердечной недостаточности. Бюллетень экспериментальной биологии и медицины 2024; 178(10): 497–502, https://doi.org/10.47056/0365-9615-2024-178-10-497-502.
- El'darov C.M., Vays V.B., Vangeli I.M., Bakeeva L.E., Kolosova N.G. Morphometric examination of mitochondrial ultrastructure in aging cardiomyocytes. Biochemistry 2015; 80(5): 604–609, https://doi.org/10.1134/s0006297915050132.
- Гарганеева А.А., Кужелева Е.А., Тукиш О.В., Витт К.Н., Андреев С.Л., Муслимова Э.Ф., Корепанов В.А., Афанасьев С.А., Гуля М.О., Сыромятникова Е.Е., Владимирова Е.А., Степанов И.В. Возможности диагностики митохондриальной дисфункции при хронической сердечной недостаточности. Сибирский журнал клинической и экспериментальной медицины 2024; 39(3): 51–57, https://doi.org/10.29001/2073-8552-2024-39-3-51-57.
- McDonagh T.A., Metra M., Adamo M., Gardner R.S., Baumbach A., Böhm M., Burri H., Butler J., Čelutkienė J., Chioncel O., Cleland J.G.F., Crespo-Leiro M.G., Farmakis D., Gilard M., Heymans S., Hoes A.W., Jaarsma T., Jankowska E.A., Lainscak M., Lam C.S.P., Lyon A.R., McMurray J.J.V., Mebazaa A., Mindham R., Muneretto C., Francesco Piepoli M., Price S., Rosano G.M.C., Ruschitzka F., Skibelund A.K.; ESC Scientific Document Group 2023. Focused Update of the 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2023; 44(37): 3627–3639, https://doi.org/10.1093/eurheartj/ehad195.
- Dabravolski S.A., Zhuravlev A.D., Kartuesov A.G., Borisov E.E., Sukhorukov V.N., Orekhov A.N. Mitochondria-mediated cardiovascular benefits of sodium-glucose co-transporter 2 inhibitors. Int J Mol Sci 2022; 23(10): 5371, https://doi.org/10.3390/ijms23105371.
- Schwemmlein J., Maack C., Bertero E. Mitochondria as therapeutic targets in heart failure. Curr Heart Fail Rep 2022; 19(2): 27–37, https://doi.org/10.1007/s11897-022-00539-0.
- Hayashi D., Ohshima S., Isobe S., Cheng X.W., Unno K., Funahashi H., Shinoda N., Okumura T., Hirashiki A., Kato K., Murohara T. Increased (99m)Tc-sestamibi washout reflects impaired myocardial contractile and relaxation reserve during dobutamine stress due to mitochondrial dysfunction in dilated cardiomyopathy patients. J Am Coll Cardiol 2013; 61(19): 2007–2017, https://doi.org/10.1016/j.jacc.2013.01.074.
- Bidaoui G., Assaf A., Marrouche N. Atrial fibrillation in heart failure: novel insights, challenges, and treatment opportunities. Curr Heart Fail Rep 2024; 22(1): 3, https://doi.org/10.1007/s11897-024-00691-9.
- Carlisle M.A., Fudim M., DeVore A.D., Piccini J.P. Heart failure and atrial fibrillation, like fire and fury. JACC Heart Fail 2019; 7(6): 447–456, https://doi.org/10.1016/j.jchf.2019.03.005.
- Zdebik N., Poręba R., Gać P. Importance of T1-mapping sequence in patients with hypertrophic cardiomyopathy without foci of non-ischemic myocardial injury in late gadolinium enhancement sequence. Biomedicines 2024; 12(6): 1330, https://doi.org/10.3390/biomedicines12061330.
- Сухачева Т.В., Васковский В.А., Ревишвили А.Ш., Серов Р.А. Морфологические особенности миокарда ушек предсердий у пациентов с разными формами фибрилляции предсердий. Архив патологии 2017; 79(4): 3–12, https://doi.org/10.17116/patol20177943-12.
- Guttipatti P., Saadallah N., Ji R., Avula U.M.R., Goulbourne C.N., Wan E.Y. Quantitative 3D electron microscopy characterization of mitochondrial structure, mitophagy, and organelle interactions in murine atrial fibrillation. J Struct Biol 2024; 216(3): 108110, https://doi.org/10.1016/j.jsb.2024.108110.
- Qi X., Xiong F., Xiao J., Muthukumarasamy K.M., Altuntas Y., Zhong Y., Abu-Taha I., Bruns F., Tekook M., Kamler M., Villeneuve L., Nozza A., Sirois M., Karch J., Pasdois P., Bers D.M., Dobrev D., Nattel S. Time-dependent mitochondrial remodeling in experimental atrial fibrillation and potential therapeutic relevance. Preprint. bioRxiv 2025; 2025.01.29.635508, https://doi.org/10.1101/2025.01.29.635508.
- Paillard M., Abdellatif M., Andreadou I., Bär C., Bertrand L., Brundel B.J.J.M., Chiva-Blanch G., Davidson S.M., Dawson D., Di Lisa F., Evans P., Giricz Z., Hausenloy D.J., Kleinbongard P., Lezoualc'h F., Liehn E., Maack C., Maguy A., Murphy E., Perrino C., Pesce M., Rainer P.P., Streckfuss-Bömeke K., Thielmann M., Tian R., Tocchetti C.G., Van Der Velden J., Van Linthout S., Zacchigna S., Krieg T. Mitochondrial targets in ischaemic heart disease and heart failure, and their potential for a more efficient clinical translation. A scientific statement of the ESC Working Group on Cellular Biology of the Heart and the ESC Working Group on Myocardial Function. Eur J Heart Fail 2025; 27(9): 1720–1736, https://doi.org/10.1002/ejhf.3674.