Применение машинного обучения для прогнозирования результатов велоэргометрической пробы: проспективное когортное исследование
Цель исследования — разработка оптимального метода прогнозирования результатов велоэргометрической (ВЭМ) пробы на основе параметров, регистрируемых во время теста с шестиминутной ходьбой (ТШХ), с использованием методов машинного обучения.
Материалы и методы. В исследовании участвовали 56 пациентов, перенесших острый инфаркт миокарда и проходивших второй этап кардиореабилитации. Выполнено комплексное обследование, включающее сбор анамнеза, физикальное обследование, антропометрическую оценку, а также симптом-лимитированную ВЭМ-пробу и ТШХ. Во время ТШХ регистрировали пройденную дистанцию, частоту сердечных сокращений, артериальное давление, сатурацию кислорода, воспринимаемое напряжение по шкале Борга, количество пройденных шагов и электрокардиографические данные. Для построения моделей машинного обучения использовали алгоритмы случайного леса, градиентного бустинга, метода k-ближайших соседей и множественной линейной регрессии. Производительность моделей оценивали на основе коэффициента детерминации, средней абсолютной ошибки, среднеквадратичной ошибки и корня из среднеквадратичной ошибки. Для интерпретации результатов применяли SHAP-анализ.
Результаты. Модель градиентного бустинга обеспечивает наилучшее качество прогноза с высоким коэффициентом детерминации (R2 около 0,99) и низкими значениями ошибок для обеих целевых метрик: пройденной дистанции в ТШХ и метаболического эквивалента, достигнутого при ВЭМ-пробе. Анализ значимости признаков выявил, что частота сердечных сокращений, возраст и индекс массы тела оказывают наибольшее влияние на прогнозирование дистанции ТШХ, в то время как для прогнозирования метаболического эквивалента наиболее значимыми являются пройденное расстояние, количество пройденных шагов и индекс массы тела.
Заключение. Разработанная модель машинного обучения на основе градиентного бустинга продемонстрировала высокую эффективность в прогнозировании результатов ВЭМ-пробы на основе данных ТШХ. Предложенный метод может служить ценным вспомогательным инструментом для планирования программ кардиореабилитации, особенно в случаях, когда проведение ВЭМ-пробы затруднено или невозможно. Использование SHAP-анализа способствовало пониманию вклада каждого признака в прогноз, повышая доверие к результатам модели.
Введение
Сердечно-сосудистые заболевания (ССЗ) представляют собой серьезную проблему для мирового здравоохранения, являясь ведущей причиной заболеваемости и смертности [1]. По данным Всемирной организации здравоохранения, ССЗ ответственны за 19 млн смертей в год, что соответствует примерно 32% от общей глобальной летальности [2]. Важным элементом комплексного ведения пациентов с ССЗ является кардиореабилитация, обеспечивающая целостный подход к восстановлению и вторичной профилактике. Результаты систематических обзоров свидетельствуют о положительном влиянии кардиореабилитации на выживаемость пациентов, перенесших острый коронарный синдром, по сравнению с группами контроля, не участвовавшими в программах кардиореабилитации [3–5]. Отмечено снижение смертности от ССЗ на 26% и уменьшение частоты повторных госпитализаций на 18% [6]. Конечной целью кардиореабилитации является восстановление пациента и обеспечение его полноценной реинтеграции в привычную среду без функциональных ограничений, что в совокупности способствует улучшению клинического статуса, качества жизни и прогноза выживаемости [7].
Для оценки переносимости физической нагрузки при назначении тренировок в кардиореабилитации используются различные нагрузочные пробы. При помощи велоэргометра (велоэргометрическая проба — ВЭМ-проба) определяется метаболический эквивалент (metabolic equivalent of task — МЕТ) выполняемой нагрузки. Однако данный метод характеризуется относительно высокой стоимостью и значительными временными затратами [8]. Несмотря на возможность периодического использования ВЭМ-пробы в рамках проведения программы кардиореабилитации, для рутинного мониторинга физической работоспособности пациентов чаще применяется тест с шестиминутной ходьбой (ТШХ). Данный тест представляет собой экономичный, относительно быстрый и безопасный метод оценки функциональной переносимости физической нагрузки у пациентов с патологией сердечно-сосудистой системы. Его широкое применение обусловлено возможностью мониторинга течения различных ССЗ, а также оценки эффективности терапевтических и реабилитационных вмешательств [9, 10]. Следует отметить, что ВЭМ-проба и ТШХ принципиально различаются. ВЭМ-проба предполагает достижение максимальной физической нагрузки в течение 8–12 мин посредством использования протокола с постепенно возрастающей интенсивностью [11], в то время как ТШХ является пробой с постоянной интенсивностью нагрузки и традиционно классифицируется как субмаксимальная, что делает ее более безопасной. В частности, выполнение максимального теста, такого как ВЭМ-проба, сопряжено с более высоким риском для пациентов с тяжелым клиническим состоянием по сравнению с субмаксимальными нагрузками (ТШХ) [12]. Данный факт подтверждается различиями в требованиях к обеспечению безопасности при проведении этих двух тестов, включая необходимость наличия квалифицированного персонала, дефибриллятора, электрокардиографического мониторинга и средств для оказания неотложной помощи. Таким образом, в клинической практике часто возникает проблема определения оптимальной интенсивности физических нагрузок при проведении тренировок в рамках кардиореабилитации, особенно в тех случаях, когда выполнение ВЭМ-пробы невозможно по различным причинам.
В последние годы в медицинском сообществе растет интерес к достижениям в области искусственного интеллекта (ИИ), что, в частности, стимулировало внедрение систем мониторинга в реабилитационную практику [13]. Одной из ключевых сфер применения ИИ является обработка и категоризация изображений, что уже реализовано во многих медицинских направлениях, включая радиологию, онкологию, дерматологию и кардиологию [14–17]. ИИ все чаще используется в роботизированной хирургии, геномике, прогнозировании клинических исходов и в процессах принятия решений. Результаты исследований нередко демонстрируют, что ИИ может достигать уровня компетентности клиницистов или даже превосходить его.
Методы машинного обучения применяются для моделирования комплексных взаимодействий между множеством переменных [14–17]. В частности, оценка эффективности кардиореабилитации требует анализа клинических, психологических и антропометрических параметров, а также показателей, связанных с факторами риска и кардиопротективными привычками. Технологии ИИ способны обеспечивать интеграцию данных, получаемых из различных источников, включая сенсоры для регистрации физиологических параметров, таких как артериальное давление, частота сердечных сокращений (ЧСС), данные электрокардиографии при физической нагрузке, сатурация кислорода (SpO2) в крови и другие. Таким образом, появляется потенциальная возможность прогнозирования данных ВЭМ-пробы на основе различных параметров, получаемых с дистанционных биосенсоров во время проведения ТШХ.
Несмотря на растущий интерес к ИИ в медицине, в области реабилитации проведено лишь несколько исследований. Почти двадцать лет назад M. Zhu с соавт. [18] в сравнительном исследовании с участием более 20 000 пациентов, получающих уход на дому, показали, что даже простой алгоритм k-ближайших соседей может точнее предсказать реабилитационный потенциал, чем стандартные протоколы клинической оценки. В дальнейших исследованиях M. Zhu с соавт. [19] установили, что метод опорных векторов и случайные леса значительно превосходят традиционные методы анализа данных, применяемые в области реабилитации.
W.Y. Lin с соавт. [20] использовали машинное обучение для прогнозирования результатов реабилитации после инсульта. Анализ данных примерно 300 пациентов с помощью логистической регрессии, метода опорных векторов и случайного леса показал, что регрессионные алгоритмы позволяют оценить значение индекса Бартела (Barthel index) со средней абсолютной ошибкой около 10, а классификаторы обеспечивают точность более 70% при разделении пациентов на три категории по уровню активности.
Цель исследования — разработка оптимального метода прогнозирования результатов ВЭМ-пробы на основе параметров, регистрируемых во время ТШХ, с использованием методов машинного обучения. Данное исследование направлено на создание эффективного вспомогательного инструмента для планирования программ кардиореабилитации.
Материалы и методы
Проведено проспективное когортное исследование, в котором были проанализированы данные 56 пациентов, перенесших острый инфаркт миокарда: 45 мужчин (79,4%) и 11 женщин (20,6%). Исследование выполнено в Кардиологическом диспансере (Иваново), где в условиях круглосуточного стационара пациенты проходили второй этап кардиореабилитации.
Все пациенты прошли комплексное обследование, включающее сбор жалоб и анамнестических данных, физикальное обследование, а также антропометрическую оценку (рост, масса тела, индекс массы тела — ИМТ). Всем пациентам в течение 24 ч до начала программ физической реабилитации были проведены симптом-лимитированная ВЭМ-проба и ТШХ. Основанием для прекращения ВЭМ-пробы служил отказ пациента от дальнейшего выполнения теста по причине субъективной непереносимости физической нагрузки (выраженная усталость, болевой синдром в нижних конечностях, одышка и т.п.). Данное состояние интерпретировалось как достижение предела переносимости физической нагрузки. ТШХ проводили под ЭКГ-контролем с использованием телемедицинской системы «Аккордикс» (ООО «Нейрософт», Иваново). Система «Аккордикс» предназначена для дистанционного мониторинга и регистрации физиологических параметров, в частности ЭКГ в состоянии покоя и при физической нагрузке. Функциональные возможности системы включают автоматизированный анализ регистрируемых данных в режиме реального времени, в том числе при проведении ТШХ. На начальном этапе оценивали следующие показатели: дистанцию, пройденную пациентами в ходе ТШХ; достигнутую мощность нагрузки при выполнении ВЭМ-пробы (в МЕТ); наличие динамических изменений на ЭКГ в процессе выполнения обеих проб. До прохождения нагрузочных проб измеряли ЧСС, артериальное давление и SpO2. При проведении ТШХ кроме пройденного расстояния оценивали воспринимаемое напряжение по шкале Борга (шкала 6–20 баллов) и количество пройденных шагов.
Для достижения поставленных целей были построены несколько моделей машинного обучения: регрессия случайного леса (random forest regression, RFR), градиентный бустинг (gradient boosting), k-ближайших соседей (k-nearest neighbors, kNN) и множественная линейная регрессия (multiplelinearregression, MLR). Разработку моделей машинного обучения и визуальный анализ результатов проводили на языке программирования Python с использованием сервиса Google Colab.
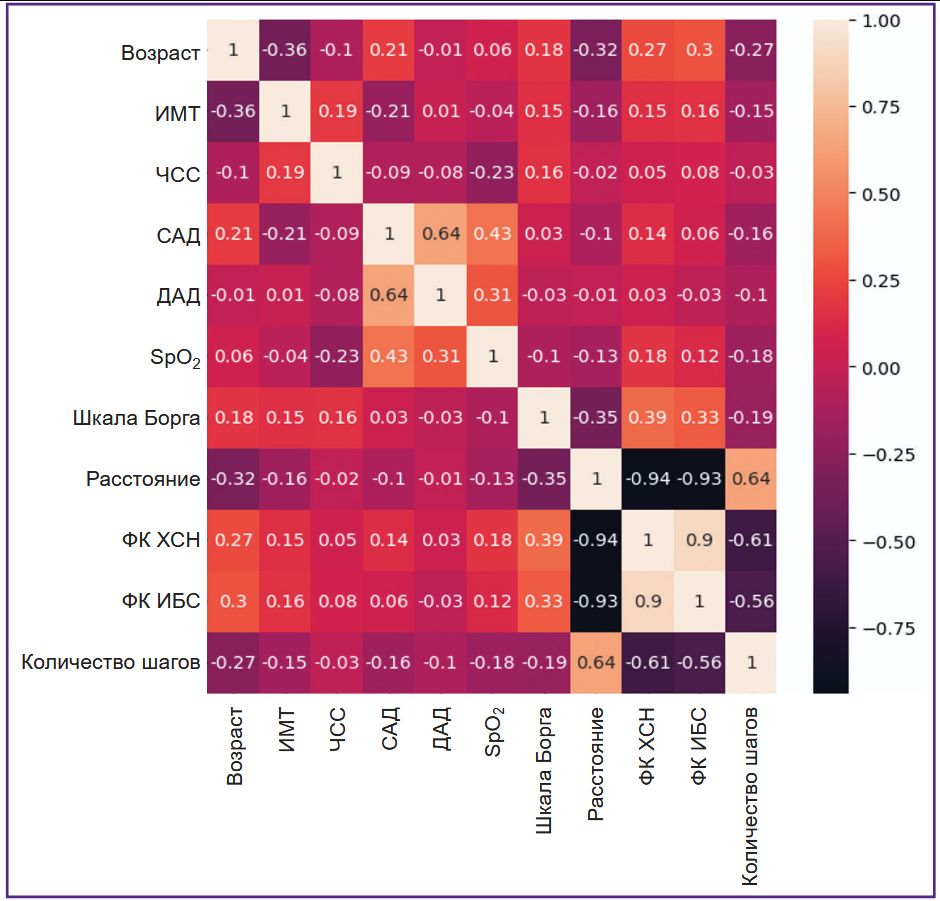
Как известно, наличие сильно коррелирующих показателей приводит к снижению производительности модели из-за высокой дисперсии и меньшей интерпретируемости [21]. По этой причине было задано пороговое значение коэффициента корреляции для рассматриваемых признаков, равное 0,7. При превышении этого порога один из коррелирующих признаков исключался. В результате построения матрицы корреляции признаков исходной выборки были найдены два показателя, которые исключили из дальнейшего анализа: функциональный класс хронической сердечной недостаточности и функциональный класс ишемической болезни сердца (рис. 1).
Результаты
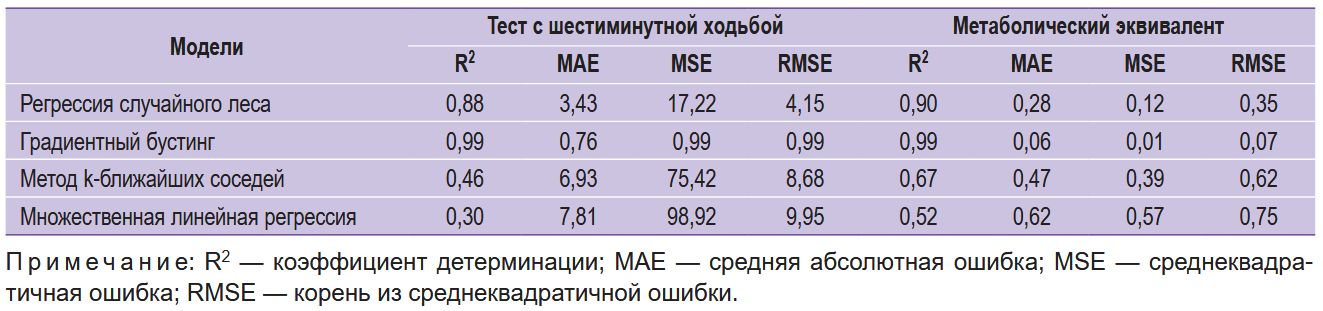
Две полученные модели (регрессия случайного леса и градиентный бустинг) характеризуются достаточно высоким коэффициентом детерминации. В модели k-ближайших соседей и множественной линейной регрессии значения данного коэффициента меньше 0,5 в случае предсказания величины ТШХ. Это означает, что на долю вариационных факторных признаков приходится меньшая часть дисперсии по сравнению с остальными факторами, не учтенными в модели и влияющими на изменение результативного показателя. Построенные при таких условиях регрессионные модели имеют низкое практическое значение. Модель градиентного бустинга показала лучшие результаты по всем показателям, демонстрируя самые высокие значения корректировки и самую низкую частоту ошибок (см. таблицу).
|
Параметры предсказуемых моделей |
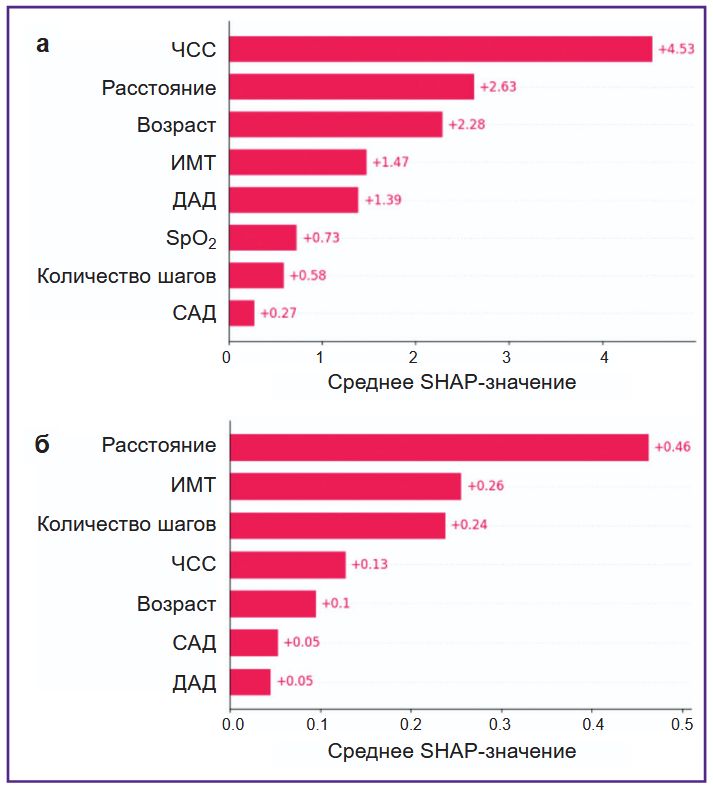
Для более подробного разбора факторов, влияющих на прогнозируемые величины в модели градиентного бустинга, была построена столбчатая диаграмма признаков, отсортированных по среднему SHAP-значению (рис. 2, а). Можно видеть, что абсолютная важность некоторых признаков довольно велика. Так, для прогнозирования величины ТШХ наиболее значимым является показатель ЧСС с SHAP-значением 4,53; меньший вклад в прогнозирование оказывают пройденное расстояние (SHAP-значение 2,63) и возраст пациента (SHAP-значение 2,28). ИМТ имеет SHAP-значение 1,47. В случае прогнозирования МЕТ (рис. 2, б) наибольший вклад вносит пройденное расстояние с SHAP-значением 0,46; далее по нисходящей — ИМТ (SHAP-значение 0,26) и количество пройденных шагов (SHAP-значение 0,24). ЧСС, возраст, систолическое и диастолическое артериальное давление имеют наименьшее влияние на прогнозирование величины MET.
Обсуждение
В отличие от работ Н. De Cannière с соавт. [22], F. Desai с соавт. [23] и N. Alshurafa с соавт. [24], которые использовали метод опорных векторов, случайные леса, деревья решений или нейронные сети для мониторинга пациентов, мы применили градиентный бустинг, что представляет собой относительно новый подход в данной области. Н. De Cannière с соавт. [22] в модели опорных векторов достигли средней абсолютной ошибки 42,8±36,8 при прогнозировании функциональной работоспособности, оцениваемой по дистанции ТШХ, в то время как указанная модель градиентного бустинга продемонстрировала значительно более низкие значения ошибок для обеих целевых метрик (ТШХ и МЕТ).
SHAP-анализ, использованный для интерпретации результатов модели градиентного бустинга, позволил определить наиболее значимые переменные в прогнозировании исходов ВЭМ-пробы. Этот анализ также выявил различия в значимости признаков для прогнозирования дистанции ТШХ и МЕТ.
Для прогнозирования дистанции ТШХ наиболее важными оказались ЧСС до начала теста, возраст пациента и ИМТ. Более высокий ИМТ часто ассоциирован с ухудшением физической формы, снижением аэробной способности и повышенной нагрузкой на опорно-двигательный аппарат, что может ограничивать пройденное расстояние [25]. Исходная ЧСС отражает вегетативный тонус и функциональное состояние сердечно-сосудистой системы, что влияет на физическую работоспособность [26]. С возрастом происходит снижение функциональных резервов организма, что также негативно сказывается на пройденном расстоянии [27].
В свою очередь для прогнозирования параметра МЕТ наиболее важными оказались количество пройденных шагов и ИМТ. Количество пройденных шагов напрямую связано с уровнем физической активности и энергозатратами. ИМТ, как и в случае с дистанцией ТШХ, может ограничивать достижение более высоких уровней МЕТ. Важно отметить, что такие параметры, как ЧСС, систолическое и диастолическое артериальное давление, продемонстрировали меньшую значимость. Это может быть связано с их большей вариабельностью и зависимостью от множества факторов, не учтенных в модели.
Клиническая значимость разработанной модели градиентного бустинга заключается в ее потенциальной возможности оптимизировать программы кардиореабилитации. В случаях, когда проведение ВЭМ-пробы затруднено или невозможно (например, у пациентов с тяжелым клиническим состоянием или при отсутствии необходимого оборудования), наша модель может служить ценным вспомогательным инструментом для оценки функциональной работоспособности и планирования индивидуализированных программ тренировок. Это позволит врачам принимать более обоснованные решения об интенсивности физических нагрузок, продолжительности тренировок и других аспектах кардиореабилитации, что в свою очередь может привести к улучшению результатов лечения и повышению безопасности пациентов. Модель также может быть использована для мониторинга прогресса пациентов в процессе кардиореабилитации и своевременной корректировки программы тренировок. Это может способствовать улучшению качества жизни и прогноза выживаемости пациентов с ССЗ.
Основным ограничением настоящего исследования является относительно небольшой объем выборки, что потенциально ограничивает обобщаемость полученных результатов.
Заключение
Проведенное проспективное когортное исследование продемонстрировало эффективность использования современных методов машинного обучения для прогнозирования результатов ВЭМ-пробы на основе данных, полученных в ходе ТШХ. Использование алгоритмов случайного леса, градиентного бустинга, k-ближайших соседей и многофакторной линейной регрессии позволило идентифицировать наиболее информативные признаки, оказывающие влияние на прогнозируемые величины ТШХ и MET.
Установлено, что модель градиентного бустинга обеспечивает наилучшие показатели качества прогноза, характеризующиеся высоким коэффициентом детерминации (R2 около 0,99) и низкими значениями ошибок (МАЕ, MSE, RMSE) для обеих целевых метрик. Это подтверждает эффективность выбранного подхода для прогнозирования результатов ВЭМ-пробы на основе данных ТШХ без необходимости проведения дорогостоящих и ресурсоемких проб. Данная методика особенно актуальна в отношении пациентов с тяжелым клиническим состоянием, для которых выполнение максимальных нагрузочных тестов сопряжено с повышенными рисками.
Финансирование. Данное исследование было проведено в рамках выполнения государственного задания для Ивановского государственного медицинского университета «Дистанционный кардиомониторинг в медицинской реабилитации» (SLFW-2024-0022), номер государственного учета в ЕГИСУ НИОКТР 124031100012-3.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Литература
- Gaidai O., Cao Y., Loginov S. Global cardiovascular diseases death rate prediction. Curr Probl Cardiol 2023; 48(5): 101622, https://doi.org/10.1016/j.cpcardiol.2023.101622.
- World Health Organization. Cardiovascular diseases (CVDs). 31 July 2025. URL: https://www.who.int/en/news-room/fact-sheets/detail/cardiovascular-diseases-(cvds).
- Shokri K., Karimian A., Radfar A., Mohammadi A., Amerizadeh A., Karimi R., Sadeghi M. Effect of exercise-based cardiac rehabilitation in patients with acute coronary syndrome: a systematic review and meta-analysis. BMC Sports Sci Med Rehabil 2025; 17(1): 233, https://doi.org/10.1186/s13102-025-01270-8.
- Meng Y., Zhuge W., Huang H., Zhang T., Ge X. The effects of early exercise on cardiac rehabilitation-related outcome in acute heart failure patients: a systematic review and meta-analysis. Int J Nurs Stud 2022; 130: 104237, https://doi.org/10.1016/j.ijnurstu.2022.104237.
- Mahmood A., Ray R., Bin Salam S.S.T., Haque F., Akkaldevi J., Masmoum M.D., Hassan M.S., Essani B., Anjum T., Mirza M.S.S. The effectiveness of cardiac rehabilitation programs in improving cardiovascular outcomes: systematic review and meta-analysis. Cureus 2024; 16(10): e72450, https://doi.org/10.7759/cureus.72450.
- Moghei M., Turk-Adawi K., Isaranuwatchai W., Sarrafzadegan N., Oh P., Chessex C., Grace S.L. Cardiac rehabilitation costs. Int J Cardiol 2017; 244: 322–328, https://doi.org/10.1016/j.ijcard.2017.06.030.
- Thomas R.J., Beatty A.L., Beckie T.M., Brewer L.C., Brown T.M., Forman D.E., Franklin B.A., Keteyian S.J., Kitzman D.W., Regensteiner J.G., Sanderson B.K., Whooley M.A. Home-based cardiac rehabilitation: a scientific statement from the american association of cardiovascular and pulmonary rehabilitation, the American Heart Association, and the American College of Cardiology. Circulation 2019; 140(1): e69–e89, https://doi.org/10.1161/CIR.0000000000000663.
- Кардиореабилитация и вторичная профилактика. Под ред. Аронова Д.М. М: ГЭОТАР-Медиа; 2021, https://doi.org/10.33029/9704-6218-8-car-2021-1-464.
- Coulshed A., Coulshed D., Pathan F. Systematic review of the use of the 6-minute walk test in measuring and improving prognosis in patients with ischemic heart disease. CJC Open 2023; 5(11): 816–825, https://doi.org/10.1016/j.cjco.2023.08.003.
- Mikhailovskaya T.V., Nazarova O.A., Dovgalyuk Yu.V., Chistyakova Yu.V., Mishina I.E. Methodological issues of assessment of sixminute walk test in patients with coronary artery disease. Bulletin of Rehabilitation Medicine 2021; 20(3): 37–44, https://doi.org/10.38025/2078-1962-2021-20-3-37-44.
- Mapelli M., Salvioni E., Paneroni M., Gugliandolo P., Bonomi A., Scalvini S., Raimondo R., Sciomer S., Mattavelli I., La Rovere M.T., Agostoni P. Brisk walking can be a maximal effort in heart failure patients: a comparison of cardiopulmonary exercise and 6 min walking test cardiorespiratory data. ESC Heart Fail 2022; 9(2): 812–821, https://doi.org/10.1002/ehf2.13781.
- Cavero-Redondo I., Saz-Lara A., Bizzozero-Peroni B., Núñez-Martínez L., Díaz-Goñi V., Calero-Paniagua I., Matínez-García I., Pascual-Morena C. Accuracy of the 6-minute walk test for assessing functional capacity in patients with heart failure with preserved ejection fraction and other chronic cardiac pathologies: results of the ExIC-FEp trial and a meta-analysis. Sports Med Open 2024; 10(1): 74, https://doi.org/10.1186/s40798-024-00740-6.
- Rasa A.R. Artificial intelligence and its revolutionary role in physical and mental rehabilitation: a review of recent advancements. Biomed Res Int 2024; 2024: 9554590, https://doi.org/10.1155/bmri/9554590.
- Norgeot B., Glicksberg B.S., Butte A.J. A call for deep-learning healthcare. Nat Med 2019; 25(1): 14–15, https://doi.org/10.1038/s41591-018-0320-3.
- Esteva A., Robicquet A., Ramsundar B., Kuleshov V., DePristo M., Chou K., Cui C., Corrado G., Thrun S., Dean J. A guide to deep learning in healthcare. Nat Med 2019; 25(1): 24–29, https://doi.org/10.1038/s41591-018-0316-z.
- Chilamkurthy S., Ghosh R., Tanamala S., Biviji M., Campeau N.G., Venugopal V.K., Mahajan V., Rao P., Warier P. Deep learning algorithms for detection of critical findings in head CT scans: a retrospective study. Lancet 2018; 392(10162): 2388–2396, https://doi.org/10.1016/S0140-6736(18)31645-3.
- Ehteshami Bejnordi B., Veta M., Johannes van Diest P., van Ginneken B., Karssemeijer N., Litjens G., van der Laak JAWM; the CAMELYON16 Consortium; Hermsen M., Manson Q.F., Balkenhol M., Geessink O., Stathonikos N., van Dijk M.C., Bult P., Beca F., Beck A.H., Wang D., Khosla A., Gargeya R., Irshad H., Zhong A., Dou Q., Li Q., Chen H., Lin H.J., Heng P.A., Haß C., Bruni E., Wong Q., Halici U., Öner M.Ü., Cetin-Atalay R., Berseth M., Khvatkov V., Vylegzhanin A., Kraus O., Shaban M., Rajpoot N., Awan R., Sirinukunwattana K., Qaiser T., Tsang Y.W., Tellez D., Annuscheit J., Hufnagl P., Valkonen M., Kartasalo K., Latonen L., Ruusuvuori P., Liimatainen K., Albarqouni S., Mungal B., George A., Demirci S., Navab N., Watanabe S., Seno S., Takenaka Y., Matsuda H., Ahmady Phoulady H., Kovalev V., Kalinovsky A., Liauchuk V., Bueno G., Fernandez-Carrobles M.M., Serrano I., Deniz O., Racoceanu D., Venâncio R. Diagnostic assessment of deep learning algorithms for detection of lymph node metastases in women with breast cancer. JAMA 2017; 318(22): 2199–2210, https://doi.org/10.1001/jama.2017.14585.
- Zhu M., Chen W., Hirdes J.P., Stolee P. The k-nearest neighbor algorithm predicted rehabilitation potential better than current Clinical Assessment Protocol. J Clin Epidemiol 2007; 60(10): 1015–1021, https://doi.org/10.1016/j.jclinepi.2007.06.001.
- Zhu M., Cheng L., Armstrong J.J., Poss J.W., Hirdes J.P., Stolee P. Using machine learning to plan rehabilitation for home care clients: beyond "black-box" predictions. In: Dua S., Acharya U., Dua P. (editors). Machine learning in healthcare informatics. Intelligent systems reference library, vol 56. Springer, Berlin, Heidelberg; 2014, https://doi.org/10.1007/978-3-642-40017-9_9.
- Lin W.Y., Chen C.H., Tseng Y.J., Tsai Y.T., Chang C.Y., Wang H.Y., Chen C.K. Predicting post-stroke activities of daily living through a machine learning-based approach on initiating rehabilitation. Int J Med Inform 2018; 111: 159–164, https://doi.org/10.1016/j.ijmedinf.2018.01.002.
- Sharma A., Lysenko A., Jia S., Boroevich K.A., Tsunoda T. Advances in AI and machine learning for predictive medicine. J Hum Genet 2024; 69(10): 487–497, https://doi.org/10.1038/s10038-024-01231-y.
- De Cannière H., Corradi F., Smeets CJP, Schoutteten M., Varon C., Van Hoof C., Van Huffel S., Groenendaal W., Vandervoort P. Wearable monitoring and interpretable machine learning can objectively track progression in patients during cardiac rehabilitation. Sensors (Basel) 2020; 20(12): 3601, https://doi.org/10.3390/s20123601.
- Desai F., Chowdhury D., Kaur R., Peeters M., Arya R.C., Wander G.S., Gill S.S., Buyya R. HealthCloud: a system for monitoring health status of heart patients using machine learning and cloud computing. Internet of Things 2022; 17: 10048, https://doi.org/10.1016/j.iot.2021.100485.
- Alshurafa N., Sideris C., Pourhomayoun M., Kalantarian H., Sarrafzadeh M., Eastwood J.A. Remote health monitoring outcome success prediction using baseline and first month intervention data. IEEE J Biomed Health Inform 2017; 21(2): 507–514, https://doi.org/10.1109/JBHI.2016.2518673.
- den Uijl I., van den Berg-Emons R.J.G., Sunamura M., Lenzen M.J., Stam H.J., Boersma E., Tenbült-van Limpt N.C.C.W., Kemps H.M.C., Geleijnse M.L., Ter Hoeve N. Effects of a dedicated cardiac rehabilitation program for patients with obesity on body weight, physical activity, sedentary behavior, and physical fitness: the OPTICARE XL randomized controlled trial. Phys Ther 2023; 103(9): pzad055, https://doi.org/10.1093/ptj/pzad055.
- O'Connor F.K., Chen D., Sharma P., Adsett J., Hwang R., Roberts L., Bach A., Louis M., Morris N. Physiological responses to sit-to-stand and six-minute walk tests in heart failure: a randomised trial. Heart Lung Circ 2025; 34(8): 789–797, https://doi.org/10.1016/j.hlc.2025.03.002.
- Büsching G., Schmid J.P. 6-minute walk test: exploring factors influencing perceived intensity in older patients undergoing cardiac rehabilitation-a qualitative study. Healthcare (Basel) 2025; 13(7): 735, https://doi.org/10.3390/healthcare13070735.