Современные методы исследования апоптотической гибели клеток (обзор)
Рассмотрены современные методы изучения апоптотической гибели клеток in vitro и in vivo. Показано, что наблюдение апоптоза основано на регистрации характерных клеточных изменений: потери целостности и деполяризации плазматической мембраны, экспозиции фосфатидилсерина и фосфатидилэтаноламина на поверхности клеточной мембраны, активации каспаз, деполяризации митохондриальной мембраны, фрагментации ДНК, изменении уровня биохимических маркеров. Основными методами исследования апоптоза in vitro являются: световая и электронная микроскопия, проточная цитометрия, флюоресцентная микроскопия, иммуногистохимия, иммуноферментный анализ, вестерн-блот, электрофорез и TUNEL-метод. Важную роль в наше время играют неинвазивные методы изучения апоптоза in vivo с возможностью регистрации этого процесса в тканях, органах и организме в целом: позитронно-эмиссионная томография (ПЭТ), однофотонная эмиссионная компьютерная томография (ОФЭКТ), магнитно-резонансная томография (МРТ), флюоресцентная спектроскопия, FLIM/FRET-имиджинг. Большое внимание уделено поиску контрастных агентов, специфичных к различным молекулам апоптотического каскада. Показано, что характер апоптотических реакций может служить маркером эффективности рациональной химиотерапии и помогать в ее выборе. Отмечено, что все бльшую популярность приобретает комбинация нескольких методов исследования апоптотической гибели клеток, например ОФЭКТ и оптический имиджинг, ПЭТ и оптический имиджинг, ПЭТ и МРТ. В перспективе с помощью этих методов можно будет не только определять тяжесть заболевания, но и оценивать эффективность лечения.
Апоптоз представляет собой процесс программируемой клеточной гибели, который контролируется генетически и присущ всем клеткам млекопитающих [1–3]. Он играет важную роль в росте и дифференцировке клеток, развитии целого организма и поддержании тканевого гомеостаза. Знание молекулярных механизмов, участвующих в запуске и реализации апоптоза, способствует пониманию процессов, вовлеченных в развитие многих заболеваний, в том числе онкологических [3, 4]. Факторы, участвующие в регуляции клеточной гибели, в настоящее время рассматриваются в качестве основных мишеней противоопухолевого воздействия, а характер апоптотических реакций может служить маркером эффективности рациональной химиотерапии и помогать в ее выборе [4–7].
К настоящему времени для качественного и количественного анализа апоптотических реакций в клетке предложено большое количество методов, позволивших раскрыть многие механизмы, лежащие в основе апоптоза [8]. Эти методы наблюдения основаны на регистрации характерных клеточных изменений — морфологических, биохимических и молекулярных (рис. 1) [8, 9]. Накоплен значительный материал о механизмах апоптотической гибели клеток, однако бóльшая часть работ, посвященных ее изучению, на сегодняшний день выполнена на клеточных культурах — in vitro. В последние годы идет активный поиск и разработка неинвазивных методов изучения апоптоза in vivo с возможностью регистрации этого процесса в тканях, органах и организме в целом [8, 10].
 Рис. 1. Основные клеточные изменения при апоптозе [8] Рис. 1. Основные клеточные изменения при апоптозе [8]
|
Морфологические изменения и деполяризация плазматической мембраны
Морфологическая картина апоптоза включает уменьшение объема клетки, сморщивание цитоплазматической мембраны, конденсацию ядра, разрывы нити ядерной ДНК и последующий распад ядра на части, фрагментацию клетки на мембранные везикулы с внутриклеточным содержимым (апоптотические тельца), фагоцитирующиеся макрофагами и соседними клетками [5].
Наиболее доступным и простым методом выявления апоптотических клеток и изучения их морфологических особенностей служит световая микроскопия гистологических препаратов. Для этого используют тонкослойные срезы тканей, окрашенные азуром А или гематоксилином и эозином [11–14].
Характерные для апоптотических клеток ультраструктурные изменения можно обнаружить методом электронной микроскопии. С помощью этого метода продемонстрированы ультраструктурные особенности клеток при апоптозе, активированном различными индукторами. В целом электронная микроскопия считается более надежным способом изучения апоптоза по сравнению со световой [15, 16].
Морфологические изменения доступны для исследования также с помощью метода проточной цитометрии. Снижение интенсивности светорассеяния отмечено на ранних стадиях апоптотического процесса вследствие сморщивания цитоплазмы клетки. Однако изменения светорассеяния не являются специфическими маркерами при развитии любой формы клеточной гибели, поэтому данный анализ следует совмещать с другими методами, обеспечивающими тонкую идентификацию молекулярного профиля клеточной гибели [17].
Для оценки нарушения структуры и деполяризации плазматической мембраны при апоптозе in vivo продемонстрированы возможности использования методов позитронно-эмиссионной томографии (ПЭТ) и однофотонной эмиссионной компьютерной томографии (ОФЭКТ) [10, 18]. В основе этого подхода лежит применение меченных радиоизотопами веществ, специфичных к различным молекулам и накапливающихся в апоптотических клетках. В последние годы создано большое число радионуклидных изотопов с использованием различных хелаторов и ко-лигандов. В частности, для изучения деполяризации цитоплазматической мембраны и внутриклеточного pH при апоптотической гибели клеток разработано семейство маленьких молекул ApoSense [10, 18, 19]. На основе этих молекул в 2008 г. для оценки деполяризации клеточной мембраны методом ПЭТ был создан радиоизотоп 18F-ML-10 (18F-меченая 5-фторпентил-2-метилмалоновая кислота) [20, 21]. Первое исследование использования данного радиоизотопа на людях показало его безопасность, стабильность и быстрое выведение из организма [22, 23]. В настоящее время клинические исследования выполняются с применением 18F-ML-10 для изучения деполяризации плазматической мембраны при апоптозе опухолевых клеток и оценки эффективности химиотерапии [24].
Для визуализации апоптоза in vivo методом ОФЭКТ предложен радиоизотоп 123I-меченый ML-10. Показано его поглощение опухолевыми клетками линии Daudi в зависимости от уровня pH у мышей при лечении циклофосфамидом и радиотерапией [25].
Экспозиция фосфатидилсерина и фосфатидилэтаноламина на поверхности цитоплазматической мембраны
В живых клетках фосфолипиды плазматической мембраны характеризуются асимметричным распределением: фосфатидилхолин и сфингомиелин расположены на наружной стороне липидного бислоя, в то время как фосфатидилсерин (ФС) и фосфатидилэтаноламин (ФЭ) локализованы на его внутренней поверхности. В процессе апоптоза эта асимметрия нарушается, ФС и ФЭ появляются на поверхности мембраны клетки и могут служить показателем запуска процесса апоптоза [7, 8, 18, 26].
В качестве соединения, маркирующего апоптотические клетки, используют рекомбинантный белок аннексин V, обладающий высокой аффинностью к ФС. Аннексин V — Ca2+-зависимый белок с молекулярной массой 35–36 кДа [18, 27]. Для детекции ФС применяют методы проточной цитометрии и флюоресцентной микроскопии с использованием аннексина V, конъюгированного с флюоресцентным красителем, например FITC [10, 28]. Однако из-за того, что перемещение ФС с внутренней поверхности цитоплазматической мембраны на наружную наблюдается и при некрозе, аннексин V стал использоваться вместе с такими катионными красителями, как 7-ADD или пропидиум иодид (PI), которые связываются с неповрежденной ДНК, но способны проникать внутрь клетки только при нарушении целостности цитоплазматической мембраны. Комбинированная окраска аннексином V — FITC и PI позволяет идентифицировать живые клетки (аннексин V–/PI–), ранние проапоптотические изменения (аннексин V+/PI–), позднюю стадию апоптоза, сопровождающуюся вторичным некрозом клеток, и некротический вариант клеточной гибели (PI+). Таким образом, данный метод позволяет отличить живые клетки от клеток, находящихся в апоптозе, и некротических клеток [17, 28, 29].
Благодаря высокому сродству аннексина V к мембранному ФС были разработаны различные радионуклидные изотопы с аннексином V для визуализации ФС in vivo методами ПЭТ и ОФЭКТ [9, 10]. Наиболее изученный и широко используемый радиоизотоп для изучения апоптоза — 99mTc-меченый-аннексин V, который нашел свое применение в онкологии [18, 30]. В настоящее время 99mTc-HYNIC-аннексин V — единственный радиоизотоп, который прошел 2-ю и 3-ю фазы клинических испытаний при лечении пациентов с раком легких [31, 32]. У всех пациентов отмечено увеличение поглощения аннексина V опухолью, кроме того, существенные корреляции были найдены между поглощением аннексина V и результатом лечения. Разработаны также 18F- и 68Ga-меченый аннексин V для исследования апоптотической гибели клеток in vivo [10, 18, 33] (рис. 2). Тем не менее использование аннексина V in vivo сопряжено с такими трудностями, как медленная фармакокинетика и высокая иммуногенность.
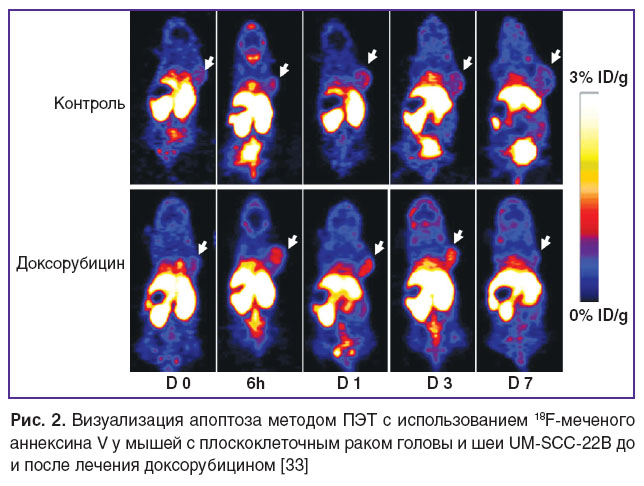 Рис. 2. Визуализация апоптоза методом ПЭТ с использованием 18F-меченого аннексина V у мышей с плоскоклеточным раком головы и шеи UM-SCC-22B до и после лечения доксорубицином [33] Рис. 2. Визуализация апоптоза методом ПЭТ с использованием 18F-меченого аннексина V у мышей с плоскоклеточным раком головы и шеи UM-SCC-22B до и после лечения доксорубицином [33]
|
В последние годы ведется поиск низкомолекулярных соединений для изучения апоптоза [34]. В 1995 г. из ФС карбоксилазы был получен пептид из 14 аминокислот, PSBP-0, специфически связывающий ФС [35]. В 2011 г. он был модифицирован и приобрел большую аффинность к ФС [36]. Исследования показали, что уровень радиоизотопа SAAC(99mTc)-PSBP-6 у мышей с меланомой становился выше после лечения. Это указывает на то, что данный пептид может быть использован для изучения раннего ответа опухоли на химиотерапию [37].
Для определения ФЭ на поверхности клеточной мембраны методом ПЭТ разработан тетрациклический пептид, состоящий из 19 аминокислот, с молекулярной массой 2 кДа — дурамицин [38]. В 2008 г. 99mTc-меченый дурамицин с HYNICв качестве лиганда был применен для визуализации апоптоза in vivo [39, 40]. Позднее в качестве нового радиоизотопа для визуализации апоптоза был предложен 18F-меченый дурамицин — [18F]FPДурамицин [41]. Он был успешно использован для изучения апоптоза опухолевых клеток после лечения циклофосфамидом и цисплатином у мышей методом ПЭТ. Однако фармакокинетика показала аккумуляцию [18F]FPДурамицина в печени и селезенке, что ограничивает его применение in vivo.
Другой метод, используемый для изучения апоптоза в клетках in vivo, — оптический имиджинг [42, 43]. Недавно разработанные способы оптического имиджинга обеспечивают визуализацию апоптоза в тканях и целом организме животных [10]. В последние годы все большее внимание исследователей в этой области привлекает комбинация различных инфракрасных флюорофоров и лигандов [44]. Для оптического имиджинга апоптоза в опухолях in vivo был применен аннексин V, меченный инфракрасным флюорофором Cy 5.5 [45]. В частности, он был использован при исследовании апоптоза в опухолях во время химиотерапии методом флюоресцентной томографии. Было установлено увеличение флюорофор-ассоциированного сигнала в леченых опухолях в сравнении с контролем [46].
Метод магнитно-резонансной томографии (МРТ) также используется для имиджинга апоптоза in vivo. Для определения ФС на поверхности плазматической мембраны методом МРТ применяют биотинилированный аннексин V, связанный с Gd-DTPA-мечеными липосомами [47, 48]. Для метода МРТ используют и суперпарамагнитные наночастицы оксида железа, конъюгированные с С2A-доменом белка синаптотагмина, специфичного к ФС [49]. Визуализация апоптоза методом МРТ была продемонстрирована in vitro в изолированных опухолевых клетках и in vivo в опухолях, леченных химиопрепаратами. Показано более высокое накопление контраста в опухоли в сравнении с контролем [50].
Активация каспаз
В большинстве случаев в клетках животных и человека апоптоз связан с протеолитической активацией каскада каспаз — семейства эволюционно консервативных цистеиновых протеаз, которые специфически расщепляют пептидную связь, образованную после остатков аспарагиновой кислоты [51]. Каспазы классифицируются на две основные группы: каспазы-1 (каспаза-1, 4, 5, 13 и 14) и каспазы-2, играющие центральную роль в процессе апоптоза (каспаза-2, 3, 6–10). Последняя группа подразделяется на инициаторные (каспаза-2, 8, 9 и 10) и эффекторные (каспаза-3, 6 и 7) [51, 52]. Различные механизмы индукции апоптоза через мембранные рецепторы или митохондрии сходятся на уровне каспазы-3, поэтому измерение ее активности является одним из наиболее информативных методов выявления апоптоза [6, 10].
Активность каспазы-3 может быть определена методами иммуногистохимии (ИГХ), иммуноферментного анализа (ИФА) или вестерн-блота с использованием моно- и поликлональных антител, специфичных для каспазы-3. Однако данные методы не позволяют регистрировать динамику активации фермента [28, 29, 53–55].
Другим широко применяемым методом для изучения активности каспаз является проточная цитометрия с использованием высокоспецифичных пептидных субстратов или ингибиторов, меченных флюорофорами [17].
В последние годы визуализацию апоптоза в живых клетках в динамике проводят с помощью флюоресцентного имиджинга (микроскопия, томография) и флюоресцентной спектроскопии. В качестве маркеров активации каспазы-3 при этом широко используются флюоресцентные белки. Основной подход заключается в применении так называемых FRET (Förster resonance energy transfer) сенсоров, которые представляют собой пару белков (донор и акцептор), связанных пептидной последовательностью DEVD. В связанном состоянии при возбуждении донора происходит резонансный перенос энергии на акцептор, что ведет к уменьшению интенсивности флюоресценции донора, в то время как флюоресценция акцептора увеличивается [56–63]. При этом время жизни флюоресценции донора во FRET-паре ниже по сравнению с его свободным состоянием [59, 64]. При запуске апоптоза и активации каспазы-3 последовательность DEVD расщепляется и FRET-реакция становится невозможной. Наиболее популярный FRET-сенсор для детекции активации каспазы-3 — SCAT3, состоящий из белков ECFP и Venus [63, 65–69]. Недавно был предложен сенсор для одновременного исследования активности каспазы-8 и каспазы-3, состоящий из трех флюоресцентных белков — seCFP, Venus и mRFP1, связанных двумя линкерами IETDи DEVD [70]. Использование FRET-сенсоров и методов флюоресцентной визуализации позволяет наблюдать пространственно-временную динамику активации каспазы-3 в отдельных живых клетках in vitro и in vivo по изменению интенсивности или времени жизни флюоресценции. Следует отметить, что флюоресцентный имиджинг с временным разрешением FLIM (fluorescence life-time imaging microscopy) считается одним из наиболее точных методов оценки эффективности FRET-реакции [59, 66, 71–77] (рис. 3). С помощью данного метода на различных линиях опухолевых клеток invitroиinvivoпоказана, в частности, активация процесса апоптоза при использовании химиопрепаратов [58, 59, 66].
Ключевое значение для прижизненного оптического наблюдения апоптоза в органах и тканях имеет глубина проникновения света. Известно, что ткани животных наиболее прозрачны в красной и ближнеинфракрасной областях спектра, поэтому усилия ученых в последние годы направлены на создание флюоресцентных белков и разработку FRET-сенсоров, работающих в данном диапазоне. Были выделены следующие флюоресцентные белки с эмиссией в оранжево-красной области: mRFP, Katushka, mKate2, IFP1.4, iRFP670, iRFP682, iRFP702, iRFP720 и др. [78–80]. Применение их позволяет увеличить глубину визуализации, снизить влияние собственной флюоресценции тканей и токсическое действие зондирующего излучения [81–86].
Другой подход к оценке активности каспаз состоит в использовании различных веществ, меченых радиоизотопами. В 2001 г. появились первые данные об активности и селективности ряда изатиновых аналогов каспазы-3. В 2008 г. был синтезирован и охарактеризован 18F-меченый аналог изатина. Радиоизотоп [18F]ICMT-11 был использован при изучении апоптоза in vitro и in vivo на животных методом ПЭТ. Исследование in vivo с помощью [18F]ICMT-11 выявило более высокую активность каспазы-3 в опухолевых клетках после лечения циклофосфамидом. При этом сигнал увеличивался в течение первых 24 ч после химиотерапии у мышей с В-клеточной лимфомой 38C13 [87]. Доклинические исследования [18F]ICMT-11 показали безопасность его применения на человеке [88].
Для визуализации активности ферментов апоптотического каскада ведутся разработки в области магнитно-резонансной томографии 1Н-МРТ. Однако существенным ограничением данного метода является высокий фоновый сигнал, и потому внимание многих исследователей сфокусировано на использовании 19F-МРТ. Для определения активности каспазы-3 был синтезирован 19F-МРТ-контраст Gd-DOTA-DEVD-Tfb, состоящий из Gd3+-комплекса, пептидной группы DEVD и 19F-содержащей группы (Tfb). При расщеплении DEVD-последовательности каспазой-3 19F-МРТ-пик становится острее и выше, что указывает на нарушение парамагнитного эффекта между Gd3+ и 19F [10].
Деполяризация митохондриальной мембраны
Известно, что митохондрии играют важную роль в апоптозе [10, 89, 90]. Нарушение мембранного потенциала Δψm и проницаемости мембраны митохондрий может возникнуть в результате окислительного стресса или после химиотерапии, что приводит к высвобождению внутримембранных белков, включая цитохром С [91, 92]. Деполяризация мембраны митохондрий происходит на ранних стадиях апоптоза до основных морфологических и биохимических изменений. Мониторинг мембранного потенциала может дать информацию о кинетике апоптотических процессов в исследуемых тканях [8].
Благодаря способности накапливаться в митохондриях в качестве молекул-зондов для выявления Δψm используются мембраносвязанные липофильные катионные флюорофоры, в частности родамин 123 (Rh123); 3,3'-дигексилоксакарбоцианин (DiOC6); 5,5',6,6'-тетрахлоро-1,1',3,3'-тетраэтилбензимидазолил-карбоцианин йодид (JC-1) и другие флюоресцентные красители (например, TMRE, TMRM), что позволяет регистрировать Δψm по интенсивности флюоресценции [28, 29, 55, 93]. При этом анализ Δψm проводится как в одиночных клетках, так и в изолированных митохондриях методом проточной цитометрии.
В 2007 г. 18F-меченый катион фосфония (18F-FBnTP) был использован для неинвазивного определения мембранного потенциала митохондрий методом ПЭТ [94]. Катионы фосфония могут проходить через липидный бислой благодаря их липофильности и положительному заряду и аккумулироваться внутри митохондрий. При потере мембранного потенциала во время апоптоза концентрация катионов фосфония в клетке уменьшается. В 2009 г. 18F-FBnTP был применен in vivo при лечении опухолей простаты у мышей [95].
Фрагментация ДНК
Во время апоптоза под действием эндонуклеаз происходят многочисленные разрывы нитей ДНК, в результате чего образуется множество 3'-концов [96]. Для выявления этого процесса широко применяют TUNEL-метод (terminal deoxynucleotided transferase-mediated dUTP-biotin nick-end labelling), или терминальное дезоксиуридиновое мечение концов [55]. Суть TUNEL-метода заключается в специфическом связывании с 3'-концом разорванной нити ДНК дезоксиуридинтрифосфата, меченого биотином. Такое связывание осуществляется ферментом дезоксинуклеотидтрансферазой. Этот метод считается надежным и специфическим способом выявления апоптоза, так как направлен на верификацию основного феномена — распада ДНК под действием Mg2+/Ca2+-зависимых эндонуклеаз с образованием фрагментов, размеры которых кратны размеру одной нуклеосомы [10–12, 97, 98]. Одна из последних модификаций TUNEL-метода позволяет выявить фрагментацию ДНК в образце, содержащем всего 5 нг ДНК, так что чувствительность этого метода более чем в 200 раз выше, чем при рутинном способе окраски.
Стоит отметить, что олигонуклеосомная деградация хроматина выявляется значительно раньше признаков апоптоза, видимых при световой микроскопии, и может быть определена методом электрофореза [99, 100]. Доказательством наличия апоптоза служит выявление дискретной «лесенки» с размером фрагментов, кратным 200 парам азотистых оснований (одной нуклеосоме), что подтверждается с помощью маркеров молекулярной массы. Необходимость такого контроля обусловлена тем, что при разрушении ДНК с помощью дезоксирибонуклеаз, наблюдаемом при некрозе, также возможно выявление «лесенки», однако не олигонуклеосомной, а олигонуклеотидной, с массой фрагментов, кратной одному основанию. Все эти обстоятельства вынуждают контролировать результаты TUNEL-метода и ДНК-электрофореза световой микроскопией с верификацией морфологических признаков апоптоза.
Выход моно- и олигонуклеотидных фрагментов ДНК из ядра в цитоплазму апоптотирующих клеток можно регистрировать методами ИГХ и ИФА с использованием моно- и поликлональных антител, специфичных для нуклеосомных фрагментов ДНК, содержащихся в лизате апоптотических клеток [100]. Чувствительность такого метода более чем в 500 раз выше выявления фрагментации ДНК с помощью гель-электрофореза. К существенным преимуществам метода следует отнести возможность одновременного анализа большого количества образцов, к основным недостаткам — необходимость анализа свежих образцов, поскольку хранение может привести к существенному ослаблению реакции.
Часто для выявления апоптотических клеток используется метод флюоресцентной микроскопии с флюоресцентными красителями, специфически связывающимися с ДНК: DAРI, Hoechst 33342, акридиновый оранжевый и бромистый этидий [63, 68]. При этом исследуют как витально окрашенные клетки во взвеси, так и фиксированные препараты. Обычно признаком апоптоза при использовании флюоресцентной микроскопии служит выявление ярко светящегося конденсированного хроматина. Совмещая обработку ДНК специфическими красителями с применением проточной цитометрии, можно произвести количественный учет апоптоза в клеточной суспензии. Чаще всего для этой цели используют обработку йодидом пропидия [16, 17].
Для детекции повреждения ДНК при апоптозе в условиях in vivo продемонстрировано применение метода ОФЭКТ [101]. Обнаружение повреждений в этом случае производят по сигнальному белку gH2AX, который связывается при апоптозе с поврежденной нитью ДНК и может быть выявлен с помощью флюорофор- или 111In-DOTA-меченых антител. Показано увеличение сигнала при использовании метода ОФЭКТ после лечения блеомицином рака груди на модели животных.
Биохимические маркеры апоптоза
Методы ИГХ, ИФА и вестерн-блот используют для определения протеинов, составляющих каскад биохимических процессов, приводящих к апоптозу [54]. На основании этих данных делают выводы о возможности вступления клеток в апоптоз, но не об уровне этого процесса в популяции клеток [16, 29, 67, 102]. Обычно используют поли- и моноклональные антитела к протеинам р53 — ДО-7, РАВ-1801 (для выявления wt р53 и mt р53), РАВ-240 (для определения только mt р53) и др. Кроме антител к р53 применяют иммуноглобулины к другим ключевым точкам генетической программы апоптоза — всl-2, bax, MPM-2, RB, Fas (моноклональные антитела ICO-160, анти-Fas, анти-АРО-1), циклинам, каспазам и т.д.
Для визуализации апоптоза в живых клетках применяют флюоресцентный имиджинг и FLIM с использованием FRET-сенсоров к проапоптотическим факторам. В частности, разработан сенсор, состоящий из флюоресцентных белков YFP и CFP, для определения активации Bid и запуска апоптоза [103].
Сведения о различных методах выявления апоптотической гибели клеток in vitro и in vivo обобщены в таблице.
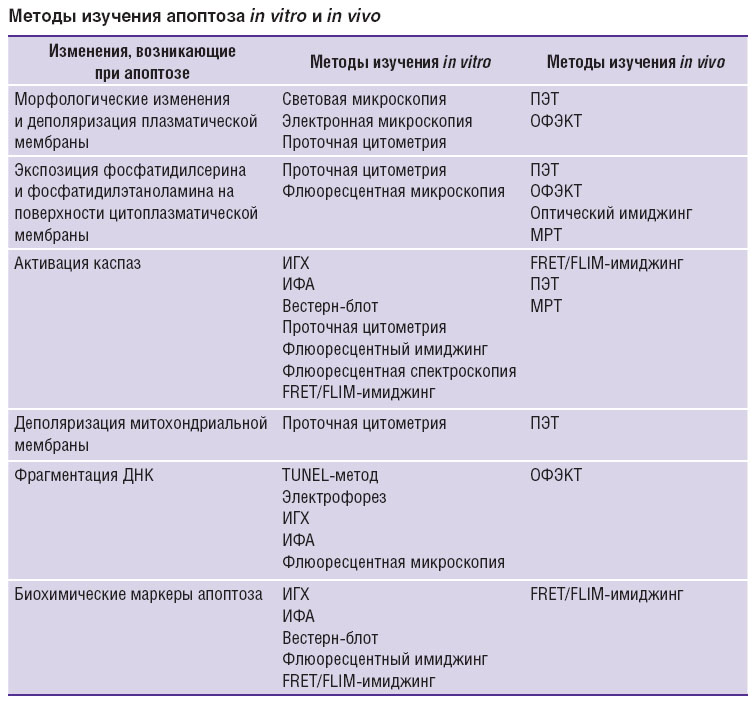 Методы изучения апоптоза in vitro и in vivo Методы изучения апоптоза in vitro и in vivo
|
Следует подчеркнуть, что в последние годы основные исследования в данной области посвящены разработке методов наблюдения апоптоза in vivo, что имеет большое значение для клинической медицины. Большую популярность приобретает комбинирование нескольких методов, например ОФЭКТ и КТ, ОФЭКТ и оптического имиджинга, ПЭТ и оптического имиджин га, ПЭТ, ОФЭКТ и КТ, ПЭТ и МРТ [10, 104–106]. В перспективе с помощью таких комбинаций методов можно будет не только определять тяжесть заболевания, злокачественность опухоли, но и оценивать эффективность лечения и прогнозировать рецидивы.
Финансирование. Работа выполнена при финансовой поддержке Российского научного фонда (проект №14-25-00129).
Конфликт интересов. У авторов нет конфликта интересов.
Литература
- Goldar S., Khaniani M.S., Derakhshan S.M., Baradaran B. Molecular mechanisms of apoptosis and roles in cancer development and treatment. Asian Pac J Cancer Prev 2015; 16(6): 2129–2144.
- Labi V., Erlacher M. How cell death shapes cancer. Cell Death Dis 2015; 6: e1675, http://dx.doi.org/10.1038/cddis.2015.20.
- Wong R.S. Apoptosis in cancer: from pathogenesis to treatment. J Exp Clin Cancer Res 2011; 30: 87, http://dx.doi.org/10.1186/1756-9966-30-87.
- Su Z., Yang Z., Xu Y., Chen Y., Yu Q. Apoptosis, autophagy, necroptosis, and cancer metastasis. Mol Cancer 2015; 14(1): 48, http://dx.doi.org/10.1186/s12943-015-0321-5.
- Lopez J., Tait S.W. Mitochondrial apoptosis: killing cancer using the enemy within. Br J Cancer 2015; 112(6): 957–962, http://dx.doi.org/10.1038/bjc.2015.85.
- Huang Q., Li F., Liu X., Li W., Shi W., Liu F.F., O’Sullivan B., He Z., Peng Y., Tan A.C., Zhou L., Shen J., Han G., Wang X.J., Thorburn J., Thorburn A., Jimeno A., Raben D., Bedford J.S., Li C.Y. Caspase 3-mediated stimulation of tumor cell repopulation during cancer radiotherapy. Nat Med 2011 Jul; 17(7): 860–866, http://dx.doi.org/10.1038/nm.2385.
- Smith B.A., Smith B.D. Biomarkers and molecular probes for cell death imaging and targeted therapeutics. Bioconjug Chem 2012; 23(10): 1989–2006, http://dx.doi.org/10.1021/bc3003309.
- Neves A.A., Brindle K.M. Imaging cell death. J Nucl Med 2014; 55(1): 1–4, http://dx.doi.org/10.2967/jnumed.112.114264.
- Bernsen M.R., Kooiman K., Segbers M., van Leeuwen F.W., de Jong M. Biomarkers in preclinical cancer imaging. Eur J Nucl Med Mol Imaging 2015; 42(4): 579–596, http://dx.doi.org/10.1007/s00259-014-2980-7.
- Zeng W., Wang X., Xu P., Liu G., Eden H.S., Chen X. Molecular imaging of apoptosis: from micro to macro. Theranostics 2015; 5(6): 559–582, http://dx.doi.org/10.7150/thno.11548.
- Kasagi N., Gomyo Y., Shirai H., Tsujitani S., Ito H. Apoptotic cell death in human gastric carcinoma: analysis by terminal deoxynucleotidyl transferase-mediated dUTP-biotin nick end labeling. Jpn J Cancer Res 1994; 85(9): 939–945, http://dx.doi.org/10.1111/j.1349-7006.1994.tb02972.x.
- Jolly P.D., Smith P.R., Heath D.A., Hudson N.L., Lun S., Still L.A., Watts C.H., McNatty K.P. Morphological evidence of apoptosis and the prevalence of apoptotic versus mitotic cells in the membrana granulosa of ovarian follicles during spontaneous and induced atresia in ewes. Biol Reprod 1997; 56(4): 837–846, http://dx.doi.org/10.1095/biolreprod56.4.837.
- Drachenberg C.B., Ioffe O.B., Papadimitriou J.C. Progressive increase of apoptosis in prostatic intraepithelial neoplasia and carcinoma: comparison between in situ end-labeling of fragmented DNA and detection by routine hematoxylin-eosin staining. Arch Pathol Lab Med 1997; 121(1): 54–58.
- Chyle V., Pollack A., Czerniak B., Stephens L.C., Zagars G.K., Terry N.H., Meyn R.E. Apoptosis and downstaging after preoperative radiotherapy for muscle-invasive bladder cancer. Int J Radiat Oncol Biol Phys 1996; 35(2): 281–287, http://dx.doi.org/10.1016/0360-3016(96)00089-2.
- Huang R.F., Wei Y.J., Inbaraj B.S., Chen B.H. Inhibition of colon cancer cell growth by nanoemulsion carrying gold nanoparticles and lycopene. Int J Nanomedicine 2015; 10: 2823–2846, http://dx.doi.org/10.2147/IJN.S79107.
- Li Q., Ren F.Q., Yang C.L., Zhou L.M., Liu Y.Y., Xiao J., Zhu L., Wang Z.G. Anti-proliferation effects of isorhamnetin on lung cancer cells in vitro and in vivo. Asian Pac J Cancer Prev 2015; 16(7): 3035–3042.
- Voitkova V.V. Study of apoptosis with use of flow cytometry. Bulletin of the East Siberian Scientific Center SB RAMS 2010; 76(6 Part 1): 220–225.
- Ogawa K., Aoki M. Radiolabeled apoptosis imaging agents for early detection of response to therapy. Scientific World Journal 2014; 2014: 732603, http://dx.doi.org/10.1155/2014/732603.
- Damianovich M., Ziv I., Heyman S.N., Rosen S., Shina A., Kidron D., Aloya T., Grimberg H., Levin G., Reshef A., Bentolila A., Cohen A., Shirvan A. ApoSense: a novel technology for functional molecular imaging of cell death in models of acute renal tubular necrosis. Eur J Nucl Med Mol Imaging 2006; 33(3): 281–291, http://dx.doi.org/10.1007/s00259-005-1905-x.
- Reshef A., Shirvan A., Akselrod-Ballin A., Wall A., Ziv I. Small-molecule biomarkers for clinical PET imaging of apoptosis. J Nucl Med 2010; 51(6): 837–840, http://dx.doi.org/10.2967/jnumed.109.063917.
- Reshef A., Shirvan A., Waterhouse R. N., Grimberg H., Levin G., Cohen A., Ulysse L.G., Friedman G., Antoni G., Ziv I. Molecular imaging of neurovascular cell death in experimental cerebral stroke by PET. J Nucl Med 2008; 49(9): 1520–1528, http://dx.doi.org/10.2967/jnumed.107.043919.
- Höglund J., Shirvan A., Antoni G., Gustavsson S.A., Langström B., Ringheim A., Sörensen J., Ben-Ami M., Ziv I. 18F-ML-10, a PET tracer for apoptosis: first human study. J Nucl Med 2011; 52(5): 720–725, http://dx.doi.org/10.2967/jnumed.110.081786.
- Shirvan A., Reshef A., Allen A., Fenig E., Stenmetz A., Groshar D., et al. Apoptosis imaging with PET-18F-ML-10 for early assessment of response of brain metastases to radiotherapy. J Nucl Med 2009; 50(Suppl 2): S453.
- Allen A.M., Ben-Ami M., Reshef A., Steinmetz A., Kundel Y., Inbar E., Djaldetti R., Davidson T., Fenig E., Ziv I. Assessment of response of brain metastases to radiotherapy by PET imaging of apoptosis with 18F-ML-10. Eur J Nucl Med Mol Imaging 2012; 39(9): 1400–1408, http://dx.doi.org/10.1007/s00259-012-2150-8.
- Bauwens M., de Saint-Hubert M., Cleynhens J., Vandeputte C., Li J., Devos E., Hendrickx S., Ni Y., Reutelingsperger C., Mortelmans L., Mottaghy F.M., Verbruggen A. In vitro and in vivo comparison of 18F and 123I-labeled ML10 with 68Ga-Cys2-AnxA5 for molecular imaging of apoptosis. Q J Nucl Med Mol Imaging 2013; 57(2): 187–200.
- Alam I.S., Neves A.A., Witney T.H., Boren J., Brindle K.M. Comparison of the C2A domain of synaptotagmin-I and annexin-V as probes for detecting cell death. Bioconjug Chem 2010; 21: 884–891, http://dx.doi.org/10.1021/bc9004415.
- Gerke V., Moss S.E. Annexins: from structure to function. Physiol Rev 2002; 82(2): 331–371.
- Lu Y.Y., Chen T.S., Qu J.L., Pan W.L., Sun L., Wei X.B. Dihydroartemisinin (DHA) induces caspase-3-dependent apoptosis in human lung adenocarcinoma ASTC-a-1 cells. J Biomed Sci 2009; 16: 16, http://dx.doi.org/10.1186/1423-0127-16-16.
- Fomin A.S., Koval O.A., Semenov D.V., Potapenko M.O., Kuligina E.V., Kit Yu.Ya. Richter V.A. The analysis of biomedical markers of MCF-7 cells apoptosis induced by recombinant analog of lactaptin. Russian Journal of Bioorganic Chemistry 2012; 38(1): 77–82, http://dx.doi.org/10.1134/s1068162012010086.
- Blankenberg F.G., Katsikis P.D., Tait J.F., Davis R.E., Naumovski L., Ohtsuki K., Kopiwoda S., Abrams M.J., Darkes M., Robbins R.C., Maecker H.T., Strauss H.W. In vivo detection and imaging of phosphatidylserine expression during programmed cell death. Proc Natl Acad Sci USA 1998; 95(11): 6349–6354, http://dx.doi.org/10.1073/pnas.95.11.6349.
- Kartachova M., van Zandwijk N., Burgers S., van Tinteren H., Verheij M., Valdés Olmos R.A. Prognostic significance of 99mTc Hynic-rh-annexin V scintigraphy during platinum-based chemotherapy in advanced lung cancer. J Clin Oncol 2007; 25(18): 2534–2539, http://dx.doi.org/10.1200/jco.2006.10.1337.
- Kartachova M.S., Valdés Olmos R.A., Haas R.L., Hoebers F.J., Herk M., Verheij M. 99mTc-HYNIC-rh-annexin-V scintigraphy: visual and quantitative evaluation of early treatment-induced apoptosis to predict treatment outcome. Nucl Med Commun 2008; 29(1): 39–44, http://dx.doi.org/10.1097/MNM.0b013e3282f1bc22.
- Hu S., Kiesewetter D.O., Zhu L., Guo N., Gao H., Liu G., Hida N., Lang L., Niu G., Chen X. Longitudinal PET imaging of doxorubicin-induced cell death with 18F-annexin V. Mol Imaging Biol 2012; 14(6): 762–770, http://dx.doi.org/10.1007/s11307-012-0551-5.
- Niu G., Chen X. Apoptosis imaging: beyond annexin V. J Nucl Med 2010; 51(11): 1659–1662, http://dx.doi.org/10.2967/jnumed.110.078584.
- Igarashi K., Kaneda M., Yamaji A., Saido T.C., Kikkawa U., Ono Y., Inoue K., Umeda M. A novel phosphatidylserine-binding peptide motif defined by an anti-idiotypic monoclonal antibody. Localization of phosphatidylserine-specific binding sites on protein kinase C and phosphatidylserine decarboxylase. J Biol Chem 1995; 270(49): 29075–29078, http://dx.doi.org/10.1074/jbc.270.49.29075.
- Xiong C., Brewer K., Song S., Zhang R., Lu W., Wen X., Li C. Peptide-based imaging agents targeting phosphatidylserine for the detection of apoptosis. J Med Chem 2011; 54(6): 1825–1835, http://dx.doi.org/10.1021/jm101477d.
- Song S., Xiong C., Lu W., Ku G., Huang G., Li C. Apoptosis imaging probe predicts early chemotherapy response in preclinical models: a comparative study with 8F-FDG PET. J Nucl Med 2013; 54(1): 104–110, http://dx.doi.org/10.2967/jnumed.112.109397.
- Marconescu A., Thorpe P.E. Coincident exposure of phosphatidylethanolamine and anionic phospholipids on the surface of irradiated cells. Biochim Biophys Acta 2008; 1778(10): 2217–2224, http://dx.doi.org/10.1016/j.bbamem.2008.05.006.
- Zhao M., Li Z., Bugenhagen S. 99mTc-labeled duramycin as a novel phosphatidylethanolamine-binding molecular probe. J Nucl Med 2008; 49(8): 1345–1352, http://dx.doi.org/10.2967/jnumed.107.048603.
- Johnson S.E., Li Z., Liu Y., Moulder J.E., Zhao M. Whole-body imaging of high-dose ionizing irradiation-induced tissue injuries using 99mTc-duramycin. J Nucl Med 2013; 54(8): 1397–1403, http://dx.doi.org/10.2967/jnumed.112.112490.
- Yao S., Hu K., Tang G., Liang X., Du K., Nie D., Jiang S., Zang L. Positron emission tomography imaging of cell death with [18F]FPDuramycin. Apoptosis 2014; 19(5): 841–850, http://dx.doi.org/10.1007/s10495-013-0964-x.
- Luker G.D., Luker K.E. Optical imaging: current applications and future directions. J Nucl Med 2008; 49(1): 1–4, http://dx.doi.org/10.2967/jnumed.107.045799.
- Kumar S., Richards-Kortum R. Optical molecular imaging agents for cancer diagnostics and therapeutics. Nanomedicine 2006; 1: 23–30, http://dx.doi.org/10.2217/17435889.1.1.23.
- Achilefu S. The insatiable quest for near-infrared fluorescent probes for molecular imaging. Angew Chem Int Ed 2010; 49(51): 9816–9818, http://dx.doi.org/10.1002/anie.201005684.
- Petrovsky A., Schellenberger E., Josephson L., Weissleder R., Bogdanov A. Jr. Near-infrared fluorescent imaging of tumor apoptosis. Cancer Res 2003; 63(8): 1936–1942.
- Ntziachristos V., Schellenberger E.A., Ripoll J., Yessayan D., Graves E., Bogdanov A. Jr., et al. Visualization of antitumor treatment by means of fluorescence molecular tomography with an annexin V-Cy5.5 conjugate. Proc Natl Acad Sci USA 2004; 101(33): 12294–12299, http://dx.doi.org/10.1073/pnas.0401137101.
- Hiller K.H., Waller C., Nahrendorf M., Bauer W.R., Jakob P.M. Assessment of cardiovascular apoptosis in the isolated rat heart by magnetic resonance molecular imaging. Mol Imaging 2006; 5(2): 115–121.
- van Tilborg G.A., Mulder W.J., Deckers N., Storm G., Reutelingsperger C.P., Strijkers G.J., Nicolay K. Annexin A5-functionalized bimodal lipid-based contrast agents for the detection of apoptosis. Bioconjug Chem 2006; 17(3): 741–749, http://dx.doi.org/10.1021/bc0600259.
- Zhao M., Beauregard D.A., Loizou L., Davletov B., Brindle K.M. Non-invasive detection of apoptosis using magnetic resonance imaging and a targeted contrast agent. Nat Med 2001; 7(11): 1241–1244, http://dx.doi.org/10.1038/nm1101-1241.
- Krishnan A.S., Neves A.A., de Backer M.M., Hu D.E., Davletov B., Kettunen M.I., Brindle K.M. Detection of cell death in tumors by using MR imaging and a gadolinium-based targeted contrast agent. Radiology 2008; 246(33): 854–862, http://dx.doi.org/10.1148/radiol.2463070471.
- Pop C., Salvesen G.S. Human caspases: activation, specificity, and regulation. J Biol Chem 2009; 284(33): 21777–21781, http://dx.doi.org/10.1074/jbc.R800084200.
- Nicholson D.W., Thornberry N.A. Caspases: killer proteases. Trends Biochem Sci 1997; 22(8): 299–306, http://dx.doi.org/10.1016/S0968-0004(97)01085-2.
- Delgado M.E., Olsson M., Lincoln F.A., Zhivotovsky B., Rehm M. Determining the contributions of caspase-2, caspase-8 and effector caspases to intracellular VDVADase activities during apoptosis initiation and execution. Biochim Biophys Acta 2013; 1833(10): 2279–2292, http://dx.doi.org/10.1016/j.bbamcr.2013.05.025.
- Laussmann M.A., Passante E., Hellwig C.T., Tomiczek B., Flanagan L., Prehn J.H., Huber H.J., Rehm M. Proteasome inhibition can impair caspase-8 activation upon submaximal stimulation of apoptotic tumor necrosis factor-related apoptosis inducing ligand (TRAIL) signaling. J Biol Chem 2012; 287(18): 14402–14411, http://dx.doi.org/10.1074/jbc.M111.304378.
- Yang F., Tu J., Pan J.Q., Luo H.L., Liu Y.H., Wan J., Zhang J., Wei P.F., Jiang T., Chen Y.H., Wang L.P. Light-controlled inhibition of malignant glioma by opsin gene transfer. Cell Death Dis 2013; 4: e893, http://dx.doi.org/10.1038/cddis.2013.425.
- Paulsson J.F., Schultz S.W., Köhler M., Leibiger I., Berggren P.O., Westermark G.T. Real-time monitoring of apoptosis by caspase-3-like protease induced FRET reduction triggered by amyloid aggregation. Exp Diabetes Res 2008; 2008: 865850, http://dx.doi.org/10.1155/2008/865850.
- Li I.T., Pham E., Truong K. Protein biosensors based on the principle of fluorescence resonance energy transfer for monitoring cellular dynamics. Biotechnol Lett 2006; 28(24): 1971–1982, http://dx.doi.org/10.1007/s10529-006-9193-5.
- Keese M., Offterdinger M., Tischer C., Girod A., Lommerse P.H., Yagublu V., Magdeburg R., Bastiaens P.I. Quantitative imaging of apoptosis commitment in colorectal tumor cells. Differentiation 2007; 75(9): 809–818, http://dx.doi.org/10.1111/j.1432-0436.2007.00186.x.
- Keese M., Yagublu V., Schwenke K., Post S., Bastiaens P. Fluorescence lifetime imaging microscopy of chemotherapy-induced apoptosis resistance in a syngenic mouse tumor model. Int J Cancer 2010; 126(1): 104–113, http://dx.doi.org/10.1002/ijc.24730.
- Kawai H., Suzuki T., Kobayashi T., Sakurai H., Ohata H., Honda K., Momose K., Namekata I., Tanaka H., Shigenobu K., Nakamura R., Hayakawa T., Kawanishi T. Simultaneous real-time detection of initiator- and effector-caspase activation by double fluorescence resonance energy transfer analysis. J Pharmacol Sci 2005; 93(7): 361–368, http://dx.doi.org/10.1254/jphs.fp0040592.
- Seervi M., Sobhan P.K., Mathew K.A., Joseph J., Pillai P.R., Santhoshkumar T.R. A high-throughput image-based screen for the identification of Bax/Bak-independent caspase activators against drug-resistant cancer cells. Apoptosis 2014; 19(1): 269–284, http://dx.doi.org/10.1007/s10495-013-0921-8.
- Rehm M., Dussmann H., Janicke R.U., Tavare J.M., Kogel D., Prehn J.H. Single-cell fluorescence resonance energy transfer analysis demonstrates that caspase activation during apoptosis is a rapid process. Role of caspase-3. J Biol Chem 2002; 277(27): 24506–24514, http://dx.doi.org/10.1074/jbc.m110789200.
- Wu Y., Xing D., Luo S., Tang Y., Chen Q. Detection of caspase-3 activation in single cells by fluorescence resonance energy transfer during photodynamic therapy induced apoptosis. Cancer Lett 2006; 235(2): 239–247, http://dx.doi.org/10.1016/j.canlet.2005.04.036.
- Janssen A., Beerling E., Medema R., van Rheenen J. Intravital FRET imaging of tumor cell viability and mitosis during chemotherapy. PLoS One 2013; 8(5): e64029, http://dx.doi.org/10.1371/journal.pone.0064029.
- Joseph J., Seervi M., Sobhan P.K., Retnabai S.T. High throughput ratio imaging to profile caspase activity: potential application in multiparameter high content apoptosis analysis and drug screening. PLoS One 2011; 6(5): e20114, http://dx.doi.org/10.1371/journal.pone.0020114.
- Pan W., Qu J., Chen T., Sun L., Qi J. FLIM and emission spectral analysis of caspase-3 activation inside single living cell during anticancer drug-induced cell death. Eur Biophys J 2009; 38(4): 447–456, http://dx.doi.org/10.1007/s00249-008-0390-0.
- Wang L., Chen T., Qu J., Wei X. Quantitative analysis of caspase-3 activation by fitting fluorescence emission spectra in living cells. Micron 2009; 40(8): 811–820, http://dx.doi.org/10.1016/j.micron.2009.07.001.
- Zhou F., Xing D., Wu S., Chen W.R. Intravital imaging of tumor apoptosis with FRET probes during tumor therapy. Mol Imaging Biol 2010; 12(1): 63–70, http://dx.doi.org/10.1007/s11307-009-0235-y.
- Wang F., Chen T.S., Xing D., Wang J.J., Wu Y.X. Measuring dynamics of caspase-3 activity in living cells using FRET technique during apoptosis induced by high fluence low-power laser irradiation. Lasers Surg Med 2005; 36(1): 2–7, http://dx.doi.org/10.1002/lsm.20130.
- Kominami K., Nagai T., Sawasaki T., Tsujimura Y., Yashima K., Sunaga Y., Tsuchimochi M., Nishimura J., Chiba K., Nakabayashi J., Koyamada K., Endo Y., Yokota H., Miyawaki A., Manabe N., Sakamaki K. In vivo imaging of hierarchical spatiotemporal activation of caspase-8 during apoptosis. PLoS One 2012; 7(11): e50218, http://dx.doi.org/10.1371/journal.pone.0050218.
- Pepperkok R., Squire A., Geley S., Bastiaens P.I. Simultaneous detection of multiple green fluorescent proteins in live cells by fluorescence lifetime imaging microscopy. Curr Biol 1999; 9(5): 269–272, http://dx.doi.org/10.1016/s0960-9822(99)80117-1.
- van Kuppeveld F.J., Melchers W.J., Willems P.H., Gadella T.W. Homomultimerization of the coxsackievirus 2B protein in living cells visualized by fluorescence resonance energy transfer microscopy. J Virol 2002; 76(18): 9446–9456, http://dx.doi.org/10.1128/jvi.76.18.9446-9456.2002.
- Chen N.T., Wu C.Y., Chung C.Y., Hwu Y., Cheng S.H., Mou C.Y., Lo L.W. Probing the dynamics of doxorubicin-DNA intercalation during the initial activation of apoptosis by fluorescence lifetime imaging microscopy (FLIM). PLoS One 2012; 7(9): e44947, http://dx.doi.org/10.1371/journal.pone.0044947.
- Verveer P.J., Squire A., Bastiaens P.I. Global analysis of fluorescence lifetime imaging microscopy data. Biophys J 2000; 78(4): 2127–2137, http://dx.doi.org/10.1016/s0006-3495(00)76759-2.
- Angres B., Steuer H., Weber P., Wagner M., Schneckenburger H. A membrane-bound FRET-based caspase sensor for detection of apoptosis using fluorescence lifetime and total internal reflection microscopy. Cytometry A 2009; 75(5): 420–427, http://dx.doi.org/10.1002/cyto.a.20698.
- Weber P., Schickinger S., Wagner M., Angres B., Bruns T., Schneckenburger H. Monitoring of apoptosis in 3D cell cultures by FRET and light sheet fluorescence microscopy. Int J Mol Sci 2015; 16(3): 5375–5385, http://dx.doi.org/10.3390/ijms16035375.
- Bozza W.P., Di X., Takeda K., Rivera Rosado L.A., Pariser S., Zhang B. The use of a stably expressed FRET biosensor for determining the potency of cancer drugs. PLoS One 2014; 9(9): e107010, http://dx.doi.org/10.1371/journal.pone.0107010.
- Savitsky A.P., Rusanov A.L., Zherdeva V.V., Gorodnicheva T.V., Khrenova M.G., Nemukhin A.V. FLIM-FRET imaging of caspase-3 activity in live cells using pair of red fluorescent proteins. Theranostics 2012; 2(2): 215–226, http://dx.doi.org/10.7150/thno.3885.
- Rusanov A.L., Ivashina T.V., Vinokurov L.M., Fiks I.I., Orlova A.G., Turchin I.V., Meerovich I.G., Zherdeva V.V., Savitsky A.P. Lifetime imaging of FRET between red fluorescent proteins. J Biophotonics 2010; 3(12): 774–783, http://dx.doi.org/10.1002/jbio.201000065.
- Shcherbo D., Souslova E.A., Goedhart J., Chepurnykh T.V., Gaintzeva A., Shemiakina I.I., Gadella T.W., Lukyanov S., Chudakov D.M. Practical and reliable FRET/FLIM pair of fluorescent proteins. BMC Biotechnol 2009; 9: 24, http://dx.doi.org/10.1186/1472-6750-9-24.
- Shcherbo D., Shemiakina I.I., Ryabova A.V., Luker K.E., Schmidt B.T., Souslova E.A., Gorodnicheva T.V., Strukova L., Shidlovskiy K.M., Britanova O.V., Zaraysky A.G., Lukyanov K.A., Loschenov V.B., Luker G.D., Chudakov D.M. Near-infrared fluorescent proteins. Nat Methods 2010; 7(10): 827–829, http://dx.doi.org/10.1038/nmeth.1501.
- Shu X., Royant A., Lin M.Z., Aguilera T.A., Lev-Ram V., Steinbach P.A., Tsien R.Y. Mammalian expression of infrared fluorescent proteins engineered from a bacterial phytochrome. Science 2009; 324(5928): 804–807, http://dx.doi.org/10.1126/science.1168683.
- Shcherbakova D.M., Verkhusha V.V. Near-infrared fluorescent proteins for multicolor in vivo imaging. Nat Methods 2013; 10(8): 751–754, http://dx.doi.org/10.1038/nmeth.2521.
- Subach O.M., Gundorov I.S., Yoshimura M., Subach F.V., Zhang J., Grüenwald D., Souslova E.A., Chudakov D.M., Verkhusha V.V. Conversion of red fluorescent protein into a bright blue probe. Chem Biol 2008; 15(10): 1116–1124, http://dx.doi.org/10.1016/j.chembiol.2008.08.006.
- Filonov G.S., Piatkevich K.D., Ting L.M., Zhang J., Kim K., Verkhusha V.V. Bright and stable near-infrared fluorescent protein for in vivo imaging. Nat Biotechnol 2011; 29(8): 757–761, http://dx.doi.org/10.1038/nbt.1918.
- Rajoria S., Zhao L., Intes X., Barroso M. FLIM-FRET for cancer applications. Curr Mol Imaging 2014; 3(2): 144–161, http://dx.doi.org/10.2174/2211555203666141117221111.
- Nguyen Q.D., Lavdas I., Gubbins J., Smith G., Fortt R., Carroll L.S., Graham M.A., Aboagye E.O. Temporal and spatial evolution of therapy-induced tumor apoptosis detected by caspase-3-selective molecular imaging. Clin Cancer Res 2013; 19: 3914–3924, http://dx.doi.org/10.1158/1078-0432.CCR-12-3814.
- Challapalli A., Kenny L.M., Hallett W.A., Kozlowski K., Tomasi G., Gudi M., Al-Nahhas A., Coombes R.C., Aboagye E.O. 18F-ICMT-11, a caspase-3-specific PET tracer for apoptosis: biodistribution and radiation dosimetry. J Nucl Med 2013; 54(9): 1551–1556, http://dx.doi.org/10.2967/jnumed.112.118760.
- Susin S.A., Lorenzo H.K., Zamzami N., Marzo I., Snow B.E., Brothers G.M., Mangion J., Jacotot E., Costantini P., Loeffler M., Larochette N., Goodlett D.R., Aebersold R., Siderovski D.P., Penninger J.M., Kroemer G. Molecular characterization of mitochondrial apoptosis-inducing factor. Nature 1999; 397(6718): 441–446, http://dx.doi.org/10.1038/17135.
- Maltese W.A., Overmeyer J.H. Non-apoptotic cell death associated with perturbations of macropinocytosis. Front Physiol 2015; 6: 38, http://dx.doi.org/10.3389/fphys.2015.00038.
- Susin S.A., Zamzami N., Kroemer G. Mitochondria as regulators of apoptosis: doubt no more. Biochim Biophys Acta 1998; 1366(1–2): 151–165, http://dx.doi.org/10.1016/S0005-2728(98)00110-8.
- Green D.R., Kroemer G. The pathophysiology of mitochondrial cell death. Science 2004; 305(5684): 626–629, http://dx.doi.org/10.1126/science.1099320.
- Bouchier-Hayes L., Muсoz-Pinedo C., Connell S., Green D.R. Measuring apoptosis at the single cell level. Methods 2008; 44(3): 222–228, http://dx.doi.org/10.1016/j.ymeth.2007.11.007.
- Madar I., Ravert H., Nelkin B., Abro M., Pomper M., Dannals R., Frost J.J. Characterization of membrane potential-dependent uptake of the novel PET tracer 18F-fluorobenzyl triphenylphosphonium cation. Eur J Nucl Med Mol Imaging 2007; 34(12): 2057–2065, http://dx.doi.org/10.1007/s00259-007-0500-8.
- Madar I., Huang Y., Ravert H., Dalrymple S.L., Davidson N.E., Isaacs J.T., Dannals R.F., Frost J.J. Detection and quantification of the evolution dynamics of apoptosis using the PET voltage sensor F-18-fluorobenzyl triphenyl phosphonium. J Nucl Med 2009; 50: 774–780, http://dx.doi.org/10.2967/jnumed.108.061283.
- Bortner C.D., Oldenburg N.B., Cidlowski J.A. The role of DNA fragmentation in apoptosis. Trends Cell Biol 1995; 5(1): 21–26, http://dx.doi.org/10.1016/S0962-8924(00)88932-1.
- Gorczyca W., Gong J., Darzynkiewicz Z. Detection of DNA strand breaks in individual apoptotic cells by the in situ terminal deoxynucleotidyl transferase and nick translation assays. Cancer Res 1993; 53: 1945–1951.
- Negoescu A., Guillermet C., Lorimier P., Brambilla E., Labat-Moleur F. Importance of DNA fragmentation in apoptosis with regard to TUNEL specificity. Biomed Pharmacother 1998; 52(6): 252–258, http://dx.doi.org/10.1016/S0753-3322(98)80010-3.
- Diaconu C.C., Szathmári M., Kéri G., Venetianer A. Apoptosis is induced in both drug-sensitive and multidrug-resistant hepatoma cells by somatostatin analogue TT-232. Br J Cancer 1999; 80(8): 1197–1203, http://dx.doi.org/10.1038/sj.bjc.6690486.
- Naruse I., Keino H., Kawarada Y. Antibody against single-stranded DNA detects both programmed cell death and drug-induced apoptosis. Histochemistry 1994; 101(1): 73–78, http://dx.doi.org/10.1007/bf00315834.
- Cornelissen B., Kersemans V., Darbar S., Thompson J., Shah K., Sleeth K., Hill M.A., Vallis K.A. Imaging DNA damage in vivo using gammaH2AX-targeted immunoconjugates. Cancer Res 2011; 71(13): 4539–4549, http://dx.doi.org/10.1158/0008-5472.CAN-10-4587.
- Porębska I., Kosacka M., Sobańska E., Wyrodek E., Jankowska R. Comparative expression of apoptotic markers in lung adenocarcinoma and squamous cell carcinoma. Adv Exp Med Biol 2015, http://dx.doi.org/10.1007/5584_2015_121. [Epub ahead of print].
- Wu Y., Kim S.G., Xing D., Liu L., Park J.C., Chen T., Chen W.R. Fluorescence resonance energy transfer analysis of bid activation in living cells during ultraviolet-induced apoptosis. Acta Biochim Biophys Sin (Shanghai) 2007; 39(1): 37–45, http://dx.doi.org/10.1111/j.1745-7270.2007.00246.x.
- Louie A. Multimodality imaging probes: design and challenges. Chem Rev 2010; 110(5): 3146–3195, http://dx.doi.org/10.1021/cr9003538.
- Sapsford K.E., Algar W.R., Berti L., Gemmill K.B., Casey B.J., Oh E., Stewart M.H., Medintz I.L. Functionalizing nanoparticles with biological molecules: developing chemistries that facilitate nanotechnology. Chem Rev 2013; 113(3): 1904–2074, http://dx.doi.org/10.1021/cr300143v.
- Xing Y., Zhao J., Conti P.S., Chen K. Radiolabeled nanoparticles for multimodality tumor imaging. Theranostics 2014; 4: 290–306, http://dx.doi.org/10.7150/thno.7341.











