Моделирование морфологической разупорядоченности элементов минерального матрикса на наноуровне
Цель исследования — разработка наноуровневой функциональной модели костного матрикса с объединением его минеральных элементов в единую структуру минеральными соединениями и определение методом конечных элементов влияния осевой разупорядоченности элементов структуры на эффективные упругие модули и распределение полей деформаций и напряжений в моделируемой структуре.
Материалы и методы. Предложена новая морфологическая модель костной ткани на наноуровне (на уровне коллагеновых фибрилл), учитывающая минеральные связи между объединениями кристаллов гидроксиапатита на основе модели Ю.И. Денисова-Никольского. Методами прямого конечно-элементного моделирования и гомогенизации проведен анализ влияния вариации морфологических характеристик на локальное напряженно-деформированное состояние и механические свойства представительного объема кости на наноуровне.
Результаты. Установлено, что увеличение степени разупорядоченности минеральных элементов сопровождается увеличением деформаций и напряжений в моделируемой структуре. Значение модуля упругости при этом практически не меняется. Биологическая значимость данного феномена в том, что разупорядоченность минералов, независимо от направления действующих сил, всегда увеличивает риск разрушения костного матрикса.
Заключение. Разработана наноуровневая функциональная модель костного матрикса с объединением его минеральных элементов в единую структуру минеральными соединениями. Методом конечных элементов определено влияние осевой разупорядоченности элементов данной структуры на эффективные упругие модули и распределение полей деформаций и напряжений в моделируемой структуре. Показано качественное соответствие полученных результатов с экспериментом.
Современные методы диагностики, основанные на атомно-силовой микроскопии [1–3], позволяют изучать морфологию и механические свойства костных тканей на наноуровне, однако обладают рядом ограничений, обусловленных, в частности, возможностью исследования только поверхностного слоя образца. Изучение методов компьютерного моделирования в дополнение к прямым объективным методам позволяет получать информацию о процессах, происходящих внутри объема, а также изучать влияние микроструктуры на механические свойства костной ткани путем проведения многовариантных вычислительных экспериментов. Остеологические вычислительные модели позволяют при меньших экономических и временных затратах определить переменные, влияющие на конкретный результат реакции биосистемы [4].
Однако необходимо учитывать, что при проведении компьютерного моделирования используются упрощенные модели исследуемого объекта и правильность результата определяется структурно-функциональным соответствием модели ее естественному прототипу. В нашем случае упрощенная модель должна отражать основные морфофункциональные характеристики костной ткани на наноуровне. ее прототипом была выбрана морфологическая модель структуры костного матрикса, предложенная Ю.И. Денисовым-Никольским с соавт. [3], которая, в отличие от других моделей, учитывает наличие межкристаллических минеральных перемычек, оказывающих влияние на механические свойства костной ткани [5].
Данная модель имеет следующие характеристики [3, 6, 7]. Минералы располагаются в основном веществе вне- и внутрифибриллярно (рис. 1). В межфибриллярных пространствах объединения кристаллитов, прилегающие к коллагеновым фибриллам, окружают их, формируя манжетки, и контактируют с внутрифибриллярными объединениями. На отдалении от коллагеновых фибрилл кристаллиты образуют конгломераты, в которых они ориентированы в одном направлении. По отношению друг к другу эти конгломераты расположены под разными углами. Внутрифибриллярные объединения кристаллитов образуют ряд параллельных спирально закрученных пластов, которые ориентированы под углом 8–25° к оси фибрилл. Отдельные объединения минералов связывают соседние пласты, обеспечивая непрерывность минерального компонента фибрилл после удаления органической составляющей.
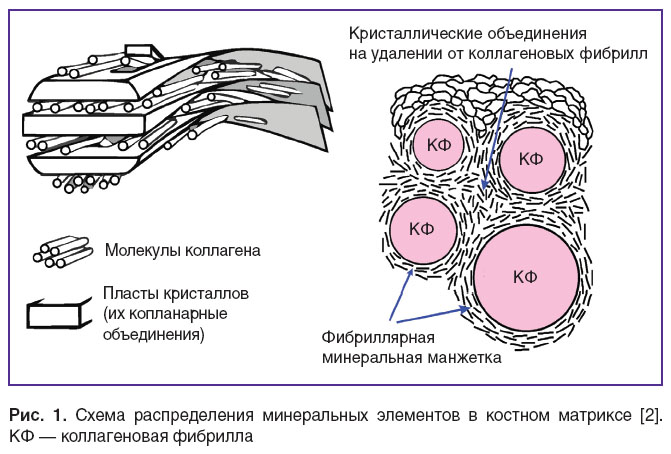 Рис. 1. Схема распределения минеральных элементов в костном матриксе [2]. КФ — коллагеновая фибрилла Рис. 1. Схема распределения минеральных элементов в костном матриксе [2]. КФ — коллагеновая фибрилла
|
Из приведенных морфологических характеристик костного матрикса выделяем две основополагающие: 1) пространственную упорядоченность минералов по их продольным осям относительно продольной оси фибрилл и 2) наличие между ними минеральных связей, которые формируют единый минеральный массив в каждой кости. Это позволит с биологических позиций оценить роль органического матрикса и его взаимоотношения с минеральным матриксом.
Структурная упорядоченность минерального матрикса зависит от упорядоченности органического, так как последний инициирует нуклеацию минералов и детерминирует их направленный рост, тем самым определяя пространственную организацию [8]. Другими словами, минеральный матрикс в каждом локусе костной ткани представляет собой запрограммированное отражение ультраструктуры органического матрикса. Следовательно, чем оптимальнее пространственная организация последнего по отношению к доминирующим направлениям постоянных механических нагрузок, тем оптимальнее механические свойства костных структур в каждом участке скелета.
Одной из основных причин возникновения отклонений в структуре органического матрикса являются нейрогуморальные сдвиги, происходящие в организме, вызываемые острыми заболеваниями, экстремальными факторами (операция, нервно-эмоциональный раздражитель и др.), хроническими болезнями, старением и т.д. Формирующиеся при этом изменения структуры костного матрикса носят адаптационный характер и аналогичны, по своей сути, происходящим в крови, но в отличие от них структурно стабильны. В процессе ремоделирования происходит постепенное накопление этих отклонений [9], проявлением чего, по нашему мнению, является изменение осевой сопряженности элементов минерального матрикса, наблюдаемое, например, при старении организма [10]. Это вызвано тем, что при старении в процессе формирования органического матрикса под влиянием ферментов происходит денатурация коллагена, т.е. разрывы и развертывание тройной винтовой структуры молекул. Кроме этого изменяется характер связей и геометрии коллагеновых фибрилл и волокон, растет количество пентозидиновых поперечных сшивок коллагена и отклонение ориентации волокон. Такие сдвиги сопровождаются снижением предела прочности костных структур, которая при старении значительно ниже [11–14]. Это показывает, почему оценка влияния степени разупорядоченности минеральных структур на механические свойства костного матрикса является одной из важнейших патогенетических задач, решение которой позволит точнее понять наноуровневые механизмы инициации усталостных повреждений, вызывающих развитие усталостных и низкоэнергетических переломов.
Минеральные связи между минералами [3, 5–7] объединяют минеральный матрикс в единый комплекс в каждой кости и заставляют по-новому оценить роль органической и минеральной составляющей в формировании механических свойств костных структур. Учет таких связей является существенным дополнением к доминирующим в настоящее время концепциям, которые не учитывают их существование. Согласно одной [15], коллаген препятствует разрушению костных структур при их растяжении, а минерал — при сжатии. Согласно другой [16], кость является двухкомпонентным композитом типа коллагеновой матрицы с несвязанными минеральными включениями.
Цель исследования — разработка наноуровневой функциональной модели костного матрикса с объединением его минеральных элементов в единую структуру минеральными соединениями и определение методом конечных элементов влияния осевой разупорядоченности структуры этой модели на эффективные упругие модули и распределение полей деформаций и напряжений в моделируемой структуре.
Материалы и методы
Общие характеристики расчетной морфофункциональной модели. Для оценки влияния структурной разупорядоченности минерального матрикса на жесткость и прочность в рамках морфологической модели Ю.И. Денисова-Никольского с соавт. [3] в расчетах использовали ее упрощенный вариант — элементарный представительный объем (ЭПО) материала — наименьший объем, содержащий априори всю статистическую информацию относительно распределения и морфологии неоднородностей материала на рассматриваемом уровне. В структуре ЭПО объединения кристаллитов распределены в шахматном порядке и представляют собой единый минеральный массив, поскольку соединены друг с другом минеральными перемычками.
Простейший вариант ЭПО (ячейка квазипериодичности) (рис. 2, а), схематично интерпретирующий нанонеоднородность, представлен отклоненным от вертикального направления центральным конгломератом кристаллитов и четырьмя фрагментами соседних неотклоненных минералов (1/4 площади каждого) с четырьмя перемычками между ними и центральным минералом. Дальнейший учет возможности взаимной разориентации конгломератов и перемычек, случайного распределения ориентаций, местоположений центров и размеров требует рассмотрения ЭПО, содержащих большее число конгломератов (рис. 2, б, в). Увеличение числа конгломератов в ЭПО наряду с расширением возможностей учета нерегулярности микроструктуры костной ткани позволяет более точно прогнозировать эффективные механические свойства, поскольку снижается влияние внешних границ.
Описанная модель [3] реализована в конечно-элементном программном комплексе PANTOCRATOR [17]. Метод конечных элементов в теории упругости вводится на основе уравнения виртуальных работ и представляет собой численный метод решения уравнений равновесия в частных производных путем минимизации потенциальной энергии, сводя задачу к поиску решения системы линейных алгебраических уравнений. Программный комплекс PANTOCRATOR позволяет автоматически генерировать дискретные модели ЭПО произвольной геометрии, получать решения краевых задач теории упругости и определять эффективные упругие модули и прочностные свойства ЭПО, анализировать распределения полей напряжений и деформаций для фрагмента морфологической структуры матрикса в наномасштабе. При решении краевых задач исследуются равновесные конфигурации ЭПО гетерогенной среды на основе законов сохранения количества движения и момента количества движения.
Основные параметры разработанной конечно-элементной модели ЭПО нанокомпозита костной ткани.
1. Задача решается в двумерной постановке — плоское деформируемое состояние. ЭПО имеет прямоугольную форму (см. рис. 2). Сравнение с результатами решения задачи в трехмерной постановке показало приемлемую точность двумерной постановки для разыскиваемых параметров напряженного состояния.
2. В модели ЭПО минеральные конгломераты также имеют прямоугольную форму (см. рис. 2), так как она соответствует среднестатистической форме кристаллита [18] и копланарного объединения [3], а также позволяет использовать при формировании ЭПО более простые конечно-элементные модели для проведения расчетов.
3. Размеры каждого объединения кристаллитов по главным осям составляют 2500×350 нм. Размеры минеральных перемычек варьируются в зависимости от их ориентации и ориентации кристаллитов, средний их размер — 200×30 нм; общая массовая доля минерального компонента в ЭПО — 70% (соответствует 55% площади ЭПО), что характерно для зрелой костной ткани. Указанные габариты минералов соответствуют размерам калькосферитов, описанных А. Boyde [19, 20] в формирующихся участках кости. Учитывая, что в минерализующемся костном матриксе у взрослого человека расстояния между фибриллами не превышают 20–30 нм, морфологический субстрат минерала включает в себя фрагменты минерализованных коллагеновых фибрилл (диаметром 50–80 нм и длиной до 2000 нм) с окружающими их манжетками, единичные матриксные везикулы (диаметром 30–200 нм) и разнонаправленные плотные группы кристаллов, связывающие манжетки соседних фибрилл.
4. Объединения кристаллитов расположены в шахматном порядке и погружены в органический матрикс. Между каждой парой соседних объединений кристаллитов существует только одна перемычка.
5. В рассматриваемой модели учитывается наличие отклонений осей минералов от вертикали и осей перемычек — от горизонтали. Угол отклонения осей минералов, характеризующих степень разупорядоченности, задавался детерминистически и варьировался в диапазоне от 0 до 8°. Углы отклонения перемычек от нормалей к конгломератам варьировались в диапазоне от –45 до 45°.
6. ЭПО представляет собой гетерогенный трехкомпонентный материал (минеральные конгломераты, минеральные перемычки и органический матрикс); краевые задачи определения напряженно-деформированного состояния ЭПО решаются в линейно-упругой постановке.
7. Механические свойства отдельных компонентов модели принимались соответствующими изотропным материалам, значения упругих модулей на наноуровне заимствованы из литературы [18–20] (см. таблицу).
 Используемые значения упругих модулей отдельных компонентов элементарного представительного объема Используемые значения упругих модулей отдельных компонентов элементарного представительного объема
|
Оценка эффективных упругих свойств на основе конечно-элементных расчетов. Эффективные свойства костной ткани на субмикроскопическом уровне принимались соответствующими ортотропному упругому материалу, для которого закон Гука можно записать в виде

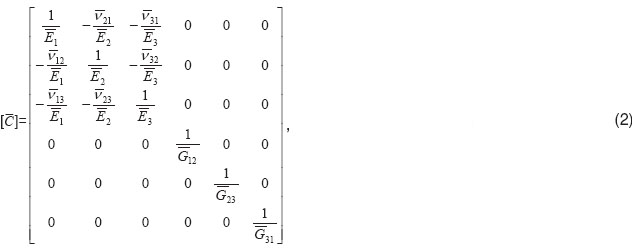
где 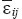 — тензор деформаций;
— тензор деформаций; 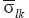 — тензор напряжений;
— тензор напряжений; 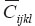 — тензор упругих податливостей 4-го ранга. Черта над введенными тензорами означает соответствие гомогенному (осредненному) материалу. Характеристики отдельных компонентов гетерогенного материала обозначены без черты. Для ортотропного материала тензору
— тензор упругих податливостей 4-го ранга. Черта над введенными тензорами означает соответствие гомогенному (осредненному) материалу. Характеристики отдельных компонентов гетерогенного материала обозначены без черты. Для ортотропного материала тензору 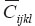 в собственных осях анизотропии соответствует симметричная матрица упругих податливостей
в собственных осях анизотропии соответствует симметричная матрица упругих податливостей 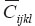 ]
]
где 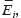
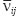 и
и 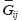 — модули Юнга, коэффициенты Пуассона и модули сдвига (i, j = 1, 2, 3), для определения которых решалась серия краевых задач с различными граничными условиями, соответствующими нагружению ЭПО в различных направлениях. Определяемые константы гомогенизированного материала должны обеспечивать равенство энергий при деформировании гомогенизированного и гетерогенного материала ЭПО. Для вычисления компонентов матрицы эффективных упругих податливостей
— модули Юнга, коэффициенты Пуассона и модули сдвига (i, j = 1, 2, 3), для определения которых решалась серия краевых задач с различными граничными условиями, соответствующими нагружению ЭПО в различных направлениях. Определяемые константы гомогенизированного материала должны обеспечивать равенство энергий при деформировании гомогенизированного и гетерогенного материала ЭПО. Для вычисления компонентов матрицы эффективных упругих податливостей 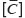 (2) использовались осредненные по представительному объему значения тензоров деформаций и напряжений, полученных в конечно-элементном решении:
(2) использовались осредненные по представительному объему значения тензоров деформаций и напряжений, полученных в конечно-элементном решении:

При решении задачи в двумерной постановке (плоское деформированное состояние) достаточно найти четыре упругие константы: 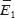 ,
,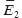 ,
,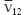 и
и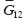 . Модули упругости в направлении оси, ортогональной рассматриваемой плоскости ЭПО, могут быть оценены без потери точности по правилу смесей.
. Модули упругости в направлении оси, ортогональной рассматриваемой плоскости ЭПО, могут быть оценены без потери точности по правилу смесей.
Результаты и обсуждение. При проведении исследований последовательно решались следующие задачи:
1) электронно-микроскопическое подтверждение появления морфологической разупорядоченности минеральных связей между минералами и минералов между собой по сравнению с нормой при патологических условиях или при старении;
2) оценка влияния угла наклона основных осей минералов по отношению к основным осям ЭПО (степень разупорядоченности) на механические свойства костного матрикса;
3) оценка влияния величины отклонения основных осей минеральных перемычек от горизонтального направления на механические свойства костного матрикса.
Морфологическая разупорядоченность минеральных связей между минералами и минералов между собой при патологических условиях или при старении по сравнению с нормой имеет свое подтверждение в литературе [21]. Причины возникновения этой разупорядоченности рассмотрены выше.
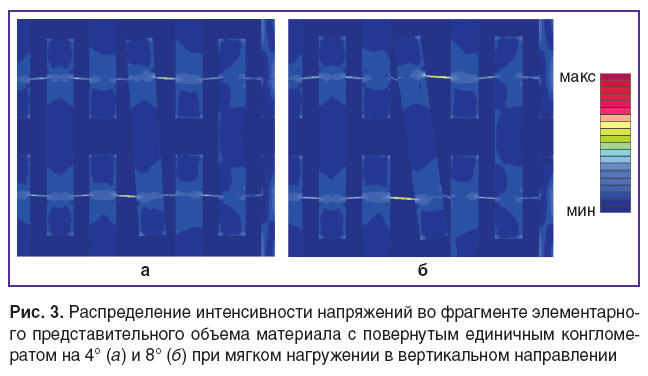
Влияние углов наклона минерала. Для оценки влияния угла разориентации минералов в ЭПО на его напряженно-деформированное состояние и эффективные упругие свойства проведены конечно-элементные расчеты с тремя различными углами: 0, 4 и 8°. Бóльших значений угла поворота для рассматриваемых геометрических параметров модели не удается достичь из-за ограничений вследствие контакта поворачиваемого конгломерата с соседними неповернутыми минералами (рис. 3). Результаты проведенных вычислительных экспериментов с ЭПО от П 1×1 до П 8×8 (П N×N означает, что ЭПО имеет прямоугольную форму и состоит из N простейших ячеек квазипериодичности по горизонтали и N по вертикали) показали, что поворот только одного конгломерата практически не оказывает влияния на значения эффективных упругих модулей 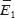 ,
, 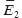 (отличия менее 1%), но влияет на уровень максимальной интенсивности напряжений (рис. 4), который определяет возможность локального разрушения. При повороте конгломерата на 8° максимальная интенсивность напряжений при жестком нагружении (механическое воздействие в условиях заданных перемещений, или компонент тензора деформаций) в вертикальном направлении возрастает на 36% и на 18% — при нагружении в горизонтальном направлении по сравнению с соответствующими идеализированными вариантами без отклонения ориентации. При мягком нагружении (механическое воздействие в условиях заданных внешних сил, или компонент тензора напряжений) эффект возрастания интенсивности напряжений при повороте конгломерата имеет тот же порядок и составляет 31 и 26% соответственно.
(отличия менее 1%), но влияет на уровень максимальной интенсивности напряжений (рис. 4), который определяет возможность локального разрушения. При повороте конгломерата на 8° максимальная интенсивность напряжений при жестком нагружении (механическое воздействие в условиях заданных перемещений, или компонент тензора деформаций) в вертикальном направлении возрастает на 36% и на 18% — при нагружении в горизонтальном направлении по сравнению с соответствующими идеализированными вариантами без отклонения ориентации. При мягком нагружении (механическое воздействие в условиях заданных внешних сил, или компонент тензора напряжений) эффект возрастания интенсивности напряжений при повороте конгломерата имеет тот же порядок и составляет 31 и 26% соответственно.
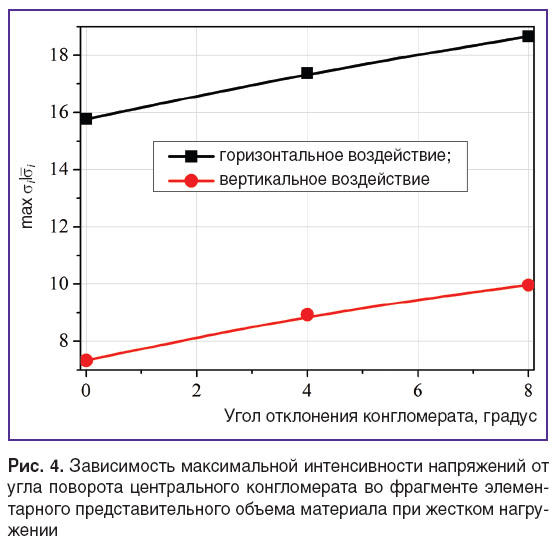 Рис. 4. Зависимость максимальной интенсивности напряжений от угла поворота центрального конгломерата во фрагменте элементарного представительного объема материала при жестком нагружении Рис. 4. Зависимость максимальной интенсивности напряжений от угла поворота центрального конгломерата во фрагменте элементарного представительного объема материала при жестком нагружении
|
При вычислении максимальных значений напряжений в угловых сингулярных точках перемычек использовали локально осредненные значения в пределах одного конечного элемента с характерным размером 5 нм. Следует отметить, что процесс разрушения перемычек определяется всем напряженным состоянием в пределах составляющего простейшего структурного элемента перемычки и поэтому именно локально осредненные значения напряжений обладают наибольшей информативностью при оценке прочности перемычек. Выбор размера области локального осреднения требует дальнейшего тщательного исследования.
На основании изложенного можно утверждать, что разупорядоченность минералов по продольным осям относительно направления нагрузки приводит к увеличению напряжений в костном матриксе. С патогенетических позиций это означает, что разупорядоченность минеральных конгломератов снижает прочностные свойства костного матрикса на наноуровне, а значит, и скелета в целом. Следовательно, разупорядоченность минералов является одним из основополагающих факторов, ведущих к увеличению плотности усталостных микроповреждений костной ткани, которая, например при старении, нарастает экспоненциально у женщин после четвертого десятилетия, а у мужчин — после пятого [13, 14].
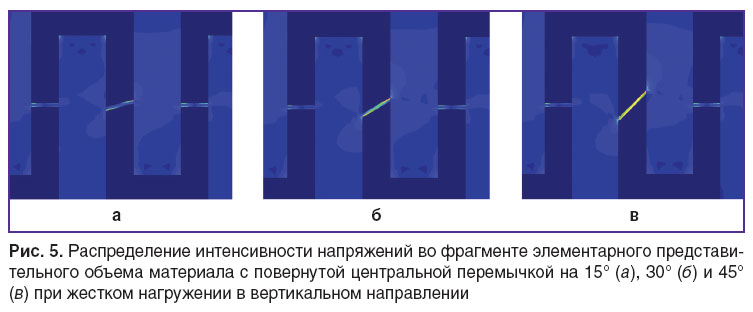
Влияние углов наклона перемычки. Для оценки этого влияния на напряженно-деформированное состояние и эффективные упругие свойства ЭПО проведены конечно-элементные расчеты с различными углами отклонения от горизонтального уровня — на 15, 30 и 45° (рис. 5). Результаты расчетов с ЭПО от П 1×1 до П 8×8 показали, что поворот только одной перемычки слабо влияет на значения эффективных упругих модулей ЭПО 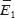 ,
,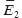 (отличия менее 1%), но сказывается на уровне максимальной интенсивности напряжений (рис. 6).
(отличия менее 1%), но сказывается на уровне максимальной интенсивности напряжений (рис. 6).
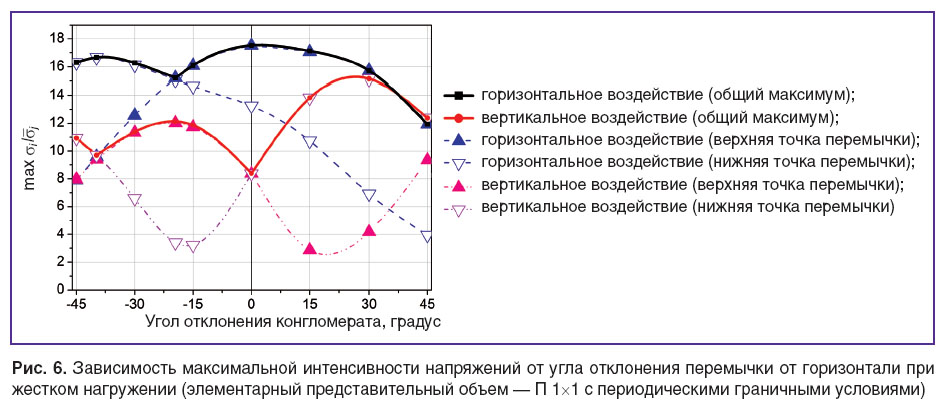
Установлено, что поворот отдельной перемычки в ЭПО при одних условиях нагружения увеличивает уровень экстремальных напряжений в ней, а при других — уменьшает. Так, при отклонении перемычки на 15° в направлении против часовой стрелки растяжение в горизонтальном направлении (жесткое нагружение, условия периодичности) характеризуется снижением максимальной относительной интенсивности напряжений на 2%, при 30° — на 12%, при 45° — на 47% в сравнении с идеализированным вариантом без поворота (см. рис. 6). Этот эффект вызван тем, что при растяжении в горизонтальном направлении ЭПО сжимается в вертикальном, поэтому соседние конгломераты смещаются по вертикали друг по отношению к другу, приводя к повороту соединяющей их перемычки и к возникновению в ней дополнительных усилий. В зависимости от направления начального отклонения перемычки от горизонтали вертикальные смещения конгломератов могут создать в них как дополнительное сжимающее напряжение (для перемычек, у которых поворот под нагрузкой компенсирует начальный поворот), так и дополнительное растягивающее напряжение (для перемычек, у которых поворот под нагрузкой увеличивает начальное отклонение).
Данный сценарий реализуется и при нагружении в вертикальном направлении, для которого отклонение перемычки на 15° в направлении против часовой стрелки приводит к увеличению максимальной относительной интенсивности напряжений на 65%, при 30° — на 80%, при 45° — на 47% в сравнении с идеализированным вариантом без поворота (см. рис. 6).
При отклонении перемычки в противоположную сторону (по часовой стрелке) наблюдается еще более сложный немонотонный характер зависимости интенсивности напряжений от угла отклонения (см. рис. 6), вызванный сменой места реализации экстремальных значений напряжений (рис. 7). При растяжении в горизонтальном направлении точка с максимумом интенсивности напряжений смещается с верхней стороны перемычки на нижнюю при углах наклона менее –20°, а при растяжении в вертикальном направлении смещается, наоборот, с нижней на верхнюю сторону при углах наклона менее 0° с повторной последующей сменой точки реализации максимума с верхней стороны на нижнюю при углах наклона менее –38°.
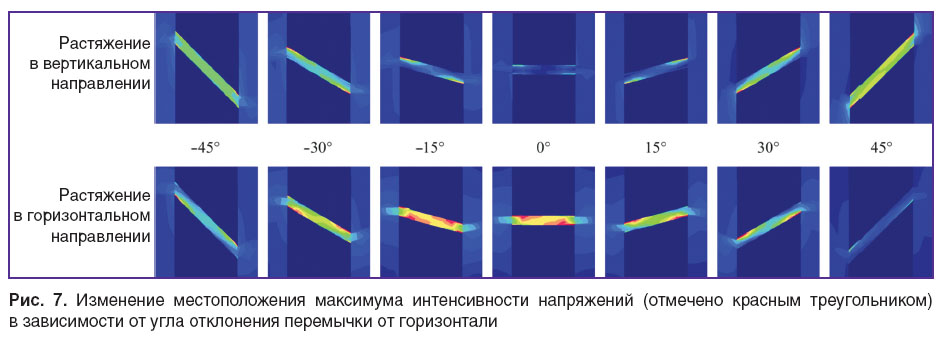 |
Рис. 7. Изменение местоположения максимума интенсивности напряжений (отмечено красным треугольником) в зависимости от угла отклонения перемычки от горизонтали |
Неповернутая перемычка при вертикальном нагружении обеспечивает минимальное значение (среди всех углов поворота) максимальных (по всем точкам ЭПО) интенсивностей напряжений (см. рис. 6), т.е. является оптимальной ориентацией с позиции локальной прочности ЭПО. При отклонении на 15–30° вне зависимости от направления наблюдаются локальные максимумы интенсивности напряжений, превосходящие значение в точке 0° в 1,5–2 раза (см. рис. 6). В то же время неповернутая перемычка при горизонтальном нагружении обеспечивает максимальное значение (среди всех углов поворота) максимальных (по всем точкам ЭПО) интенсивностей напряжений, однако следует учитывать, что уровень горизонтальных воздействий при стандартных повседневных локомоциях значительно ниже уровня вертикальных воздействий.
Полученные данные позволяют утверждать, что существуют неоптимальные направления минеральных связей по отношению к трендовым направлениям механических нагрузок. В результате повышается риск их разрушения, что можно рассматривать как начальный этап формирования усталостных повреждений. Данный биомеханический феномен имеет важное патогенетическое значение и позволяет предположить, что в условиях in vivo происходит «разрыхление» костного матрикса. Последнее при использовании гистологической технологии выявления усталостных повреждений проявляется локусами диффузной окраски [13, 21, 22].
Патогенетически необходимо учитывать, что разрушение отдельных перемычек ведет к увеличению нагрузки на оставшиеся и, следовательно, увеличивает риск их последующего разрушения [23]. Однако этот процесс в физиологических условиях развивается относительно медленно и поэтому был предложен постоянно действующий гипотетический механизм восстановления разрушенных соединений, который функционирует при выполнении следующих условий [23]:
пространственное возвращение минеральных конгломератов в исходное положение, существовавшее до разрушения связей между ними, за счет упругих деформаций костной ткани, окружающей поврежденный объем;
прекращение выполнения локомоторных функций и, соответственно, прекращение деформирования костных структур (например, во время сна).
Таким образом, структурная разупорядоченность минерального матрикса обусловлена разупорядоченностью органического матрикса, возникающей вследствие нейрогуморальных сдвигов в организме при ряде патологий и старении. Разупорядоченность на наноуровне приводит к разрушению минеральных связей, неоптимально ориентированных по отношению к трендовым направлениям механических нагрузок, что проявляется на следующих иерархических уровнях (микро, макро) структурной организации костной ткани в виде снижения ее прочностных характеристик и «разрыхления».
Независимо от направления механического воздействия, чем выше степень разупорядоченности минералов, тем, как правило, выше максимальные значения деформаций и напряжений в моделируемой структуре, при том что величина модуля упругости практически не меняется. Данный феномен биологически значим, так как предполагает, что разупорядоченность минералов независимо от направления действующих сил всегда увеличивает риск разрушения костного матрикса.
Полученные в настоящей работе данные представляют несомненный медико-биологический интерес, однако требуют дальнейших детальных модельных исследований, в том числе в условиях изменения степени минерализации костного матрикса, а также поиска количественного соответствия полученных результатов расчета наблюдаемым в экспериментах при появлении эффектов разупорядоченности элементов минерального матрикса.
Заключение. В рамках известной морфологической модели костного матрикса [3] разработана наноуровневая морфофункциональная модель с объединением минеральных элементов в единую структуру минеральными соединениями. Методом конечных элементов определено влияние осевой разупорядоченности элементов структуры на эффективные упругие модули и распределение полей деформаций и напряжений в моделируемой структуре.
Благодарности. Авторы выражают благодарность д.м.н. А.С. Аврунину за плодотворные научные дискуссии по постановке задачи и обсуждению полученных результатов.
Финансирование. Исследование выполнено за счет гранта Российского научного фонда (проект №15-19-00091).
Конфликт интересов. У авторов нет конфликта интересов.
Литература
- Wallace J.M. Applications of atomic force microscopy for the assessment of nanoscale morphological and mechanical properties of bone. Bone 2012; 50(1): 420–427, http://dx.doi.org/10.1016/j.bone.2011.11.008.
- Milovanovic P., Potocnik J., Djonic D., Nikolic S., Zivkovic V., Djuric M., Rakocevic Z. Age-related deterioration in trabecular bone mechanical properties at material level: nanoindentation study of the femoral neck in women by using AFM. Exp Gerontol 2012; 47(2): 154–159, http://dx.doi.org/10.1016/j.exger.2011.11.011.
- Денисов-Никольский Ю.И., Миронов С.П., Омельяненко Н.П., Матвейчук И.В. Актуальные проблемы теоретической и клинической остеоартрологии. М: ОАО «Типография «Новости»; 2005; 336 с.
- Knothe Tate M.L. Multiscale computational engineering of bones: state-of-the-art insights for the future. In: Engineering of functional skeletal tissues. Series title: Topics in bone biology. Vol. 3. Springer London; 2007; p. 141–160, http://dx.doi.org/10.1007/978-1-84628-366-6_10.
- Аврунин А.С., Семенов А.С., Федоров И.В., Мельников Б.Е., Докторов А.А., Паршин Л.К. Влияние минеральной связи между объединениями кристаллитов на механические свойства костного матрикса. Моделирование методом конечных элементов. Травматология и ортопедия России 2013; 2(68): 72–83.
- Докторов А.А., Денисов-Никольский Ю.И. Особенности рельефа минерализованной поверхности лакун и канальцев в пластинчатой кости. Бюллетень экспериментальной биологии и медицины 1993; 115(1): 61–65.
- Жилкин Б.А., Денисов-Никольский Ю.И., Докторов А.А. Особенности строения пластинчатой кости позвонков человека при возрастной инволюции и остеопорозе. Бюллетень экспериментальной биологии и медицины 2003; 135(4): 476–480.
- Аврунин А.С., Тихилов Р.М., Аболин А.Б., Щербак И.Г. Уровни организации минерального матрикса костной ткани и механизмы, определяющие параметры их формирования. Морфология 2005; 127(2): 78–82.
- Корнилов Н.В., Аврунин А.С. Адаптационные процессы в органах скелета. СПб: МОРСАР АВ; 2001; 296 с.
- Chatterji S., Wall C., Jeffery J. Changes in degree of orientation of bone minerals with age in the human femur. Experientia 1972; 28(2): 156–157, http://dx.doi.org/10.1007/bf01935727.
- Wang X., Li X., Shen X., Agrawal С.M. Age-related changes of noncalcified collagen in human cortical bone. Ann Biomed Eng 2003; 31(11): 1365–1371, http://dx.doi.org/10.1114/1.1623488.
- Wang X., Puram S. The toughness of cortical bone and its relationship with age. Ann Biomed Eng 2004; 32(1): 123–135, http://dx.doi.org/10.1023/b:abme.0000007797.92559.5e.
- Akkus O., Yeni Y.N., Wasserman N. Fracture mechanics of cortical bone tissue: a hierarchical perspective. Crit Rev Biomed Eng 2004; 32(5–6): 379–425, http://dx.doi.org/10.1615/critrevbiomedeng.v32.i56.10.
- Akkus O., Adar F., Schaffler M.B. Age-related changes in physicochemical properties of mineral crystals are related to impaired mechanical function of cortical bone. Bone 2004; 34(3): 443–453, http://dx.doi.org/10.1016/j.bone.2003.11.003.
- Currey J.D. Three analogies to explain the mechanical properties of bone. Biorheology 1964; 2: 1–10.
- Jäger I., Fratzl P. Mineralized collagen fibrils: a mechanical model with a staggered arrangement of mineral particles. Biophys J 2000; 79(4): 1737–1746, http://dx.doi.org/10.1016/S0006-3495(00)76426-5.
- Семенов А.С. PANTOCRATOR — конечно-элементный программный комплекс, ориентированный на решение нелинейных задач механики. В кн.: Труды V международной конференции «Научно-технические проблемы прогнозирования надежности и долговечности конструкций и методы их решения». СПб: Изд-во СПбГПУ; 2003; с. 466–480.
- Ньюман У., Ньюман М. Минеральный обмен кости. М: Иностранная литература; 1961; 269 с.
- Boyde A., Hobdell M.H. Scanning electron microscopy of lamellar bone. Z Zellforsch Mikrosk Anat 1969; 93(2): 213–231, http://dx.doi.org/10.1007/bf00336690.
- Boyde A. Scanning electron microscope studies of bone. In: The biochemistry and physiology of bone. Vol I: Structure. Edited by Bourne G.H. Elsevier BV; 1972; p. 259–310, http://dx.doi.org/10.1016/b978-0-12-119201-3.50015-9.
- Fazzalari N.L., Forwood M.R., Manthey B.A., Smith K., Kolesik P. Three-dimensional confocal images of microdamage in cancellous bone. Bone 1998; 23(4): 337–378, http://dx.doi.org/10.1016/s8756-3282(98)00111-2.
- Wenzel T.E., Schaffler M.B., Fyhrie D.P. In vivo trabecular microcracks in human vertebral bone. Bone 1996; 19(1): 89–95, http://dx.doi.org/10.1016/8756-3282(96)88871-5.
- Аврунин А.С., Тихилов Р.М., Паршин Л.К., Мельников Б.Е. Иерархическая организация скелета — фактор, регламентирующий структуру усталостных повреждений. Часть II. Гипотетическая модель формирования и разрушения связей между объединениями кристаллитов. Травматология и ортопедия России 2010; 1(55): 48–57.