Особенности сплайсинг-ориентированных ДНК-микрочипов и их применение в биомедицинских исследованиях (обзор)
Альтернативный сплайсинг (АС) обеспечивает многообразие изоформ белков и зрелых мРНК, относящихся к одному гену, и является необходимым звеном в ходе дифференцировки и функционирования клеток и тканей. ДНК-микрочипы — высокопроизводительный метод изучения транскриптома как на уровне суммарной экспрессии генов, так и на уровне репертуара альтернативно-сплайсированных изоформ мРНК. Изучение паттернов АС обусловливает необходимость тщательных процедур подбора последовательностей зондов для обеспечения надлежащей точности анализа.
Существует два основных типа ДНК-микрочипов, ориентированных на изучение АС. Микрочипы первого типа содержат зонды, направленные на участки внутри границ экзонов (тела экзонов); микрочипы второго типа содержат зонды, направленные как на тела экзонов, так и на участки соединений экзон–экзон, экзон–интрон. Рассмотрены особенности подбора последовательностей зондов и общий дизайн двух типов ДНК-микрочипов, охарактеризованы их основные преимущества и ограничения.
Отдельный раздел посвящен результатам исследований АС, полученным с применением ДНК-микрочипов. В частности, с применением ДНК-микрочипов был выявлен ряд механизмов процессинга и сплайсинга пре-мРНК, описаны паттерны АС, ассоциированные с онкологическими заболеваниями, процессами дифференцировки клеток и тканей. Показано, что регуляция аппарата сплайсинга является необходимой составляющей в ходе канцерогенеза и дифференцировки. Рассмотрены примеры использования сплайсинг-ориентированных ДНК-микрочипов при выявлении диагностических маркеров и механизмов развития патологий. Перспективным направлением исследований является изучение роли и механизмов АС при дифференцировке и поддержании плюрипотентного состояния индуцированных стволовых клеток, функционировании иммуноцитов и инфицированных клеток в ходе иммунного ответа на инфекцию. Сплайсинг-ориентированные ДНК-микрочипы являются сравнительно недорогим, но информативным инструментом исследований, что дает основание предполагать их внедрение в клиническую практику в течение ближайших лет.
Предшественники мРНК (пре-мРНК) более 90% генов человека подвергаются альтернативному сплайсингу (АС) [1, 2]. Продукты трансляции изоформ мРНК, образующихся в результате АС, могут выполнять разные функции в клетке, вплоть до антагонистических. АС является одним из фундаментальных механизмов, вовлеченных в реализацию функций клеток и тканей, а также в процессы их дифференцировки. Выделяют 8 типов АС (рис. 1). Основным результатом АС является многообразие комбинаций конститутивных и альтернативных экзонов, составляющих зрелый транскрипт. Конститутивные экзоны в норме присутствуют во всех зрелых изоформах мРНК, тогда как наличие альтернативных экзонов определяется составом и особенностями функционирования аппарата сплайсинга. Таким образом, АС приводит к образованию совокупности мРНК, формирующих транскриптом клетки.
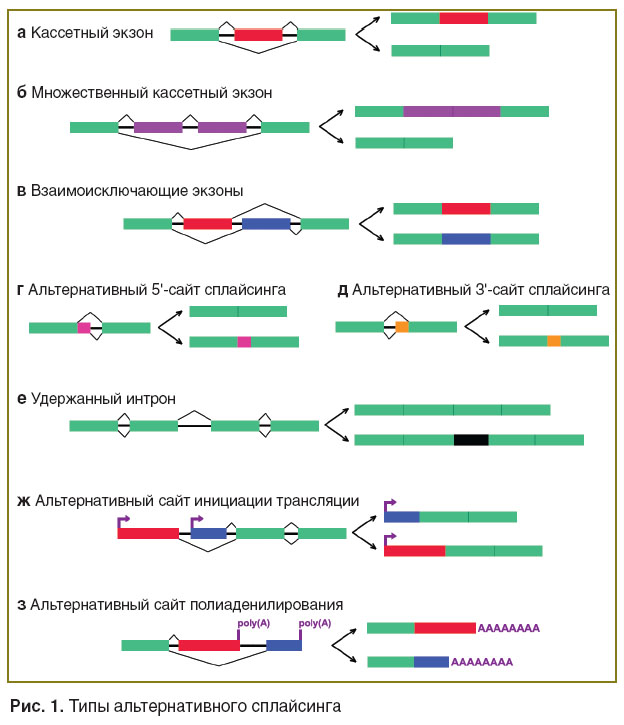 Рис. 1. Типы альтернативного сплайсинга Рис. 1. Типы альтернативного сплайсинга
|
Исследование транскриптома проводится в двух основных направлениях: 1) оценка изменения суммарного уровня представленности всех мРНК гена (экспрессии гена); 2) анализ состава и количественного соотношения сплайсированных изоформ зрелых мРНК данного гена. Комплексное изучение транскриптома требует использования высокопроизводительных и точных методов. Такие методы, как ОТ-ПЦР (обратная транскрипция-полимеразная цепная реакция) и ПЦР в режиме реального времени, сопряжены с большими время- и трудозатратами, позволяют анализировать лишь несколько генов в рамках одного эксперимента, однако являются «золотым стандартом» точности. В настоящее время для анализа транскриптома клеток и тканей применяются сравнительно новые методы, обладающие большей производительностью — использование ДНК-микрочипов и РНК-секвенирования на базе технологии пиросеквенирования [3, 4]. При отсутствии значительных различий в точности получаемых результатов РНК-секвенирование является более дорогостоящим методом [5–7]. Таким образом, ДНК-микрочипы обеспечивают оптимальное сочетание между производительностью, стоимостью исследования и точностью получаемых результатов.
В обзоре рассмотрены современные подходы к дизайну ДНК-микрочипов, ориентированных на изучение АС, освещены ключевые аспекты их применения в биологических и медицинских исследованиях.
Особенности дизайна сплайсинг-ориентированных ДНК-микрочипов
Основным этапом разработки дизайна сплайсинг-ориентированных ДНК-микрочипов является формирование пула зондов, комплементарных определенным участкам последовательности изоформ мРНК. Для достижения максимальной точности анализа зонды должны удовлетворять следующим требованиям: 1) узкий диапазон температур плавления (Tпл) и процента содержания нуклеотидов G и C (%GC); 2) минимальная вероятность образования устойчивой вторичной структуры зонда (шпильки); 3) минимальная вероятность кросс-гибридизации (связывания с нецелевой мРНК).
При изучении АС важным аспектом является выбор локализации участков гибридизации зондов в составе целевой мРНК. Выделяют два основных типа локализации зондов: 1-й тип — внутри границ экзонов и удержанных интронов; 2-й тип — в местах соединения участков экзонов (экзон–экзон) или экзонов и интронов (экзон–интрон) (рис. 2). Для 1-го типа более высока вероятность успешного нахождения зондов, удовлетворяющих заданным критериям, что связано с большой протяженностью экзонов и интронов человека [8]. Использование зондов 2-го типа позволяет сделать однозначные выводы об изменении качественного состава и уровня представленности сплайсированных вариантов мРНК. Однако в силу ограничений по локализации вероятность подбора зондов, полностью удовлетворяющих всем вышеперечисленным критериям, меньше, чем для 1-го типа. Таким образом, для изучения особенностей АС применяются экзон-направленные ДНК-микрочипы, содержащие зонды 1-го типа, и ДНК-микрочипы, использующие зонды обоих типов.
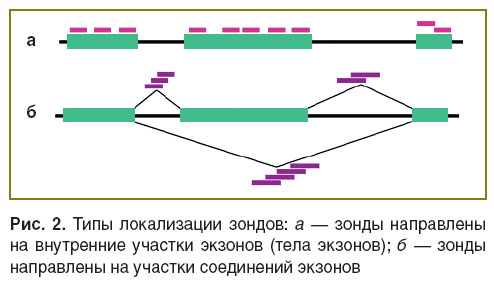 Рис. 2. Типы локализации зондов: а — зонды направлены на внутренние участки экзонов (тела экзонов); б — зонды направлены на участки соединений экзонов Рис. 2. Типы локализации зондов: а — зонды направлены на внутренние участки экзонов (тела экзонов); б — зонды направлены на участки соединений экзонов
|
Экзон-направленные микрочипы. Дизайн с локализацией зондов 1-го типа реализован в микрочипах серии Exon 1.0 ST Array (Affymetrix, США) — наиболее часто используемых при исследованиях АС. Чип содержит более 5,5 млн. зондов для детекции и квантификации большинства аннотированных экзонов. Каждому экзону соответствует набор из 4 зондов длиной 25 нуклеотидных оснований (н.о.) [9]. Несмотря на высокую плотность покрытия транскриптома, данный микрочип имеет ряд недостатков: 1) относительно малая длина зондов повышает вероятность кросс-гибридизации; 2) высокий уровень гетерогенности зондов (процент нуклеотидов G и C варьирует от 0 до 100) обусловливает очень широкий разброс интенсивности сигнала и затрудняет анализ данных [10]; 3) невозможность надежно оценивать малые (менее 25 н.о.) сдвиги 5’- и 3’-сайтов сплайсинга (см. рис. 1, г, д).
Основной проблемой, вытекающей из перечисленных «врожденных» недостатков микрочипов компании Affymetrix, является значительная доля ложноположительных результатов. Доля подтвержденных событий АС (с помощью ОТ-ПЦР, ПЦР в режиме реального времени) варьирует в пределах 20–80% [11–13].
Предложенный компанией Affymetrix критерий изменения экспрессии экзонов — индекс сплайсинга (SI) — вычисляется следующим образом:


На первом этапе вычисляется нормализованная интенсивность (NI) сигнала экзона. Для этого усредненный уровень сигнала зондов, соответствующих i-му экзону (ei), делится на суммарную интенсивность всех экзонов исследуемого гена j (1). Индекс сплайсинга вычисляется как логарифм отношения нормализованных интенсивностей опыта и контроля (2) [14]. В силу гетерогенности зондов, суммарных значений уровня экспрессии генов, а также наличия неизвестных и предсказанных сплайсированных изоформ данный критерий приводит к весомой доле ошибочных результатов. В связи с этим часть исследований с применением микрочипов Exon 1.0 ST Array связана c разработкой алгоритмов и введением более жестких критериев, направленных на корректную дискриминацию сигнал/фон, получение воспроизводимых результатов, повышение специфичности анализа [15, 16]. Разработка алгоритмов и программных продуктов для обработки первичного сигнала, коррекции сигнал/фон, анализа данных, полученных с применением экзон-направленных микрочипов компании Affymetrix, является развивающимся сегментом биоинформатики [17–19].
Микрочипы Agilent Exon Arrays применяются в гораздо меньшей степени. Основным отличием продуктов Agilent является длина зондов — 50–60 н.о. Минимальная длина экзонов, к которым подобраны зонды, составляет 35 н.о., «короткие» экзоны достраиваются до 50 н.о. при помощи поли-Т-спейсеров. Таким образом, охват экзома (совокупности экзонов) в микрочипах Agilent Exon Arrays существенно меньше. В микрочипе Human Exon 1.0 ST Array число охваченных экзонов (длиной ≥25 н.о.) — 1 084 639, тогда как число зондов микрочипа Agilent Human Exon 400K Microarray — 233 164 [9, 20]. Данных о точности анализа с применением микрочипов Agilent Exon Array в литературе мало. При исследовании изменений транскриптома мезенхимальных стволовых клеток человека в ответ на тяжелую гипоксию было выявлено 53 гена, подвергшихся АС, однако для валидации авторами было выбрано лишь 2 — наличие кассетных экзонов было успешно подтверждено [21].
ДНК-микрочипы, ориентированные на соединения экзонов. Микрочипы, содержащие зонды, комплементарные как телам, так и участкам соединения экзонов, являются более информативными по сравнению с предыдущим классом микрочипов. Во-первых, зонды, направленные на гибридизацию с граничными участками, позволяют однозначно детектировать все события АС. Во-вторых, совокупная информация о степени гибридизации зондов с конститутивными и альтернативными экзонами позволяет сделать более надежные выводы о событиях АС. Например, включение/пропуск экзона должно быть выражено не только в изменении степени гибридизации зонда и данного экзона, но и в изменениях сигнала гибридизации смежных конститутивных и альтернативных соединений (рис. 3), что является дополнительным критерием отбора истинно-положительных результатов. Так, исследование АС 16 генов, клинически значимых при опухолевом процессе, выявило 100% истинно-положительных результатов с учетом анализа совокупной информации со всех зондов, направленных на выявление событий АС [22]. Стратегия отбора согласованных изменений интенсивности гибридизации зондов, дискриминирующих событие АС, обеспечивает примерно 75% точность анализа [23, 24].
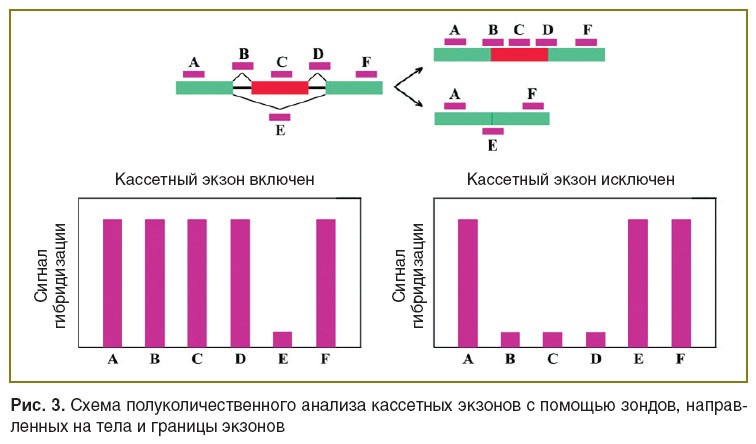 Рис. 3. Схема полуколичественного анализа кассетных экзонов с помощью зондов, направленных на тела и границы экзонов Рис. 3. Схема полуколичественного анализа кассетных экзонов с помощью зондов, направленных на тела и границы экзонов
|
Несмотря на явные преимущества зондов, комплементарных местам соединений экзон–экзон и экзон–интрон, подбор их часто является затруднительным. Пограничная локализация зондов оставляет очень мало степеней свободы для подбора последовательностей с узким диапазоном значений Тпл и %GC. Пограничная локализация также накладывает ограничения на длину зондов. Слишком длинный зонд будет эффективно гибридизоваться одной из своих «половин» с последовательностью целевого экзона в составе всех сплайсированных изоформ, имеющих данный экзон (рис. 4). Наоборот, зонд малой длины будет гибридизоваться менее эффективно, снижая чувствительность анализа. В работе K. Srinivasan и соавт. [25] установлено, что оптимальная длина зондов, направленных на участки соединения экзон–экзон или экзон–интрон, составляет 36–40 н.о. С другой стороны, пилотные испытания микрочипа hGWSA (human Genome Wide Splicing Array; ExonHit, США–Франция) показали, что удовлетворительная специфичность обеспечивается относительно короткими зондами 24–25 н.о. [26]. Данные различия прежде всего могут быть обусловлены типом гибридизуемой нуклеиновой кислоты. Так, в первом примере на чип гибридизовалась ДНК, а в случае hGWSA — РНК. Накопленный экспериментальный материал свидетельствует, что гибридизуемая на микрочип ДНК обеспечивает более высокие чувствительность и специфичность анализа в сравнении с РНК [27]. Сплайсинг-ориентированные микрочипы на платформе Affymetrix содержат 25-нуклеотидные зонды, гибридизующиеся с молекулой ДНК при температуре гибридизации 45°С [28]. Микрочипы на платформе Agilent содержат зонды длиной 60 н.о., гибридизующиеся с РНК при температуре 60–65°С [29–33]. Вариантом подбора зондов к местам соединения экзонов является не поиск «лучшего из возможных», а равномерное покрытие «стыка» набором зондов. В экспериментальном чипе на платформе Agilent 5 зондов длиной 36 н.о. с шагом 9 н.о. равномерно покрывали весь участок соединения, валидация показала 70–85% точность детекции [34]. Микрочип Human Transcriptome Array 2.0 (Affymetrix) содержит зонды к 260 488 соединениям, каждое соединение «покрыто» 4 зондами с шагом 2 н.о. [35].
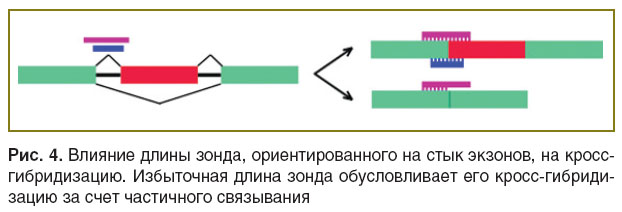 Рис. 4. Влияние длины зонда, ориентированного на стык экзонов, на кросс-гибридизацию. Избыточная длина зонда обусловливает его кросс-гибридизацию за счет частичного связывания Рис. 4. Влияние длины зонда, ориентированного на стык экзонов, на кросс-гибридизацию. Избыточная длина зонда обусловливает его кросс-гибридизацию за счет частичного связывания
|
Таким образом, несмотря на трудности, обусловленные термодинамическими ограничениями, зонды, ориентированные на соединения экзон–экзон или экзон–интрон в составе мРНК, обеспечивают высокую точность оценки событий АС в сравнении с экзон-направленными зондами. Поэтому большинство экспериментальных микрочипов для исследования АС содержат оба вида зондов.
Результаты исследований АС, полученные с применением ДНК-микрочипов
Механизмы процессинга и сплайсинга пре-мРНК. Изучение механизмов процессинга пре-мРНК и выявление генов-мишеней факторов сплайсинга явилось одной из первых фундаментальных областей исследований с применением сплайсинг-ориентированных ДНК-микрочипов. В работе J.C. Castle и соавт. [30], охватывающей 48 образцов тканей и клеточных линий человека, выявлено более 9500 событий АС. Совокупный анализ уровней экспрессии факторов сплайсинга, кассетных экзонов, последовательностей пре-мРНК обнаружил или подтвердил наличие 143 цис-элементов сплайсинга.
Дальнейшее развитие данного направления исследований проводилось с использованием экспериментального сплайсинг-ориентированного микрочипа на платформе Agilent, содержащего зонды для оценки 1804 событий АС у 482 генов, ассоциированных с онкогенезом и процессингом пре-мРНК [31]. В частности, выявлен профиль генов-мишеней регулятора CPEB1, отвечающего за выбор альтернативных сайтов полиаденилирования пре-мРНК, подтверждены сплайсинг-ассоциированный и сплайсинг-независимый механизмы смещения сайта полиаденилирования [33]. В ходе изучения антипролиферативного механизма молекулы сплайсеостатина А (SSA) была предложена механистическая модель взаимодействия пре-мРНК с элементами сплайсосомы SF-3b-155 и U2 snRNP, описаны нарушения данного взаимодействия под влиянием молекулы SSA [36]. Обработка клеток HCT116 камптоцетином (CPT), ингибитором топоизомеразы I, вызывала изменения паттерна сплайсинга 998 генов, 140 из которых участвовали в регуляции сплайсинга и процессинга пре-мРНК. Предложен механизм, согласно которому ингибирование топоизомеразы I приводит к гиперфосфорилированию РНК-полимеразы II, снижению скорости транскрипции и нарушению работы ассоциированных с полимеразой факторов сплайсинга [37, 38]. В работе M. Dutertre и соавт. [39] показано, что ингибиторы топоизомераз обусловливают АС 3’-экзонов за счет интерференции связывания альтернативного 3’-экзона с компонентом сплайсосомы HuR/ELAVL1.
Механизмы АС с участием РНК-хеликаз Ddx5 и Ddx17, являющихся компонентами сплайсосомы [40], были исследованы с использованием микрочипа Human Exon Array [41]. Установлено, что взаимодействие Ddx5/17 с ядерным рибонуклеопротеином hnRNP H/F обеспечивает также его взаимодействие с «сильными» (распознаваемыми в первую очередь) сайтами сплайсинга и включение экзонов, фланкированных такими сайтами, в состав зрелой мРНК. Кроме того, выявлена роль Ddx5/17 как регуляторов сплайсинга в ходе внутриклеточного сигналинга в ответ на связывание стероидных гормонов с соответствующими рецепторами [41, 42].
Масштабные исследования с применением микрочипов, направленных на соединения экзонов, позволили установить базовые механизмы функционирования первичных факторов сплайсинга — SRSF1 и SRSF2 [43], PTB [44], семейства hnRNP [45]. Данные регуляторы опосредуют как включение, так и пропуск экзонов, что зависит от многих факторов: силы и локализации сайтов сплайсинга, длины соседних интронов и состава сплайсосомы.
Паттерны АС при онкологических заболеваниях. Исследования дифференциальной экспрессии генов в ходе канцерогенеза являются самой обширной областью применения ДНК-микрочипов. Однако лишь небольшая часть работ затрагивает изучение опухоль-ассоциированных паттернов сплайсинга. Выявление специфических сплайсированных изоформ, характерных для определенного вида опухоли, является обоснованным подходом к поиску таргетных препаратов, терапевтических и прогностических маркеров.
В ходе изучения паттернов АС при раке легкого [46, 47], раке кишечника [48], опухолях мозга [49, 50], лейкемии [51–54], лимфоме Ходжкина [55], плоскоклеточном раке головы и шеи [56] выявлено, что чаще других в ходе канцерогенеза АС подвергаются гены компонентов цитоскелета, реализации и контроля клеточного цикла, межклеточного взаимодействия, реализации и регуляции апоптоза.
Целый блок исследований АС, выполняемых с применением ДНК-микрочипов, посвящен изучению опухольассоциированных механизмов сплайсинга и процессинга пре-мРНК. В масштабном исследовании A. Sveen и соавт. [57, 58], охватывающем 7 типов солидных опухолей, нестабильность транскриптома признана генеральной особенностью канцерогенеза, что обусловлено снижением экспрессии факторов сплайсинга. Схожие результаты получены в работе P.E. Carrigan и соавт. [59]. Они свидетельствуют о снижении разнообразия сплайсированных изоформ, а также уровня экспрессии 28 генов сплайсосомы в клеточных линиях рака поджелудочной железы Capan-1 и MiaPaCa2 по сравнению с клетками протока поджелудочной железы HPDE6. Избыточная активация фактора c-Jun ассоциирована с онкогенной трансформацией и обусловливает резистентность клеток к апоптозу [60–63]. Нокаут транскрипционного фактора c-Jun в клетках эпителия молочной железы мышей приводил к изменениям уровня экспресии 114 генов процессинга и сплайсинга пре-мРНК. При этом целый ряд апоптоз-ассоциированных генов (Сasp-8, Casp-9, Kifap3, Wisp1 и др.) подвергались АС. Выявлен механизм онкогенного действия c-Jun, ингибирующего проапоптотический фактор сплайсинга SRSF2 и работу сплайсосомы [64]. Исследование 31 линии опухолей молочной железы, принадлежащих к 3 подтипам, выявило схожие паттерны АС внутри каждого подтипа [65]. Показано, что тканеспецифичный фактор сплайсинга Fox2 является одним из основных регуляторов, определяющих специфичные для каждого подтипа паттерны АС.
Паттерны АС, ассоциированные с дифференцировкой клеток и тканей. Дифференцировка клеток и тканей реализуется путем регуляции экспрессии генов как на количественном уровне, так и путем изменения паттернов АС, приводящих к наработке тканеспецифичных белковых изоформ. Тканеспецифичный сплайсинг реализуется координированной активностью общих факторов (белки семейств SR, hnRNP) и специфических факторов, таких как Nova, nPTB, Fox, nSR100, MBNL, CELF [66–68]. В исследованиях C.C. Warzecha с соавт. [69] были идентифицированы факторы сплайсинга, ответственные за дифференцировку эпителиальной ткани и поддержание эпителиального фенотипа — ESRP1 и ESRP2. Авторами [70, 71] установлены спектр генов-мишеней, основной мотив цис-элементов — UGG, принцип регуляции сплайсинга: цис-элементы, находясь в составе нижележащего интрона, ведут к включению экзона в зрелый транскрипт, а находясь в составе экзона, ведут к его исключению. Нокаут ESRP1 и ESRP2 приводит к драматическим изменениям паттернов сплайсинга и к утрате эпителиального фенотипа, что было интерпретировано как эпителиально-мезенхимальный переход. Схожим образом проанализированы особенности регуляции сплайсинга фактором Fox, специфичным для мозга, сердца и поперечно-полосатых мышц. Исследован спектр генов-мишеней, определен основной регуляторный цис-элемент UGCAUG, являющийся энхансером или сайленсером в составе нижележащего или вышележащего интронов соответственно [72, 73].
С применением сплайсинг-ориентированных микрочипов были исследованы процессы дифференцировки и паттерны АС, характерные для нервной ткани. Дифференцировка клеток мышиной эмбриональной карциномы Р19 в нейроны, индуцированная трансретиноевой кислотой, сопровождалась появлением нейроспецифического фактора сплайсинга nPTB и исчезновением общего репрессора сплайсинга PTB. Установлено, что сплайсинг 26% экзонов (54 из 202) в ходе дифференцировки регулируется нейроспецифическим фактором nPTB [74]. Масштабное сравнительное исследование транскриптома мозга интактных мышей и мышей c нокаутированным специфическим для мозга регулятором сплайсинга Nova выявило около 600 событий АС. Полученные данные, интегрированные с анализом цис-регуляторных элементов, позволили установить: а) цис-элементы Nova в составе нижележащего интрона являются энхансерами, а в составе экзона и вышележащего интрона — сайленсерами сплайсинга; б) факторы Nova и Fox совместно регулируют около 100 экзонов; в) Nova выполняет двухуровневую регуляцию белок-белковых взаимодействий, задействованных в синаптических контактах, — как генов киназ и фосфатаз (25 и 9 соответственно), так и экзонов, кодирующих фосфорилируемые участки белков [75].
Анализ транскриптома трех типов клеток — эпителиоцитов, фибробластов и клеток эндотелия — выявил характерный для каждого типа паттерн сплайсированных изоформ, который сохранялся независимо от происхождения. Например, эпителиоциты легкого, простаты, почки, молочной железы и других органов имели общий паттерн сплайсированных изоформ. Характерные для каждого типа клеток паттерны АС были обусловлены экспрессией тканеспецифичных ре гуляторов сплайсинга. Так, в эпителиоцитах усиленно экспрессировались факторы ESRP и hnRNP, в фибробластах — NOVA1 и RBFox2, в клетках эндотелия — PTBP и MBNL [76].
Таким образом, результаты исследований четко демонстрируют, что АС является необходимым инструментом поддержания клеточной и тканевой идентичности.
Поиск диагностических маркеров и исследование механизмов развития патологий с использованием сплайсинг-ориентированных микрочипов. Поскольку отделы центральной нервной системы обладают максимальным разнообразием репертуара сплайсированных изоформ [14, 30], то сплайсинг-ориентированные ДНК-микрочипы находят применение при исследованиях и диагностике нейродегенеративных заболеваний. В настоящее время ведется поиск сплайсированных вариантов мРНК, присутствующих в крови, с целью ранней диагностики болезни Альцгеймера и Паркинсона — до наступления клинических проявлений [77–79].
Сравнение возрастных и обусловленных патологиями изменений транскриптома височной доли коры головного мозга [80] выявило, что развитие болезни Альцгеймера и лобно-височной долевой дегенерации ассоциировано со снижением уровня экспрессии регулятора сплайсинга Nova. Было показано, что снижение активности регулятора напрямую обусловливает дисбаланс в АС у 20 экзонов нейронспецифичных генов, ответственных за синаптическую передачу. Такое нейродегенеративное заболевание, как боковой амиотрофический склероз, обусловлено мутацией гена TARDBP, кодирующего компонент сплайсосомы TBP-43 [81]. В результате сравнения транскриптома моторных нейронов у здоровых волонтеров и пациентов с боковым амиотрофическим склерозом обнаружены различия в паттернах сплайсинга более 4000 генов, большинство из которых участвует в формировании цитоскелета и поддержании формы клетки [82].
Изучение паттернов сплайсинга в биоптатах дистальных мышц у пациентов c миотонической дистрофией позволило подтвердить механизм развития и выявить ранние маркеры заболевания. Усиленное связывание регулятора сплайсинга MBNL1 c амплифицированными CUG- или CCUG-повторами в составе пре-мРНК мутантных генов DMPK или ZNF9/CNBP вызывает блокировку MBNL1 и нарушение сплайсинга остальных мРНК, являющихся мишенями данного регулятора [83, 84]. Показано, что у пациентов без выраженных клинических проявлений заболевания выявлялись сплайсированные изоформы генов INSR, TTN, RYR1, CAMK2B, ARFGAP2. При этом все обозначенные гены являлись мишенями регулятора сплайсинга MBNL1 [85].
Таким образом, сплайсинг-ориентированные ДНК-микрочипы служат инструментом поиска новых диагностических маркеров и исследований патогенеза заболеваний на молекулярном уровне, но пока не применяются в диагностике. Вместе с тем ДНК-микрочипы, используемые для генотипирования, уже сейчас являются инструментом диагностики. В 2010 г. международная рабочая группа по вопросам клинической геномики рекомендовала использование микрочипов в диагностике врожденных аномалий развития в качестве теста первого выбора вместо кариотипирования [86]. В ряде стран метод ДНК-микрочипов используется в клинико-диагностической практике для выявления хромосомных перестроек, ассоциированных с широким спектром нарушений [87–90]. Можно ожидать, что в дальнейшем будут валидированы пулы мРНК, имеющие диагностическую и прогностическую значимость при заболеваниях различного генеза, а введение сплайсинг-ориентированных микрочипов в клинико-диагностическую практику представляется делом ближайших лет.
Перспективные направления исследований
Разработка генно-инженерных способов получения индуцированных плюрипотентных стволовых клеток (ИПСК) [91–93] открыла широкие перспективы для регенеративной медицины. В настоящее время основная часть работ, касающихся транскриптома СК, посвящена динамике суммарной экспрессии генов в ходе дифференцировки и поддержания плюрипотентного состояния СК [94–98]. Немногочисленные работы, касающиеся АС в ИПСК, свидетельствуют о том, что данный процесс является критически важным для поддержания плюрипотентного состояния [99, 100] и дифференцировки СК [101–103]. Можно ожидать, что изучение процессов АС в ходе индукции и коммитирования ИПСК с помощью сплайсинг-ориентированных ДНК-микрочипов станет развивающимся сегментом биомедицины.
Другим важным разделом исследований, остающимся относительно малоизученным в контексте АС, является моделирование инфекционного процесса — изучение паттернов АС клеток иммунной системы и инфицированных клеток в ходе развития инфекционного процесса и реализации иммунного ответа. Так, детально изучены динамические особенности транскриптома в ходе дифференцировки и активации различных субпопуляций иммуноцитов [104–110]. Изменения суммарной экспрессии генов изучены при инфицировании клеток нервной системы вирусом аргентинской геморрагической лихорадки [111], HSV-1 [112], при инфицировании гепатоцитов вирусом гепатита С [113], при моделировании бактериальной инфекции астроцитов [114], клеток эпителия кишечника [115]. При этом вопросы регуляции АС ключевых генов иммунного ответа в контексте инфекционного процесса освещены очень скудно и требуют дальнейшего изучения [116, 117].
Несмотря на все более широкое применение технологии РНК-секвенирования, ДНК-микрочипы по-прежнему остаются основным инструментом исследований транскриптома. Благодаря компромиссу между финансовыми затратами, ценностью и объемом получаемых результатов, в ближайшее десятилетие следует ожидать значительного увеличения доли биомедицинских исследований АС с применением ДНК-микрочипов, а также внедрения сплайсинг-ориентированных микрочипов в клиническую практику.
Финансирование исследования и конфликт интересов. Исследование не финансировалось какими-либо источниками, и конфликты интересов, связанные с данным исследованием, отсутствуют.
Литература
- Wang E.T., Sandberg R., Luo S., Khrebtukova I., Zhang L., Mayr C., Kingsmore S.F., Schroth G.P., Burge C.B. Alternative isoform regulation in human tissue transcriptomes. Nature 2008; 456(7221): 470–476, http://dx.doi.org/10.1038/nature07509.
- Pan Q., Shai O., Lee L.J., Frey B.J., Blencowe B.J. Deep surveying of alternative splicing complexity in the human transcriptome by high throughput sequencing. Nat Genet 2008; 40(12): 1413–1435, http://dx.doi.org/10.1038/ng.259.
- Novais R.C., Thorstenson Y.R. The evolution of Pyrosequencing® for microbiology: from genes to genomes. J Microbiol Methods 2011; 86(1): 1–7, http://dx.doi.org/10.1016/j.mimet.2011.04.006.
- Wang Z., Gerstein M., Snyder M. RNA-Seq: a revolutionary tool for transcriptomics. Nat Rev Genet 2009; 10(1): 57–63, http://dx.doi.org/10.1038/nrg2484.
- Ramani A.K., Calarco J.A., Pan Q., Mavandadi S., Wang Y., Nelson A.C., Lee L.J., Morris Q., Blencowe B.J., Zhen M., Fraser A.G. Genome-wide analysis of alternative splicing in Caenorhabditis elegans. Genome Res 2011; 21(2): 342–348, http://dx.doi.org/10.1101/gr.114645.110.
- Malone J.H., Oliver B. Microarrays, deep sequencing and the true measure of the transcriptome. BMC Biology 2011; 9: 34, http://dx.doi.org/10.1186/1741-7007-9-34.
- RNA-Seq misses what HTA delivers. URL: http://www.affymetrix.com/fa/media/hta_array_2_0_flyer.pdf.
- Affymetrix. GeneChip® Exon Array design. URL: http://media.affymetrix.com/support/technical/technotes/exon_array_design_technote.pdf.
- Affymetrix. GeneChip® Exon Array System for human, mouse, and rat. URL: http://www.affymetrix.com/support/technical/datasheets/exon_arraydesign_datasheet.pdf.
- Jaksik R., Marczyk M., Polanska J., Rzeszowska-Wolny J. Sources of high variance between probe signals in Affymetrix short oligonucleotide microarrays. Sensors (Basel) 2014; 14(1): 532–548; http://dx.doi.org/10.3390/s140100532.
- Hung L.H., Heiner M., Hui J., Schreiner S., Benes V., Bindereif A. Diverse roles of hnRNP L in mammalian mRNA processing: a combined microarray and RNAi analysis. RNA 2008; 14(2): 284–296, http://dx.doi.org/10.1261/rna.725208.
- Kurokawa K., Akaike Y., Masuda K., Kuwano Y., Nishida K., Yamagishi N., Kajita K., Tanahashi T., Rokutan K. Downregulation of serine/arginine-rich splicing factor 3 induces G1 cell cycle arrest and apoptosis in colon cancer cells. Oncogene 2014; 33(11): 1407–1417, http://dx.doi.org/10.1038/onc.2013.86.
- Yamashita Y., Matsuura T., Shinmi J., Amakusa Y., Masuda A., Ito M., Kinoshita M., Furuya H., Abe K., Ibi T., Sahashi K., Ohno K. Four parameters increase the sensitivity and specificity of the exon array analysis and disclose 25 novel aberrantly spliced exons in myotonic dystrophy. J Hum Genet 2012; 57(6): 368–374, http://dx.doi.org/10.1038/jhg.2012.37.
- Clark T.A., Schweitzer A.C., Chen T.X., Staples M.K., Lu G., Wang H., Williams A., Blume J.E. Discovery of tissue specific exons using comprehensive human exon microarrays. Genome Biol 2007; 8(4): R64, http://dx.doi.org/10.1186/gb-2007-8-4-r64.
- Xing Y., Stoilov P., Kapur K., Han A., Jiang H., Shen S., Black D.L., Wong W.H. MADS: a new and improved method for analysis of differential alternative splicing by exon-tiling microarrays. RNA 2008; 14(8): 1470–1479, http://dx.doi.org/10.1261/rna.1070208.
- Risueño A., Roson-Burgo B., Dolnik A., Hernandez-Rivas J.M., Bullinger L., De Las Rivas J. A robust estimation of exon expression to identify alternative spliced genes applied to human tissues and cancer samples. BMC Genomics 2014; 15: 879, http://dx.doi.org/10.1186/1471-2164-15-879.
- Chen P., Lepikhova T., Hu Y., Monni O., Hautaniemi S. Comprehensive exon array data processing method for quantitative analysis of alternative spliced variants. Nucleic Acids Research 2011; 39(18): e123, http://dx.doi.org/10.1093/nar/gkr513.
- Kapetis D., Clarelli F., Vitulli F., de Rosbo N.K., Beretta O., Foti M., Ricciardi-Castagnoli P., Zolezzi F. AMDA 2.13: a major update for automated cross-platform microarray data analysis. Biotechniques 2012; 53(1): 33–40.
- Liu X., Gao Z., Zhang L., Rattray M. puma 3.0: improved uncertainty propagation methods for gene and transcript expression analysis. BMC Bioinformatics 2013; 14: 39, http://dx.doi.org/10.1186/1471-2105-14-39.
- Agilent Technologies. Comprehensive coverage with the Agilent SurePrint G3 Exon Microarray system. URL: http://www.agilent.com/cs/library/brochures/5990-6928en_lo.pdf.
- Hu X., Wu R., Shehadeh L.A., Zhou Q., Jiang C., Huang X., Zhang L., Gao F., Liu X., Yu H., Webster K.A., Wang J. Severe hypoxia exerts parallel and cell-specific regulation of gene expression and alternative splicing in human mesenchymal stem cells. BMC Genomics 2014; 15: 303, http://dx.doi.org/10.1186/1471-2164-15-303.
- Pesson M., Eymin B., De La Grange P., Simon B., Corcos L. A dedicated microarray for in-depth analysis of pre-mRNA splicing events: application to the study of genes involved in the response to targeted anticancer therapies. Molecular Cancer 2014, 13: 9, http://dx.doi.org/10.1186/1476-4598-13-9.
- Li C., Kato M., Shiue L., Shively J.E., Ares M. Jr., Lin R.J. Cell type and culture condition-dependent alternative splicing in human breast cancer cells revealed by splicing-sensitive microarrays. Cancer Res 2006; 66(4): 1990–1999, http://dx.doi.org/10.1158/0008-5472.can-05-2593.
- Zhou W., Calciano M.A., Jordan H., Brenner M., Johnson S., Wu D., Lei L., Pallares D., Beurdeley P., Rouet F., Gill P.S., Bracco L., Soucaille C., Einstein R. High resolution analysis of the human transcriptome: detection of extensive alternative splicing independent of transcriptional activity. BMC Genet 2009; 10: 63, http://dx.doi.org/10.1186/1471-2156-10-63.
- Srinivasan K., Shiue L., Hayes J.D., Centers R., Fitzwater S., Loewen R., Edmondson L.R., Bryant J., Smith M., Rommelfanger C., Welch V., Clark T.A., Sugnet C.W., Howe K.J., Mandel-Gutfreund Y., Ares M. Jr. Detection and measurement of alternative splicing using splicing-sensitive microarrays. Methods 2005; 37: 345–359, http://dx.doi.org/10.1016/j.ymeth.2005.09.007.
- Fehlbaum P., Guihal C., Bracco L., Cochet O. A microarray configuration to quantify expression levels and relative abundance of splice variants. Nucleic Acids Res 2005; 33(5): e47, http://dx.doi.org/10.1093/nar/gni047.
- Harrison A., Binder H., Buhot A., Burden C.J., Carlon E., Gibas C., Gamble L.J., Halperin A., Hooyberghs J., Kreil D.P., Levicky R., Noble P.A., Ott A., Pettitt B.M., Tautz D., Pozhitkov A.E. Physico-chemical foundations underpinning microarray and next-generation sequencing experiments. Nucleic Acids Res 2013; 41(5): 2779–2796, http://dx.doi.org/10.1093/nar/gks1358.
- Affymetrix. GeneChip® WT PLUS Reagent Kit. URL: http://media.affymetrix.com/support/downloads/manuals/wtplus_reagentkit_assay_manual.pdf.
- Agilent 2015. Agilent One-Color Microarray-Based Exon Analysis — Low Input Quick Amp WT Labeling. URL: http://www.agilent.com/cs/library/usermanuals/Public/G4140-90042_Exon_One-color_2.0.pdf.
- Castle J.C., Zhang C., Shah J.K., Kulkarni A.V., Kalsotra A., Cooper T.A., Johnson J.M. Expression of 24,426 human alternative splicing events and predicted cis regulation in 48 tissues and cell lines. Nat Gen 2008; 40(12): 1416–1425, http://dx.doi.org/10.1038/ng.264.
- Muñoz M.J., Pérez Santangelo M.S., Paronetto M.P., de la Mata M., Pelisch F., Boireau S., Glover-Cutter K., Ben-Dov C., Blaustein M., Lozano J.J., Bird G., Bentley D., Bertrand E., Kornblihtt A.R. DNA damage regulates alternative splicing through inhibition of RNA polymerase II elongation. Cell 2009; 137(4): 708–720, http://dx.doi.org/10.1016/j.cell.2009.03.010.
- Paronetto M.P., Miñana B., Valcarcel J. The Ewing sarcoma protein regulates DNA damage-induced alternative splicing. Mol Cell 2011; 43(3): 353–368, http://dx.doi.org/10.1016/j.molcel.2011.05.035.
- Bava F.A., Eliscovich C., Ferreira P.G., Miсana B., Ben-Dov C., Guigó R., Valcárcel J., Méndez R. CPEB1 coordinates alternative 3’-UTR formation with translational regulation. Nature 2013; 495(7429): 121–125, http://dx.doi.org/10.1038/nature11901.
- Le K., Mitsouras K., Roy M., Wang Q., Xu Q., Nelson S.F., Lee C. Detecting tissue-specific regulation of alternative splicing as a qualitative change in microarray data. Nucleic Acids Res 2004; 32(22): e180, http://dx.doi.org/10.1093/nar/gnh173.
- Xu W., Seok J., Mindrinos M.N., Schweitzer A.C., Jiang H., Wilhelmy J., Clark T.A., Kapur K., Xing Y., Faham M., Storey J.D., Moldawer L.L., Maier R.V., Tompkins R.G., Wong W.H., Davis R.W., Xiao W.; Inflammation and Host Response to Injury Large-Scale Collaborative Research Program. Human transcriptome array for high-throughput clinical studies. Proc Natl Acad Sci USA 2011; 108(9): 3707–3712, http://dx.doi.org/10.1073/pnas.1019753108.
- Corrionero A., Miñana B., Valcárcel J. Reduced fidelity of branch point recognition and alternative splicing induced by the anti-tumor drug spliceostatin A. Gen Dev 2011; 25(5): 445–459, http://dx.doi.org/10.1101/gad.2014311.
- Solier S., Barb J., Zeeberg B.R., Varma S., Ryan M.C., Kohn K.W., Weinstein J.N., Munson P.J., Pommier Y. Genome-wide analysis of novel splice variants induced by topoisomerase I poisoning shows preferential occurrence in genes encoding splicing factors. Cancer Res 2010; 70(20): 8055–8065, http://dx.doi.org/10.1158/0008-5472.CAN-10-2491.
- Solier S., Ryan M.C., Martin S.E., Varma S., Kohn K.W., Liu H., Zeeberg B.R., Pommier Y. Transcription poisoning by Topoisomerase I is controlled by gene length, splice sites, and miR-142-3p. Cancer Res 2013; 73(15): 4830–4839, http://dx.doi.org/10.1158/0008-5472.CAN-12-3504.
- Dutertre M., Chakrama F.Z., Combe E., Desmet F.O., Mortada H., Polay Espinoza M., Gratadou L., Auboeuf D. A recently evolved class of alternative 3’-terminal exons involved in cell cycle regulation by topoisomerase inhibitors. Nat Commun 2014; 5: 3395, http://dx.doi.org/10.1038/ncomms4395.
- Liu Z.-R. p68 RNA helicase is an essential human splicing factor that acts at the U1 snRNA-5’ splice site duplex. Mol Cell Biol 2002; 22(15): 5443–5450, http://dx.doi.org/10.1128/mcb.22.15.5443-5450.2002.
- Dardenne E., Polay Espinoza M., Fattet L., Germann S., Lambert M.P., Neil H., Zonta E., Mortada H., Gratadou L., Deygas M., Chakrama F.Z., Samaan S., Desmet F.O., Tranchevent L.C., Dutertre M., Rimokh R., Bourgeois C.F., Auboeuf D. RNA helicases DDX5 and DDX17 dynamically orchestrate transcription, miRNA, and splicing programs in cell differentiation. Cell Rep 2014; 7(6): 1900–1913, http://dx.doi.org/10.1016/j.celrep.2014.05.010.
- Samaan S., Tranchevent L.-C., Dardenne E., Espinoza M.P., Zonta E., Germann S., Gratadou L., Dutertre M., Auboeuf D. The Ddx5 and Ddx17 RNA helicases are cornerstones in the complex regulatory array of steroid hormone-signaling pathways. Nucleic Acids Res 2014; 42(4): 2197–2207, http://dx.doi.org/10.1093/nar/gkt1216.
- Pandit S., Zhou Y., Shiue L., Coutinho-Mansfield G., Li H., Qiu J., Huang J., Yeo G.W., Ares M., Fu X.-D. Genome-wide analysis reveals SR protein cooperation and competition in regulated splicing. Mol Cell 2013; 50(2): 223–235, http://dx.doi.org/10.1016/j.molcel.2013.03.001.
- Huelga S.C., Vu A.Q., Arnold J.D., Liang T.Y., Liu P.P., Yan B.Y., Donohue J.P., Shiue L., Hoon S., Brenner S., Ares M. Jr., Yeo G.W. Integrative genome-wide analysis reveals cooperative regulation of alternative splicing by hnRNP proteins. Cell Rep 2012; 1(2): 167–178, http://dx.doi.org/10.1016/j.celrep.2012.02.001.
- Llorian M., Schwartz S., Clark T.A., Hollander D., Tan L.Y., Spellman R., Gordon A., Schweitzer A.C., de la Grange P., Ast G., Smith C.W. Position-dependent alternative splicing activity revealed by global profiling of alternative splicing events regulated by PTB. Nat Struct Mol Biol 2010; 17(9): 1114–1123, http://dx.doi.org/10.1038/nsmb.1881.
- Xi L., Feber A., Gupta V., Wu M., Bergemann A.D., Landreneau R.J., Litle V.R., Pennathur A., Luketich J.D., Godfrey T.E. Whole genome exon arrays identify differential expression of alternatively spliced, cancer-related genes in lung cancer. Nucleic Acids Res 2008; 36(20): 6535–6547, http://dx.doi.org/10.1093/nar/gkn697.
- de Miguel F.J., Sharma R.D., Pajares M.J., Montuenga L.M., Rubio A., Pio R. Identification of alternative splicing events regulated by the oncogenic factor SRSF1 in lung cancer. Cancer Res 2014; 74(4): 1105–1115, http://dx.doi.org/10.1158/0008-5472.CAN-13-1481.
- Gardina P.J., Clark T.A., Shimada B., Staples M.K., Yang Q., Veitch J., Schweitzer A., Awad T., Sugnet C., Dee S., Davies C., Williams A., Turpaz Y. Alternative splicing and differential gene expression in colon cancer detected by a whole genome exon array. BMC Genomics 2006; 7(1): 325, http://dx.doi.org/10.1186/1471-2164-7-325.
- Guo X., Chen Q.R., Song Y.K., Wei J.S., Khan J. Exon array analysis reveals neuroblastoma tumors have distinct alternative splicing patterns according to stage and MYCN amplification status. BMC Med Genomics 2011; 4: 35, http://dx.doi.org/10.1186/1755-8794-4-35.
- Yu F., Fu W.-M. Identification of differential splicing genes in gliomas using exon expression profiling. Mol Med Rep 2015; 11(2): 843–850, http://dx.doi.org/10.3892/mmr.2014.2775.
- Gerber J.M., Gucwa J.L., Esopi D., Gurel M., Haffner M.C., Vala M., Nelson W.G., Jones R.J., Yegnasubramanian S. Genome-wide comparison of the transcriptomes of highly enriched normal and chronic myeloid leukemia stem and progenitor cell populations. Oncotarget 2013; 4(5): 715–728, http://dx.doi.org/10.18632/oncotarget.990.
- Adamia S., Haibe-Kains B., Pilarski P.M., Bar-Natan M., Pevzner S., Avet-Loiseau H., Lode L., Verselis S., Fox E.A., Burke J., Galinsky I., Dagogo-Jack I., Wadleigh M., Steensma D.P., Motyckova G., Deangelo D.J., Quackenbush J., Stone R., Griffin J.D. A genome-wide aberrant RNA splicing in patients with acute myeloid leukemia identifies novel potential disease markers and therapeutic targets. Clin Cancer Res 2014; 20(5): 1135–1145, http://dx.doi.org/10.1158/1078-0432.CCR-13-0956.
- Adamia S., Bar-Natan M., Haibe-Kains B., Pilarski P.M., Bach C., Pevzner S., Calimeri T., Avet-Loiseau H., Lode L., Verselis S., Fox E.A., Galinsky I., Mathews S., Dagogo-Jack I., Wadleigh M., Steensma D.P., Motyckova G., Deangelo D.J., Quackenbush J., Tenen D.G., Stone R.M., Griffin J.D. NOTCH2 and FLT3 gene mis-splicings are common events in patients with acute myeloid leukemia (AML): new potential targets in AML. Blood 2014; 123(18): 2816–2825, http://dx.doi.org/10.1182/blood-2013-02-481507.
- Relógio A., Ben-Dov C., Baum M., Ruggiu M., Gemund C., Benes V., Darnell R.B., Valcárcel J. Alternative splicing microarrays reveal functional expression of neuron-specific regulators in Hodgkin lymphoma cells. J Biol Chem 2005; 280(6): 4779–4784, http://dx.doi.org/10.1074/jbc.m411976200.
- Li R., Ochs M.F., Ahn S.M., Hennessey P., Tan M., Soudry E., Gaykalova D.A., Uemura M., Brait M., Shao C., Westra W., Bishop J., Fertig E.J., Califano J.A. Expression microarray analysis reveals alternative splicing of LAMA3 and DST genes in head and neck squamous cell carcinoma. PLoS One 2014; 9(3): e91263, http://dx.doi.org/10.1371/journal.pone.0091263.
- Liu J., Xiao Y., Xiong H.-M., Li J., Huang B., Zhang H.-B., Feng D.-Q., Chen X.-M., Wang X.-Z. Alternative splicing of apoptosis-related genes in imatinib-treated K562 cells identified by exon array analysis. Int J Mol Med 2012; 29(4): 690–698, http://dx.doi.org/10.3892/ijmm.2011.872.
- Sveen A., Еgesen T.H., Nesbakken A., Rognum T.O., Lothe R.A., Skotheim R.I. Transcriptome instability in colorectal cancer identified by exon microarray analyses: Associations with splicing factor expression levels and patient survival. Genome Med 2011; 3(5): 32, http://dx.doi.org/10.1186/gm248.
- Sveen A., Johannessen B., Teixeira M.R., Lothe R.A., Skotheim R.I. Transcriptome instability as a molecular pan-cancer characteristic of carcinomas. BMC Genomics 2014; 15: 672, http://dx.doi.org/10.1186/1471-2164-15-672.
- Carrigan P.E., Bingham J.L., Srinvasan S., Brentnall T.A., Miller L.J. Characterization of alternative spliceoforms and the RNA splicing machinery in pancreatic cancer. Pancreas 2011; 40(2): 281–288, http://dx.doi.org/10.1097/MPA.0b013e31820128d2.
- Katiyar S., Casimiro M.C., Dettin L., Ju X., Wagner E.F., Tanaka H., Pestell R.G. C-jun inhibits mammary apoptosis in vivo. Mol Biol Cell 2010; 21(23): 4264–4274, http://dx.doi.org/10.1091/mbc.E10-08-0705.
- Albanese C., Johnson J., Watanabe G., Eklund N., Vu D., Arnold A., Pestell R.G. Transforming p21ras mutants and c-Ets-2 activate the cyclin D1 promoter through distinguishable regions. J Biol Chem 1995; 270(40): 23589–23597, http://dx.doi.org/10.1074/jbc.270.40.23589.
- Eferl R., Ricci R., Kenner L., Zenz R., David J.P., Rath M., Wagner E.F. Liver tumor development: c-Jun antagonizes the proapoptotic activity of p53. Cell 2003; 112(2): 181–192, http://dx.doi.org/10.1016/s0092-8674(03)00042-4.
- Shaulian E., Schreiber M., Piu F., Beeche M., Wagner E.F., Karin M. The mammalian UV response: c-Jun induction is required for exit from p53-imposed growth arrest. Cell 2000; 103(6): 897–907, http://dx.doi.org/10.1016/s0092-8674(00)00193-8.
- Katiyar S., Jiao X., Addya S., Ertel A., Covarrubias Y., Rose V., Casimiro M.C., Zhou J., Lisanti M.P., Nasim T., Fortina P., Pestell R.G. Mammary gland selective excision of c-Jun identifies its role in mRNA splicing. Cancer Res 2012; 72(4): 1023–1034, http://dx.doi.org/10.1158/0008-5472.CAN-11-3647.
- Lapuk A., Marr H., Jakkula L., Pedro H., Bhattacharya S., Purdom E., Hu Z., Simpson K., Pachter L., Durinck S., Wang N., Parvin B., Fontenay G., Speed T., Garbe J., Stampfer M., Bayandorian H., Dorton S., Clark T.A., Schweitzer A., Wyrobek A., Feiler H., Spellman P., Conboy J., Gray J.W. Exon-level microarray analyses identify alternative splicing programs in breast cancer. Mol Cancer Res 2010; 8(7): 961–974, http://dx.doi.org/10.1158/1541-7786.MCR-09-0528.
- Chen M., Manley J.L. Mechanisms of alternative splicing regulation: insights from molecular and genomics approaches. Nat Rev Mol Cell Biol 2009; 10: 741–754, http://dx.doi.org/10.1038/nrm2777.
- Hartmann B., Valcárcel J. Decrypting the genome’s alternative messages. Curr Opin Cell Biol 2009; 21(3): 377–386, http://dx.doi.org/10.1016/j.ceb.2009.02.006.
- Nilsen T.W., Graveley B.R. Expansion of the eukaryotic proteome by alternative splicing. Nature 2010; 463(7280): 457–463, http://dx.doi.org/10.1038/nature08909.
- Warzecha C.C., Sato T.K., Nabet B., Hogenesch J.B., Carstens R.P. ESRP1 and ESRP2 are epithelial cell-type-specific regulators of FGFR2 splicing. Mol Cell 2009; 33(5): 591–601, http://dx.doi.org/10.1016/j.molcel.2009.01.025.
- Warzecha C.C., Shen S., Xing Y., Carstens R.P. The epithelial splicing factors ESRP1 and ESRP2 positively and negatively regulate diverse types of alternative splicing events. RNA Biol 2009; 6(5): 546–562, http://dx.doi.org/10.4161/rna.6.5.9606.
- Warzecha C.C., Jiang P., Amirikian K., Dittmar K.A., Lu H., Shen S., Guo W., Xing Y., Carstens R.P. An ESRP-regulated splicing programme is abrogated during the epithelial-mesenchymal transition. EMBO J 2010; 29(19): 3286–3300, http://dx.doi.org/10.1038/emboj.2010.195.
- Das D., Clark T.A., Schweitzer A., Yamamoto M., Marr H., Arribere J., Minovitsky S., Poliakov A., Dubchak I., Blume J.E., Conboy J.G. A correlation with exon expression approach to identify cis-regulatory elements for tissue-specific alternative splicing. Nucleic Acids Res 2007; 35(14): 4845–4857, http://dx.doi.org/10.1093/nar/gkm485.
- Zhang C., Zhang Z., Castle J., Sun S., Johnson J., Krainer A.R., Zhang M.Q. Defining the regulatory network of the tissue-specific splicing factors Fox-1 and Fox-2. Genes Dev 2008; 22(18): 2550–2563, http://dx.doi.org/10.1101/gad.1703108.
- Boutz P.L., Stoilov P., Li Q., Lin C.H., Chawla G., Ostrow K., Shiue L., Ares M. Jr., Black D.L. A post-transcriptional regulatory switch in polypyrimidine tract-binding proteins reprograms alternative splicing in developing neurons. Genes Dev 2007; 21(13): 1636–1652, http://dx.doi.org/10.1101/gad.1558107.
- Zhang C., Frias M.A., Mele A., Ruggiu M., Eom T., Marney C.B., Wang H., Licatalosi D.D., Fak J.J., Darnell R.B. Integrative modeling defines the Nova splicing-regulatory network and its combinatorial controls. Science 2010; 329(5990): 439–443, http://dx.doi.org/10.1126/science.1191150.
- Mallinjoud P., Villemin J.P., Mortada H., Polay Espinoza M., Desmet F.O., Samaan S., Chautard E., Tranchevent L.C., Auboeuf D. Endothelial, epithelial, and fibroblast cells exhibit specific splicing programs independently of their tissue of origin. Genome Res 2014; 24(3): 511–521, http://dx.doi.org/10.1101/gr.162933.113.
- Potashkin J.A., Santiago J.A., Ravina B.M., Watts A., Leontovich A.A. Biosignatures for Parkinson’s disease and atypical parkinsonian disorders patients. PLoS One 2012; 7(8): e43595, http://dx.doi.org/10.1371/journal.pone.0043595.
- Calciano M., Lemarié J.C., Blondiaux E., Einstein R., Fehlbaum-Beurdeley P. A predictive microarray-based biomarker for early detection of Alzheimer’s disease intended for clinical diagnostic application. Biomarkers 2013; 18(3): 264–272, http://dx.doi.org/10.3109/1354750X.2013.773083.
- Lai M.K.P., Esiri M.M., Tan M.G.K. Genome-wide profiling of alternative splicing in Alzheimer’s disease. Genomics Data 2014; 2: 290–292, http://dx.doi.org/10.1016/j.gdata.2014.09.002.
- Tollervey J.R., Wang Z., Hortobagyi T., Witten J.T., Zarnack K., Kayikci M., Clark T.A., Schweitzer A.C., Rot G., Curk T., Zupan B., Rogelj B., Shaw C.E., Ule J. Analysis of alternative splicing associated with aging and neurodegeneration in the human brain. Genome Res 2011; 21(10): 1572–1582, http://dx.doi.org/10.1101/gr.122226.111.
- Pesiridis G.S., Lee V.M., Trojanowski J.Q. Mutations in TDP-43 link glycine-rich domain functions to amyotrophic lateral sclerosis. Hum Mol Gen 2009; 18(R2): R156–R162, http://dx.doi.org/10.1093/hmg/ddp303.
- Highley J.R., Kirby J., Jansweijer J.A., Webb P.S., Hewamadduma C.A., Heath P.R., Higginbottom A., Raman R., Ferraiuolo L., Cooper-Knock J., McDermott C.J., Wharton S.B., Shaw P.J., Ince P.G. Loss of nuclear TDP-43 in amyotrophic lateral sclerosis (ALS) causes altered expression of splicing machinery and widespread dysregulation of RNA splicing in motor neurons. Neuropathol Appl Neurobiol 2014; 40(6): 670–685, http://dx.doi.org/10.1111/nan.12148.
- Miller J.W., Urbinati C.R., Teng-Umnuay P., Stenberg M.G., Byrne B.J., Thornton C.A., Swanson M.S. Recruitment of human muscleblind proteins to (CUG)(n) expansions associated with myotonic dystrophy. EMBO J 2000; 19(17): 4439–4448, http://dx.doi.org/10.1093/emboj/19.17.4439.
- Osborne R.J., Lin X., Welle S., Sobczak K., O’Rourke J.R., Swanson M.S., Thornton C.A. Transcriptional and post-transcriptional impact of toxic RNA in myotonic dystrophy. Hum Mol Genet 2009; 18(8): 1471–1481, http://dx.doi.org/10.1093/hmg/ddp058.
- Nakamori M., Sobczak K., Puwanant A., Welle S., Eichinger K., Pandya S., Dekdebrun J., Heatwole C.R., McDermott M.P., Chen T., Cline M., Tawil R., Osborne R.J., Wheeler T.M., Swanson M.S., Moxley R.T. 3rd, Thornton C.A. Splicing biomarkers of disease severity in myotonic dystrophy. Ann Neurol 2013; 74(6): 862–872, http://dx.doi.org/10.1002/ana.23992.
- Miller D.T., Adam M.P., Aradhya S., Biesecker L.G., Brothman A.R., Carter N.P., Church D.M., Crolla J.A., Eichler E.E., Epstein C.J., Faucett W.A., Feuk L., Friedman J.M., Hamosh A., Jackson L., Kaminsky E.B., Kok K., Krantz I.D., Kuhn R.M., Lee C., Ostell J.M., Rosenberg C., Scherer S.W., Spinner N.B., Stavropoulos D.J., Tepperberg J.H., Thorland E.C., Vermeesch J.R., Waggoner D.J., Watson M.S., Martin C.L., Ledbetter D.H. Consensus statement: chromosomal microarray is a first-tier clinical diagnostic test for individuals with developmental disabilities or congenital anomalies. Am J Hum Genet 2010; 86(5): 749–764, http://dx.doi.org/10.1016/j.ajhg.2010.04.006.
- Chong W.W., Lo I.F., Lam S.T., Wang C.C., Luk H.M., Leung T.Y., Choy K.W. Performance of chromosomal microarray for patients with intellectual disabilities/developmental delay, autism, and multiple congenital anomalies in a Chinese cohort. Mol Cytogenet 2014; 7: 34, http://dx.doi.org/10.1186/1755-8166-7-34.
- Emy Dorfman L., Leite J.C., Giugliani R., Riegel M. Microarray-based comparative genomic hybridization analysis in neonates with congenital anomalies: detection of chromosomal imbalances. J Pediatr (Rio J) 2015; 91(1): 59–67, http://dx.doi.org/10.1016/j.jped.2014.05.007.
- Yuen R.K., Merkoulovitch A., MacDonald J.R., Vlasschaert M., Lo K., Grober E., Marshall C.R., Jarvi K.A., Kolomietz E., Scherer S.W. Development of a high-resolution Y-chromosome microarray for improved male infertility diagnosis. Fertil Steril 2014; 101(4): 1079–1085, http://dx.doi.org/10.1016/j.fertnstert.2013.12.027.
- Krepischi A.C., Capelli L.P., Silva A.G., de Araújo É.S., Pearson P.L., Heck B., da Costa C.M., de Camargo B., Rosenberg C. Large germline copy number variations as predisposing factor in childhood neoplasms. Future Oncol 2014; 10(9): 1627–1633, http://dx.doi.org/10.2217/fon.14.41.
- Takahashi K., Yamanaka S. Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors. Cell 2006; 126(4): 663–676, http://dx.doi.org/10.1016/j.cell.2006.07.024.
- Woltjen K., Michael I.P., Mohseni P., Desai R., Mileikovsky M., Hämäläinen R., Cowling R., Wang W., Liu P., Gertsenstein M., Kaji K., Sung H.K., Nagy A. рiggyBack transposition reprograms fibroblasts to induced pluripotent stem cells. Nature 2009; 458(7239): 766–770, http://dx.doi.org/10.1038/nature07863.
- Lowry W.E., Plath K. The many ways to make an iPS cell. Nat Biotechnol 2008; 26(11): 1246–1248, http://dx.doi.org/10.1038/nbt1108-1246.
- Fathi A., Hatami M., Hajihosseini V., Fattahi F., Kiani S., Baharvand H., Salekdeh G.H. Comprehensive gene expression analysis of human embryonic stem cells during differentiation into neural cells. PLoS One 2011; 6(7): e22856, http://dx.doi.org/10.1371/journal.pone.0022856.
- Dixon J.R., Jung I., Selvaraj S., Shen Y., Antosiewicz-Bourget J.E., Lee A.Y., Ye Z., Kim A., Rajagopal N., Xie W., Diao Y., Liang J., Zhao H., Lobanenkov V.V., Ecker J.R., Thomson J.A., Ren B. Chromatin architecture reorganization during stem cell differentiation. Nature 2015; 518(7539): 331–336, http://dx.doi.org/10.1038/nature14222.
- Lee J.H., Lee J.B., Shapovalova Z., Fiebig-Comyn A., Mitchell R.R., Laronde S., Szabo E., Benoit Y.D., Bhatia M. Somatic transcriptome priming gates lineage-specific differentiation potential of human-induced pluripotent stem cell states. Nat Commun 2014; 5: 5605, http://dx.doi.org/10.1038/ncomms6605.
- Busskamp V., Lewis N.E., Guye P., Ng A.H., Shipman S.L., Byrne S.M., Sanjana N.E., Murn J., Li Y., Li S., Stadler M., Weiss R., Church G.M. Rapid neurogenesis through transcriptional activation in human stem cells. Mol Syst Biol 2014; 10: 760, http://dx.doi.org/10.15252/msb.20145508.
- Dorn I., Klich K., Arauzo-Bravo M.J., Radstaak M., Santourlidis S., Ghanjati F., Radke T.F., Psathaki O.E., Hargus G., Kramer J., Einhaus M., Kim J.B., Kögler G., Wernet P., Schöler H.R., Schlenke P., Zaehres H. Erythroid differentiation of human induced pluripotent stem cells is independent of donor cell type of origin. Haematologica 2015; 100(1): 32–41, http://dx.doi.org/10.3324/haematol.2014.108068.
- Gabut M., Samavarchi-Tehrani P., Wang X., Slobodeniuc V., O’Hanlon D., Sung H.K., Alvarez M., Talukder S., Pan Q., Mazzoni E.O., Nedelec S., Wichterle H., Woltjen K., Hughes T.R., Zandstra P.W., Nagy A., Wrana J.L., Blencowe B.J. An alternative splicing switch regulates embryonic stem cell pluripotency and reprogramming. Cell 2011; 147(1): 132–146, http://dx.doi.org/10.1016/j.cell.2011.08.023.
- Rao S., Zhen S., Roumiantsev S., McDonald L.T., Yuan G.C., Orkin S.H. Differential roles of Sall4 isoforms in embryonic stem cell pluripotency. Mol Cell Biol 2010; 30(22): 5364–5380, http://dx.doi.org/10.1128/MCB.00419-10.
- Han H., Irimia M., Ross P.J., Sung H.K., Alipanahi B., David L., Golipour A., Gabut M., Michael I.P., Nachman E.N., Wang E., Trcka D., Thompson T., O’Hanlon D., Slobodeniuc V., Barbosa-Morais N.L., Burge C.B., Moffat J., Frey B.J., Nagy A., Ellis J., Wrana J.L., Blencowe B.J. MBNL proteins repress ES-cell-specific alternative splicing and reprogramming. Nature 2013; 498(7453): 241–245, http://dx.doi.org/10.1038/nature12270.
- Wu J.Q., Habegger L., Noisa P., Szekely A., Qiu C., Hutchison S., Raha D., Egholm M., Lin H., Weissman S., Cui W., Gerstein M., Snyder M. Dynamic transcriptomes during neural differentiation of human embryonic stem cells revealed by short, long, and paired-end sequencing. Proc Natl Acad Sci USA 2010; 107(11): 5254–5259, http://dx.doi.org/10.1073/pnas.0914114107.
- Salomonis N., Schlieve C.R., Pereira L., Wahlquist C., Colas A., Zambon A.C., Vranizan K., Spindler M.J., Pico A.R., Cline M.S., Clark T.A., Williams A., Blume J.E., Samal E., Mercola M., Merrill B.J., Conklin B.R. Alternative splicing regulates mouse embryonic stem cell pluripotency and differentiation. Proc Natl Acad Sci USA 2010; 107(23): 10514–10519, http://dx.doi.org/10.1073/pnas.0912260107.
- Royo S., Sainz B. Jr., Hernández-Jiménez E., Reyburn H., López-Collazo E., Guerra S. Differential induction of apoptosis, interferon signaling, and phagocytosis in macrophages infected with a panel of attenuated and nonattenuated poxviruses. J Virol 2014; 88(10): 5511–5523, http://dx.doi.org/10.1128/JVI.00468-14.
- Iglesias M.J., Reilly S.J., Emanuelsson O., Sennblad B., Pirmoradian Najafabadi M., Folkersen L., Mälarstig A., Lagergren J., Eriksson P., Hamsten A., Odeberg J. Combined chromatin and expression analysis reveals specific regulatory mechanisms within cytokine genes in the macrophage early immune response. PLoS One 7(2): e32306, http://dx.doi.org/10.1371/journal.pone.0032306.
- Saeed S., Quintin J., Kerstens H.H., Rao N.A., Aghajanirefah A., Matarese F., Cheng S.C., Ratter J., Berentsen K., van der Ent M.A., Sharifi N., Janssen-Megens E.M., Ter Huurne M., Mandoli A., van Schaik T., Ng A., Burden F., Downes K., Frontini M., Kumar V., Giamarellos-Bourboulis E.J., Ouwehand W.H., van der Meer J.W., Joosten L.A., Wijmenga C., Martens J.H., Xavier R.J., Logie C., Netea M.G., Stunnenberg H.G. Epigenetic programming of monocyte-to-macrophage differentiation and trained innate immunity. Science 2014; 345(6204): 1251086, http://dx.doi.org/10.1126/science.1251086.
- Olex A.L., Hiltbold E.M., Leng X., Fetrow J.S. Dynamics of dendritic cell maturation are identified through a novel filtering strategy applied to biological time-course microarray replicates. BMC Immunology 2010; 11: 41, http://dx.doi.org/10.1186/1471-2172-11-41.
- Wang P., Xue Y., Han Y., Lin L., Wu C., Xu S., Jiang Z., Xu J., Liu Q., Cao X. The STAT3-binding long noncoding RNA Inc-DC controls human dendritic cell differentiation. Science 2014; 344(6181): 310–313, http://dx.doi.org/10.1126/science.1251456.
- Zak D.E., Andersen-Nissen E., Peterson E.R., Sato A., Hamilton M.K., Borgerding J., Krishnamurty A.T., Chang J.T., Adams D.J., Hensley T.R., Salter A.I., Morgan C.A., Duerr A.C., De Rosa S.C., Aderem A., McElrath M.J. Merck Ad5/HIV induces broad innate immune activation that predicts CD8+ T-cell responses but is attenuated by preexisting Ad5 immunity. Proc Natl Acad Sci USA 2012; 109(50): E3503–E3512, http://dx.doi.org/10.1073/pnas.1208972109.
- Gattinoni L., Lugli E., Ji Y., Pos Z., Paulos C.M., Quigley M.F., Almeida J.R., Gostick E., Yu Z., Carpenito C., Wang E., Douek D.C., Price D.A., June C.H., Marincola F.M., Roederer M., Restifo N.P. A human memory T cell subset with stem cell-like properties. Nat Med 2011; 17(10): 1290–1298, http://dx.doi.org/10.1038/nm.2446.
- Kolokoltsova O.A., Yun N.E., Paessler S. Reactive astrogliosis in response to hemorrhagic fever virus: microarray profile of Junin virus-infected human astrocytes. Virol J 2014; 11: 126, http://dx.doi.org/10.1186/1743-422X-11-126.
- D’Aiuto L., Prasad K.M., Upton C.H., Viggiano L., Milosevic J., Raimondi G., McClain L., Chowdari K., Tischfield J., Sheldon M., Moore J.C., Yolken R.H., Kinchington P.R., Nimgaonkar V.L. Persistent Infection by HSV-1 is associated with changes in functional architecture of iPSC-derived neurons and brain activation patterns underlying working memory performance. Schizophr Bull 2015; 41(1): 123–132, http://dx.doi.org/10.1093/schbul/sbu032.
- Thomas E., Gonzalez V.D., Li Q., Modi A.A., Chen W., Noureddin M., Rotman Y., Liang T.J. HCV infection induces a unique hepatic innate immune response associated with robust production of type III interferons. Gastroenterology 2012; 142(4): 978–988, http://dx.doi.org/10.1053/j.gastro.2011.12.055.
- Zamanian J.L., Xu L., Foo L.C., Nouri N., Zhou L., Giffard R.G., Barres B.A. Genomic analysis of reactive astrogliosis. J Neuroscience 2012; 32(18): 6391–6410, http://dx.doi.org/10.1523/JNEUROSCI.6221-11.2012.
- Shulzhenko N., Morgun A., Hsiao W., Battle M., Yao M., Gavrilova O., Orandle M., Mayer L., Macpherson A.J., McCoy K.D., Fraser-Liggett C., Matzinger P. Crosstalk between B lymphocytes, microbiota and the intestinal epithelium governs immunity versus metabolism in the gut. Nat Med 2011; 17(12): 1585–1594, http://dx.doi.org/10.1038/nm.2505.
- Rodrigues R., Grosso A.R., Moita L. Genome-wide analysis of alternative splicing during dendritic cell response to a bacterial challenge. PLoS One 2013; 8(4): e61975, http://dx.doi.org/10.1371/journal.pone.0061975.
- Ip J.Y., Tong A., Pan Q., Topp J.D., Blencowe B.J., Lynch K.W. Global analysis of alternative splicing during T-cell activation. RNA 2007; 13(4): 563–572, http://dx.doi.org/10.1261/rna.457207.










