Функциональная структура связей в диссоциированной культуре гиппокампа, выращиваемой на микроэлектродной матрице
Диссоциированные нейрональные культуры используют в качестве удобной модели мозга для изучения фундаментальных механизмов обработки сигналов, памяти, обучения, а также синаптической пластичности в нейронных сетях. Изучение краткосрочной и долговременной памяти в гиппокампальных культурах требует одновременной регистрации сигналов с большого числа электродов и стимулирования биоэлектрической активности.
Цель исследования — выявление особенностей пластичности на уровне нейронной сети в модели первичных культур клеток гиппокампа, изучение стабильности изменений импульсной активности культур, как спонтанной, так и индуцированной электрической стимуляцией.
Материалы и методы. Произведена оценка долгосрочных изменений функциональных характеристик импульсов, распространяющихся между нейронами в гиппокампальных культурах, растущих на микроэлектродных матрицах. Исследовано влияние низкочастотной стимуляции (0,1–0,5 Гц) с частотой, равной частоте спонтанной пачечной активности, на изменение функциональных связей в сети на разных временны'х интервалах.
Результаты. Установлено, что низкочастотная стимуляция гиппокампальных культур, растущих на микроэлектродных матрицах, индуцирует реорганизацию структуры связей сети. Данный эффект сохраняется на протяжении десятков минут. В случае наблюдений на протяжении часов спонтанные изменения структуры связей сети могут подавить индуцированные стимуляцией изменения.
Культуры диссоциированных нейрональных клеток, выращиваемые на микроэлектродных матрицах, широко используются в качестве удобных моделей для исследования фундаментальных механизмов обработки сигналов, обучения и памяти, а также синаптической пластичности в нейронных сетях [1–4]. Известно, что низкочастотные стимулы культуры нейронов могут вызвать пачечный сетевой ответ, направление распространения которого зависит от расположения стимулирующего электрода [5, 6]. Индуцированные реверберирующие пачки играют ключевую роль в изменении функциональных связей в сети [7–11]. В культурах диссоциированных нейрональных клеток существуют доминирующие спонтанные паттерны активности, которые способствуют усилению имеющихся связей [12]. Низкочастотная стимуляция одного электрода индуцирует генерацию откликов сети в виде реверберирующих пачек активности, отличных от доминирующего паттерна спонтанной активности. Такая стимуляция изменяет пути распространения сигнала и приводит к изменениям связей [12]. Несколько научных групп показали, что низкочастотная стимуляция может вызвать сетевую пластичность [13–15].
Однако спонтанная электрическая активность в культивируемых нейронных сетях демонстрирует высокий уровень изменчивости при функционировании зрелой культуры на протяжении более 30 дней in vitro [16]. Эта изменчивость может быть связана со спонтанными изменениями синаптической пластичности вследствие наличия циклических связей в нейронной сети. Спонтанные изменения функциональных связей в сети могут скрывать изменения, вызванные стимуляцией. Для выявления вызванных изменений следует оценивать динамику спонтанных изменений в сети.
Цель исследования — оценка долгосрочных изменений функциональных характеристик импульсов, распространяющихся между нейронами в гиппокампальных культурах, растущих на микроэлектродных матрицах.
В данном исследовании мы проводили долговременные эксперименты по записи спонтанной активности нейронной сети. Для того чтобы вызвать пачечный ответ от стимуляции в определенном участке сети, использовали низкочастотную стимуляцию напряжением, подаваемую на 12 электродов. Мы предположили, что изменения функциональной сетевой активности индуцированы синаптической пластичностью. Структура функциональных связей в сети была оценена с помощью метода кросс-корреляционного анализа последовательностей импульсов спонтанной сетевой активности, регистрируемой различными микроэлектродами (по аналогии с [17]). Изменения, вызванные в структуре связей электрической стимуляцией, были обнаружены на 20-минутных интервалах времени. Кроме того, низкочастотная стимуляция изменяла динамику активации сетевой пачки (путь распространения сигнала, вызывающего активацию пачки) и частоту спонтанной импульсной активности сети.
Материалы и методы
Клеточная культура. Клетки гиппокампа диссоциировали из эмбрионов мышей (Е18) и высеивали на микроэлектродные матрицы c 60 электродами (MultiChannel Systems MCS GmbH, Германия) с плотностью приблизительно 9000–10 000 кл./мм2 [18]. Половину питательной среды меняли на новую каждые 2 дня. Клетки культивировали в стабильных условиях в инкубаторе (МСО-18AIC, Sanyo, Япония) при температуре 35,5°С, 5% концентрации СО2 и 95% влажности воздуха. Возраст культур на момент проведения экспериментов составлял 3–5 нед in vitro.
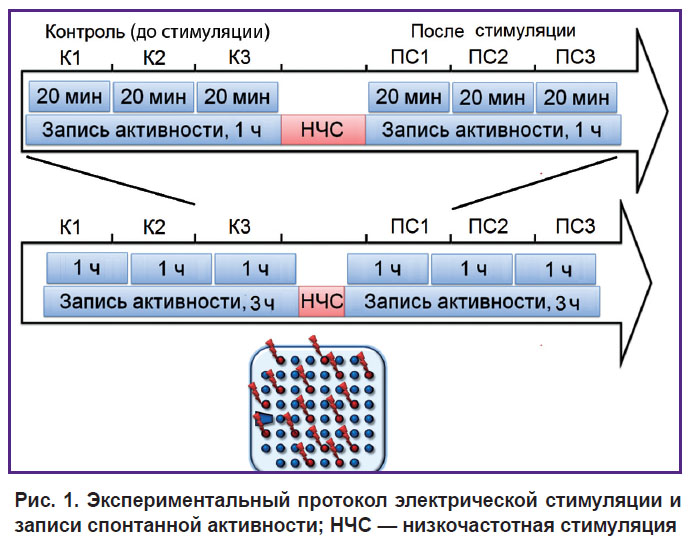
Запись и электрическая стимуляция культуральных клеток. Сигналы записывались с микроэлектродных матриц с 59 плоскими электродами и 1 референс-электродом, диаметр электродов составлял 30 мкм, расстояние между электродами — 200 мкм. При детектировании импульсов использовали порог, вычисляемый на основе анализа уровня шумового сигнала отдельно для каждого канала. Амплитуды зафиксированных импульсов находились в диапазоне 10–80 мкВ. Анализ сигналов и статистические расчеты были выполнены с использованием авторского программного обеспечения, разработанного в Matlab® [5]. Применялась стимуляция импульсами напряжения (±600 мВ, 260 мкс на фазу, напряжение первой фазы — положительное). Экспериментальный протокол состоял из трехчасовой записи спонтанной активности до и после стимуляции. Эти трехчасовые записи были разделены на 60- и 20-минутные интервалы для проведения анализа. Протокол низкочастотной стимуляции заключался в подаче 30 стимулов на каждый из выбранных 12–15 электродов с 5-секундным межимпульсным интервалом (рис. 1).
|
Рис. 1. Экспериментальный протокол электрической стимуляции и записи спонтанной активности; НЧС — низкочастотная стимуляция |
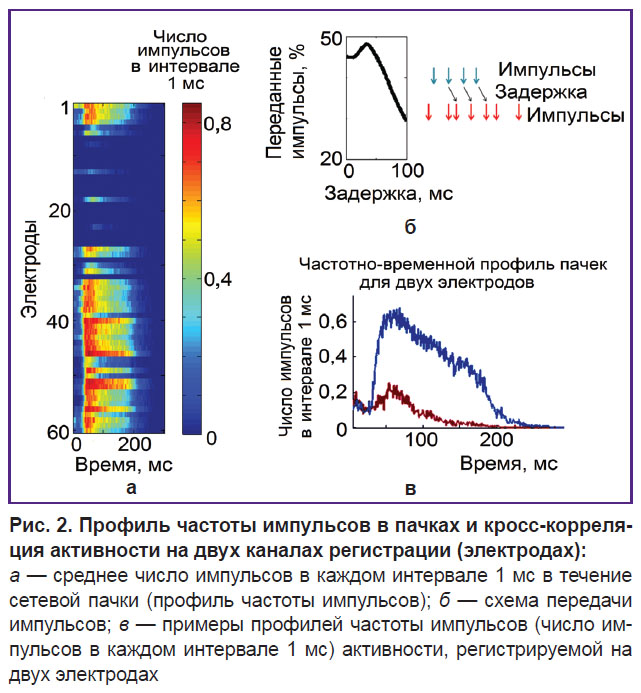
Анализ структуры связей. Кросс-корреляцию активности каждой случайно выбранной пары электродов (i, j) вычисляли как процент импульсов с i-го электрода, зарегистрированных на j-м электроде с различными временными задержками. Мы обозначили термином «задержка связи» временную задержку максимума кросс-корреляционной функции, которая рассматривалась в качестве силы связи. Если задержка связи была более 3 мс (рис. 2), то пара электродов считалась связанной синаптически [17]. Для каждого растра продолжительностью 20 или 60 мин мы определили карту связи, состоявшую из силы и задержек связей. Для оценки изменений характеристик связей во времени были проведены сравнение каждой записи с первой записью и вычисление двух основных параметров: «коэффициент изменения связей» (ADC%), который рассчитывался как процент появившихся и исчезнувших связей, и «коэффициент изменения силы стабильных связей» (SCSC), который рассчитывался как разница обнаруженных в обеих записях сил связей. SCSC измерялся в процентах, означающих разность между максимумами кросс-корреляционной функции, характеризующими количество переданных импульсов.
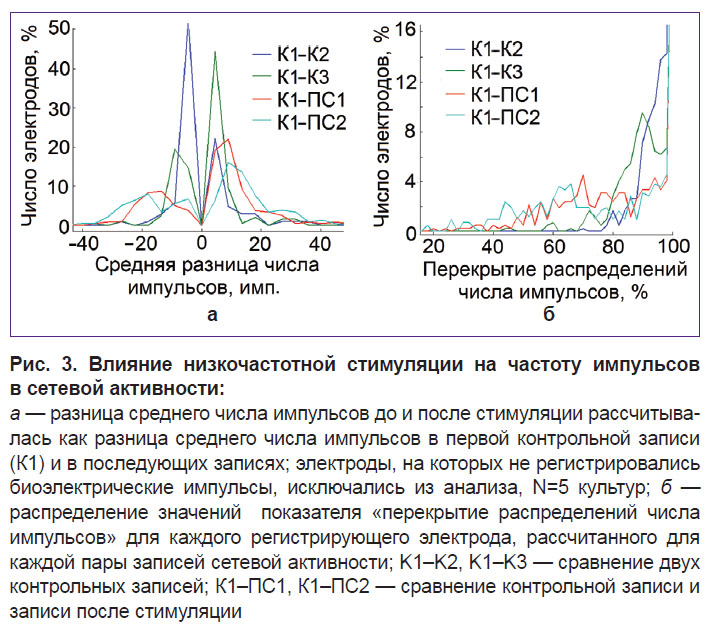
Сравнение пачечной активности. Проведено сравнение частоты импульсов в пачках на каждом электроде для каждой пары записей (растров) соответственно. Различие определялось как разница среднего числа импульсов в сетевых пачках для каждой пары записей (растров), отдельно для каждого регистрирующего электрода (рис. 3, а). Затем была проведена количественная оценка различия частоты импульсов в пачках для каждой пары записей (растров) отдельно для каждого электрода с помощью параметра «перекрытие распределений числа импульсов». При вычислении этого параметра использовали метод кластеризации двух наборов частоты импульсов в пачках. Кластеризация выполнялась для всех пачек с применением метода К-средних для каждой пары записей (растров А и В). В результате пачки разделялись на два набора данных (A’ и B’). Наборы пачек из известных растров (наборы А и В) сравнивались с набором пачек после кластерного анализа (A’ и B’). В этом случае ошибка классификации представляла собой число некорректно определенных паттернов в соответствии с известными записями (Na=A’∩B и Nb=B’∩A), где Na — количество пачек из набора В, отнесенных с использованием метода К-средних к набору А, Nb — количество пачек из набора А, отнесенных с использованием метода К-средних к набору В.
Процент отношения таких паттернов к общему числу пачек ([Na+Nb])/Nc·100%, где Nc — общее число пачек в растрах А и В) определялся как перекрытие распределений числа импульсов для двух записей и изменялся в диапазоне от 0 до 100%. В отличие от статистического теста это измерение представляет собой степень различия. Таким образом, перекрытие может составлять 0%, если все значения частот импульсов одного растра больше, чем частоты импульсов другого растра, или наоборот.
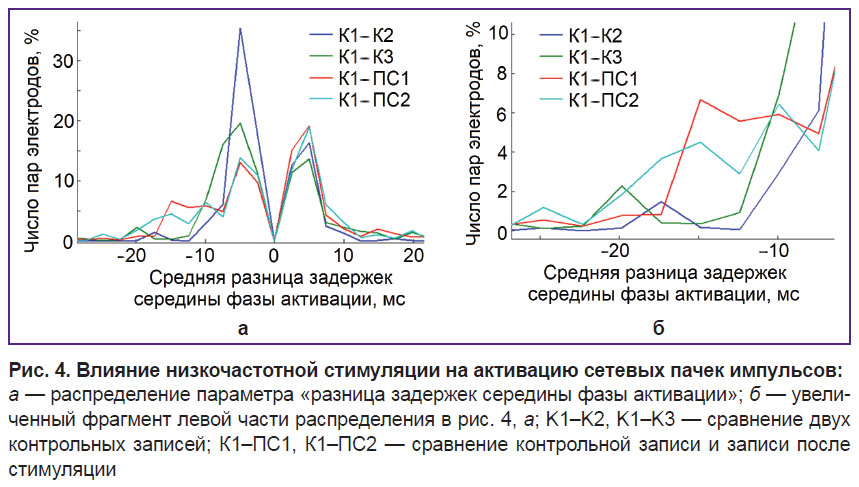
Кроме того, сравнивали параметр «середина фазы активации», который определялся как время превышения активностью 50% значений от максимальной частоты импульсов в интервале 1 мс на каждом отдельном электроде. Различие середины фазы активации для каждой пары записей (растров) определялось как разница задержек середины фазы активации сетевых пачек отдельно для каждого регистрирующего электрода.
Результаты
Изменения в частоте импульсов, индуцированные низкочастотной стимуляцией. Культивирование диссоциированных культур гиппокампа (E18) производили на микроэлектродных матрицах в течение 40 дней. Спонтанную пачечную активность записывали в культурах после 20-го дня на протяжении 7–8 ч ежедневно (не включались в анализ первые 0,5–1,5 ч, так как механическое сотрясение при перемещении культуры клеток приводит к изменению импульсной активности, 3 ч до стимуляции, 20 мин стимуляции и 3 ч после стимуляции). Связи оценивали в каждом 60-минутном или 20-минутном интервале до и после стимуляции. Зарегистрированная активность согласовывалась с полученными ранее результатами [18].
Далее проводили исследование возможности изменения частоты импульсов в пачках под действием низкочастотной стимуляции с межимпульсным интервалом, равным интервалу между пачками спонтанной активности (0,1–0,5 Гц). Мы проанализировали параметры «разница среднего числа импульсов» и «перекрытие распределений числа импульсов» в пачке для каждого канала до и после стимуляции. Записи спонтанной активности были разделены на интервалы 1 ч и 20 мин (см. рис. 1). Вызванные низкочастотной стимуляцией изменения в частоте импульсов были больше, чем спонтанные изменения, но только в пределах небольшой группы электродов (участков сети) (см. рис. 3, а, в). Количество электродов со значением изменения средней частоты импульсов >20 и бóльшим перекрытием частот импульсов увеличилось после стимуляции. Обнаружены несколько электродов, на которых наблюдалась повышенная частота импульсов в пачках в течение 2 ч после стимуляции.
Изменения в активации пачек, индуцированные низкочастотной стимуляцией. Доминантное направление распространения сигнала определяли на основании задержек активации пачек для различных участков сети. Середину фазы активации сетевой пачки анализировали для каждого канала до и после стимуляции. Индуцированные низкочастотной стимуляцией изменения в активации сетевой пачки были больше спонтанных изменений электродов на небольшой группе (на участках сети) (рис. 4, а, в).
Реорганизация связей в сети, индуцированных низкочастотной стимуляцией. Оценку изменений связи, индуцируемых стимуляцией, проводили с помощью анализа трехчасовой активности: двух часовых растров, записанных до стимуляции, и одного часового растра, записанного после стимуляции. Мы проанализировали изменения коэффициента изменения связей ADC% (количество появившихся/исчезнувших связей) в течение каждого часа сравнением всех растров с первым часом записи (К1 и ПС1). Статистическую значимость обнаруженного различия оценивали с помощью критерия Манна–Уитни, р<0,01, n=5 (рис. 5, а). Средние значения ADC%, вычисленные для данных, полученных до и после стимуляции, составили 31,0 и 54,4, т.е. изменились в 1,75 раза. Также были найдены различия (критерий Манна–Уитни, р<0,05, n=5) при сравнении коэффициента изменения силы стабильных связей SCSC. Значение медиан составило 0,006 и 0,0125, их относительная разница — 2,08. Однако на временнóм интервале 20 мин различия коэффициента SCSC до и после стимуляции были больше (тест Манна–Уитни, р<0,001). Медианы коэффициента ADC% составили 0,5 в контроле и 33,1 — при сравнении активности до и после стимуляции (рис. 5, в). Относительное изменение равнялось 66,2 в отличие от 1,75 в 60-минутной записи. Медианы коэффициента SCSC были равны 0,0001 в контроле и 0,0095 — при сравнении активности до и после стимуляции. Относительное изменение составило 95,0 в отличие от 2,08, полученного при анализе 60-минутной записи.
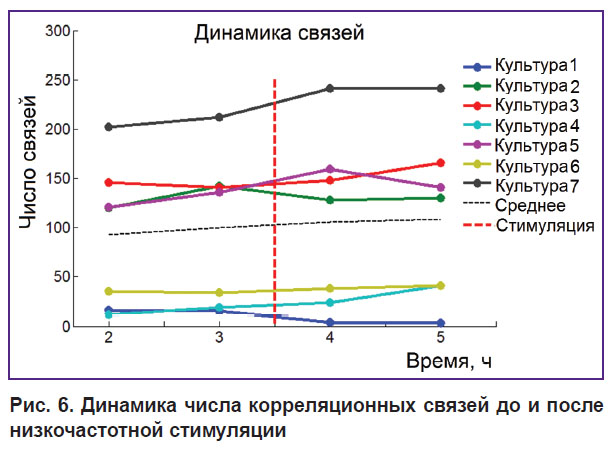
Было обнаружено, что общее число связей на 60-минутном интервале времени не изменялось после стимуляции (рис. 6). Существенные изменения коэффициента SCSC и изменение коэффициента связи ADC% указывают на реорганизацию связей в сети после действия низкочастотной стимуляции.
|
Рис. 6. Динамика числа корреляционных связей до и после низкочастотной стимуляции |
Обсуждение. В данном исследовании диссоциированные клетки гиппокампа культивировали на микроэлектродных матрицах. Спонтанную пачечную активность записывали на протяжении нескольких часов (до 8), после чего подавали электрическую стимуляцию. Применяли два протокола стимуляции: низкочастотную и высокочастотную стимуляцию. Низкочастотная стимуляция подавалась через 12 выбранных электродов с частотой 0,1–0,5 Гц, высокочастотная — через 2 канала и 8 электродов (по 4 электрода на канал стимуляции). Подавалось 150 серий по 20 стимулов, интервал между стимулами — 100 мс, между сериями — 6 с, задержка между стимулами первого и второго каналов была равной 10 мс. Записанную активность разделяли на интервалы продолжительностью 60 и 20 мин, после чего проводили анализ характеристик передачи импульсов для оценки структуры связей.
Структура функциональных связей в сети была оценена с помощью метода кросс-корреляционного анализа последовательностей импульсов спонтанной сетевой активности, регистрируемой различными микроэлектродами (по аналогии с [17]). В работе J. le Feber [12] установлено, что после электрической стимуляции изменяется интегральный показатель реорганизации связей в нейронной сети — эвклидово расстояние между матрицами силы связей для всех пар регистрирующих электродов до и после электрической стимуляции.
Мы разработали показатели изменения активности нейронной сети: коэффициент изменения связей, коэффициент изменения силы стабильных связей, разница среднего числа импульсов, перекрытие распределений числа импульсов, разница задержек середины фазы активации, которые позволяют детально оценить изменение функциональных связей в нейронной сети. Изменения в силе связей и реорганизации связей (число появившихся/исчезнувших связей) указывают на значительные функциональные изменения в сети после низкочастотной стимуляции. Интересно отметить, что общее количество связей при этом не изменялось.
С помощью разработанных показателей впервые было установлено, что изменения активности нейронной сети на интервале времени 20 мин гораздо больше, чем на интервале 1 ч. Это может объясняться тем, что спонтанные изменения структуры связей сети могут подавить индуцированные стимуляцией изменения.
Разработанные показатели изменения активности нейронной сети представляют собой действенные и простые инструменты для оценки функционального состояния нейронной сети in vitro при проведении длительных электрофизиологических записей на микроэлектродных матрицах. Показатели могут применяться в работах по тестированию фармакологических препаратов, направленных на улучшение или восстановление функционального состояния нервной ткани.
Заключение. Электрическая стимуляция короткими двухфазными прямоугольными импульсами (±800 мВ, 260 мс на фазу, напряжение первой фазы — положительное) с низкой частотой (интервал между стимулами 3 с, в течение 20 мин) вызывает в сети длительно культивируемых диссоциированных клеток мозга функциональные изменения, а именно — изменения архитектуры связей в сетевой активности при стабильном общем количестве кросс-корреляционных связей. Разработанные показатели «коэффициент изменения связей» и «коэффициент изменения силы стабильных связей» являются чувствительными индикаторами активностьзависимой пластичности в нейронной сети. Изменение параметров «разница среднего числа импульсов», «перекрытие распределений числа импульсов», «разница задержек середины фазы активации» после стимуляции наблюдается только на части участков сети (регистрирующих электродов). Вызванные низкочастотной стимуляцией изменения сетевой активности сохраняются на протяжении десятков минут. На большем интервале времени (1 ч) спонтанные изменения структуры связей сети могут подавить изменения, индуцированные стимуляцией.
Финансирование исследования. Исследование выполнено при поддержке Российского научного фонда (№14-19-01381).
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Литература
- Chiappalone M., Massobrio P., Martinoia S. Network plasticity in cortical assemblies. Eur J Neurosci 2008; 28(1): 221–237, https://doi.org/10.1111/j.1460-9568.2008.06259.x.
- Bakkum D.J., Chao Z.C., Potter S.M. Long-term activity-dependent plasticity of action potential propagation delay and amplitude in cortical networks. PLoS One 2008; 3(5): e2088, https://doi.org/10.1371/journal.pone.0002088.
- Eytan D., Brenner N., Marom S. Selective adaptation in networks of cortical neurons. J Neurosci 2003; 23(28): 9349–9356.
- Marom S., Shahaf G. Development, learning and memory in large random networks of cortical neurons: lessons beyond anatomy. Q Rev Biophys 2002; 35(01): 63–87, https://doi.org/10.1017/s0033583501003742.
- Pimashkin A., Kastalskiy I., Simonov A., Koryagina E., Mukhina I., Kazantsev V. Spiking signatures of spontaneous activity bursts in hippocampal cultures. Front Comput Neurosci 2011; 5: 46, https://doi.org/10.3389/fncom.2011.00046.
- Shahaf G., Eytan D., Gal A., Kermany E., Lyakhov V., Zrenner C., Marom S. Order-based representation in random networks of cortical neurons. PLoS Comput Biol 2008; 4(11): e1000228, https://doi.org/10.1371/journal.pcbi.1000228.
- Maccione A., Garofalo M., Nieus T., Tedesco M., Berdondini L., Martinoia S. Multiscale functional connectivity estimation on low-density neuronal cultures recorded by high-density CMOS Micro Electrode Arrays. J Neurosci Methods 2012; 207(2): 161–171, https://doi.org/10.1016/j.jneumeth.2012.04.002.
- Makarov V.A., Panetsos F., de Feo O. A method for determining neural connectivity and inferring the underlying network dynamics using extracellular spike recordings. J Neurosci Methods 2005; 144(2): 265–279, https://doi.org/10.1016/j.jneumeth.2004.11.013.
- Ullo S., Nieus T.R., Sona D., Maccione A., Berdondini L., Murino V. Functional connectivity estimation over large networks at cellular resolution based on electrophysiological recordings and structural prior. Front Neuroanat 2014; 8: 137, https://doi.org/10.3389/fnana.2014.00137.
- Wagenaar D.A. Controlling bursting in cortical cultures with closed-loop multi-electrode stimulation. J Neurosci 2005; 25(3): 680–688, https://doi.org/110.1523/jneurosci.4209-04.2005.
- Poli D., Pastore V.P., Massobrio P. Functional connectivity in in vitro neuronal assemblies. Front Neural Circuits 2015; 9: 57, https://doi.org/10.3389/fncir.2015.00057.
- le Feber J., Witteveen T., van Veenendaal T.M., Dijkstra J. Repeated stimulation of cultured networks of rat cortical neurons induces parallel memory traces. Learn. Mem 2015; 22(12): 594–604, https://doi.org/10.1101/lm.039362.115.
- Bologna L.L., Nieus T., Tedesco M., Chiappalone M., Benfenati F., Martinoia S. Low-frequency stimulation enhances burst activity in cortical cultures during development. Neuroscience 2010; 165(3): 692–704, https://doi.org/10.1016/j.neuroscience.2009.11.018.
- Maeda E., Kuroda Y., Robinson H.P.C., Kawana A. Modification of parallel activity elicited by propagating bursts in developing networks of rat cortical neurones. Eur J Neurosci 1998; 10(2): 488–496, https://doi.org/10.1046/j.1460-9568.1998.00062.x.
- Vajda I., van Pelt J., Wolters P., Chiappalone M., Martinoia S., van Someren E., van Ooyen A. Low-frequency stimulation induces stable transitions in stereotypical activity in cortical networks. Biophys J 2008; 94(12): 5028–5039, https://doi.org/10.1529/biophysj.107.112730.
- Wagenaar D.A., Pine J., Potter S.M. An extremely rich repertoire of bursting patterns during the development of cortical cultures. BMC Neurosci 2006; 7(1): 11, https://doi.org/10.1186/1471-2202-7-11.
- le Feber J., Rutten W.L., Stegenga J., Wolters P.S., Ramakers G.J., van Pelt J. Conditional firing probabilities in cultured neuronal networks: a stable underlying structure in widely varying spontaneous activity patterns. J Neural Eng 2007; 4(2): 54–67, https://doi.org/10.1088/1741-2560/4/2/006.
- Pimashkin A., Gladkov A., Agrba E., Mukhina I., Kazantsev V. Selectivity of stimulus induced responses in cultured hippocampal networks on microelectrode arrays. Cogn Neurodyn 2016; 10(4): 287–299, https://doi.org/10.1007/s11571-016-9380-6.