Использование метода 16S рРНК метабаркодинга для идентификации этиологических агентов инфекционного эндокардита
Цель исследования — оценить эффективность идентификации бактериальных агентов в нативных клапанах сердца, пораженных инфекционным эндокардитом, методом 16SрРНК метабаркодинга.
Материалы и методы. Материалом для исследования послужили 20 образцов нативных клапанов сердца, полученных от 16 пациентов. Секвенирование проводили в Центре коллективного пользования «Геномика» (Институт химической биологии и фундаментальной медицины Сибирского отделения РАН, Новосибирск) на секвенаторе MiSeq (Illumina, США), используя набор MiSeq Reagent Kit v. 3 (2×300 bp; Illumina, США).
Результаты. Выявлены мажорные микроорганизмы (доля которых в анализируемом образце составила более 5% от всех идентифицированных бактериальных агентов), относящиеся к родам Streptococcus (40% от всех проанализированных клапанов), Sphingomonas (35%), Pseudomonas (35%), Roseateles (25%), Phyllobacterium (25%) и Enterococcus (15%). Кроме того, в изученных клапанах обнаружены единичные случаи присутствия Ralstoniapickettii и представителей родов Bacillus и Klebsiella.
Заключение. Результаты исследования продемонстрировали эффективность метода 16SрРНК метабаркодинга для идентификации бактериальных агентов по сравнению с рутинными неинвазивными методами диагностики. Нативные клапаны сердца, удаленные у пациентов с инфекционным эндокардитом, характеризовались большим количеством условно-патогенных микроорганизмов при отрицательных результатах посева крови.
Введение
Инфекционный эндокардит (ИЭ) — воспалительное заболевание преимущественно бактериальной природы, характеризующееся локализацией возбудителей на нативных клапанных структурах сердца, эндокарде, а также на протезах клапанов сердца и кардиостимуляторах [1]. Эпидемиологические исследования демонстрируют рост заболеваемости ИЭ и увеличение летальных исходов от осложнений, сопряженных с данным патологическим состоянием [2, 3]. Идентификация возбудителя является крайне важным аспектом диагностики ИЭ, что влияет на антибиотикотерапию и риск рецидива бактериемии у пациентов с протезированными клапанами сердца [4]. «Золотым стандартом» определения этиологии ИЭ считается микробиологический посев крови или ткани иссеченного клапана сердца. Однако стоит отметить, что в большинстве случаев результаты посевов являются отрицательными. В таких ситуациях, согласно действующим клиническим рекомендациям [5], возможно использование молекулярно-генетических методов (например, полимеразной цепной реакции) [6]. Предоперационная антибиотикотерапия, проводимая в стационаре, затрудняет обнаружение возбудителей стандартными методами, вследствие чего возрастает потребность в более точной диагностике и идентификации бактериальных агентов для снижения смертности от ИЭ [7].
На сегодняшний день одним из перспективных методов является секвенирование нового поколения (NGS), которое позволяет идентифицировать патогены в тех случаях, когда стандартные молекулярно-генетические тесты не дают положительного результата [8]. Стоит отметить, что чувствительность и специфичность данного метода выше для эксплантированной ткани, чем для периферической крови [9]. На начальном этапе метагеномного секвенирования 16S рРНК происходит амплификация вариабельных участков с использованием специфических праймеров, после чего осуществляется секвенирование полученного продукта, что позволяет идентифицировать бактериальный агент на уровне рода и вида. Ген 16S рРНК, который кодирует субъединицу рибосомы 16S, обнаружен во всех бактериях и включает в себя высококонсервативные области с вариабельными последовательностями [10]. Несомненным преимуществом данного метода является выявление бактериальной ДНК нежизнеспособных микроорганизмов, а также бактериальных агентов у пациентов после курса терапии антибиотиками [11].
Цель исследования — оценить эффективность идентификации бактериальных агентов в нативных клапанах сердца, пораженных инфекционным эндокардитом, методом 16S рРНК метабаркодинга.
Материалы и методы
Исследуемая группа. Материалом для исследования послужили 20 образцов нативных клапанов сердца, пораженных ИЭ, которые были получены от 16 пациентов во время кардиохирургического вмешательства. Стоит отметить, что в большинстве случаев преобладал левосторонний ИЭ, правосторонний наблюдался только у одного пациента.
Клиническая характеристика пациентов:
мужской пол — 12 человек (75%);
средний возраст (Me [Q1; Q3]) — 57,0 [35,0; 63,0] года;
индекс массы тела (mean±SD) — 24,63±3,95;
фракция выброса левого желудочка (mean±SD) — (63,64±9,50)%;
легочная гипертензия — 10 пациентов (62,5%);
гипертоническая болезнь — 7 пациентов (43,75%);
хроническая сердечная недостаточность — 16 пациентов (100%);
фибрилляция предсердий — 3 пациента (18,75%);
острое нарушение мозгового кровообращения — 4 пациента (25%);
хроническая болезнь почек — 8 пациентов (50%);
хроническая обструктивная болезнь легких — 4 пациента (25%);
антибиотики, принимаемые до госпитализации, — 12 пациентов (75%);
пораженный клапан: аортальный, митральный и трикуспидальный — 9 (45%), 10 (50%) и 1 (5%) пациент соответственно.
Лабораторные показатели (Me [Q1; Q3]):
лейкоциты — 7,20 [5,40; 9,30]·109/л;
нейтрофилы — 4,40 [2,90; 5,85]·109/л;
С-реактивный белок — 4,80 [2,00; 16,40] мг/л;
скорость оседания эритроцитов — 18,0 [5,50; 51,50] мм/ч.
Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации (2024). Все участники подписывали добровольное информированное согласие на участие в исследовании. Работа одобрена локальным этическим комитетом Научно-исследовательского института комплексных проблем сердечно-сосудистых заболеваний (протокол №1 от 26 января 2024).
Диагноз «инфекционный эндокардит» устанавливали на основе клинических, микробиологических и лабораторных данных, а также результатов эхокардиографии (эхоКГ). По данным эхоКГ, у всех пациентов, включенных в исследование, визуализировались подвижные вегетации на клапанах. Кроме того, диагноз был верифицирован в соответствии с международными критериями Дьюка. Исследуемым пациентам проводили забор периферической крови для микробиологического тестирования в трех повторах с интервалом в 6 ч за неделю до оперативного вмешательства. Гистологическую окраску по Граму осуществляли посредством коммерческого набора (Abcam, Великобритания).
16S рРНК метабаркодинг. Из образцов эксплантированных клапанов выделяли ДНК с помощью набора HostZERO Microbial DNA Kit (Zymo Research, США). Регион V3–V4 гена 16S рРНК был амплифицирован с помощью праймеров 343F (5’-CTCCTACGGRRSGCAGCAG-3’) и 806R (5’-GGACTACNVGGGTWTCTAAT-3’), содержащих адаптерные последовательности (Illumina, США), линкер и баркод [12]. Амплификацию проводили в 20 мкл реакционной смеси (в трех повторах), содержащей 0,4 ЕД Hot Start Taq ДНК полимеразы («Биолабмикс», Россия) и однократный HS Taq ПЦР-буфер («Биолабмикс», Россия); по 0,2 мкM прямого и обратного праймеров; 10 нг ДНК; 2,3 мМ MgCl2 («Биолабмикс», Россия) и 0,2 мM dNTP (Life Technologies, США). Количество циклов для каждого образца ДНК подбирали, проводя ПЦР с детекцией флуоресцентного сигнала в режиме реального времени на ДНК-амплификаторе CFX-96 (Bio-Rad, США). В качестве интеркалирующего флуорофора использовали краситель Eva488 (Lumiprobe, США). Условием выбора цикла являлось нахождение флуоресцентного сигнала на фазе линейного логарифмического роста. В случае низкой эффективности ПЦР максимальным количеством циклов было 34. Выход целевого продукта анализировали на приборе MultiNA с помощью набора 12000 DNA Base Pair Kit (Shimadzu, Япония). ПЦР проводили по следующей программе: 5 мин при 95oС; далее до 40 циклов — 15 с при 95oС, 15 с при 62oС, 30 с при 72oС; последний этап — 5 мин при 72oС. Ампликоны (по 200 нг каждый) объединяли и очищали при помощи магнитных частиц AMPure XP Beads (Beckman Coulter, США) согласно инструкции фирмы-производителя.
Секвенирование проводили в Центре коллективного пользования «Геномика» (Институт химической биологии и фундаментальной медицины Сибирского отделения РАН, Новосибирск) на секвенаторе MiSeq (Illumina, США), используя набор MiSeq Reagent Kit v. 3 (2×300 bp; Illumina, США). Количество ридов, полученных для каждого образца, определяли с помощью программы Seqkit [13]. Анализ качества проводили с использованием FastQC [14]. Парные последовательности анализировали с помощью UPARSE-скриптов [15], используя Usearch v. 11.0.667 [16]. Биоинформатическая обработка включала перекрывание парных ридов, фильтрацию по качеству и длине, учет одинаковых последовательностей, отбрасывание синглетонов, удаление химер и получение ОТЕ с помощью алгоритма кластеризации UPARSE [17]. Таксономическую принадлежность последовательностей ОТЕ определяли с помощью SINTAX [18] и референсной базы 16S RDP training set v. 19 [19].
Статистическую обработку данных проводили в программе Prism 8 (GraphPad Software, США). Количественные результаты представляли в виде среднего арифметического (М) и среднеквадратического отклонения (SD), а также медианы (Me), нижнего и верхнего квартилей [Q1; Q3].
Результаты
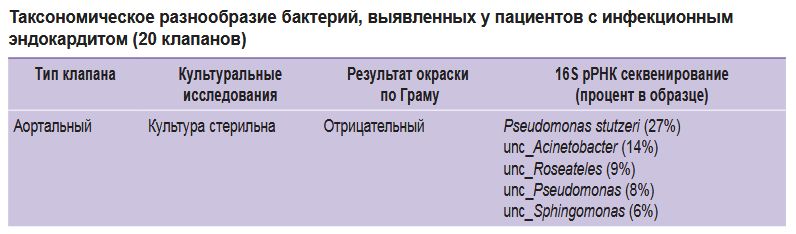
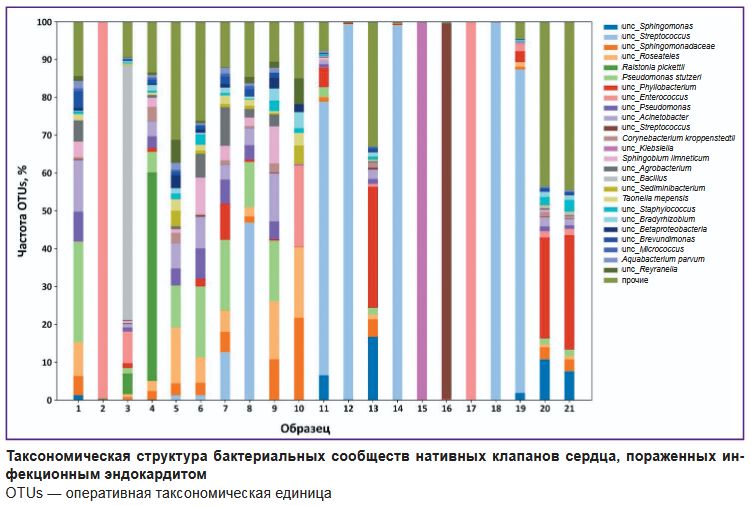
Микробиологический анализ крови, выполненный в соответствии со стандартным протоколом, описанным в клинических рекомендациях [5], позволил установить этиологическую принадлежность ИЭ только в 25% случаев, в которых возбудители ИЭ были представлены грамположительными бактериями. При гистологической окраске по Граму иссеченных створок нативных клапанов сердца удалось идентифицировать бактериальные агенты в 45% случаев (см. таблицу). Методом 16S рРНК метабаркодинга в большинстве образцов выявлены мажорные микроорганизмы (доля которых в анализируемом образце составила более 5% от всех идентифицированных бактериальных агентов), относящиеся к родам Streptococcus (40% от всех проанализированных клапанов), Sphingomonas (35%), Pseudomonas (35%), Roseateles (25%), Phyllobacterium (25%) и Enterococcus (15%). Однако в основной массе митральных и небольшой доле аортальных клапанов практически полностью отсутствует разнообразие бактерий и присутствует только один мажорный род: либо Streptococcus, либо Klebsiella или Enterococcus (см. рисунок).
|
Таксономическое разнообразие бактерий, выявленных у пациентов с инфекционным эндокардитом (20 клапанов) |
|
Таксономическая структура бактериальных сообществ нативных клапанов сердца, пораженных инфекционным эндокардитом ОТUs — оперативная таксономическая единица |
Обсуждение
В основе ИЭ лежит колонизация клапанов сердца микроорганизмами. Несмотря на достижения в профилактике, диагностике и лечении этого заболевания, на сегодняшний день сохраняется высокий уровень летальности: внутригоспитальная летальность составляет от 6 до 50%, пятилетняя смертность — от 19 до 82% [20]. Эпидемиологические исследования показывают, что распространенность ИЭ составляет от 5,0 до 14,3 случаев на 100 000 тысяч взрослого населения [21]. Кроме того, отмечено изменение этиологической структуры ИЭ. Так, на сегодняшний день на долю основных возбудителей (Streptococcus spp. и Staphylococcus spp.) приходится почти 80% случаев ИЭ. Примерно в 10% случаев этиологическим агентом являются энтерококки, в частности Enterococcus faecalis, причем процент этих бактерий выше у лиц старше 65 лет [22]. Грамотрицательные палочки, включая организмы группы HACEK (виды Haemophilus, Aggregatibacter, Cardiobacterium, Eikenella и Kingella), выявляются гораздо реже (на их долю приходится около 5% случаев ИЭ).
Корректная идентификация возбудителя является крайне важным аспектом диагностики ИЭ [4]. Рутинное определение этиологического агента ИЭ путем посева крови или резецированного участка ткани может давать ложноотрицательные результаты в диапазоне от 2,5 до 31,0% случаев, что зачастую сопряжено с антибиотикотерапией до поступления в стационар [20]. Кроме того, ряд вызывающих ИЭ бактерий могут относиться к труднокультивируемым или некультивируемым группам [23]. В результате проведенного нами исследования продемонстрировано, что на долю выявленных с использованием микробиологических тестов возбудителей приходилось всего около 30% изученных случаев ИЭ, в то время как идентификация бактериальных агентов методом 16S рРНК метабаркодинга составила 100%. Так, 16S рРНК метабаркодинг позволил выявить бактерии родов Streptococcus, Enterococcus, Sphingomonas, Roseateles, Phyllobacterium, Pseudomonas, Ralstonia, Bacillus и Klebsiella. Не отмечено ни одного случая Staphylococcus, несмотря на то что микроорганизмы данного рода являются одними из наиболее распространенных возбудителей, поражающих ткани клапанных структур сердца.
Представители рода Streptococcus занимают второе место по значимости в патогенезе ИЭ после Staphylococcus aureus. Род Streptococcus представляет собой гетерогенную группу бактерий с 50 идентифицированными видами. Ряд исследований демонстрируют, что отдельные виды стрептококков, особенно из группы Mitis, являются основными возбудителями ИЭ [24, 25]. Показано, что Streptococcus gordonii и Streptococcus mutans — это наиболее часто встречающиеся виды стрептококков (наблюдаются в 50% случаев), реже распространены Streptococcus pneumoniae и Streptococcus pyogenes (1–2%) [25].
Род Enterococcus включает в себя грамположительные бактерии, занимающие лидирующие позиции среди возбудителей ИЭ. До 20% всех случаев ИЭ может быть обусловлено бактериями данного рода, преимущественно Enterococcus faecalis [26]. Терапия ИЭ, вызванного представителями рода Enterococcus, сопряжена с определенными трудностями, поскольку данный патоген способен образовывать биопленки и сохранять микроорганизмы не только на нативных клапанах сердца, но и на протезированных клапанных структурах [27, 28]. Стоит отметить, что, по сравнению с другими этиологиями, для ИЭ, вызванного E. faecalis, характерны рецидивы после протезирования клапанов сердца, которые могут возникать после отмены антибиотикотерапии [29, 30].
Кроме того, в нашем исследовании выявлено два случая бактериальной инвазии более редкими микроорганизмами, такими как Ralstonia pickettii и Bacillus spp. R. pickettii, относящаяся к роду Ralstonia, представляет собой аэробную грамотрицательную оксидазоположительную бациллу, которую в последнее время рассматривают как оппортунистический патоген у пациентов с ослабленным иммунитетом. R. pickettii способнавыживать в широком диапазоне температур (от 15 до 42ºC), а также образовывать биопленку, устойчивую к иммунному ответу хозяина и ряду антибиотиков [31]. Кроме того, на сегодняшний день нет стандартизированного протокола лечения инфекций, вызванных R. pickettii, из-за различий в чувствительности к антибиотикам. Пациенты с ослабленным иммунитетом, особенно индивидуумы с приобретенной (ВИЧ) или фармацевтической иммуносупрессией, находятся в группе риска заражения данным видом бактерий [32], что в целом описывает наш случай выявления R. pickettii у пациента с поражением аортального клапана и сопутствующим ВИЧ, а также гепатитом С.
В результате проведенного 16S рРНК метабаркодинга в одном случае нами также был идентифицирован возбудитель рода Bacillus в митральном клапане пациента, посев крови которого показал положительный результат на E. faecalis. Бактерии рода Bacillus — грамположительныефакультативные анаэробы, встречающиеся в окружающей среде, в пище, а также в микрофлоре кишечника [33]. Кроме того, отмечено, что бактерии рода Bacillus способны вызывать ИЭ, поражая в большинстве случаев митральный клапан сердца, и ассоциированы с высокой летальностью у пациентов с протезированными клапанными структурами [34]. Показано, что эндокардит, вызванный бактериями рода Bacillus, чаще встречался у пациентов с внутривенным употреблением наркотиков, венозными катетерами, протезами клапанов сердца, злокачественными новообразованиями, а также иммуносупрессией [35].
Важно заметить, что в нашем исследовании в одном случае также выявлена грамотрицательная бактерия из рода Klebsiella. Наиболее распространенными видами из данного рода являются Klebsiella pneumoniae и Klebsiella oxytoca. Klebsiella granulomatis, Klebsiella ozaenae и Klebsiella rhinoscleromatis встречаются реже. Среди известных видов именно K. pneumoniae наиболее часто вызывает ИЭ, характеризующийся тяжелым течением заболевания, главным образом за счет того, что данный вид бактерии является устойчивым к некоторым видам антибиотиков [36].
Заключение
Таким образом, результаты нашего исследования показали, что нативные клапаны сердца, удаленные у пациентов с ИЭ, характеризовались большим количеством условно-патогенных микроорганизмов при отрицательных результатах посева крови. Это свидетельствует о том, что остаточная бактериемия у пациентов, которым проводилась предоперационная антибактериальная терапия, направленная в основном против известных возбудителей ИЭ, может приводить к развитию протезного ИЭ в послеоперационном периоде с последующей повторной операцией, ухудшением качества жизни пациента и повышением риска летального исхода. Полученные результаты показывают значимость 16S рРНК метабаркодинга удаленных клапанов сердца и необходимость углубленного изучения таксономического разнообразия клапанов сердца, пораженных ИЭ, с использованием высокопроизводительных методов.
Финансирование. Исследование выполнено на средства гранта Российского научного фонда №23-75-10020 «Молекулярно-генетические основы патогенеза инфекционного эндокардита нативных клапанов сердца и их биопротезов», https://rscf.ru/project/23-75-10020/.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Литература
- Li M., Kim J.B., Sastry B.K.S., Chen M. Infective endocarditis. Lancet 2024; 404(10450): 377–392, https://doi.org/10.1016/S0140-6736(24)01098-5.
- Martínez-Sellés M., Muñoz P. Epidemiology, diagnosis, treatment, and prognosis of infective endocarditis. J Clin Med 2023; 12(17): 5705, https://doi.org/10.3390/jcm12175705.
- Стасев А.Н., Рутковская Н.В., Кокорин С.Г., Левадин Ю.В. Сальмонелезный эндокардит митральнго клапана: клиническое наблюдение. Комплексные проблемы сердечно-сосудистых заболеваний 2017; 2: 123–126, https://doi.org/10.17802/2306-1278-2017-2-123-126.
- Oberbach A., Schlichting N., Feder S., Lehmann S., Kullnick Y., Buschmann T., Blumert C., Horn F., Neuhaus J., Neujahr R., Bagaev E., Hagl C., Pichlmaier M., Rodloff A.C., Gräber S., Kirsch K., Sandri M., Kumbhari V., Behzadi A., Behzadi A., Correia J.C., Mohr F.W., Friedrich M. New insights into valve-related intramural and intracellular bacterial diversity in infective endocarditis. PLoS One 2017; 12(4): e0175569, https://doi.org/10.1371/journal.pone.0175569.
- Демин А.А., Кобалава Ж.Д., Скопин И.И., Тюрин В.П., Бойцов С.А., Голухова Е.З., Гордеев М.Л., Гудымович В.Г., Демченко Е.А., Дробышева В.П., Домонова Э.А., Драпкина О.М., Загородникова К.А., Иртюга О.Б., Кахкцян П.В., Козлов Р.С., Котова Е.О., Медведев А.П., Муратов Р.М., Николаевский Е.Н., Писарюк А.С., Пономарева Е.Ю., Попов Д.А., Рачина С.А., Ревишвили А.Ш., Резник И.И., Рыжкова Д.В., Сафарова А.Ф., Тазина С.Я., Чипигина Н.С., Шипулина О.Ю., Шляхто Е.В., Шнейдер Ю.А., Шостак Н.А. Инфекционный эндокардит и инфекция внутрисердечных устройств. Клинические рекомендации 2021. Российский кардиологический журнал 2022; 27(10): 5233, https://doi.org/10.15829/1560-4071-2022-5233.
- Котова Е.О., Домонова Э.А., Кобалава Ж.Д., Моисеева А.Ю., Писарюк А.С., Сильвестрова О.Ю., Караулова Ю.Л., Акимкин В.Г. Клинико-диагностическая ценность включения ПЦР-исследования крови в традиционный алгоритм идентификации возбудителей инфекционного эндокардита: когортное исследование 124 пациентов. Терапевтический архив 2023; 95(1): 23–31, https://doi.org/10.26442/00403660.2023.01.202042.
- Zeng X., Wu J., Li X., Xiong W., Tang L., Li X., Zhuang J., Yu R., Chen J., Jian X., Lei L. Application of metagenomic next-generation sequencing in the etiological diagnosis of infective endocarditis during the perioperative period of cardiac surgery: a prospective cohort study. Front Cardiovasc Med 2022; 9: 811492, https://doi.org/10.3389/fcvm.2022.811492.
- Haddad S.F., DeSimone D.C., Chesdachai S., Gerberi D.J., Baddour L.M. Utility of metagenomic next-generation sequencing in infective endocarditis: a systematic review. Antibiotics (Basel) 2022; 11(12): 1798, https://doi.org/10.3390/antibiotics11121798.
- Burban A., Słupik D., Reda A., Szczerba E., Grabowski M., Kołodzińska A. Novel diagnostic methods for infective endocarditis. Int J Mol Sci 2024; 25(2): 1245, https://doi.org/10.3390/ijms25021245.
- Martinez-Porchas M., Villalpando-Canchola E., Ortiz Suarez L.E., Vargas-Albores F. How conserved are the conserved 16S-rRNA regions? PeerJ 2017; 5: e3036, https://doi.org/10.7717/peerj.3036.
- Anton-Vazquez V., Dworakowski R., Cannata A., Amin-Youssef G., Gunning M., Papachristidis A., MacCarthy P., Baghai M., Deshpande R., Khan H., Byrne J., Fife A. 16S rDNA PCR for the aetiological diagnosis of culture-negative infective endocarditis. Infection. 2022;50(1):243-249. doi: https://doi.org/10.1007/s15010-021-01690-x.
- Fadrosh D.W., Ma B., Gajer P., Sengamalay N., Ott S., Brotman R.M., Ravel J. An improved dual-indexing approach for multiplexed 16S rRNA gene sequencing on the Illumina MiSeq platform. Microbiome 2014; 2(1): 6, https://doi.org/10.1186/2049-2618-2-6.
- Shen W., Le S., Li Y., Hu F. SeqKit: a cross-platform and ultrafast toolkit for FASTA/Q file manipulation. PLoS One 2016; 11(10): e0163962, https://doi.org/10.1371/journal.pone.0163962.
- https://www.bioinformatics.babraham.ac.uk/projects/fastqc/.
- Edgar R.C. UPARSE: highly accurate OTU sequences from microbial amplicon reads. Nat Methods 2013; 10(10): 996–998, https://doi.org/10.1038/nmeth.2604.
- Edgar R.C. Search and clustering orders of magnitude faster than BLAST. Bioinformatics 2010; 26(19): 2460–2461, https://doi.org/10.1093/bioinformatics/btq461.
- Edgar R.C. UNOISE2: improved error-correction for Illumina 16S and ITS amplicon sequencing. bioRxiv 2016, https://doi.org/10.1101/081257.
- Edgar R.C. SINTAX: a simple non-Bayesian taxonomy classifier for 16S and ITS sequences. bioRxiv 2016, https://doi.org/10.1101/074161.
- Wang Q., Garrity G.M., Tiedje J.M., Cole J.R. Naive Bayesian classifier for rapid assignment of rRNA sequences into the new bacterial taxonomy. Appl Environ Microbiol 2007; 73(16): 5261–5267, https://doi.org/10.1128/AEM.00062-07.
- Kouijzer J.J.P., Noordermeer D.J., van Leeuwen W.J., Verkaik N.J., Lattwein K.R. Native valve, prosthetic valve, and cardiac device-related infective endocarditis: a review and update on current innovative diagnostic and therapeutic strategies. Front Cell Dev Biol 2022; 10: 995508, https://doi.org/10.3389/fcell.2022.995508.
- Thornhill M.H., Dayer M.J., Nicholl J., Prendergast B.D., Lockhart P.B., Baddour L.M. An alarming rise in incidence of infective endocarditis in England since 2009: why? Lancet 2020; 395(10233): 1325–1327, https://doi.org/10.1016/S0140-6736(20)30530-4.
- Кобалава Ж.Д., Котова Е.О. Глобальные и национальные тренды эволюции инфекционного эндокардита. Кардиология 2023; 63(1): 3–11, https://doi.org/10.18087/cardio.2023.1.n2307.
- Reisinger M., Kachel M., George I. Emerging and re-emerging pathogens in valvular infective endocarditis: a review. Pathogens 2024; 13(7): 543, https://doi.org/10.3390/pathogens13070543.
- Cai S., Yang Y., Pan J., Miao Q., Jin W., Ma Y., Zhou C., Gao X., Wang C., Hu B. The clinical value of valve metagenomic next-generation sequencing when applied to the etiological diagnosis of infective endocarditis. Ann Transl Med 2021; 9(19): 1490, https://doi.org/10.21037/atm-21-2488.
- Kim S.L., Gordon S.M., Shrestha N.K. Distribution of streptococcal groups causing infective endocarditis: a descriptive study. Diagn Microbiol Infect Dis 2018; 91(3): 269–272, https://doi.org/10.1016/j.diagmicrobio.2018.02.015.
- Chamat-Hedemand S., Dahl A., Østergaard L., Arpi M., Fosbøl E., Boel J., Oestergaard L.B., Lauridsen T.K., Gislason G., Torp-Pedersen C., Bruun N.E. Prevalence of infective endocarditis in streptococcal bloodstream infections is dependent on streptococcal species. Circulation 2020; 142(8): 720–730, https://doi.org/10.1161/CIRCULATIONAHA.120.046723.
- Habib G., Lancellotti P., Erba P.A., Sadeghpour A., Meshaal M., Sambola A., Furnaz S., Citro R., Ternacle J, Donal E., Cosyns B., Popescu B., Iung B., Prendergast B., Laroche C., Tornos P., Pazdernik M., Maggioni A., Gale C.P.; EURO-ENDO Investigators. The ESC-EORP EURO-ENDO (European Infective Endocarditis) registry. Eur Heart J Qual Care Clin Outcomes 2019; 5(3): 202–207, https://doi.org/10.1093/ehjqcco/qcz018. Erratum in: Eur Heart J Qual Care Clin Outcomes 2020; 6(1): 91, https://doi.org/10.1093/ehjqcco/qcz060.
- Conwell M., Dooley J.S.G., Naughton P.J. Enterococcal biofilm — a nidus for antibiotic resistance transfer? J Appl Microbiol 2022; 132(5): 3444–3460, https://doi.org/10.1111/jam.15441.
- Lecomte R., Laine J.B., Issa N., Revest M., Gaborit B., Le Turnier P., Deschanvres C., Benezit F., Asseray N., Le Tourneau T., Pattier S., Al Habash O., Raffi F., Boutoille D., Camou F. Long-term outcome of patients with nonoperated prosthetic valve infective endocarditis: is relapse the main issue? Clin Infect Dis 2020; 71(5): 1316–1319, https://doi.org/10.1093/cid/ciz1177.
- Calderón-Parra J., Kestler M., Ramos-Martínez A., Bouza E., Valerio M., de Alarcón A., Luque R., Goenaga M.Á., Echeverría T., Fariñas M.C., Pericàs J.M., Ojeda-Burgos G., Fernández-Cruz A., Plata A., Vinuesa D., Muñoz P.; on behalf of the GAMES investigators. Clinical factors associated with reinfection versus relapse in infective endocarditis: prospective cohort study. J Clin Med 2021; 10(4): 748, https://doi.org/10.3390/jcm10040748.
- Danneels P., Hamel J.F., Picard L., Rezig S., Martinet P., Lorleac’h A., Talarmin J.P., Buzelé R., Guimard T., Le Moal G., Brochard-Libois J., Beaudron A., Letheulle J., Codde C., Chenouard R., Boutoille D., Lemaignen A., Bernard L., Cattoir V., Dubée V; EFEMER study group. Impact of Enterococcus faecalis endocarditis treatment on risk of relapse. Clin Infect Dis 2023; 76(2): 281–290, https://doi.org/10.1093/cid/ciac777.
- Basso M., Venditti C., Raponi G., Navazio A.S., Alessandri F., Giombini E., Nisii C., Di Caro A., Venditti M. A case of persistent bacteraemia by Ralstonia mannitolilytica and Ralstonia pickettii in an intensive care unit. Infect Drug Resist 2019; 12: 2391–2395, https://doi.org/10.2147/IDR.S206492.
- Orme J., Rivera-Bonilla T., Loli A., Blattman N.N. Native valve endocarditis due to Ralstonia pickettii: a case report and literature review. Case Rep Infect Dis 2015; 2015: 324675, https://doi.org/10.1155/2015/324675.
- Wright W.F. Central venous access device-related bacillus cereus endocarditis: a case report and review of the literature. Clin Med Res 2016; 14(2): 109–115, https://doi.org/10.3121/cmr.2016.1312.
- Gopinathan A., Kumar A., Sen A.C., Sudha S., Varma P., Gs S., Eapen M., Dinesh K.R. A case series and review of bacillus cereus endocarditis from India. Open Microbiol J 2018; 12: 28–33, https://doi.org/10.2174/1874285801812010028.
- Ioannou P., Miliara E., Baliou S., Kofteridis D.P. Infective endocarditis by Klebsiella species: a systematic review. J Chemother 2021; 33(6): 365–374, https://doi.org/10.1080/1120009X.2021.1888025.










