Эффективность сетей Колмогорова–Арнольда в малых медицинских выборках (на примере сегментации двухмерных МРТ-изображений головного мозга)
Цель исследования — оценка эффективности архитектуры нейронной сети KANU-Net 2D, основанной на архитектуре U-Net, в задаче сегментации двухмерных МРТ-изображений головного мозга из набора данных BraTS при ограниченном количестве обучающих примеров.
Материалы и методы. В рамках работы были проведены эксперименты с подвыборками объемом 50, 100 и 150 изображений. Описаны этапы предобработки данных, включая нормализацию, гамма-коррекцию, обрезку и аугментацию. В качестве функции потерь использовали комбинацию Dice loss и BCE loss. Оптимизацию сети проводили с помощью AdamW. Производительность работы сети оценивали с использованием метрик Accuracy и коэффициента Dice для каждого региона и его среднего значения.
Результаты. Экспериментально продемонстрировано, что KANU-Net 2D достигает конкурентоспособной производительности, сравнимой с современными SOTA-моделями сверточных нейронных сетей, при обучении на малых выборках. В частности, средний коэффициент Dice составил 0,851 при использовании 100 обучающих примеров.
Заключение. Проведенные исследования показали, что сеть KANU-Net 2D превосходит модель для сегментации Med-DANet как по среднему значению, так и по отдельным классам. Эффективность модели для различных зон опухоли обусловливает возможность адаптации подхода на основе KAN (сети Колмогорова–Арнольда) к различным характеристикам изображений в задаче медицинской сегментации. Полученные результаты подчеркивают несомненную перспективность применения KAN для сегментации медицинских изображений на малых выборках и могут служить фундаментом для проведения дальнейших исследований в этой области.
Введение
Сегментация опухолей на МРТ-изображениях головного мозга является сложнейшей задачей для цифровой обработки медицинских данных. Раннее обнаружение и своевременная диагностика играют решающую роль в эффективном лечении. По данным Всемирной организации здравоохранения, в 2020 г. от онкологических заболеваний во всем мире умерло почти 10 млн человек [1]. В отличие от скрининговых рентгенографических обследований легких [2], для головного мозга, согласно источнику [3], аналогичные исследования не проводятся, а обнаружение онкомаркеров заболеваний в организме пациентов при плановых обследованиях не позволяет определить точное расположение новообразований [3]. Снимки, полученные с использованием различных модальностей МРТ, имеют разные настройки параметров яркости, гаммы и пр. [4], а существующие в настоящее время компьютерные алгоритмы обработки изображений не могут эффективно адаптироваться под любые магнитно-резонансные исследования.
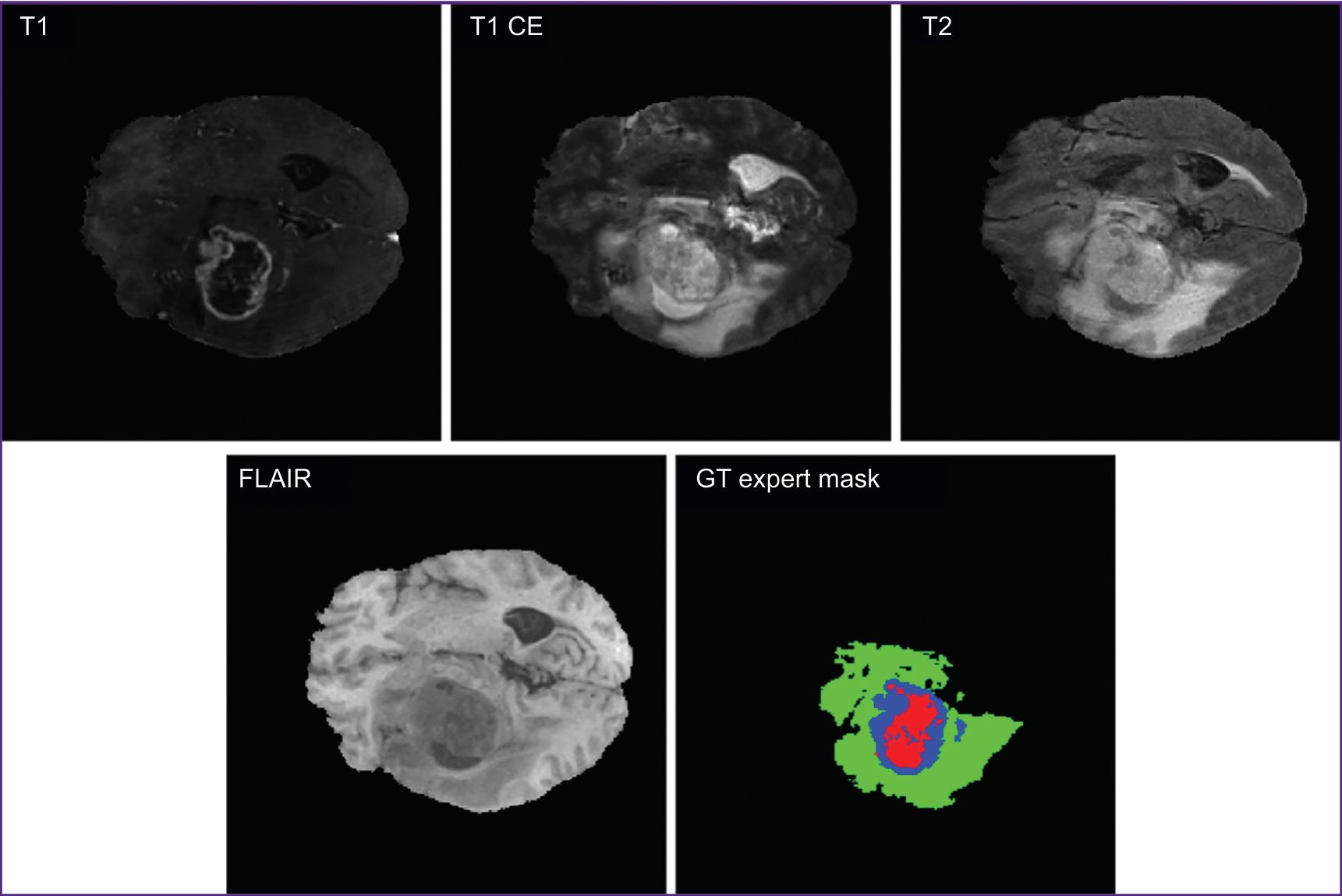
Современные методы сегментации медицинских изображений включают в себя пороговую сегментацию, метод разделения и слияния областей, морфологическую сегментацию, методы кластеризации, метод наращивания областей и т. д. [5, 6]. Однако зачастую анализ полученных МРТ-изображений проводится врачами вручную, что является ресурсозатратным и сложным процессом [7]. На рис. 1 приведены МРТ-изображения в различных модальностях (T1, T1 CE, T2, FLAIR [3]) и маска сегментации (GT expert mask), отмеченная врачами-экспертами.
Передовыми методами в сегментации медицинских изображений на сегодняшний день являются алгоритмы на базе сверточных нейронных сетей [8]. Примером такого алгоритма может послужить сеть U-Net [9], зарекомендовавшая себя как одна из лучших архитектур для работы с медицинскими изображениями. На базе этой сети разработаны многие другие современные решения.
Сеть U-Net включает в себя два основных блока — энкодер и декодер. Первый осуществляет свертку изображения в меньший пиксельный формат, а второй, наоборот, увеличивает разрешение итогового изображения. Данные блоки связаны между собой сверточными слоями, которые реализуют алгоритмы выделения ключевых признаков на разных уровнях абстракции. Каждый слой энкодера отвечает за поиск определенных пикселей на изображении и за создание карты признаков, а слои декодера обеспечивают повышение дискретизации полученной карты признаков. На следующем этапе применяются такие операции, как батч-нормализация и нелинейная функция активации ReLU, после чего выполняется еще одна свертка и операция maxpooling размером 2×2, которая уменьшает пространственные размеры полученной матрицы признаков, тем самым сжимая информацию для последующего прохода в сети. На выходе сети мы получаем вероятность принадлежности изображения к какому-либо из заранее заданных классов.
Анализ работ с моделями на базе архитектуры U-Net 2D [10–12] показал, что высокие значения основной метрики качества сети коэффициента Dice достигаются на больших объемах обучающей выборки — 369 снимков и более. В силу того, что современным моделям нейронных сетей требуются огромные наборы данных для обучения, существует проблема создания алгоритмов, работающих на малых выборках с той же эффективностью [13].
Малые выборки возникают потому, что в медицине встречаются достаточно редкие заболевания, и это обусловливает небольшое количество наблюдений. В результате мы не можем применить серьезные разработки на основе моделей сверточных нейронных сетей к реальным практическим задачам [14]. В нейроонкологии проблема малых выборок особенно актуальна для редких видов опухолей головного мозга или опухолей с нетипичной локализацией. Разработка инструментов, способных эффективно работать в условиях малого количества данных, позволит ускорить внедрение систем поддержки принятия решений в рутинную клиническую практику.
Нейронные сети на базе теоремы Колмогорова–Арнольда (KAN) [15] перспективны именно в плане применимости на малых выборках. Среди достоинств этих сетей в литературе [16] отмечают устойчивость при обучении на малых данных, хотя для медицинских данных этот подход недостаточно исследован. Из недостатков указывают низкую скорость обучения. Обзоры остальных свойств сетей KAN представлены в источниках [15, 16].
Существующие исследования KANв медицине на сегодняшний день слабо освещены, несмотря на то что очень перспективны в области изучения малых выборок медицинских данных. К тому же имеющиеся работы в основном фокусируются только на задачах классификации и простых изображениях с высокой контрастной различимостью, таких как MedMNIST(масштабная коллекция стандартизированных медицинских изображений) и рентгенография грудной клетки с четко видимыми особенностями [17, 18], что не позволяет охватить весь спектр задач, основанных на обработке медицинских изображений.
Цель исследования — оценка эффективности архитектуры нейронной сети KANU-Net 2D, основанной на архитектуре U-Net, в задаче сегментации двухмерных МРТ-изображений головного мозга из набора данных BraTS при ограниченном количестве обучающих примеров.
Материалы и методы
Архитектура сети. В работе использована сеть KANU-Net2D [19], которая основана на классическом U-Netс энкодер–декодерной структурой и остаточными соединениями. В этой архитектуре стандартные сверточные слои Сonv2D заменены на FastKANConvLayers. Каждый FastKANConvLayer включает преобразование входных признаков с использованием радиально-базисной функции (radial basis function, RBF):
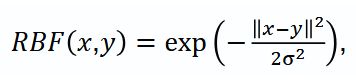
где x — входной вектор изображения, y — центр функции, σ — ширина ядра.
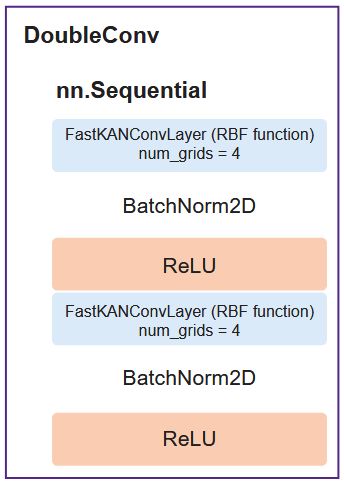
Сеть включает в себя энкодер — серию блоков DoubleConv (рис. 2) (два последовательных FastKANConvLayers, за которыми следуют пакетная нормализация и активация ReLU) и декодер.
|
Рис. 2. Блок DoubleConv с встроенными слоями FastKANConvLayer |
Сеть обрабатывает 2D-срезы с 4 входными каналами, которые соответствуют четырем модальностям, и выдает четырехканальную сегментационную маску, представляющую вероятностное распределение анатомических структур.
Набор данных. В качестве набора данных использован бенчмарковый датасет BraTS2020 [20], из которого случайным образом извлекли 3 обучающие подвыборки объемом 50, 100, 150 примеров. Один четырехканальный снимок из датасета состоит из нескольких модальностей: T1 — взвешенное изображение; T1 CE — взвешенное изображение с контрастированием гадолинием; T2 — взвешенное изображение; FLAIR (fluid attenuated inversion recovery) — изображение инверсионного восстановления с подавлением сигнала от жидкости.
Кроме того, для каждого снимка имеются аннотации, указывающие на тип ткани и верифицированные 4 клиническими экспертами: нормальная ткань; перитуморальная зона/зона отека–инфильтрации; неконтрастируемое ядро; некротическое ядро; контрастнакапливающая часть опухоли.
Для экспериментов в работе использованы 2D-срезы, извлеченные из объемных данных, с акцентом на аксиальные срезы, которые наилучшим образом представляют зоны опухоли. Данная сегментация позволяет выделить ключевые области интереса согласно стандартам BraTS по трем классам: все опухолевые ткани (whole tumor, WT); ядро опухоли (tumor core, TC); контрастнакапливающая часть опухоли (ET).
Предобработка данных. Метод предобработки, примененный в настоящей работе, включал несколько шагов для улучшения качества и однородности входных данных:
1) каждая модальность МРТ была независимо нормализована в диапазоне [–1,0; 1,0] с использованием масштабирования min–max для стандартизации распределения интенсивностей по различным сканам;
2) гамма-коррекция со значениями гаммы 1,0; 1,5; 1,5; 1,2 для срезов T1, T1 CE, T2 и FLAIR соответственно;
3) изображения были обрезаны до фиксированного размера 224×224 пикселей и центрированы на области мозга.
При формировании обучающего датасета использовали аугментацию данных, которая включала случайные повороты на 90° и случайные сдвиги для улучшения способности модели к обобщению.
Функция потерь и оптимизация. В качестве функции потерь (Loss) выбрана комбинация на основе Dice loss и Binary-Cross Entropy (BCE loss), которая учитывает значительный дисбаланс классов в сегментации:
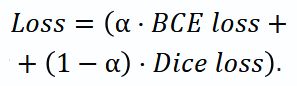
Значение α=0,2 подобрано эмпирически для обеспечения стабильности обучения и оптимального качества итоговой сегментации.
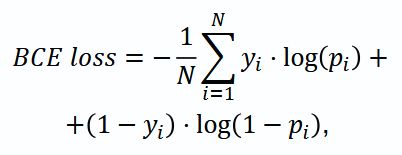
где N — количество пикселей в изображении; yi — истинная метка (0 или 1) пикселя i; pi — предсказанная моделью вероятность принадлежности пикселя iк классу 1; log — натуральный логарифм.
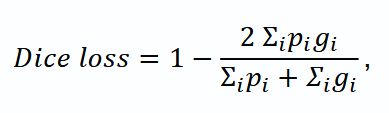
где pi — предсказанное значение для пикселя i; gi — истинная метка (0 или 1).
В качестве оптимизатора использован AdamW с начальной скоростью обучения lr=1e–4 и weight decay 1e–6. Планировщиком был выбран «косинусный отжиг» с перезапусками, с минимальной скоростью обучения 1e–3.
Метрики оценки. В работе проведена комплексная оценка, включающая метрики Accuracy, средний коэффициент Dice и коэффициент Dice для зон (Diceregion): все опухолевые ткани (WT), ядро опухоли (TC) и контраст-накапливающая часть опухоли (ET). Средний Dice, рассчитанный как среднее значение коэффициентов Dice для ET, TC и WT, служил основной метрикой для выбора лучшей модели.
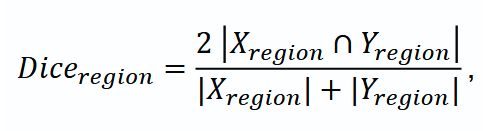
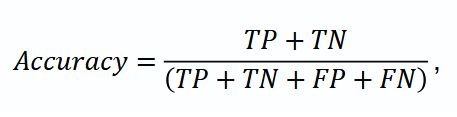
где TP (true positives) — количество истинно положительных результатов; TN (true negatives) — количество истинно отрицательных результатов; FP (false positives) — количество ложноположительных результатов; FN (false negatives) — количество ложноотрицательных результатов.
Эксперименты. Методика эксперимента заключалась в обучении сети KAN независимо на трех подвыборках с различными объемами и в сравнении результатов с существующими SOTA-моделями сверточных нейронных сетей.
Эксперименты проводили с использованием следующей конфигурации:
фреймворки pytorch, monai [21];
размеры обучающих выборок составляют 50, 100, 150 примеров;
размеры валидационной и тестовой выборки составляют 50 примеров;
размер батча — 2;
4 узловые точки в сети KAN (num grids);
[−1,0; 1,0] диапазон точек сети KAN (grid min, grid max);
количество эпох — 100.
Результаты
В табл. 1, 2 представлены основные метрики производительности модели KANU-Net 2D на тестовом наборе BraTS 2020 с фокусом на специфичных областях опухоли (ET, WT, TC). В табл. 3 приведено сравнение эффективности разработанного подхода с другими известными моделями на том же наборе данных, но с большей обучающей выборкой.
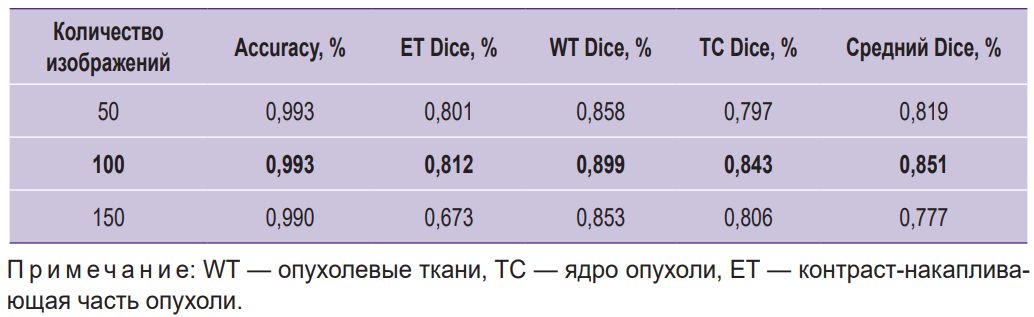 |
Таблица 1. Сравнение производительности модели KANU-Net 2D для различного объема выборок |
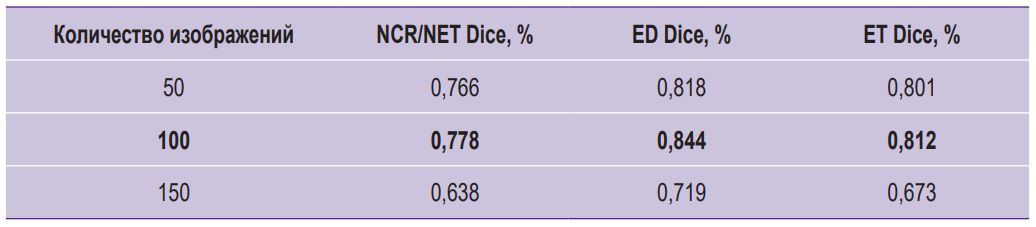 |
Таблица 2. Сравнение производительности модели KANU-Net 2D для классов: некротическое и неконтрастирующее ядро опухоли (NCR/NET), перитуморальный отек (ED) и контрастирующая часть (ET) |
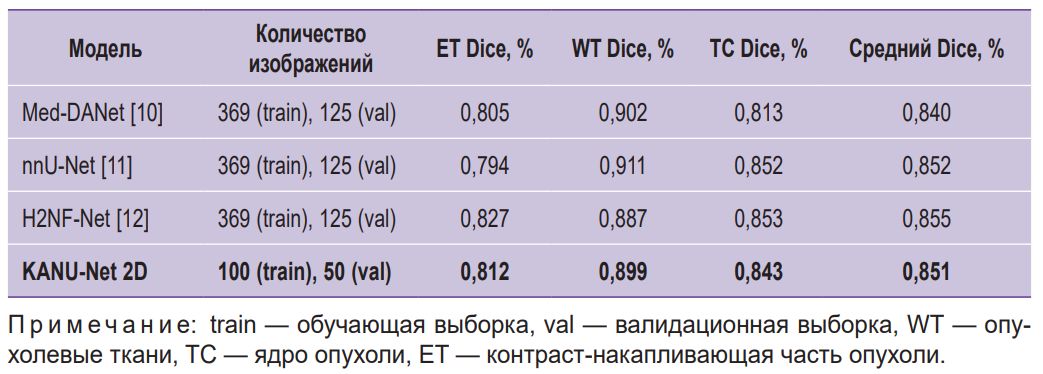 |
Таблица 3. Сравнение KANU-Net 2D с SOTA-моделями |
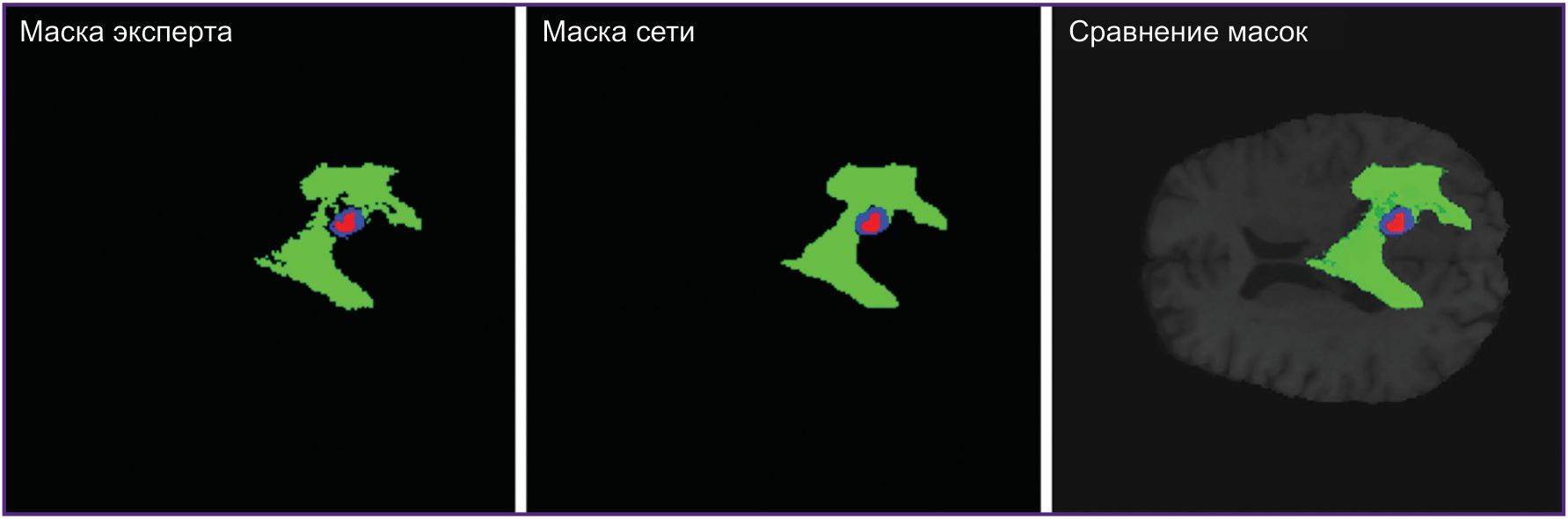
Эксперименты показали, что модель KANU-Net 2D, обученная на малых объемах выборки, достигла среднего значения коэффициента Dice, равного 0,851. Эти результаты превосходят модель, специально разработанную для медицинской сегментации Med-DANet [10], а также сравнимы с современными SOTA-моделями, обучаемыми на полном наборе данных BraTS 2020. Результаты визуализации сети представлены на рис. 3.
|
Рис. 3. Маска сегментации эксперта, маска предсказания сети KANU-Net 2D и их сравнение на одном МРТ-снимке |
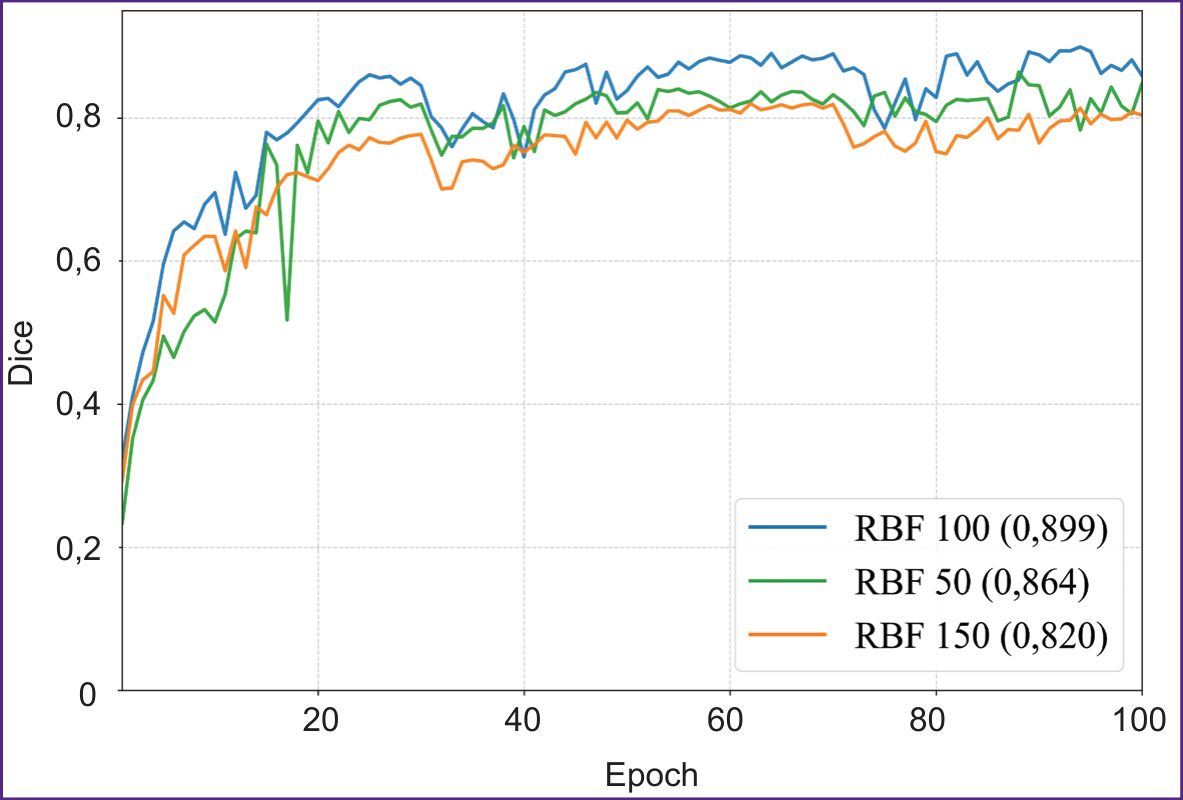
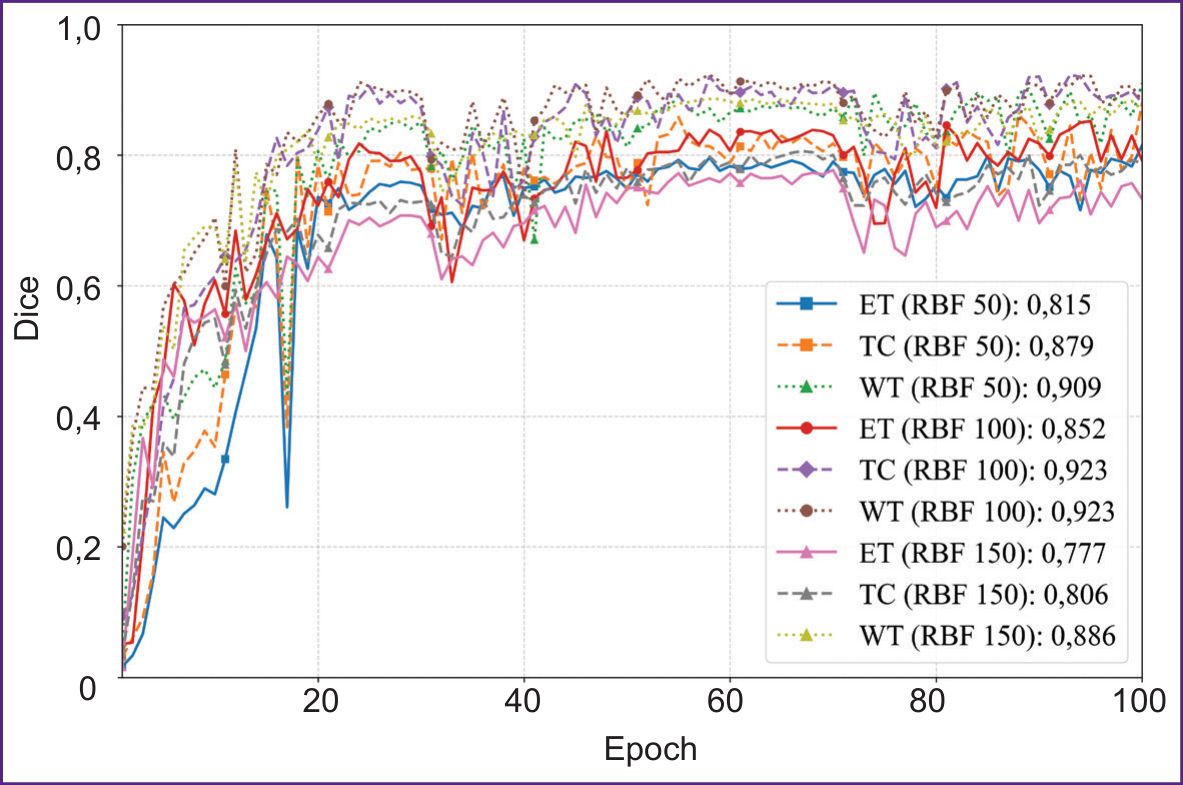
Рис. 4, 5 иллюстрируют динамику обучения модели на 50, 100 и 150 изображениях подвыборки на протяжении 100 эпох. Модель показала устойчивое улучшение метрик качества на валидационной выборке на протяжении всего обучения, с выходом на плато среднего коэффициента Dice после 60-й эпохи. Модель на основе KAN достигает точности, сопоставимой с SOTA-архитектурами сверточных нейронных сетей, используя меньшие объемы выборки, что свидетельствует о применимости подхода KAN для обработки высокотехнологичных медицинских изображений.
|
Рис. 4. График среднего значения коэффициента Dice в зависимости от эпох на сети KANU-Net 2D (50, 100, 150 изображений) |
|
Рис. 5. Графики значения коэффициента Dice в зависимости от эпох на сети KANU-Net 2D для классов ET, TC, WT (50, 100, 150 изображений) |
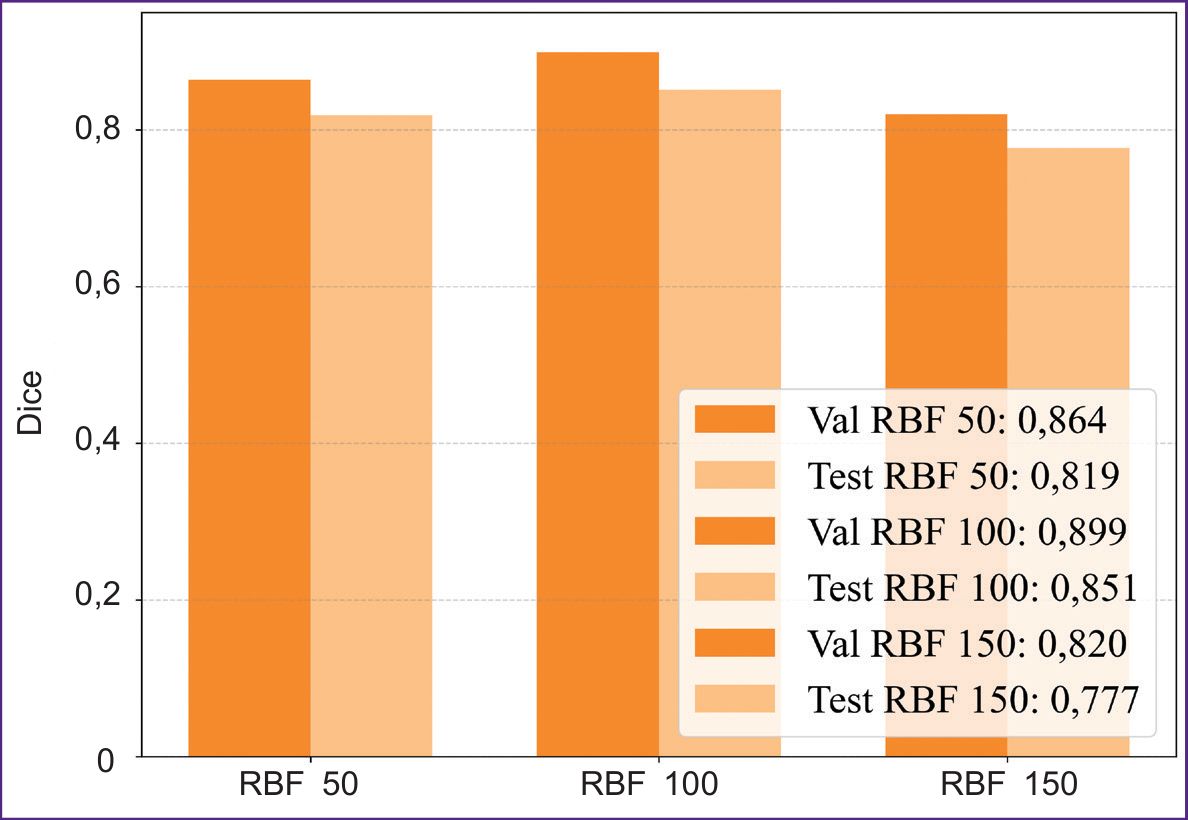
На рис. 6 представлена сравнительная диаграмма производительности модели при различных объемах выборки на валидационных и тестовых данных. Из результатов следует, что размер выборки n=100 является наилучшим по достигаемому коэффициенту Dice=0,851.
|
Рис. 6. Диаграмма сравнения коэффициента Dice для валидационной (Val) и тестовой (Test) выборок различных объемов данных (50, 100, 150 изображений) на сети KANU-Net 2D |
Обсуждение
В литературе встречаются примеры подобных исследований в задаче сегментации МРТ, однако другие авторы используют полные наборы данных или большие выборки медицинских изображений [22], обучают сеть сразу на нескольких наборах данных, похожих по своей сложной анатомической структуре [23], а также используют тяжеловесные трехмерные изображения. В работе [22] выбран похожий набор данных МРТ BraTS-GLI2024, применяется модель KAN с модулями эффективного внимания к каналам и агрегации пирамидальных признаков, что позволяет достичь коэффициента Dice, равного 0,88–0,90, на различных регионах опухоли. При этом для обучения сети использовалось значительно большее число изображений: 1080 для обучающей выборки и по 135 — для валидационной и тестовой выборок.
Полученное в настоящем исследовании среднее значение коэффициента Dice (0,851) на выборке всего из 100 изображений представляется клинически значимым. Для нейрохирурга такая точность сегментации ключевых областей опухоли (ET, WT, TC) может быть достаточной при определении тактики ведения пациента. Значение Dice для области WT, равное 0,899, указывает на возможность надежной оценки общего объема опухоли. При очень больших размерах опухоли ее радикальное удаление может быть недостижимо и ввиду этого нецелесообразно. В данной ситуации рекомендуется ограничиться проведением стереотаксической биопсии. Такой подход позволит улучшить качество предоперационного планирования, особенно в части определения объема оперативного вмешательства. При планировании стереотаксической биопсии точное выделение контраст-накапливающей части опухоли (ET, Dice=0,812) имеет принципиальное значение, так как в большинстве случаев именно эта область соответствует наиболее злокачественному компоненту опухоли.
Ограничением настоящего исследования сети KANU-Net 2D является использование лишь одной базисной функции RBF, в то время как существует огромное их разнообразие [24], а также фиксированное количество узловых точек в сети (num grids), равное 4. Данные особенности сети KAN требуют дальнейших исследований в задаче сегментации медицинских изображений.
Настоящее исследование в большей степени раскрывает технические детали применения сетей Колмогорова–Арнольда для анализа малых медицинских выборок, однако его результаты имеют очевидную клиническую направленность. Обучение моделей на малых наборах данных позволит создавать специализированные инструменты для сегментации редких патологий, где сбор сотен примеров невозможен. Внедрение указанных алгоритмов в клиническую практику открывает возможность для разработки специализированного программного обеспечения, предназначенного для предоперационного анализа изображений с разметкой снимков и оценкой объемов опухоли. Визуализация результатов, представленная на рис. 3, демонстрирует, что модель адекватно справляется с указанной задачей, а ее прогнозы визуально близки к экспертной разметке.
Заключение
Проведенные исследования показали, что сеть KANU-Net 2D превосходит модель для сегментации Med-DANet как по среднему значению, так и по отдельным классам. Кроме того, сеть достигает конкурентоспособной производительности на наборе данных BraTS 2020 в сравнении с другими моделями, о чем свидетельствует значение среднего коэффициента Dice 0,851 для трех областей опухоли в сопоставлении со значениями 0,852 и 0,855 для nnU-Net и H2NF-Net соответственно. Эффективность модели для различных зон опухоли обусловливает возможность подхода на основе KAN адаптироваться к различным характеристикам изображений в задаче медицинской сегментации.
Помимо технической эффективности, продемонстрированный подход обладает значительным клиническим потенциалом. Дальнейшие исследования должны быть направлены на валидацию модели в условиях реальной нейрохирургической практики и оценку результатов сегментации практикующими нейрохирургами. Это позволит сделать шаг от оценки метрик к оценке реальной пользы для хирургического планирования.
Финансирование. Настоящее исследование не получало внешнего финансирования.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Литература
- World Health Organization. URL: https://www.who.int/ru/news-room/fact-sheets/detail/cancer.
- Тюрин И.Е. Скрининг заболеваний органов дыхания: современные тенденции. Атмосфера. Пульмонология и аллергология 2011; 2: 12–16.
- Абдулракеб А.Р.А., Сушкова Л.Т., Лозовская Н.А. Обзор методов сегментации опухолей на МРТ-изображениях головного мозга. Прикаспийский журнал: управление и высокие технологии 2015; 1(29): 122–138.
- Sharma N., Aggarwal L.M. Automated medical image segmentation techniques. J Med Phys 2010; 35(1): 3–14, https://doi.org/10.4103/0971-6203.58777.
- Alam M.S., Rahman M.M., Hossain M.A., Islam M.K., Ahmed K.M., Ahmed K.T., Singh B.C., Miah M.S. Automatic human brain tumor detection in MRI image using template-based K means and improved fuzzy С means clustering algorithm. Big Data and Cognitive Computing 2019; 3(2): 27, https://doi.org/10.3390/bdcc3020027.
- Shahid N., Rappon T., Berta W. Applications of artificial neural networks in health care organizational decision-making: a scoping review. PLoS One 2019; 14(2): e0212356, https://doi.org/10.1371/journal.pone.0212356.
- Михелев В.М., Мирошниченко А.С. Решение задачи классификации патологий головного мозга человека на снимках МРТ. Научный результат. Информационные технологии 2019; 4(2): 43–52, https://doi.org/10.18413/2518-1092-2019-4-2-0-5.
- Zhanga Y., Liaoa Q., Dinga L., Zhanga J. Bridging 2D and 3D segmentation networks for computation efficient volumetric medical image segmentation: an empirical study of 2.5D solutions. Computerized Medical Imaging and Graphics 2022; 99: 102088, https://doi.org/10.1016/j.compmedimag.2022.102088.
- Ronneberger O., Fischer P., Brox T. U-Net: convolutional networks for biomedical image segmentation. In: Navab N., Hornegger J., Wells W., Frangi A. (editors). Medical image computing and computer-assisted intervention — MICCAI 2015. MICCAI 2015. Lecture notes in computer science, vol. 9351. Springer, Cham; 2015, https://doi.org/10.1007/978-3-319-24574-4_28.
- Wang W., Chen C., Wang J., Li J. Med-DANet: dynamic architecture network for efficient medical volumetric segmentation. In: Computer vision — ECCV 2022: 17th European conference. Tel Aviv, Israel, October 23–27, 2022. Proceedings, Part XXI. Israel; 2022; p. 506–522, https://doi.org/10.1007/978-3-031-19803-8_30.
- Isensee F., Jäger P.F., Full P.M., Vollmuth P., Maier-Hein K.H. nnU-Net for brain tumor segmentation. In: Crimi A., Bakas S. (editors). Brainlesion: glioma, multiple sclerosis, stroke and traumatic brain injuries. BrainLes 2020. Lecture notes in computer science, vol. 12659. Springer, Cham; 2021; p. 118–113, https://doi.org/10.1007/978-3-030-72087-2_11.
- Jia H., Cai W., Huang H., Xia Y. H2NF-Net for brain tumor segmentation using multimodal MR imaging: 2nd place solution to BraTS challenge 2020 segmentation task. In: Crimi A., Bakas S. (editors). Brainlesion: glioma, multiple sclerosis, stroke and traumatic brain injuries. BrainLes 2020. Lecture notes in computer science, vol. 12659. Springer, Cham; 2021, https://doi.org/10.1007/978-3-030-72087-2_6.
- Поряева Е.П., Евстафьева В.А. Искусственный интеллект в медицине. Вестник науки и образования 2019; 6-2(60): 18.
- Носовский А.М., Пихлак А.Э., Логачев В.А., Чурсинова И.И., Мутьева Н.А. Статистика малых выборок в медицинских исследованиях. Медицинская статистика и методология 2022; 3: 45–52.
- Liu Z., Tegmark M., Ma P., Matusik W., Wang Y. Kolmogorov–Arnold networks meet science. Phys Rev X 2025; 15(4), https://doi.org/10.1103/4t7t-v19l.
- Yang Z., Zhang J., Luo X., Wu X., Lu Z., Shen L. MedKAN: an advanced Kolmogorov–Arnold network for medical image classification. In: IEEE International Conference on Bioinformatics and Biomedicine (BIBM). China; 2025; p. 3090–3097, https://doi.org/10.1109/bibm66473.2025.11356561.
- Ibrahum A.D.M., Shang Z., Hong J.E. How resilient are Kolmogorov–Arnold networks in classification tasks? A robustness investigation. Applied Sciences 2024; 14(22): 10173, https://doi.org/10.3390/app142210173.
- Li C., Liu X., Li W., Wang C., Liu H., Liu Y., Chen Z., Yuan Y. U-KAN makes strong backbone for medical image segmentation and generation. Proceedings of the AAAI Conference on Artificial Intelligence 2025; 39(5): 4652–4660, https://doi.org/10.1609/aaai.v39i5.32491.
- Jaouad T. KANU-Net: Kolmogorov–Arnold networks based U-Net architecture for images segmentation. URL: https://github.com/JaouadT/KANU_Net.
- Menze B.H., Jakab A., Bauer S., Kalpathy-Cramer J., Farahani K., Kirby J., Burren Y., Porz N., Slotboom J., Wiest R., Lanczi L., Gerstner E., Weber M.A., Arbel T., Avants B.B., Ayache N., Buendia P., Collins D.L., Cordier N., Corso J.J., Criminisi A., Das T., Delingette H., Demiralp Ç., Durst C.R., Dojat M., Doyle S., Festa J., Forbes F., Geremia E., Glocker B., Golland P., Guo X., Hamamci A., Iftekharuddin K.M., Jena R., John N.M., Konukoglu E., Lashkari D., Mariz J.A., Meier R., Pereira S., Precup D., Price S.J., Raviv T.R., Reza S.M., Ryan M., Sarikaya D., Schwartz L., Shin H.C., Shotton J., Silva C.A., Sousa N., Subbanna N.K., Szekely G., Taylor T.J., Thomas O.M., Tustison N.J., Unal G., Vasseur F., Wintermark M., Ye D.H., Zhao L., Zhao B., Zikic D., Prastawa M., Reyes M., Van Leemput K. The multimodal brain tumor image segmentation benchmark (BRATS). IEEE Trans Med Imaging 2015; 34(10): 1993–2024, https://doi.org/10.1109/TMI.2014.2377694.
- Cardoso M., Li W., Brown R., Ma N., Kerfoot E., Wang Y., Murrey B., Myronenko A., Zhao C., Yang D., Nath V., He Y., Xu Z., Hatamizadeh A., Myronenko A., Zhu W., Liu Y., Zheng M., Tang Y., Yang I., Zephyr M., Hashemian B., Alle S., Darestani M. Z., Budd C., Modat M., Vercauteren T., Wang G., Li Y., Hu Y., Fu Y., Gorman B., Johnson H., Genereaux B., Erdal B.S., Gupta V., Diaz-Pinto A., Dourson A., Maier-Hein L., Jaeger P.F., Baumgartner M., Kalpathy-Cramer J., Flores M., Kirby J., Cooper L.A.D., Roth H.R., Xu D., Bericat D., Floca R., Zhou S.K., Shuaib H., Farahani K., Maier-Hein K.H., Aylward S., Dogra P., Ourselin S., Feng A. MONAI: an open-source framework for deep learning in healthcare 2022. URL: https://arxiv.org/abs/2211.02701.
- Chen Y., Tang T., Kim T., Shu H. UKAN-EP: enhancing U-KAN with efficient attention and pyramid aggregation for 3D multi-modal MRI brain tumor segmentation. BMC Medical Imaging 2025; 25(1), https://doi.org/10.1186/s12880-025-02053-w.
- Ilerioluwakiiye A., Udo A., Ojo A., Oyetunji A., Ajigbotosho H., Iorumbur A., Raymond C., Adewole M. Domain-adaptive transformer for data-efficient glioma segmentation in Sub-Saharan MRI. 2025. URL: https://arxiv.org/abs/2511.02928.
- Seydi S.T. Exploring the potential of polynomial basis functions in Kolmogorov–Arnold networks: a comparative study of different groups of polynomials. 2024. URL: https://arxiv.org/abs/2406.02583.