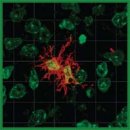
Иммуногистохимическое выявление микроглии с использованием маркера Iba-1 в норме и при патологии
Цель исследования — оценить возможности и ограничения использования метода иммуногистохимического выявления белка Iba-1 для морфофункционального анализа микроглии в разных условиях.
Материалы и методы. Материалом для исследования служили образцы головного мозга крыс линии Wistar разных возрастных групп: 7-е сутки постнатального онтогенеза (n=18), 14-е сутки постнатального онтогенеза (n=18), половозрелые животные в возрасте 4–6 мес (n=22); а также образцы головного мозга крыс-самцов линии SHR (spontaneously hypertensive rats) в возрасте 3–6 мес (n=4); образцы коры больших полушарий головного мозга человека (n=10). Для иммуногистохимического выявления микроглии использовали кроличьи поликлональные антитела против кальций-связывающего белка Iba-1 (Biocare Medical, США) с последующей идентификацией методами световой и конфокальной лазерной микроскопии. Для одновременного выявления клеток микроглии и амилоидных бляшек применяли оригинальную методику, разработанную ранее.
Результаты. В рамках проведенных исследований показано, что белок Iba-1 присутствует в клетках микроглии в сером и белом веществе во всех изученных областях головного мозга. Отмечено, что в разных областях для клеток микроглии характерны выраженные структурно-функциональные особенности при реакции на Iba-1. Помимо клеток микроглии в головном мозге крысы обнаружены другие Iba-1-иммунопозитивные клетки, которые являются тканевыми макрофагами мозга и отличаются от клеток микроглии по морфологии и локализации. Продемонстрировано, что белок Iba-1 присутствует в микроглиоцитах на всех изученных стадиях постнатального онтогенеза, что делает его удобным маркером для сравнительно-онтогенетических исследований этих клеток. Локализация Iba-1 в телах и отростках микроглиоцитов позволяет наиболее полно выявлять сложную отростчатую морфологию клеток и строить трехмерные реконструкции. Показано, что в головном мозге у спонтанно гипертензивных крыс линии SHR микроглия имеет ряд структурно-функциональных особенностей при реакции на Iba-1, указывающих на умеренную активацию микроглии. В головном мозге у крыс через 48 ч после ишемического воздействия в сером веществе стриатума ипсилатерального полушария рядом с областью повреждения выявлено аномально большое число крупных Iba-1-иммунопозитивных клеток с амебоидной морфологией. Отмечено, что в коре головного мозга человека клетки микроглии присутствуют в составе большинства выявленных амилоидных бляшек и имеют амебоидную морфологию, что указывает на их сильную активацию.
Заключение. Представленные результаты свидетельствуют о том, что белок Iba-1 является надежным и универсальным маркером микроглии. Иммуногистохимическое выявление этого белка позволяет идентифицировать, а также качественно и количественно анализировать микроглию в разных отделах головного мозга у человека и лабораторных животных в норме и при патологии. К ограничениям использования Iba-1 в качестве маркера микроглии можно отнести невозможность определения вектора активации микроглии и сложность различения микроглии и инфильтрирующих макрофагов мозга при патологии. В этих случаях необходимо совершенствовать технологию выявления микроглии, что может быть основано на использовании многомаркерного анализа.
- Adamu A., Li S., Gao F., Xue G. The role of neuroinflammation in neurodegenerative diseases: current understanding and future therapeutic targets. Front Aging Neurosci 2024; 16: 1347987, https://doi.org/10.3389/fnagi.2024.1347987.
- Muzio L., Viotti A., Martino G. Microglia in neuroinflammation and neurodegeneration: from understanding to therapy. Front Neurosci 2021; 15: 742065, https://doi.org/10.3389/fnins.2021.742065.
- Healy L.M., Zia S., Plemel J.R. Towards a definition of microglia heterogeneity. Commun Biol 2022; 5(1): 1114, https://doi.org/10.1038/s42003-022-04081-6.
- Malinovskaya N.A., Frolova O.V., Shishelova K.O., Panina Yu.A. Current methods for the isolation and cultivation of microglia (review). Sovremennye tehnologii v medicine 2021; 13(6): 89, https://doi.org/10.17691/stm2021.13.6.10.
- Jurga A.M., Paleczna M., Kuter K.Z. Overview of general and discriminating markers of differential microglia phenotypes. Front Cell Neurosci 2020; 14: 198, https://doi.org/10.3389/fncel.2020.00198.
- Cserép C., Pósfai B., Dénes Á. Shaping neuronal fate: functional heterogeneity of direct microglia-neuron interactions. Neuron 2021; 109(2): 222–240, https://doi.org/10.1016/j.neuron.2020.11.007.
- Masuda T., Sankowski R., Staszewski O., Prinz M. Microglia heterogeneity in the single-cell era. Cell Rep 2020; 30(5): 1271–1281, https://doi.org/10.1016/j.celrep.2020.01.010.
- Galatro T.F., Holtman I.R., Lerario A.M., Vainchtein I.D., Brouwer N., Sola P.R., Veras M.M., Pereira T.F., Leite R.E.P., Möller T., Wes P.D., Sogayar M.C., Laman J.D., den Dunnen W., Pasqualucci C.A., Oba-Shinjo S.M., Boddeke E.W.G.M., Marie S.K.N., Eggen B.J.L. Transcriptomic analysis of purified human cortical microglia reveals age-associated changes. Nat Neurosci 2017; 20(8): 1162–1171, https://doi.org/10.1038/nn.4597.
- Tan Y.L., Yuan Y., Tian L. Microglial regional heterogeneity and its role in the brain. Mol Psychiatry 2020; 25(2): 351–367, https://doi.org/10.1038/s41380-019-0609-8.
- Hickman S.E., Kingery N.D., Ohsumi T.K., Borowsky M.L., Wang L.C., Means T.K., El Khoury J. The microglial sensome revealed by direct RNA sequencing. Nat Neurosci 2013; 16(12): 1896–1905, https://doi.org/10.1038/nn.3554.
- Mildner A., Huang H., Radke J., Stenzel W., Priller J. P2Y12 receptor is expressed on human microglia under physiological conditions throughout development and is sensitive to neuroinflammatory diseases. Glia 2017; 65(2): 375–387, https://doi.org/10.1002/glia.23097.
- Zia S., Rawji K.S., Michaels N.J., Burr M., Kerr B.J., Healy L.M., Plemel J.R. Microglia diversity in health and multiple sclerosis. Front Immunol 2020; 11: 588021, https://doi.org/10.3389/fimmu.2020.588021.
- Fumagalli L., Nazlie Mohebiany A., Premereur J., Polanco Miquel P., Bijnens B., Van de Walle P., Fattorelli N., Mancuso R. Microglia heterogeneity, modeling and cell-state annotation in development and neurodegeneration. Nat Neurosci 2025; 28(7): 1381–1392, https://doi.org/10.1038/s41593-025-01931-4.
- Kanazawa H., Ohsawa K., Sasaki Y., Kohsaka S., Imai Y. Macrophage/microglia-specific protein Iba1 enhances membrane ruffling and Rac activation via phospholipase C-gamma-dependent pathway. J Biol Chem 2002; 277(22): 20026–20032, https://doi.org/10.1074/jbc.M109218200.
- Kolos E.A., Korzhevskii D.E. Spinal cord microglia in health and disease. Acta Naturae 2020; 12(1): 4–17, https://doi.org/10.32607/actanaturae.10934.
- Дыбан А.П., Пучков В.Ф., Баранов В.С., Самошкина Н.А., Чеботарь Н.А. Лабораторные млекопитающие: мышь Mus musculus, крыса Rattus norvegicus, кролик Oryctolagus cuniculus, хомячок Cricetus griseous. В кн.: Объекты биологии развития. М: Наука; 1975; с. 505–566.
- Коржевский Д.Э., Кирик О.В., Власов Т.Д. Появление звездчатых гладких миоцитов в головном мозгу крысы после транзиторной фокальной ишемии. Морфология 2013; 143(1): 073–075.
- Гусельникова В.В., Антипова М.В., Федорова Е.А., Сафрай А.Е., Рукавишникова А.А., Михайлова Е.В., Коржевский Д.Э. Особенности применения методов гистохимии и иммуногистохимии для выявления амилоидных бляшек в коре головного мозга человека. Журнал анатомии и гистопатологии 2019; 8(2): 91–99, https://doi.org/10.18499/2225-7357-2019-8-2-91-99.
- Коржевский Д.Э., Сухорукова Е.Г., Гилерович Е.Г., Петрова Е.С., Кирик О.В., Григорьев И.П. Преимущества и недостатки цинк-этанол-формальдегида как фиксатора для иммуноцитохимических исследований и конфокальной лазерной микроскопии. Morphology 2013; 143(2): 081–085.
- Носова О.И., Гусельникова В.В., Коржевский Д.Э. Метод одновременного выявления глиальных клеток и скоплений амилоида на светооптическом уровне. Цитология 2021; 63(6): 557–567, https://doi.org/10.31857/S0041377121060092.
- Korzhevskii D.E., Kirik O., Sukhorukova E. Immunocytochemistry of microglial cells. In: Merigh A., Lossi L. (editors). Immunocytochemistry and related techniques. Neuromethods. Vol. 101. Humana Press, New York; 2015, https://doi.org/10.1007/978-1-4939-2313-7_12.
- Bennett M.L., Bennett F.C., Liddelow S.A., Ajami B., Zamanian J.L., Fernhoff N.B., Mulinyawe S.B., Bohlen C.J., Adil A., Tucker A., Weissman I.L., Chang E.F., Li G., Grant G.A., Hayden Gephart M.G., Barres B.A. New tools for studying microglia in the mouse and human CNS. Proc Natl Acad Sci U S A 2016; 113(12): E1738–E1746, https://doi.org/10.1073/pnas.1525528113.
- Lier J., Streit W.J., Bechmann I. Beyond activation: characterizing microglial functional phenotypes. Cells 2021; 10(9): 2236, https://doi.org/10.3390/cells10092236.
- Hirasawa T., Ohsawa K., Imai Y., Ondo Y., Akazawa C., Uchino S., Kohsaka S. Visualization of microglia in living tissues using Iba1-EGFP transgenic mice. J Neurosci Res 2005; 81(3): 357–362, https://doi.org/10.1002/jnr.20480.
- Shui X., Chen J., Fu Z., Zhu H., Tao H., Li Z. Microglia in ischemic stroke: pathogenesis insights and therapeutic challenges. J Inflamm Res 2024; 17: 3335–3352, https://doi.org/10.2147/JIR.S461795.
- Taylor R.A., Sansing L.H. Microglial responses after ischemic stroke and intracerebral hemorrhage. Clin Dev Immunol 2013; 2013: 746068, https://doi.org/10.1155/2013/746068.
- Коржевский Д.Э., Кирик О.В., Сухорукова Е.Г., Власов Т.Д. Cтруктурная организация микроглиоцитов стриатума после транзиторной фокальной ишемии. Морфология 2012; 141(2): 28–32.
- Murata Y., Sugimoto K., Yang C., Harada K., Gono R., Harada T., Miyashita Y., Higashisaka K., Katada R., Tanaka J., Matsumoto H. Activated microglia-derived macrophage-like cells exacerbate brain edema after ischemic stroke correlate with astrocytic expression of aquaporin-4 and interleukin-1 alpha release. Neurochem Int 2020; 140: 104848, https://doi.org/10.1016/j.neuint.2020.104848.
- Hansen D.V., Hanson J.E., Sheng M. Microglia in Alzheimer's disease. J Cell Biol 2018; 217(2): 459–472, https://doi.org/10.1083/jcb.201709069.
- Grubman A., Choo X.Y., Chew G., Ouyang J.F., Sun G., Croft N.P., Rossello F.J., Simmons R., Buckberry S., Landin D.V., Pflueger J., Vandekolk T.H., Abay Z., Zhou Y., Liu X., Chen J., Larcombe M., Haynes J.M., McLean C., Williams S., Chai S.Y., Wilson T., Lister R., Pouton C.W., Purcell A.W., Rackham O.J.L., Petretto E., Polo J.M. Transcriptional signature in microglia associated with Aβ plaque phagocytosis. Nat Commun 2021; 12(1): 3015, https://doi.org/10.1038/s41467-021-23111-1.
- Miao J., Ma H., Yang Y., Liao Y., Lin C., Zheng J., Yu M., Lan J. Microglia in Alzheimer's disease: pathogenesis, mechanisms, and therapeutic potentials. Front Aging Neurosci 2023; 15: 1201982, https://doi.org/10.3389/fnagi.2023.1201982.
- Bubnova S., Guryanov A., Konkina D., Karapetian V., Kaldybaev l., Pavlova D., Shorina V., Sigalov M., Сhen C. Evaluation of the levels of inflammatory proteins, such as Iba1 and GFAP, in brain tissues of patients with Alzheimer’s disease by western blot analysis. Arzneimitteltherapie 2025; 1385–1397. URL: https://arzneimitteltherapie.com/archives/1520.
- Lier J., Winter K., Bleher J., Grammig J., Mueller W.C., Streit W., Bechmann I. Loss of Iba1-expression in brains from individuals with obesity and hepatic dysfunction. Brain Res 2019; 1710: 220–229, https://doi.org/10.1016/j.brainres.2019.01.006.
- Imai Y., Ibata I., Ito D., Ohsawa K., Kohsaka S. A novel gene Iba1 in the major histocompatibility complex class III region encoding an EF hand protein expressed in a monocytic lineage. Biochem Biophys Res Commun 1996; 224(3): 855–862, https://doi.org/10.1006/bbrc.1996.1112.
- Hollopeter G., Jantzen H.M., Vincent D., Li G., England L., Ramakrishnan V., Yang R.B., Nurden P., Nurden A., Julius D., Conley P.B. Identification of the platelet ADP receptor targeted by antithrombotic drugs. Nature 2001; 409(6817): 202–207, https://doi.org/10.1038/35051599.
- Butovsky O., Jedrychowski M.P., Moore C.S., Cialic R., Lanser A.J., Gabriely G., Koeglsperger T., Dake B., Wu P.M., Doykan C.E., Fanek Z., Liu L., Chen Z., Rothstein J.D., Ransohoff R.M., Gygi S.P., Antel J.P., Weiner H.L. Identification of a unique TGF-β-dependent molecular and functional signature in microglia. Nat Neurosci 2014; 17(1): 131–143, https://doi.org/10.1038/nn.3599.
- Maeda J., Minamihisamatsu T., Shimojo M., Zhou X., Ono M., Matsuba Y., Ji B., Ishii H., Ogawa M., Akatsu H., Kaneda D., Hashizume Y., Robinson J.L., Lee V.M., Saito T., Saido T.C., Trojanowski J.Q., Zhang M.R., Suhara T., Higuchi M., Sahara N. Distinct microglial response against Alzheimer's amyloid and tau pathologies characterized by P2Y12 receptor. Brain Commun 2021; 3(1): fcab011, https://doi.org/10.1093/braincomms/fcab011.
- Amadio S., Parisi C., Montilli C., Carrubba A.S., Apolloni S., Volonté C. P2Y(12) receptor on the verge of a neuroinflammatory breakdown. Mediators Inflamm 2014; 2014: 975849, https://doi.org/10.1155/2014/975849.










