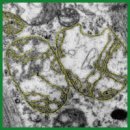
Новый количественный метод оценки ультраструктуры митохондрий кардиомиоцитов ушка правого предсердия
Цель исследования — разработать количественный метод оценки ультраструктуры митохондрий кардиомиоцитов ушка правого предсердия у больных с хронической сердечной недостаточностью (ХСН).
Материалы и методы. В одноцентровое проспективное исследование были включены 39 пациентов в возрасте 67 [58; 71] лет, перенесших коронарное шунтирование. Критериями включения стали наличие сердечной недостаточности с фракцией выброса левого желудочка <50%; атеросклеротические бляшки — 70% и более в двух или трех крупных коронарных артериях; решение кардиокоманды о проведении коронарного шунтирования. Во время операции осуществляли забор биоптата миокарда ушка правого предсердия для электронной микроскопии. Для анализа использовали два расчетных показателя: «общая площадь межфибриллярных митохондрий» и «отношение длины внешней мембраны к длине внутренней мембраны», на основе которых рассчитывали суммарный показатель по формуле «общая площадь межфибриллярных митохондрий» / «отношение длины внешней мембраны к длине внутренней мембраны».
Результаты. Медианные значения расчетных показателей, характеризующих ультраструктуру митохондрий кардиомиоцитов ушка правого предсердия, составили 43,7 [35,9; 54,3]% для показателя «общая площадь межфибриллярных митохондрий»; 31 [25; 37]% — для показателя «отношение длины внешней мембраны к длине внутренней мембраны» и 1,4 [0,95; 2,00] — для суммарного показателя, учитывающего обе ультраструктурные характеристики митохондрий: «общая площадь межфибриллярных митохондрий» / «отношение длины внешней мембраны к длине внутренней мембраны».
Для оценки клинической значимости предложенного интегрального показателя изучены ассоциации полученных значений с наличием фибрилляции предсердий (ФП). Ультраструктурные изменения митохондрий были более выраженными у пациентов с сочетанием ФП и ХСН, однако статистическая значимость различий отдельных показателей не достигалась: общая площадь межфибриллярных митохондрий была ниже в группе с ФП (42% против 49%; p=0,224), отношение длины внешней мембраны к внутренней было выше при ФП (35% против 31%; p=0,125). Величина суммарного показателя оказалась статистически значимо ниже у пациентов с ФП (0,96 против 1,75; p=0,021). Был проведен ROC-анализ для выявления связи между расчетным показателем «общая площадь межфибриллярных митохондрий» / «отношение длины внешней мембраны к длине внутренней мембраны» и наличием ФП; площадь под ROC-кривой (AUC) составила 0,773 (р=0,021).
Заключение. Предложенный суммарный показатель для анализа микрофотографий кардиомиоцитов, рассчитанный как «общая площадь межфибриллярных митохондрий» / «отношение длины внешней мембраны к длине внутренней мембраны», позволяет получить комплексную характеристику митохондрий, учитывающую не только их количество и размеры, но и внутреннюю структуру.
- Галявич А.С., Терещенко С.Н., Ускач Т.М., Агеев Ф.Т., Аронов Д.М., Арутюнов Г.П., Беграмбекова Ю.Л., Беленков Ю.Н., Бойцов С.А., Бубнова М.Г., Васюк Ю.А., Виллевальде С.В., Виноградова Н.Г., Гарганеева A.А., Гендлин Г.Е., Гиляревский С.Р., Глезер М.Г., Готье С.В., Гринштейн Ю.И., Довженко Т.В., Драпкина О.М., Дупляков Д.В., Жиров И.В., Затейщиков Д.А., Звартау Н.Э., Иртюга О.Б., Кобалава Ж.Д., Козиолова Н.А., Коротеев А.В., Либис Р.А., Лопатин Ю.М., Мареев В.Ю., Мареев Ю.В., Мацкеплишвили С.Т., Михайлов Е.Н., Насонова С.Н., Нарусов О.Ю., Недогода С.В., Недошивин А.О., Овчинников А.Г., Орлова Я.А., Перепеч Н.Б., Погосова Н.В., Римская Е.М., Самко А.Н., Саидова М.А., Сапельников О.В., Сафиуллина А.А., Ситникова М.Ю., Скворцов А.А., Скибицкий В.В., Стукалова О.В., Тарловская Е.И., Терещенко А.С., Чесникова А.И., Федотов П.А., Фомин И.В., Хасанов Н.Р., Шевченко А.О., Шапошник И.И., Шария М.А., Шляхто Е.В., Явелов И.С., Якушин С.С. Хроническая сердечная недостаточность. Клинические рекомендации 2024. Российский кардиологический журнал 2024; 29(11): 6162, https://doi.org/10.15829/1560-4071-2024-6162.
- Paillard M., Abdellatif M., Andreadou I., Bär C., Bertrand L., Brundel B.J.J.M., Chiva-Blanch G., Davidson S.M., Dawson D., Di Lisa F., Evans P., Giricz Z., Hausenloy D.J., Kleinbongard P., Lezoualc'h F., Liehn E., Maack C., Maguy A., Murphy E., Perrino C., Pesce M., Rainer P.P., Streckfuss-Bömeke K., Thielmann M., Tian R., Tocchetti C.G., Van Der Velden J., Van Linthout S., Zacchigna S., Krieg T. Mitochondrial targets in ischaemic heart disease and heart failure, and their potential for a more efficient clinical translation. A scientific statement of the ESC Working Group on Cellular Biology of the Heart and the ESC Working Group on Myocardial Function. Eur J Heart Fail 2025; 27(9): 1720–1736, https://doi.org/10.1002/ejhf.3674.
- Гарганеева А.А., Тукиш О.В., Кужелева Е.А., Муслимова Э.Ф., Гуля М.О., Жаргасова В.А., Попов С.В. Сердечная недостаточность и митохондриальная дисфункция: методы исследования в эксперименте и клинической практике. Acta Biomedica Scientifica 2025; 10(1): 103–114, https://doi.org/10.29413/ABS.2025-10.1.11.
- Stepanov A.V., Baidyuk E.V., Sakuta G.A. The features of mitochondria of cardiomyocytes from rats with chronic heart failure. Cell and Tissue Biology 2017; 11(6): 458–465, https://doi.org/10.1134/s1990519x17060086.
- Кужелева Е.А., Гарганеева А.А., Тукиш О.В., Витт К.Н., Андреев С.Л., Сыромятникова Е.Е., Владимирова Е.А. Общая площадь межфибриллярных митохондрий в кардиомиоцитах ушка правого предсердия как показатель функционального состояния сердечно-сосудистой системы при хронической сердечной недостаточности. Бюллетень экспериментальной биологии и медицины 2024; 178(10): 497–502, https://doi.org/10.47056/0365-9615-2024-178-10-497-502.
- El'darov C.M., Vays V.B., Vangeli I.M., Bakeeva L.E., Kolosova N.G. Morphometric examination of mitochondrial ultrastructure in aging cardiomyocytes. Biochemistry 2015; 80(5): 604–609, https://doi.org/10.1134/s0006297915050132.
- Гарганеева А.А., Кужелева Е.А., Тукиш О.В., Витт К.Н., Андреев С.Л., Муслимова Э.Ф., Корепанов В.А., Афанасьев С.А., Гуля М.О., Сыромятникова Е.Е., Владимирова Е.А., Степанов И.В. Возможности диагностики митохондриальной дисфункции при хронической сердечной недостаточности. Сибирский журнал клинической и экспериментальной медицины 2024; 39(3): 51–57, https://doi.org/10.29001/2073-8552-2024-39-3-51-57.
- McDonagh T.A., Metra M., Adamo M., Gardner R.S., Baumbach A., Böhm M., Burri H., Butler J., Čelutkienė J., Chioncel O., Cleland J.G.F., Crespo-Leiro M.G., Farmakis D., Gilard M., Heymans S., Hoes A.W., Jaarsma T., Jankowska E.A., Lainscak M., Lam C.S.P., Lyon A.R., McMurray J.J.V., Mebazaa A., Mindham R., Muneretto C., Francesco Piepoli M., Price S., Rosano G.M.C., Ruschitzka F., Skibelund A.K.; ESC Scientific Document Group 2023. Focused Update of the 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2023; 44(37): 3627–3639, https://doi.org/10.1093/eurheartj/ehad195.
- Dabravolski S.A., Zhuravlev A.D., Kartuesov A.G., Borisov E.E., Sukhorukov V.N., Orekhov A.N. Mitochondria-mediated cardiovascular benefits of sodium-glucose co-transporter 2 inhibitors. Int J Mol Sci 2022; 23(10): 5371, https://doi.org/10.3390/ijms23105371.
- Schwemmlein J., Maack C., Bertero E. Mitochondria as therapeutic targets in heart failure. Curr Heart Fail Rep 2022; 19(2): 27–37, https://doi.org/10.1007/s11897-022-00539-0.
- Hayashi D., Ohshima S., Isobe S., Cheng X.W., Unno K., Funahashi H., Shinoda N., Okumura T., Hirashiki A., Kato K., Murohara T. Increased (99m)Tc-sestamibi washout reflects impaired myocardial contractile and relaxation reserve during dobutamine stress due to mitochondrial dysfunction in dilated cardiomyopathy patients. J Am Coll Cardiol 2013; 61(19): 2007–2017, https://doi.org/10.1016/j.jacc.2013.01.074.
- Bidaoui G., Assaf A., Marrouche N. Atrial fibrillation in heart failure: novel insights, challenges, and treatment opportunities. Curr Heart Fail Rep 2024; 22(1): 3, https://doi.org/10.1007/s11897-024-00691-9.
- Carlisle M.A., Fudim M., DeVore A.D., Piccini J.P. Heart failure and atrial fibrillation, like fire and fury. JACC Heart Fail 2019; 7(6): 447–456, https://doi.org/10.1016/j.jchf.2019.03.005.
- Zdebik N., Poręba R., Gać P. Importance of T1-mapping sequence in patients with hypertrophic cardiomyopathy without foci of non-ischemic myocardial injury in late gadolinium enhancement sequence. Biomedicines 2024; 12(6): 1330, https://doi.org/10.3390/biomedicines12061330.
- Сухачева Т.В., Васковский В.А., Ревишвили А.Ш., Серов Р.А. Морфологические особенности миокарда ушек предсердий у пациентов с разными формами фибрилляции предсердий. Архив патологии 2017; 79(4): 3–12, https://doi.org/10.17116/patol20177943-12.
- Guttipatti P., Saadallah N., Ji R., Avula U.M.R., Goulbourne C.N., Wan E.Y. Quantitative 3D electron microscopy characterization of mitochondrial structure, mitophagy, and organelle interactions in murine atrial fibrillation. J Struct Biol 2024; 216(3): 108110, https://doi.org/10.1016/j.jsb.2024.108110.
- Qi X., Xiong F., Xiao J., Muthukumarasamy K.M., Altuntas Y., Zhong Y., Abu-Taha I., Bruns F., Tekook M., Kamler M., Villeneuve L., Nozza A., Sirois M., Karch J., Pasdois P., Bers D.M., Dobrev D., Nattel S. Time-dependent mitochondrial remodeling in experimental atrial fibrillation and potential therapeutic relevance. Preprint. bioRxiv 2025; 2025.01.29.635508, https://doi.org/10.1101/2025.01.29.635508.
- Paillard M., Abdellatif M., Andreadou I., Bär C., Bertrand L., Brundel B.J.J.M., Chiva-Blanch G., Davidson S.M., Dawson D., Di Lisa F., Evans P., Giricz Z., Hausenloy D.J., Kleinbongard P., Lezoualc'h F., Liehn E., Maack C., Maguy A., Murphy E., Perrino C., Pesce M., Rainer P.P., Streckfuss-Bömeke K., Thielmann M., Tian R., Tocchetti C.G., Van Der Velden J., Van Linthout S., Zacchigna S., Krieg T. Mitochondrial targets in ischaemic heart disease and heart failure, and their potential for a more efficient clinical translation. A scientific statement of the ESC Working Group on Cellular Biology of the Heart and the ESC Working Group on Myocardial Function. Eur J Heart Fail 2025; 27(9): 1720–1736, https://doi.org/10.1002/ejhf.3674.










